中药联合免疫检查点抑制剂治疗Ⅲ-Ⅳ期非小细胞肺癌的安全性观察
2024-05-17周麟邱思冲李柳宁柴小姝
周麟, 邱思冲, 李柳宁, 柴小姝
(1.广州中医药大学第二临床医学院,广东广州 510006;2.四川省肿瘤医院,四川成都 610041;3.广东省中医院大学城医院肿瘤科,广东广州 510006;4.广东省中医院大德路总院肿瘤科,广东广州 510120)
肺癌是我国发病率和死亡率居首位的恶性肿瘤[1],其中非小细胞肺癌(non-small cell lung cancer,NSCLC)约占所有病理类型的85%。近年来,以程序性死亡受体1(programmed cell death protein 1,PD-1)抑制剂和程序性死亡配体1(programmed cell death ligand 1,PD-L1)抑制剂为代表的免疫检查点抑制剂(immune checkpoint inhibitors,ICIs)在NSCLC 的治疗中疗效显著。由于ICIs 是通过激活肿瘤患者体内的免疫效应细胞从而达到杀伤肿瘤细胞的作用[2],免疫细胞的过度激活易引发诸如肺炎、心肌炎、肾上腺功能减退等全身各系统的免疫相关不良事件(immune-related adverse events,irAEs),严重影响患者的生活质量乃至威胁患者的生命安全。目前,irAEs 的发生与用药时间及用药剂量之间的关系尚未明确[3],irAEs 发生的部位及时间难以预见,只能在irAEs 发生后采取对症治疗或糖皮质激素治疗,而糖皮质激素治疗对ICIs 疗效的影响及其潜在的风险令人担忧,若能对irAEs进行一级预防,后续的治疗风险将大大降低。目前已有研究[3]表明,中药可能降低PD-1/PD-L1 抑制剂治疗各类晚期实体恶性肿瘤的irAEs 发生率,使患者看到irAEs 一级预防的曙光。基于此,本研究旨在通过临床数据,采用回顾性研究方法,进一步验证中药能否降低ICIs 治疗Ⅲ-Ⅳ期NSCLC 的不良反应发生率。现将研究结果报道如下。
1 对象与方法
1.1 研究对象回顾性分析2019 年9 月1 日至2022 年8 月31 日在广东省中医院大学城医院肿瘤科确诊为Ⅲ-Ⅳ期NSCLC 并接受中药联合ICIs 治疗的住院患者病例资料,共纳入100 例患者,其中10 例患者被排除,最终共有90 例中药联合ICIs 治疗的Ⅲ-Ⅳ期NSCLC 患者。本研究符合医学伦理学要求并通过广东省中医院医学伦理委员会的审核批准,批准号:BF2022-108-01。
1.2 病例选择标准
1.2.1 纳入标准 ①经细胞学或病理学确诊为NSCLC;②完善影像学检查,根据《中华医学会肺癌临床诊疗指南(2022版)》[1]中的肺癌分期确诊为Ⅲ-Ⅳ期;③接受≥1 个周期的ICIs 治疗,并同时接受≥1 个周期的中药治疗;④接受ICIs 治疗前,完善胸部及腹部CT 平扫+增强、血常规、生化34 项、甲状腺功能5 项和血清皮质醇测定等常规基线资料检查的患者。
1.2.2 排除标准 ①入组其他临床研究的患者;②合并其他恶性肿瘤的患者;③伴有严重的心、肺、肝、肾功能不全的患者;④妊娠期或哺乳期妇女;⑤精神病患者;⑥需长期服用皮质类激素的患者;⑦临床资料收集不完整的患者。
1.3 研究方法(1)临床资料收集:收集患者的年龄、性别、美国东部肿瘤协作组的功能状态(performance status,PS)评分、病理类型、疾病分期、吸烟史、有无基础疾病、治疗线数、有无纵隔淋巴结转移、有无脑转移、有无肝转移、有无肾上腺转移、有无骨转移、PD-L1 表达情况、药物治疗方案、药物不良反应、实验室检查和影像学检查等相关临床资料。(2)分析90 例Ⅲ-Ⅳ期NSCLC 患者的中医证型分布情况、中药联合ICIs治疗Ⅲ-Ⅳ期NSCLC 的安全性,并采用二元Logistic回归分析探讨ICIs治疗Ⅲ-Ⅳ期NSCLC发生irAEs的可能影响因素。
1.4 治疗方法
1.4.1 中药治疗 患者的中医辨证分型及选方用药参照《肿瘤科专病中医临床诊治》[4],结合第10 版《中医内科学》[5],根据患者实际情况酌情加减药物。煎服法:每天1 剂,常规煎取300 mL(统一采用康美智慧药房代煎中药),分2 次服用,每次150 mL。具体辨证用药如下:①气虚痰瘀证。采用扶正抗癌方[6]加减:太子参、白术、黄芪、炒薏苡仁、甘草、山慈菇、白花蛇舌草、龙葵、石见穿、八月札、蛇泡簕、莪术。血虚者,加当归、阿胶珠以补血活血;纳呆食少者,加炒山楂、麦芽、稻芽、砂仁以开胃健脾。②痰瘀阻络证。采用桃红四物汤加减:桃仁、川芎、白芍、红花、生地黄、当归、莪术、香附、延胡索、牡丹皮。痰多者,加陈皮、化橘红、厚朴、麸炒枳实理气化痰;食少、乏力、气短者,加人参、白术、黄芪以益气健脾;口干舌燥者,加沙参、天花粉、玄参以益气生津;咯血反复不愈者,加蒲黄、三七、仙鹤草以凉血活血止血。③气阴两虚证。采用沙参麦冬汤合生脉散加减:北沙参、麦冬、玉竹、天花粉、人参、五味子、扁豆、炙甘草、桑叶、白花蛇舌草、蛇莓、生地黄。咳嗽咳痰不利、痰少而黏者,加川贝母、瓜蒌、杏仁以润肺化痰止咳;腰膝酸痛者,加仙茅、巴戟天、补骨脂、肉苁蓉以补肾。④气血亏虚证。采用十全大补丸加减:党参、白术、茯苓、炙甘草、当归、川芎、白芍、熟地黄、黄芪、肉桂、生姜、大枣。血虚明显者,加阿胶、鸡血藤以补血。⑤痰热蕴结证。采用清金化痰汤加减:黄芩、栀子、知母、瓜蒌仁、浙贝母、麦冬、橘皮、茯苓、桔梗、桑白皮、甘草。食少、乏力者,加人参、白术、山楂、麦芽、砂仁以益气健脾。
1.4.2 ICIs 治疗 根据患者病情及个人意愿选择合适的ICIs 治疗,治疗前已告知患者及家属使用ICIs的风险,并已签署免疫治疗知情同意书,用药剂量及周期参考药物说明书,具体用药如下:(1)PD-L1 抑制剂:①阿替利珠单抗(泰圣奇,Roche Registration GmbH;批准文号:注册证号S20200004)1 200 mg,静脉滴注,每3 周治疗1 次,第1 天用药(d1)。②度伐利尤单抗(英飞凡,Catalent Indiana,LLC;批准文号:注册证号S20190039)10 mg/kg,静脉滴注,每2 周治疗1 次,d1。(2)PD-1抑制剂:①卡瑞利珠单抗(艾瑞卡,苏州盛迪亚生物医药有限公司,批准文号:国药准字S20190027)200 mg,静脉滴注,每3 周治疗1 次,d1。②帕博利珠单抗(可瑞达,默沙东公司,批准文号:注册证号S20180019)200 mg,静脉滴注,每3 周治疗1 次,d1。③派安普利单抗(安尼可,中山康方生物医药有限公司,批准文号:国药准字S20210033)200 mg,静脉滴注,每3 周治疗1 次,d1。④特瑞普利单抗(拓益,上海君实生物医药科技股份有限公司,批准文号:国药准字S20180015)240 mg, 静脉滴注,每3 周治疗1 次,d1。⑤替雷利珠单抗注射液(百泽安,广州百济神州生物制药有限公司,批准文号:国药准字S20190045)200 mg,静脉滴注,每3 周治疗1 次,d1。⑥信迪利单抗[达伯舒,信达生物制药(苏州)有限公司,批准文号:国药准字S20180016]200 mg,静脉滴注,每3周治疗1次,d1。
1.4.3 治疗方案 所有患者均参照以上证型服用中药汤剂,联合ICIs 单药治疗、ICIs+化疗、ICIs+抗血管生成药物、ICIs+化疗+抗血管生成药物4 种治疗方案。期间可联合放疗、介入治疗等。
1.5 不良反应评价和分级标准根据诺氏评估量表法判定药物不良反应与药品的关联性[7],评价结果为“确定”“很可能”和“可能”时为相关,评价结果为“可疑”时为不相关。同时根据《中国临床肿瘤学会(CSCO)免疫检查点抑制剂相关的毒性管理指南2021》[2]对irAEs 的严重程度分级(共分为1 ~5 级):G1 为轻度毒性,G2 为中度毒性,G3 为重度毒性,G4为危及生命的毒性,G5为与毒性相关的死亡。
1.6 统计方法应用SPSS 25.0统计学软件对数据进行统计分析。计数资料用率或构成比表示,统计分析采用χ2检验。均采用双侧检验,以P<0.05为差异有统计学意义。
2 结果
2.1 一般资料情况90 例NSCLC 患者中,男性59 例(65.6%),女性31 例(34.4%);年龄范围为34~87岁,其中≥65岁52例(57.8%);PS评分0~1 分71 例(78.9%),≥2 分19 例(21.1%);根据第8 版肺癌分期[1],Ⅲ期患者14 例(包括ⅢA 2 例,ⅢB 7 例,ⅢC 5 例),Ⅳ期患者76 例(包括ⅣA 18 例,ⅣB 58例);主要病理类型为腺癌和鳞状细胞癌,分别为64 例(71.1%)和22 例(24.4%)。患者的基本情况见表1。
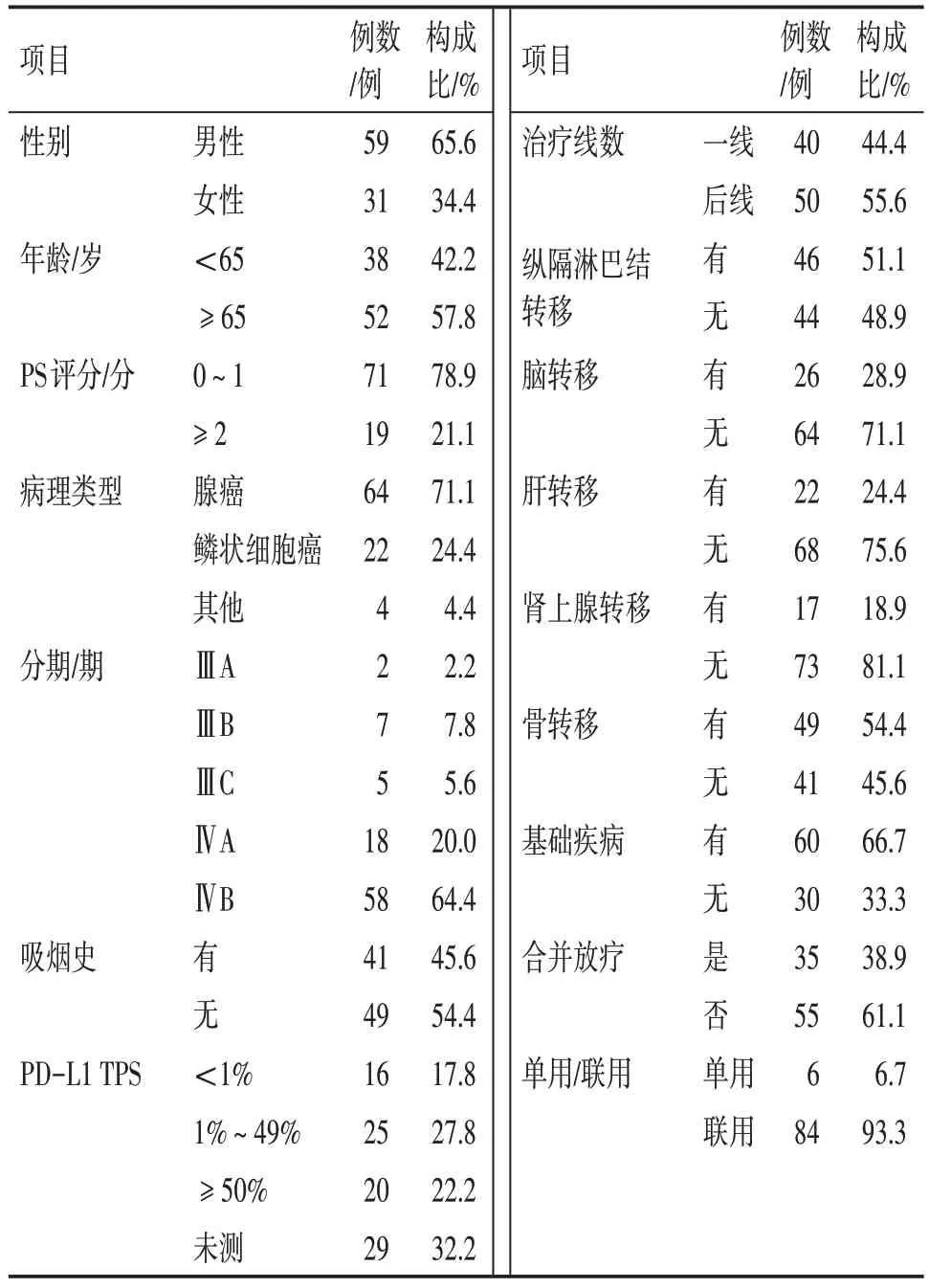
表1 接受免疫检查点抑制剂(ICIs)治疗的90例非小细胞肺癌(NSCLC)患者基线特征Table 1 Baseline characteristics of 90 patients with nonsmall cell lung cancer(NSCLC)treated with immune checkpoint inhibitors(ICIs)
2.2 中医证型分布情况将所有患者分为气虚痰瘀证、痰瘀阻络证、气阴两虚证、气血亏虚证、痰热蕴结证5 种证型,其中气虚痰瘀证最多,为80例(88.9%),其他分别为痰瘀阻络证6例(6.7%)、气阴两虚证2例(2.2%)、气血亏虚证和痰热蕴结证各1例(1.1%)。
2.3 ICIs临床应用情况90 例患者中,涉及8 种ICIs,有15 例患者应用2 种或3 种ICIs,故应用ICIs 的总频次为106 例。其中,使用替雷利珠单抗注射液占比最高(43例,40.6%),其次为信迪利单抗注射液(18 例,17.0%)和卡瑞利珠单抗注射液(17例,16.0%),派安普利单抗注射液使用占比最低(1 例,0.9%)。联合用药情况,ICIs+化疗+抗血管生成药物最多(52 例,49.1%),其次为ICIs+化疗(39 例,36.8%),ICIs+贝伐珠单抗、恩度或安罗替尼等抗血管生成药物8 例,另有7 例患者为ICIs单药治疗。ICIs的具体应用情况见表2。

表2 90例非小细胞肺癌(NSCLC)患者的免疫检查点抑制剂(ICIs)临床应用情况Table 2 The list of immune checkpoint inhibitors(ICIs)used for 90 patients with non-small cell lung cancer(NSCLC)[例(%)]
2.4 免疫相关不良事件90例NSCLC患者中,有35例发生irAEs,总体发生率为38.9%,其中发生≥3 级irAEs 的患者有5 例,占5.6%;导致停药的有7 例(7.8%)。ICIs单药治疗的≥3级irAEs 发生率高于联合治疗,差异有统计学意义(P=0.034)。所有患者irAEs 发生情况见表3。初次发生irAEs 的免疫治疗疗程主要集中在1~3程,有17例,占48.6%,结果见图1。
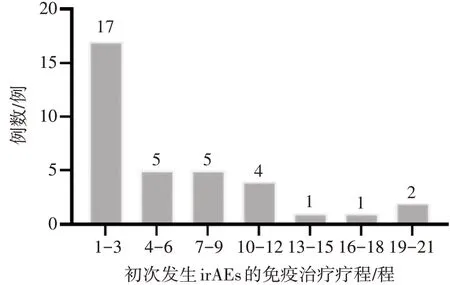
图1 初次发生免疫相关不良事件(irAEs)的免疫治疗疗程分布Figure 1 Distribution of immunotherapy courses with initial immune-related adverse events(irAEs)

表3 接受免疫检查点抑制剂(ICIs)治疗的90例非小细胞肺癌(NSCLC)患者的免疫相关不良事件(irAEs)发生情况Table 3 The incidence of immune-related adverse events(irAEs)in 90 non-small cell lung cancer(NSCLC)patients treated with immune checkpoint inhibitors(ICIs)[例(%)]
irAEs 共计发生48 例次,发生率居前3 位的分别为甲状腺功能减退10例(11.1%)、肾上腺皮质功能减退8 例(8.9%)和心脏毒性7 例(7.8%)。≥3 级irAEs 为7 例次,其余表现为皮疹、带状疱疹、反应性皮肤毛细血管增生症(RCCEP)、性激素异常、高血糖、肝功能异常、发热和肺炎等。irAEs 具体表现及分级情况见表4。

表4 接受免疫检查点抑制剂(ICIs)治疗的90例非小细胞肺癌(NSCLC)患者的免疫相关不良事件(irAEs)分类和分级情况Table 4 Classification and grading of immune-related adverse events(irAEs)in 90 non-small cell lung cancer(NSCLC)patients treated with immune checkpoint inhibitors(ICIs)[例(%)]
2.5 造成免疫相关不良事件的危险因素把患者分为无irAEs组和irAEs组,将2组患者的性别、年龄、PS 评分、病理类型、分期、吸烟史、PD-L1表达情况、治疗线数、有无纵隔淋巴结转移、有无脑转移、有无肝转移、有无肾上腺转移、有无骨转移、有无基础疾病、是否合并放疗、用药方式和中医证型进行单因素分析,结果发现PS评分、有无纵隔淋巴结转移和有无肾上腺转移的差异有统计学意义(P<0.05)。将上述3 个差异有统计学意义的因素纳入二元Logistic 回归分析,发现PS 评分为0~1 分(OR=8.218,95%CI:1.607-42.023,P= 0.011)和有肾上腺转移(OR=4.497,95%CI:1.237-16.354,P= 0.022)是ICIs 治疗Ⅲ-Ⅳ期NSCLC 发生irAEs 的独立危险因素(均P<0.05),结果见图2。
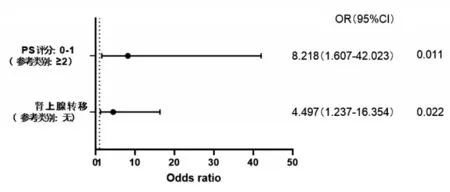
图2 造成免疫相关不良事件(irAEs)的危险因素Figure 2 Risk factors for immune-related adverse events(irAEs)
3 讨论
对于晚期非小细胞肺癌(NSCLC)患者,目前主要以全身治疗为主,《中国临床肿瘤学会(CSCO)非小细胞肺癌诊疗指南2022》推荐驱动基因阴性患者一线使用免疫联合含铂双药化疗或联合含铂双药化疗+抗血管生成药,对于程序性死亡配体1(PD-L1)表达阳性(≥1%)患者,可一线单药使用帕博利珠单抗,针对PD-L1 高表达(≥50%)患者,可单药使用阿替利珠单抗。免疫治疗的加入改变了晚期NSCLC 的治疗结局,使晚期NSCLC 的5 年生存率从原有的5%上升到31.9%[8],给患者的长期生存带来希望。在免疫治疗获得疗效的同时,由于T细胞对抗原的活性增强、已存在的自身免疫抗体水平增高,攻击人体正常组织[9],免疫相关不良事件(irAEs)随之发生。根据现有指南[2],irAEs 轻症采取观察或对症治疗,较严重则使用糖皮质激素治疗。有研究[10]表明,长期使用糖皮质激素可能会引发相关的严重不良事件,降低免疫治疗疗效,故新的irAEs治疗措施亟待挖掘。
中医药历来被认为有扶正祛邪、调节阴阳之功,现代医学针对中医药的这一特性进行研究后发现,中药对人体免疫具有双向调节作用[11],这能充分满足使用ICIs 的大部分免疫力低下的肺癌患者既要提高自身免疫又要遏制过度免疫引发irAEs 的需求。目前已有多个研究[12]表明,中医药可以通过影响机体免疫、参与肿瘤微环境等降低NSCLC 药物治疗不良反应的发生,例如吴婷婷等[13]的研究显示,健脾固肠方能改善Ⅲ、Ⅳ期肿瘤化疗患者肠道屏障功能,但少有研究关注中药对irAEs 的作用。我们在前期临床观察中发现中药可降低使用PD-1/PD-L1 治疗的各类恶性肿瘤患者irAEs 的发生率[3],本研究则进一步探究中药对NSCLC患者irAEs的影响。
《中国临床肿瘤学会(CSCO)免疫检查点抑制剂相关的毒性管理指南2021》[2]显示,PD-1 抑制剂总体irAEs 中位发生率及范围为75.7%(58.0%~82.0%),G3 以上为17.6%(7.0%~20.0%);PD-L1抑制剂总体irAEs中位发生率及范围为66.6%(66.0%~84.0%),G3 以上为15.7%(5.0%~17.0%);ICIs 联合化疗的总体irAEs 及G3 以上发生率则更高,分别为84.5%(69.0%~99.8%)及43.7%(22.9%~73.2%);PD-1/PD-L1抑制剂治疗的NSCLC 患者中有14%因出现irAEs 而中断治疗[14];有0.36%使用PD-1 抑制剂及0.38%的使用PD-L1 抑制剂的患者因irAEs 死亡[15]。有研究[16]报道,阿替利珠单抗治疗既往治疗过的NSCLC,总体irAEs 发生率为64%,G3 及以上irAEs 为15%。本研究采用中药联合免疫检查点抑制剂(ICIs)治疗NSCLC,所有级别irAEs 的发生率仅为38.9%,G3 及以上irAEs 发生率仅为5.6%,明显低于现有报道水平,表明中药有降低irAEs 发生率的可能。
本研究中,一线使用中药联合ICIs 治疗晚期NSCLC的所有级别irAEs 发生率为42.2%,G3及以上irAEs 发生率为2.5%。在ORIENT-11 研究[17]中,信迪利单抗联合化疗一线治疗局部晚期或转移性非鳞状NSCLC,所有级别irAEs 发生率为43.2%,G3及以上irAEs发生率为5.6%。KEYNOTE-042的研究[18]表明,帕博利珠单抗联合化疗一线治疗的PD-L1 表达的局部晚期或转移性NSCLC,所有级别irAEs 发生率为28%,G3 及以上irAEs 发生率为8%。本研究所有级别irAEs 发生率与ORIENT-11相当,高于KEYNOTE-042,然而这两项大型随机对照研究均对治疗人群进行了严格筛选,均为既往未经治疗、无致敏性EGFR 突变及ALK 易位,PD-L1 的肿瘤细胞阳性比例分数(TPS)为1%或更高,而在本真实世界研究中,纳入了包含PD-L1 TPS<1%、1%~49%、≥50%及未明确的患者,这可能是本研究所有级别irAEs 发生率偏高,但G3及以上irAEs 发生率明显低于其他研究[19-20],仍显示了中药在降低一线治疗的irAEs 中有一定作用的原因。
本研究中,单药治疗的G3 及以上irAEs 发生率高于联合治疗,差异有统计学意义。Li L 等[21]的研究显示,ICIs 联合化疗或抗血管生成药物可增加1~2 级irAEs,但不能证明3~5 级irAEs 有所提高。Mok T S K 和Gandhi L 等[18,22]的研究发现帕博利珠单抗联合化疗显著增加3~5 级irAEs(67.2%vs18.0%)。表明相比免疫单药治疗,中药可能对降低ICIs 联合化疗或抗血管生成药物治疗的3~5 级irAEs 作用更明显。但由于本研究纳入的免疫单药治疗仅有6例,我们期待更有力的证据。
本研究irAEs 发生率居前3 位的分别是甲状腺功能减退10 例(11.1%)、肾上腺皮质功能减退8 例(8.9%)和心脏毒性7 例(7.8%),而PD-1/PD-L1 抑制剂单药治疗的甲状腺功能减退和肾上腺皮质功能减退发生率均为0%。据报道[23-24],PD-1/PD-L1抑制剂单药治疗的甲状腺功能紊乱发生率为5%~10%,肾上腺皮质功能减退发生率为0.7%。联合治疗所致内分泌毒性则显著高于单药治疗,Li L等[21]的研究表明,联合治疗的甲状腺功能减退发生率明显高于单药治疗(24.1%vs15.8%,P<0.001)。本研究中联合治疗所致甲状腺功能减退发生率为11.1%,说明中药对降低甲状腺功能减退发生率有一定作用。
Eigentler T K 等[25]的研究表明,irAEs 通常在1~6 个月内发生。本研究中,初次发生irAEs 的免疫治疗疗程主要集中在1~3 程。那么在免疫治疗早期甚至免疫治疗前运用中药是否获益更加显著,值得进一步研究明确。
此外,我们在临床运用中药治疗NSCLC 患者时,将患者分为气虚痰瘀证、痰瘀阻络证、气阴两虚证、气血亏虚证、痰热蕴结证5种证型,其中以气虚痰瘀证患者最多(80 例,88.89%),治疗时以广东省中医院吴万垠教授所创的扶正抗癌方为底方[6],该方中太子参、白术、黄芪、炒薏苡仁、甘草平补肺脾之气,山慈菇、白花蛇舌草、龙葵、石见穿、八月札、蛇泡簕、莪术等化痰消痈、活血化瘀,全方辨病与辨证、扶正与祛邪相结合,共奏扶正抗癌、化痰消痈、活血祛瘀之功效。既往研究[6,26-28]表明,扶正抗癌方可通过多种机制抑制肺癌细胞增殖、促进肺癌细胞凋亡。本研究则初步表明了扶正抗癌方在降低irAEs 方面也有一定疗效。
综上所述,中药有降低ICIs 治疗Ⅲ-Ⅳ期NSCLC 的所有级别irAEs 尤其是G3 及以上irAEs 发生率的作用;对比免疫单药治疗,中药对降低ICIs联合化疗或抗血管生成药物治疗的3~5级irAEs作用更明显。功能状态(PS)评分为0~1 分和有肾上腺转移是ICIs 治疗Ⅲ-Ⅳ期NSCLC 发生irAEs 的独立危险因素。但由于本研究为回顾性研究,且样本量较小,特别是免疫单药治疗仅有6例,我们期待大型随机对照研究进一步论证中药对irAEs 的降低作用,特别是扶正抗癌方在降低irAEs 方面的疗效。
