慢性心力衰竭患者并发高尿酸血症的影响因素分析及模型构建
2024-05-16王云香许孟周玲
王云香,许孟,周玲
(南阳市中心医院 a.神经内科;b.CT影像科;c.CT影像诊断科,河南 南阳 473000)
慢性心力衰竭(chronic heart failure,CHF)是多种心脏病进展至终末期的表现,CHF常合并高尿酸血症,高血尿酸可参与CHF发展进程,也是预后不良的体现,而CHF患者黄嘌呤氧化酶合成过多,可增加活性氧生成,促使心肌细胞尿酸合成分泌增多[1-2]。尿酸是嘌呤代谢最终产物,高血尿酸可刺激炎症介质生成,引起血管心肌重构,正常进食后消化系统可生成嘌呤代谢产物,大部分嘌呤代谢产物可经肾排出体外,少部分可经肠道排出,若肾代谢不足可促使血清尿酸升高,引发高尿酸血症,而高尿酸血症与心血管疾病等发生密切相关[3]。本研究旨在分析CHF患者并发高尿酸血症的影响因素,并建立logistic回归模型,以更好识别高危患者,积极干预危险因素,控制尿酸水平,改善患者预后。
1 资料与方法
1.1 一般资料
经医院医学伦理委员会审核批准,回顾性选取2021年6月至2023年6月南阳市中心医院收治的100例CHF患者为研究对象,依据其是否并发高尿酸血症分为合并组(42例)、未合并组(58例),两组一般资料比较见表1。纳入标准:符合CHF诊断标准[4];合并组符合高尿酸血症诊断标准[5];既往无心脏手术史;临床资料完整。排除标准:合并急性心力衰竭、肺水肿、心源性休克等;合并严重感染;有痛风史;处于痛风急性发作期;伴有内分泌系统等严重原发性疾病;合并肺源性心脏病;伴有甲状腺功能亢进症、恶性肿瘤等;合并主动脉夹层、急性脑血管病等;伴有弥散性血管内凝血;入院前3个月内有活动性出血、外伤等。
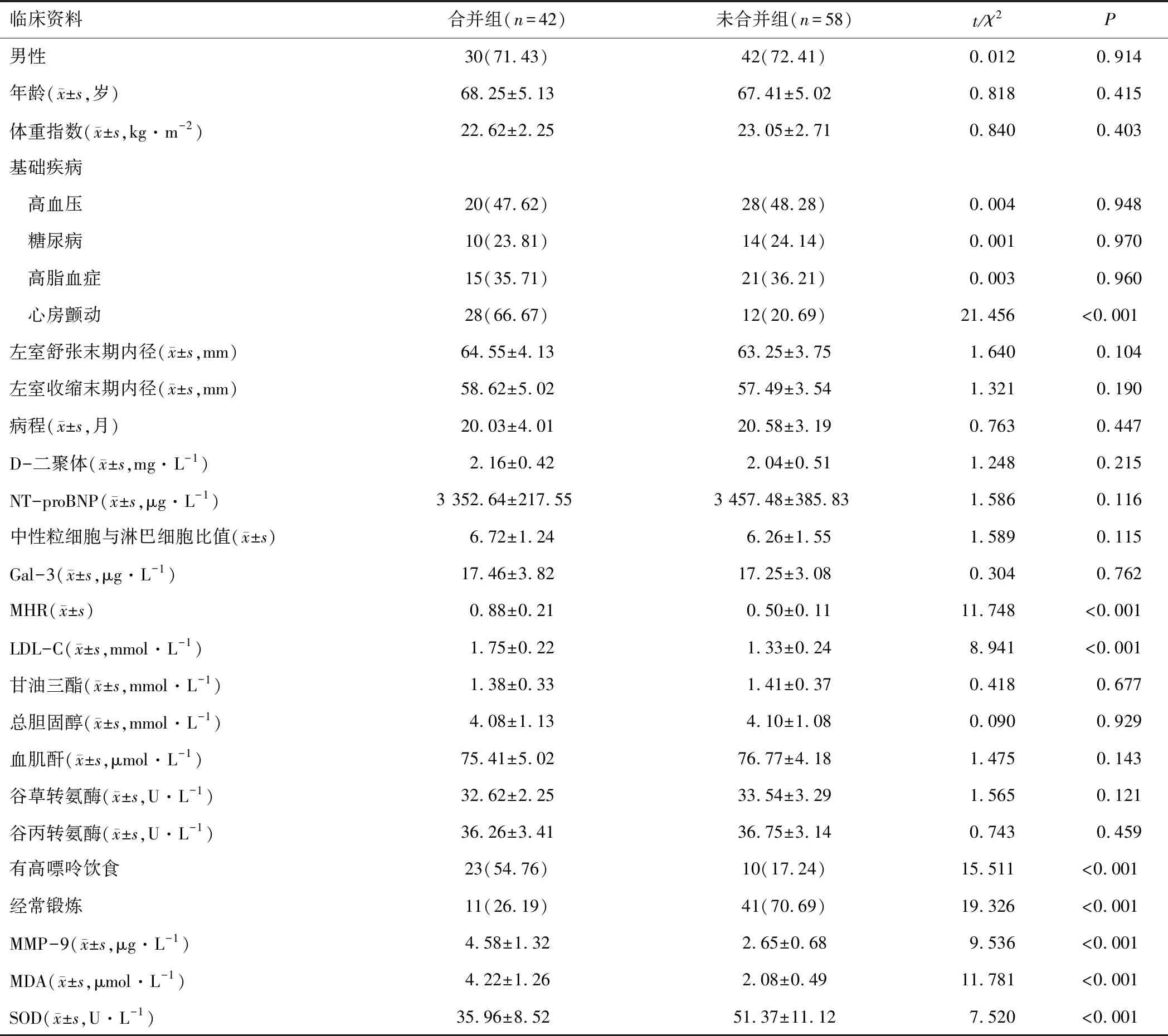
表1 两组临床资料比较
1.2 研究方法
利用知网、万方等方式查找“CHF”“高尿酸血症”相关影响因素,结合本病实际情况筛选可能与高尿酸血症发生相关因素。统一培训6名医务人员成立资料调查小组,通过调查问卷和医院病历调取等形式收集临床资料,包括性别、年龄、体重指数、基础疾病、心功能分级、房颤、左室射血分数、左室舒张末期内径、左室收缩末期内径、病程、高嘌呤饮食、经常锻炼(每周锻炼次数≥3次)、患者入院时血清学指标[血清低密度脂蛋白胆固醇(low-density lipoprotein cholesterol,LDL-C)、甘油三酯、总胆固醇、血肌酐、谷草转氨酶、谷丙转氨酶、D-二聚体、氨基末端脑钠肽前体(N-temrina pro-barin natriuretic peptide,NT-proBNP)、中性粒细胞与淋巴细胞比值、血清半乳糖凝集素3(galectin 3,Gal-3)、单核细胞/高密度脂蛋白胆固醇比值(monocyte-to-high density lipoprotein cholesterol ratio,MHR)、基质金属蛋白酶-9(matrix metalloproteinase-9,MMP-9)、丙二醛(malondialdehyde,MDA)、超氧化物歧化酶(superoxide dismutase,SOD)水平]。
1.3 质量控制
调查人员可准确讲解调查问卷中相关问题,且不可有诱导或影响调查对象填写问卷的语言或行为,以此保证数据真实有效,采用双人录入核对方式输入调查数据,实验室检查结果由数据管理员从检验系统导出,核对原始资料准确性和完整性。
1.4 统计学分析
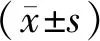
2 结果
2.1 临床资料
合并组心房颤动占比、高嘌呤饮食占比、MHR高于未合并组,LDL-C、MMP-9、MDA水平高于未合并组,经常锻炼占比、SOD低于未合并组(P<0.05),见表1。
2.2 多因素logistic回归分析高尿酸血症发生的影响因素
以是否发生高尿酸血症为因变量(未发生=0、发生=1),以心房颤动、高嘌呤饮食、MHR、LDL-C、MMP-9、MDA、经常锻炼、SOD为自变量(MHR、LDL-C、MMP-9、MDA、SOD均为实测值;无心房颤动赋值为0,有赋值为1;无高嘌呤饮食赋值0,有赋值为1;无经常锻炼赋值为0,有赋值为1),多因素logistic回归分析显示心房颤动、高嘌呤饮食、MHR、LDL-C、MMP-9、MDA为高尿酸血症发生的独立危险因素,SOD、经常锻炼为高尿酸血症发生的独立保护因素(P<0.05),见表2。
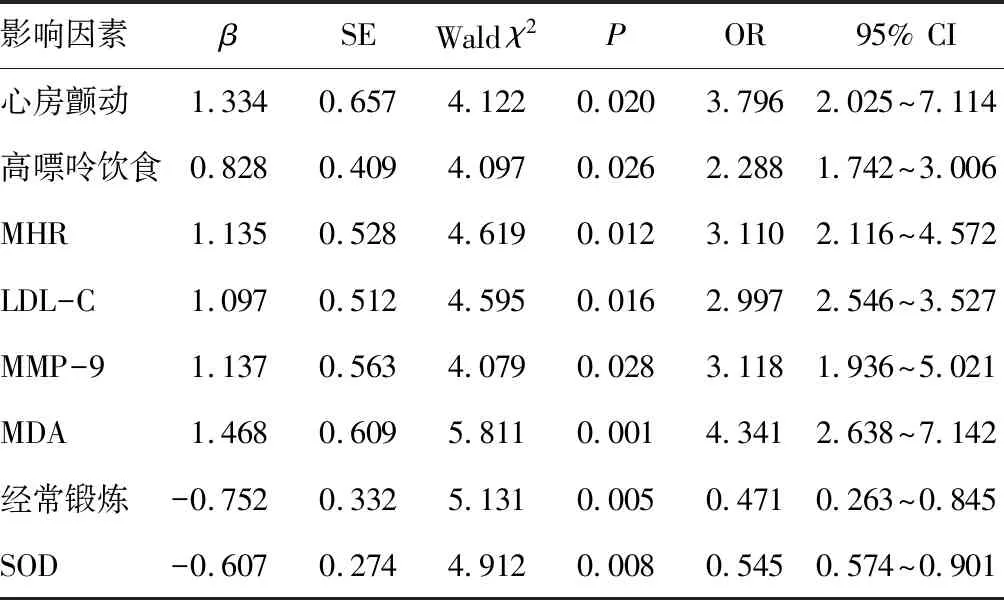
表2 多因素logistic回归分析高尿酸血症发生的影响因素
2.3 logistic回归模型建立
以心房颤动、高嘌呤饮食、经常锻炼、MHR、LDL-C纳入模型1,以心房颤动、高嘌呤饮食、MHR、LDL-C、MMP-9、MDA、SOD、经常锻炼纳入模型2。
2.4 logistic回归模型验证
模型1诊断并发高尿酸血症的AUC为0.793(95% CI:0.635~0.825),敏感度、特异度分别为76.19%、72.41%;模型2诊断并发高尿酸血症的AUC为0.908(95% CI:0.802~0.926),敏感度、特异度分别为90.48%、81.03%,且模型2对并发高尿酸血症的诊断效能较好,见表3。Hosmer-Lemeshow检验结果显示χ2=7.446,P=0.077,表明模型2与观测值拟合度良好。当高风险阈值为0.02~0.73时模型2净获益率具有临床价值。

表3 NRI与IDI分析
3 讨论
CHF患者炎症反应、氧化应激反应持续进展可增强磷酸核糖焦磷酸合成酶活性,促使血尿酸水平升高,引起体内循环瘀血,造成肾循环障碍,进一步促进高尿酸血症发生。本研究100例CHF患者中42例发生高尿酸血症(42.00%),这与既往研究[6]相似,提示临床需早期筛选高尿酸血症高危患者,并采取积极干预措施,以降低高尿酸血症发生风险。
本研究结果显示,心房颤动、高嘌呤饮食、MHR、LDL-C、MMP-9、MDA为高尿酸血症发生的独立危险因素,SOD、经常锻炼为高尿酸血症发生的独立保护因素。尿酸水平升高可损伤内皮细胞,促进血栓形成,引起心室重构、心房纤维化[7]。张宇等[8]研究表明高尿酸血症为心力衰竭患者发生心房颤动的危险因素。本研究发现合并组心房颤动占比高于未合并组,提示心房颤动与高尿酸血症发生密切相关。分析其原因可能为心房颤动发生后心室结构重构加重,影响嘌呤氧化代谢,促进尿酸水平升高,进而诱发高尿酸血症。因而临床需重视心功能分级较高、心房颤动患者,采取个体化措施以保护心功能,预防心房颤动发生。伍成凯等[9]研究表明高嘌呤饮食为高尿酸血症发生的独立危险因素。本研究发现合并组高嘌呤饮食占比高于未合并组,这与上述研究报道类似,提示临床应嘱CHF患者减少高嘌呤饮食,合理制定饮食标准,以降低高尿酸血症发生风险。原因可能为高嘌呤饮食可促进肾脏尿酸重吸收,抑制肾脏尿酸排泄,尿酸生成增多而排泄不足,导致高尿酸血症发生风险升高。本研究结果显示,合并组经常锻炼占比低于未合并组,且经常锻炼为高尿酸血症的保护因素,与既往研究结果[10]一致。原因可能为经常锻炼可改善血脂代谢、肾脏排泄能力,促进血尿酸排出体外,以降低血尿酸水平。临床应指导患者适量运动,养成良好生活方式,通过健康教育等方式向患者讲解高尿酸血症相关知识,以预防高尿酸血症发生。
炎症反应与中性粒细胞、淋巴细胞数量异常有关,可参与CHF发生过程,其中MHR水平升高可加重氧化应激-炎症反应,且与心血管疾病及不良预后有关;LDL-C水平升高可引起血管内皮细胞损伤,提高黏附分子、促炎因子表达水平,参与动脉粥样硬化发生过程[11-12]。本研究结果显示,合并组MHR、LDL-C高于未合并组,提示CHF患者外周血MHR、LDL-C可能参与高尿酸血症发生过程。推测其原因可能为MHR、LDL-C升高可加重血管内皮损伤,促使嘌呤合成、脂肪酸合成增加,引起肾血流量降低,减弱肾脏排泄尿酸能力,进而诱发高尿酸血症。因而临床需密切监测MHR、LDL-C水平,并给予降脂、保护肾功能等相关治疗,以减少高尿酸血症发生。MMP-9水平升高可加快细胞外基质降解,加重组织炎症损伤,参与痛风发生过程[13-14]。本研究中合并组MMP-9水平高于未合并组,提示MMP-9水平升高可能参与高尿酸血症发生过程。原因可能为MMP-9水平升高可提高尿酸代谢相关细胞因子水平,放大炎症级联反应,提高血尿酸水平。尿酸水平升高可诱导自由基生成,加重血管平滑肌损伤,其中MDA水平升高可增强氧化应激反应,加重关节损伤;SOD可清除氧自由基,阻断脂质过氧化反应[15-16]。本研究结果显示,合并组MDA水平高于未合并组,SOD水平低于未合并组。这可能是因为MDA、SOD水平异常可引起氧化-抗氧化失衡,促使黄嘌呤氧化酶生成量增加,引起尿酸生成量过多,促使高尿酸血症发生。因此,临床需加强对CHF患者血清MMP-9、MDA、SOD水平变化的监测,并给予抗炎、抗氧化等相关治疗。同时本研究将心房颤动、高嘌呤饮食、经常锻炼、MHR、LDL-C纳入模型1,将心房颤动、高嘌呤饮食、MHR、LDL-C、MMP-9、MDA、SOD、经常锻炼纳入模型2,模型2诊断并发高尿酸血症的AUC大于模型1,且具有良好拟合度,当高风险阈值为0.02~0.73时模型2净获益率具有临床价值。
4 小结
心房颤动、高嘌呤饮食、MHR、LDL-C、MMP-9、MDA为高尿酸血症发生的独立危险因素,SOD、经常锻炼为高尿酸血症发生的独立保护因素,基于上述影响因素建立logistic回归模型,该模型对CHF并发高尿酸血症具有良好区分度、拟合度及临床实用价值,临床可依据上述模型筛选高危患者,并开展针对性预防措施,以期降低高尿酸血症发生风险。但本研究样本量未能满足回归分析需求,可能会影响结果可靠性,仍需扩大样本量进一步验证。
