D-二聚体与纤维蛋白原比值在慢性阻塞性肺疾病急性加重期患者中的表达及临床意义
2024-05-11武晓敏李雷花
武晓敏,李雷花
(濮阳市人民医院 检验科,河南 濮阳 457100)
慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)为呼吸系统多发病,是导致慢性呼吸衰竭和慢性肺源性心脏病的最常见病因,患者肺功能呈进行性减退,严重影响其劳动能力及生活质量[1]。COPD患者经规律治疗,咳嗽、咳痰或喘息等症状控制良好时处于稳定期,一旦症状突然急性加重,每次急性发作都可能导致肺功能恶化,甚至引起严重肺部感染、呼吸衰竭等并发症,病死率较高[2-3]。既往研究表明,COPD急性加重期的发生与其血液高凝状态密切相关[4]。D-二聚体(D-dimer,D-D)和纤维蛋白原(fibrinogen,Fib)均为常规凝血检测项目,D-D与Fib比值(D dimer to fibrinogen ratio,DFR)是临床诊断血液凝结成栓活性的常用指标,具有较高灵敏度[5]。目前,DFR与COPD急性加重期生存情况的相关研究并不多见,本研究通过分析DFR在COPD急性加重期患者中的表达水平,观察其临床检测价值,具体报道如下。
1 资料与方法
1.1 一般资料
前瞻性纳入2021年2月至2023年2月医院收治的COPD急性加重期患者。本研究由医院医学伦理委员会审核批准。(1)纳入标准:符合第9版《内科学》[6]中COPD急性加重期相关诊断标准;接受无创呼吸机、高流量氧疗及糖皮质激素治疗;签署研究知情同意书。(2)排除标准:合并肺结核、肺脓肿等其他呼吸系统疾病;妊娠或哺乳期妇女;合并血液系统疾病或存在凝血功能障碍;近期接受过外科手术治疗;合并肝、肾、心等严重器质性病变;近期接受或抗凝或抗血小板治疗;合并恶性肿瘤;合并自身免疫性疾病。
1.2 方法
(1)DFR:于患者入院当日采集空腹静脉血2 mL,置入1∶4枸橼酸钠管中,颠倒混匀,以3 000 r·min-1离心处理10 min,采用全自动凝血分析仪(SYSMEX,型号CS-5100)根据免疫比浊法检测D-D、Fib,计算DFR。试剂盒购自希森美康医用电子(上海)有限公司。(2)分组:收集患者入院基线资料,观察患者28 d生存情况,将患者分为生存组和病死组。
1.3 统计学处理

2 结果
2.1 生存情况
研究最终纳入102例COPD急性加重期患者,其中18例28 d内病死,占比17.65%,纳入病死组,其余84例患者纳入生存组。两组患者性别、年龄、病程、吸烟、合并呼吸衰竭、合并糖尿病、合并高血压等比较,差异无统计学意义(P>0.05)。病死组患者第1秒用力呼吸容积(forced expiratory volume 1,FEV1)、第1秒用力呼吸容积占预计值百分比(FEV1%pred)、第1秒用力呼吸容积占用力肺活量之比值(forced expiratory volume in one second to forced vital capacity,FEV1/FVC)均低于生存组,差异有统计学意义(P<0.05)。见表1、2。
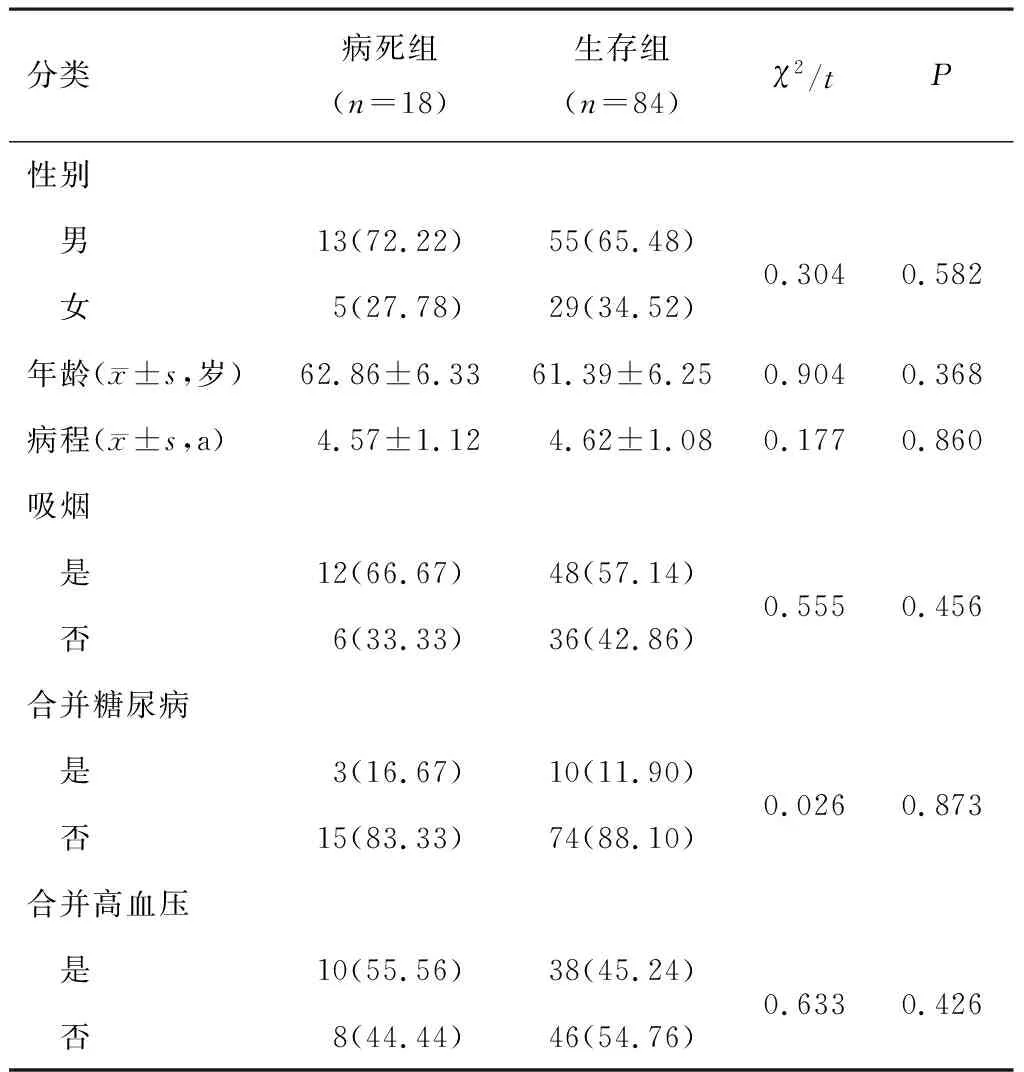
表1 两组患者基线资料比较
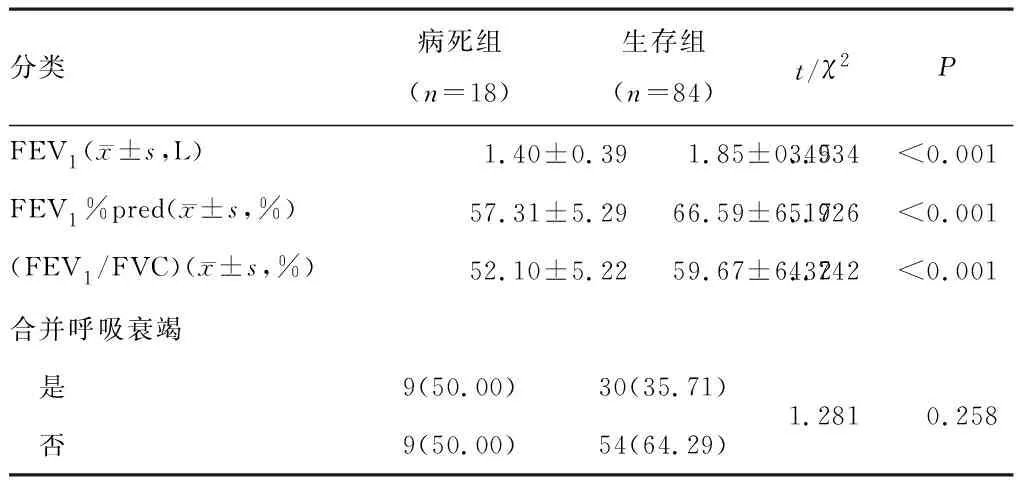
表2 两组患者病情资料比较
2.2 DFR
病死组患者D-D、Fib、DFR均高于生存组,差异有统计学意义(P<0.05)。见表3。
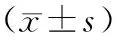
表3 两组患者DFR比较
2.3 DFR与COPD急性加重期患者生存情况的关系
经点二列相关性分析,DFR与COPD急性加重期患者病死呈正相关关系(r=0.431,P<0.001)。
2.4 DFR对COPD急性加重期患者生存情况的预测价值
ROC曲线分析显示,DFR对COPD急性加重期患者病死有一定预测价值,AUC为0.795,95% CI 为0.676~0.914,截断值为0.104,敏感度为0.722,特异度为0.798,约登指数为0.520(P<0.001)。
3 讨论
COPD属于不完全可逆的气流受限性肺疾病,患病率较高,无法治愈,容易反复发作[7]。COPD的发病与炎症机制有关,气道、肺实质和肺血管的慢性炎症是COPD的特征性改变,中性粒细胞、巨噬细胞、T淋巴细胞等炎症细胞参与了COPD的发病过程。全身炎症反应影响了凝血功能,通过活化凝血级联反应、抑制纤溶系统活性,使凝血过程向促凝方向转化,继而促进微血栓形成[8]。这两个因素是导致COPD患者病情加重的主要诱因。COPD急性加重期危害较大,如进展为Ⅱ型呼吸衰竭,可能引起人体多器官缺氧,使患者陷入昏迷,甚至诱发心脏呼吸骤停。本研究结果显示,102例COPD急性加重期患者中,有18例28 d内病死,占比17.65%,说明COPD急性加重期病死率较高,这与朱勤等[9]临床报道的结果相近。
D-D和Fib均为凝血功能检查的常用实验室指标,能反映机体微血栓形成情况。Fib由肝细胞合成分泌,在血浆中含量较高,其浓度可反映血液黏稠度。同时Fib还是一种急性时相反应蛋白,与血栓形成、炎症、感染等均有密切联系,在血栓形成过程中,血浆中Fib通过介导红细胞桥联、诱导血小板聚集,促使血液维持高凝状态[10]。D-D是纤溶系统中交联纤维蛋白的降解产物,在正常人群血浆中水平较低,可反映继发性纤溶亢进,在有形成血栓倾向疾病中,D-D可促进纤维蛋白溶解、激活凝血系统,在血浆中呈高表达[11]。但D-D易受到年龄、妊娠、组织坏死、严重感染的影响,因此D-D升高还常见于老年人、孕妇、外科手术、恶性肿瘤患者,其特异性较差[12]。因此,用D-D与Fib的比值DFR相较单独D-D、Fib在反映与凝血功能异常相关疾病患者病情则更为灵敏和准确。
本研究比较病死和生存患者的D-D、Fib、DFR发现,病死组D-D、Fib、DFR均高于生存组,表明病死组患者存在严重的高凝血栓状态。随着COPD病情进展,肺组织弹性日益减退,肺泡持续膨胀,肺泡周围大量毛细血管受挤压而退化,肺泡通气不良,持续气流受限,引起通气功能障碍,同时肺泡和毛细血管大量丧失,弥散面积减少,导致换气障碍。通气和换气障碍引起缺氧和二氧化碳潴留,患者体内氧气不足,对患者肾代谢功能造成一定影响,导致D-D、Fib等凝血因子清除减少,抗凝减弱[13]。患者体内氧气不足,缺氧细胞制造、分泌前列腺素等炎症介质,激活血液中多种炎症因子,刺激血管内皮细胞,直接损伤微血管,引起血小板黏附、聚集于内皮下胶原组织,激活凝血反应链,降低肝素抗凝活性,导致应激性上调,继发纤溶亢进[14]。凝血功能激活越明显,越多Fib被凝血酶转变为纤维蛋白,纤溶酶活性增强生成D-D,DFR越高[15]。
肺功能与COPD患者生存情况密切相关,肺功能检查是诊断COPD急性加重期的金标准,其中FEV1、FEV1%pred、FEV1/FVC是检测常用指标。本研究结果显示,病死组患者FEV1、FEV1%pred、FEV1/FVC均低于生存组。点二列相关性分析显示DFR与COPD急性加重期患者病死呈正相关关系,ROC曲线分析显示,DFR对COPD急性加重期患者病死有一定预测价值,说明DFR可成为临床预测COPD急性加重期患者病死的参考指标。DFR升高提示纤溶/凝血过程失衡,血液高凝状态逐渐加重,血流受阻导致输送氧气的效率下降,导致肺部血管的持续收缩、痉挛,加重肺部负担,导致肺功能逐渐减退,减弱小气道通气能力,增加无效通气,影响气体交换,加剧机体缺氧状态。而缺氧又会造成体内的红细胞生成素增多,引起红细胞聚集,使血红蛋白量逐渐增加,形成血液高凝状态,两者形成恶性循环,均参与COPD病情进展过程。此外,DFR升高时,机体炎症反应加重,导致肺部组织损伤,进一步恶化肺功能[16]。
4 结论
COPD急性加重期病死患者DFR呈高表达,可作为COPD急性加重期患者生存情况的预测指标。
