EDTA滴定差减法测水泥中氧化镁含量影响因素的探讨
2024-05-08龙梅
龙梅
(毕节市市场监督管理局检验检测中心,贵州 毕节 551700)
水泥的烧制温度通常在1 400 ℃左右,都是过烧而成的,结构致密,水化很慢;水泥硬化后才吸收孔隙中水分反应:CaO+H2O=Ca(OH)2,MgO+H2O=Mg(OH)2,体积膨胀97%以上,从而引起不均匀体积膨胀,使水泥石开裂;过高的氧化镁会使水泥热量放出超出标准,进而影响混凝土的热工性质。在国家标准中有相关技术要求,硅酸盐水泥和普通硅酸盐水泥中氧化镁含量≤5.0%;对于另外四种通用水泥氧化镁含量≤6.0%[1]。当水泥中氧化镁含量偏高时会引起安定性不合格,会导致水泥制品或混凝土构件产生膨胀性裂缝现象,建筑物质量降低,可能引起倒塌、断层等严重事故,因此严格控制水泥中氧化镁的含量有非常重要的意义。
目前,测定水泥中氧化镁含量使用较多的方法有两种:一种是原子吸收光谱法,另一种是EDTA滴定差减法,前者是将样品中的元素原子化后直接测定氧化镁含量,结果不受氧化钙测定等元素的影响,具有快速、简便等优点,但由于原子吸收光谱仪价格昂贵、维护费用高、成本高,大部分实验室还是选择使用EDTA滴定差减法,该法测定氧化镁含量是一种间接测定,检测成本低、可控性强,也不会因检测设备不准而影响结果值,滴定差减法步骤繁琐往往会因操作规范程度、试剂用量等因素引起氧化镁含量结果偏差,因此需对引起结果偏差的因素进行控制和预防,以期提高实验数据的准确性。
1 实验器具和试剂
1.1 器具
万分之一天平(SQP)、高温炉、容量瓶、滴定管器、磁力搅拌器、实验室pH计,所用器具应检定合格并在检定有效期内。
1.2 试剂
EDTA标准滴定溶液(0.015 mol/L)、CMP混合指示剂(国家水泥质量监督检测中心提供)、KB混合指示剂(国家水泥监督检测中心提供)、氢氧化钠(分析纯)、盐酸(分析纯)、硝酸(分析纯)、酒石酸钾钠溶液(100 g/L)、三乙醇胺溶液(1+2)、氟化钾溶液(20 g/L)、氢氧化钾溶液(200 g/L)、pH值10缓冲溶液。
2 实验过程及影响因素控制
2.1 取样控制
选取的样品应该具有代表性和有效性:如样品不具有代表性实验结果就不能说明该批产品的质量;样品吸水受潮结块会影响称样量的实际值,而导致检测结果误差,检测就没有实际意义。因此取样时应使用干燥清洁的器具在同一批次的水泥样中20个以上不同的部位取出12 kg的样品,并将水泥样品全部用0.9 mm方孔筛筛析,为保证样品的均匀有效性,取其过0.9 mm 方孔筛筛下物充分混合,同时避免与外界环境接触,预防混入杂质和物块,再将混合均匀的试验样缩分于洁净干燥的聚乙烯塑料密封瓶中,于阴凉、干燥处保存,备用,防止吸水受潮的影响。
2.2 称样控制
称取约0.5 g试样、精确0.100 0 g、置于银坩埚中:称样时将样品搅拌均匀,正确使用天平,注意避免外界干扰,能精确读数。
2.3 氢氧化钠质量控制
加入6~7 g氢氧化钠:作为溶剂的氢氧化钠,必须是干燥的,如果吸附了水分,熔融时会发生飞溅现象,导致样品损失。
2.4 坩埚盖留缝隙控制
盖上坩埚盖(留有缝隙): 因为留有一定缝隙可以让坩埚更加均匀地受热,减轻坩埚受热而变形或破裂的风险;另一方面留有一定的缝隙坩埚与熔样接触面越大,相应的热量就能够更快地传递,坩埚的温度也会更加均匀,从而减小对实验数据的误差,提高实验数据的准确性。
2.5 熔融时间、温度控制
从低温升起:灼烧时高温炉温度应从低温升起,以防止水泥中挥发性物质(如碱、氯化物、硫化物等等)因急剧受热,猛烈排出而使水泥样飞溅,造成结果偏低。在650~700 ℃的高温下熔融20 min,期间取出充分摇动1次:温度偏低时间太短都不能使样品彻底熔融;Mg的熔点是651 ℃,温度过高时间过长可能导致镁挥发,含量损失导致结果偏低;熔融过程容易出现结块,充分摇动这样可以提高熔融效果,使熔块更容易脱埚,但摇动的力度不宜过猛,以免熔液晃出,可以多次轻摇。
2.6 坩埚洗涤及溶液定容控制
将坩埚放入约有100 mL沸水的 300 mL烧杯中,盖表面皿,适当加热,待熔块完全浸出[2]。取出坩埚,用水冲洗坩埚和盖,在搅拌下加入25~30 mL盐酸[2]:坩埚放入沸水时会使溶液发生强烈跳动,盖表面皿防止溶液溅出;熔块完全浸出后,在搅拌下立即一次加入盐酸,加入盐酸时会产生大量气泡,气泡漫出导致溶液减少,一次性加入盐酸气泡很快消失,可防止溶液被气泡带出,同时防止强碱溶液对玻璃器具的腐蚀,带入硅酸到溶液中,导致结果偏低,必须尽快酸化;pH值≥13时,Mg2+与OH-反应生成Mg(OH)2沉淀,也必须尽快酸化。
2.7 EDTA标准滴定溶液浓度的控制
确保EDTA标准滴定溶液的浓度值是有效、可靠的。首先配制的标准溶液在使用前必须进行标定,按一人标定一人复标各四平行的方法取平均结果,同时标准溶液测定的绝对误差要求小于0.1%[3],浓度值应在标准要求值的±5%范围以内,标准溶液浓度值保留4位有效数字。
2.8 根据EDTA滴定氧化镁差减法原理
在pH值10的溶液中,以酒石酸钾钠、三乙醇胺为掩蔽剂,用酸性铬蓝K-萘酚绿B混合指示剂,用EDTA标准滴定溶液滴定[2]。EDTA配位滴定法测Mg2+的主要反应:
滴定前(pH值=10):(Ca2+)Mg2++ K-B=Ca2+(Mg2+)-K-B暗红色
化学计量点时:Ca2+(Mg2+)-K-B+Y4=(Ca2+)MgY2-+K-B暗红色 → 纯蓝色
当试样中一氧化锰含量>0.5%时,在盐酸羟胺存在下,测定钙、镁、锰总量,差减法测得氧化镁的含量[4];当试样中一氧化锰含量<0.5%时,测定钙、镁总量,差减法测得氧化镁的含量[4],即氧化钙含量检测直接影响氧化镁的结果。从实验原理可知影响氧化镁结果的关键因素还有以下5种,并对其做出相对应控制措施。
2.8.1 氧化钙的控制
根据EDTA滴定法(代用法)测氧化钙的原理即显色反应:在pH值>13时,CMP+Ca2+→Ca-CMP(绿色荧光);滴定终点:EDTA,H2YCa-CMP—CaY2-+2H+CMP(绿色荧光)→(红色)。滴定条件下,加入KOH溶液的量不够,会出现“返色现象”;镁生成了氢氧化镁沉淀,沉淀中夹杂着钙离子,当滴定速度过快时,溶液中局部很快发生颜色变化(绿色荧光消失变成红色)提前到达终点,此时被沉淀夹杂的钙离子又和CMP指示剂配位,生成绿色荧光配合物,也会出现“返色现象”,其实是没有达到滴定终点,因此试验过程中必须先确保KOH溶液的加入量,调控好pH值>13的滴定条件下进行滴定。滴定过快还会造成反应不充分,过慢空气中的CO2溶入,生成CaCO3,都会导致检测氧化钙结果偏低。因此滴定过程中要保持滴定速度(5~6 mL/min)近终点时要缓慢滴定,加强搅拌,另外不要在阳光直射下滴定,以免影响终点颜色判定。控制好氧化钙滴定的速度、调整好pH值、按要求规范操作等影响因素即测得氧化钙的值更准确。
氧化钙在pH值>13条件下滴定,标准要求是KOH的量加到有绿色荧光出现再过量5~8 mL,绿色荧光在溶液中不是很明显不好控制,这样有可能导致KOH溶液的加入量不足,造成试验误差过大。滴定过程为了能准确地加入KOH溶液的量更好地调整pH值以及保证溶液充分反应、更方便试验和更精准得到实验结果,做了一些方法改进并进行方法比较。将实验室pH计和磁力搅拌器加入实验中,在充分搅拌下直接将KOH的量加至pH值>13为止,可以很直观地知道pH值,避免KOH加入量不足。在加KOH溶液的过程中总结出颜色与pH值的对应关系,并用1#、2#两个水泥样(各5组)与GB/T 176—2017方法进行试验对比,结果见表1。
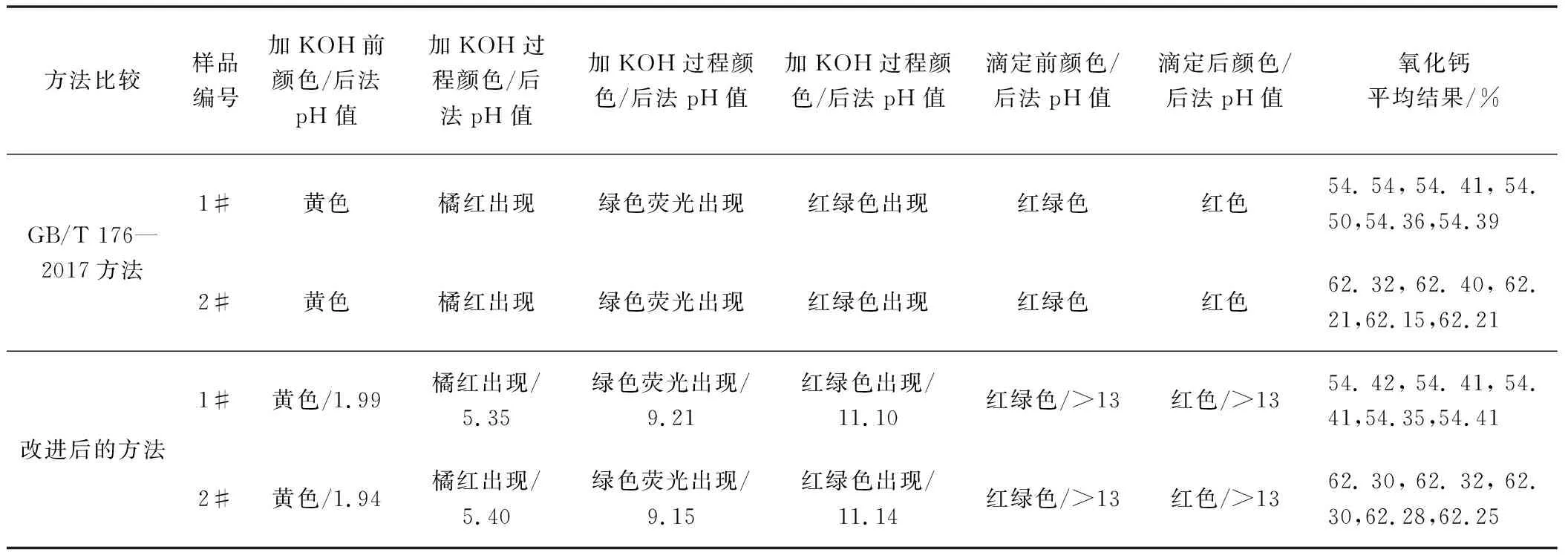
表1 GB/T 176—2017规定方法与加pH计和磁力搅拌器改进方法进行对比试验
表1结果表明:方法比较结果值都符合允许误差要求(同一实验室绝对误差不得大于±0.2%),改进后方法的重复性更好。
实验过程中磁力搅拌器可以很方便地边加试剂边搅拌均匀,确保溶液充分反应,颜色变化时pH计可以随时读数,也便于总结加KOH溶液过程中颜色变化的经验,更准确地加入KOH溶液的量更好地调整pH值,改进方法更具有可操作性。
2.8.2 显色控制
依据实验原理滴定过程影响氧化镁检测结果的主要因素还有显色观察。滴定过程的变色点、反应点、滴定终点都会使颜色发生突变而且与pH值息息相关。当加入KB混合指示剂,溶液变成暗红色,滴定时溶液要经历从暗红色变成紫色再变成蓝色这一过程[5],pH值和KB指示剂加入量直接影响颜色显示,从而影响终点读数是否正确,导致结果产生偏差,所以指示剂的加入量一定要控制好。GB/T 176—2017中滴定样加入“适量”混合指示剂,“适量”可控性差,为了更准确地加入混合指示剂量,将取酸性铬蓝K:萘酚绿B(同一比例)7个不同量的KB混合指示剂用1#水泥样进行试验,EDTA滴定量及得到结果如表2。

表2 KB混合指示不同量的比较试验
表2得出:0.10~0.12 g KB混合指示剂加入量终点颜色突变明显也符合理论变色(纯蓝色),是适合水泥样检测氧化镁KB混合指示剂用量,用量太少颜色太浅,颜色变化不明显,导致滴定过量,结果偏高;用量太大颜色太深,很难区分颜色变化,导致提前判定滴定终点,结果偏小。说明:1#水泥样一氧化锰含量<0.5%,表2中氧化镁的计算是代入了表1中方法改进后1#样氧化钙滴定的平均值。
2.8.3 pH值控制
在氧化镁滴定过程中,滴定前(pH值10)而不能使pH值大于10,当pH值大于10的时候,溶液中会有一部分Mg2+与OH-反应生成Mg(OH)2沉淀,从而使钙镁总量的测定结果偏低,因此pH值10的NH3-NH4C1缓冲溶液配制后一定用pH计或精密pH值试纸检验。加入酒石酸钾钠、三乙醇胺为掩蔽剂又必须在酸性溶液中,这样效果更好,所以要控制好pH值以及按规范顺序加入试剂。
2.8.4 终点读数控制
溶液从暗红色变成紫色再变成纯蓝色这一过程,应以白色为底,从上往下观察颜色,不要把紫色变成蓝色的那一瞬间判断为滴定终点,此时再加一滴EDTA,会发现溶液颜色比之前的蓝色亮了一些,这种亮蓝色才是真正要滴到的蓝色,滴定应持续到溶液蓝色的亮度不再发生变化为止。
2.8.5 空白控制
为了实验数据更准确,能清楚地观察滴定终点颜色(纯蓝色),至少做2组空白,并先滴定空白再与样品进行滴定前和滴定终点颜色对比。试剂的纯度不够、蒸馏水中含的杂质,都会引起检测结果的偏高或偏低,要求试剂和蒸馏水必须符合实验要求,减少空白误差,最终用被测样品的检验结果减去空白里含有的少量MgO的值,即可得到比较准确的检测结果。
3 结论
氧化镁、氧化钙检测滴定的整个过程必须在调控好pH值以及充分搅拌的条件下加试剂和滴定,这样有利于充分反应完全,控制KOH的加入量,所以在GB/T 176—2017规定的试验过程中加入磁力搅拌器、实验室pH计更利于检测工作;指示剂用量要适量,这样有利于终点颜色的判断,0.10~0.12 g KB混合指示剂加入量适合水泥样检测氧化镁用量,能准确测定氧化镁。根据实验原理从整个实验过程总结出,EDTA滴定差减法测水泥中氧化镁含量的影响因素共有样品的熔融处理、标准溶液要求、CaO的检测结果、混合指示剂加入量、试液pH值的调整、滴定终点的观察等13种。对照13种因素采取不同措施加以预防控制,按照标准规范操作,尽可能消除试验误差,也能保证氧化镁含量检测结果的准确性。
以上是EDTA滴定差减法测水泥中氧化镁含量整个试验过程的分析及控制要点的阐述,通过长期对水泥中氧化镁的检测,找到检测常见影响因素并给出解决建议,希望对水泥检验检测工作有所帮助。
