冠心病合并2 型糖尿病患者的血糖管理专家共识
2024-05-07中国医疗保健国际交流促进会心血管病学分会
中国医疗保健国际交流促进会心血管病学分会
我国冠心病合并糖尿病患者的比例较高,即使接受降压、降脂、抗栓等常规治疗仍存在残余心血管风险。近年的研究证明,一些降糖药物对2 型糖尿病患者具有明确的心血管获益。但调研显示,目前心内科医师对2 型糖尿病筛查时机、指标和诊断标准仍不熟悉,对具有明确心血管获益的新型降糖药物如胰高糖素样肽-1 受体激动剂/钠-葡萄糖共转运蛋白2 抑制剂的认知程度不够、规范应用率低。在此背景下,根据国内外指南/共识和最新的循证医学证据,本共识旨在规范急性冠状动脉综合征、慢性冠状动脉综合征以及经皮冠状动脉介入治疗围术期冠心病患者的血糖管理方案,不涉及糖尿病急性并发症,对冠心病患者中2 型糖尿病的筛查和诊断、心血管风险综合管理等内容总结了要点,明确具有心血管获益的降糖药物的临床应用实践,促进上述药物在心血管及其他相关专业领域规范应用,同时也关注患者的非降糖治疗,以全面降低其心血管风险。
糖尿病是冠心病最重要的危险因素和合并疾病之一。调查显示,我国急性冠状动脉综合征(acute coronary syndrome,ACS)患者中糖尿病合并比例高达45.0%[1],慢性稳定性冠心病患者中糖尿病合并比例为26.8%[2]。对于行经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)的患者,高血糖是全因死亡和心原性死亡的独立危险因素[3]。FOURIER 研究显示,在接受降压、降脂、抗栓等常规治疗的情况下,合并糖尿病的冠心病患者仍有很高的残余心血管风险,其治疗仍有进一步改善的空间[4]。
近年来,新型降糖药物胰高糖素样肽-1 受体激动剂(glucagon-like peptide-1 receptor agonists,GLP-1 RA,如利拉鲁肽、司美格鲁肽和度拉糖肽)和钠-葡萄糖共转运蛋白2 抑制剂(sodium-glucose cotransporter 2 inhibitors,SGLT2i,如恩格列净、达格列净和卡格列净)被证实对2 型糖尿病患者有明确的心血管获益,能进一步降低心血管事件风险。但一项针对我国342 名心内科医师和内分泌科医师的调研显示,目前GLP-1 RA 和SGLT2i 在我国动脉粥样硬化性心血管疾病(atherosclerotic cardiovascular disease,ASCVD)合并2 型糖尿病患者中的应用仍存在使用不足和不规范等诸多问题[5],因此需要规范化的理论指导和管理流程。
为此,中国医疗保健国际交流促进会心血管病学分会组织我国心血管和内分泌领域专家,结合国内外指南或共识以及最新的循证医学证据,制定了《冠心病合并2 型糖尿病患者的血糖管理专家共识》。本共识目标医师为心血管及相关专业医师,目标人群为冠心病患者,包括ACS、慢性冠状动脉综合征(chronic coronary syndrome, CCS)以及PCI 围术期患者,主要涉及冠心病患者中2 型糖尿病的筛查、诊断、管理和长期随访,为冠心病合并2 型糖尿病患者的血糖管理和疾病综合管理提供规范化指导。
1 冠心病患者中2 型糖尿病的筛查和诊断
要点
(1)应对所有冠心病患者进行2 型糖尿病筛查和评估。
(2)糖尿病筛查指标建议首选空腹血糖和糖化血红蛋白(glycated hemoglobin,HbA1c),如二者还不能确诊,则考虑进行口服葡萄糖耐量试验(oral glucose tolerance test,OGTT)。
1.1 筛查时机
无论是否有糖尿病典型症状(烦渴多饮、多尿、多食、不明原因体重下降),都应该对所有冠心病患者(包括ACS 患者入院时、门诊就诊时、PCI 围术期)进行糖尿病筛查,明确血糖水平和2 型糖尿病病史。冠心病患者中2 型糖尿病的发生率显著高于一般人群,若不重视对2 型糖尿病的筛查,很大一部分患者将被漏诊。而在ACS 患者中,无论是否存在2 型糖尿病,住院期间血糖升高都很常见,这与ACS 的应激有一定关系,该类患者预后常常不佳。
1.2 筛查指标
建议在对冠心病患者进行2 型糖尿病筛查时,首选空腹血糖和HbA1c作为检测指标。若空腹血糖和HbA1c异常不能确诊,则进一步行OGTT 以明确诊断[6]。有条件可以进行胰岛功能检测,如血清胰岛素或C 肽测定。
1.3 诊断标准
目前我国糖尿病的诊断采用1999年WHO标准,以静脉血浆葡萄糖为依据,毛细血管血糖值仅作为参考。糖代谢状态分类标准见表1[7]。根据中国2 型糖尿病防治指南(2020 年版),糖尿病的诊断标准为:典型糖尿病症状(烦渴多饮、多尿、多食、不明原因体重下降)合并随机血糖≥11.1 mmol/L;或空腹血糖≥7.0 mmol/L;或OGTT 2 h 血糖≥11.1 mmol/L;或HbA1c≥6.5%;无糖尿病典型症状者,需改日复查确认[7]。
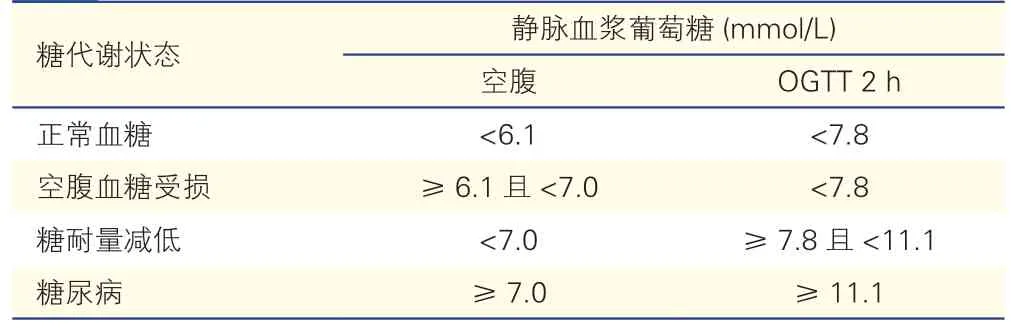
表1 糖代谢状态分类(1999 年WHO 标准)
2 冠心病合并2 型糖尿病患者的心血管综合风险管理
2.1 生活方式调整
要点
生活方式调整是冠心病合并2 型糖尿病患者心血管综合风险管理的基础,建议所有冠心病合并2 型糖尿病患者改善生活方式并长期坚持,包括减重、膳食管理、运动管理和控烟等。
2.1.1 减重
根据我国的评判标准,体重指数(body mass index,BMI)24.0~27.9 kg/m2为超重,≥28.0 kg/m2为肥胖。腹型肥胖的诊断标准为:腰围男性≥90 cm,女性≥85 cm[7]。所有伴超重或肥胖的患者均应考虑减重并长期坚持,将BMI 维持在20.0~<24.0 kg/m2,体重正常者则需避免治疗过程中体重增加。减重的主要方法包括:控制总热量摄入、坚持平衡膳食、适量运动以及作息规律等[8]。
2.1.2 膳食管理
总热量摄入应控制在25~30 kcal/kg 体重。营养应均衡,蛋白质、脂肪、碳水化合物摄入量分别占总热量的15%~20%、<30%、45%~60%。保证丰富的维生素、矿物质和膳食纤维摄入,推荐膳食纤维摄入量为25~30 g/d 或10~14 g/1 000 kcal。钠盐摄入量不高于6 g/d,高血压、心力衰竭患者需更严格控制。
2.1.3 运动管理
建议冠心病合并2 型糖尿病患者进行有氧运动或抗阻运动,运动时间和强度应根据患者情况进行个体化制定[9]。注意事项:(1)运动前应进行医学评估,严格把握适应证和禁忌证,制定个体化运动处方;(2)运动前后监测血糖,以预防低血糖;(3)2 型糖尿病合并肥胖患者,运动时应注意预防关节疼痛和不适。
2.1.4 控烟
建议冠心病合并2 型糖尿病患者不吸烟,且应避免被动吸烟,吸烟者应尽早戒烟。如果无法自行戒烟,建议尽早采用药物戒烟疗法,包括尼古丁替代疗法或安非他酮、伐尼克兰治疗[6]。
2.2 血糖管理目标
要点
(1)对于合并2 型糖尿病的CCS 患者,合理的HbA1c控制目标为<7%,可根据患者的病程进展和病情变化及时调整HbA1c控制目标。
(2)对于合并2 型糖尿病的ACS 或PCI 围术期患者,血糖管理目标需个体化,在降低血糖的同时应避免低血糖。
对于冠心病合并2 型糖尿病患者,血糖管理的总体目标是降低血糖并实现长期达标,降低心血管事件和相关并发症以及死亡风险。HbA1c是反映血糖控制情况最主要的指标,建议大多数冠心病合并2 型糖尿病患者HbA1c的控制目标为<7%,但应遵循个体化原则。在无低血糖风险或其他不良反应的情况下,年龄较轻、病程较短、预期寿命较长的2型糖尿病患者可采取更严格的HbA1c控制目标(如<6.5%)。年龄较大、病程较长、有严重低血糖史、预期寿命较短的患者可采取相对宽松的HbA1c控制目标(可放宽至<8.5%)。在治疗过程中,还需根据患者的病程进展和病情变化及时调整HbA1c控制目标,以维持风险与获益的平衡[7]。
对于合并2 型糖尿病的ACS 或PCI 围术期患者,严格控制血糖策略未能被证实获益,反而增加低血糖风险[10],因此建议采取较为宽松的血糖控制范围。病情越严重,目标应越宽松。如果患者可耐受,建议空腹或餐前血糖控制在7.8~10.0 mmol/L[7]。
2.3 降糖药物对2 型糖尿病患者心血管结局的影响
要点
(1)具有明确心血管获益的降糖药物:部分GLP-1 RA(利拉鲁肽、司美格鲁肽和度拉糖肽)以及部分SGLT2i(恩格列净、达格列净和卡格列净)。
(2)具有潜在心血管获益的降糖药物:二甲双胍和吡格列酮。
(3)心血管安全性良好但心血管获益不明确的降糖药物:二肽基肽酶-4 抑制剂(dipeptidyl peptidase-4 inhibitors,DPP-4i)、磺脲类药物(格列美脲、格列齐特)、甘精胰岛素或德谷胰岛素、α-糖苷酶抑制剂(阿卡波糖)以及其他GLP-1 RA(利司那肽、艾塞那肽)。
(4)未进行心血管安全性评估的降糖药物:其他胰岛素和其他磺脲类药物。
2.3.1 具有明确心血管获益的降糖药物
近年来一系列随机对照临床研究表明,GLP-1 RA(利拉鲁肽、司美格鲁肽和度拉糖肽)以及SGLT2i(恩格列净、达格列净和卡格列净)能显著改善心血管结局,且安全性良好。
GLP-1 RA 可结合GLP-1 受体激活腺苷酸环化酶,触发和放大葡萄糖依赖性胰岛素分泌,抑制胰高糖素分泌,增加肌肉组织对葡萄糖的摄取,减少肝糖原输出,延缓胃排空,从而发挥降糖作用。同时GLP-1 RA 具有多重抗动脉粥样硬化机制,包括降低小而密低密度脂蛋白水平、减轻氧化应激、减少体内巨噬细胞和泡沫细胞、改善内皮功能、抗炎、抗血小板、降低斑块破裂风险[11]。在国内获批的GLP-1 RA 中,利拉鲁肽、司美格鲁肽和度拉糖肽已被证实为有明确心血管获益的降糖药物。LEADER 研究显示,中位随访3.8 年期间,与安慰剂相比,利拉鲁肽可显著降低主要不良心血管事件(首次发生心血管死亡、非致死性心肌梗死或非致死性脑卒中)和心血管死亡风险,降幅分别为13%和22%[12];而且,LEADER 研究亚组分析和事后分析显示,利拉鲁肽的心血管获益独立于患者基线糖尿病病程、BMI、血压水平、血脂水平、病变血管数量、微血管病变数量、他汀类药物治疗、二甲双胍治疗、心功能状态及低血糖发生情况等[12-13]。SUSTAIN-6研究显示,中位随访2.1 年期间,与安慰剂相比,司美格鲁肽可显著降低主要不良心血管事件(首次发生心血管死亡、非致死性心肌梗死或非致死性脑卒中)和非致死性脑卒中风险,降幅分别为26%和39%[14];而且,SUSTAIN-6 研究亚组分析和事后分析显示,司美格鲁肽的心血管获益独立于基线BMI、血压水平、HbA1c、糖尿病病程、微血管病变数量、肾功能、胰岛素应用等[15]。REWIND 研究中近70%的受试者为2 型糖尿病合并ASCVD 高危因素患者,其结果显示,中位随访5.4 年期间,与安慰剂相比,度拉糖肽可显著降低主要不良心血管事件[首次发生非致死性心肌梗死、非致死性脑卒中或心血管死亡(包括未知原因)]风险,降幅为12%[16]。
SGLT2i 主要通过抑制肾脏近端小管对葡萄糖的重吸收,降低肾糖阈、促进葡萄糖从尿液中排泄,从而降低血液循环中葡萄糖水平。涉及恩格列净的EMPA-REG OUTCOME 研究[17]和涉及卡格列净的CANVAS 研究[18]证明,SGLT2i 可显著降低主要不良心血管事件和心力衰竭住院风险。在DECLARETIMI 58 研究中,达格列净组的主要复合终点事件发生率未出现有统计学意义的降低,但心血管死亡或心力衰竭住院事件发生率显著降低,这一获益主要由心力衰竭住院减少驱动[19]。
2.3.2 具有潜在心血管获益的降糖药物
由于二甲双胍上市较早,故未被要求进行心血管结局试验。但UKPDS 研究、多项观察性研究和Meta 分析均显示,二甲双胍治疗与2 型糖尿病患者心血管死亡和全因死亡风险显著下降相关,且降糖效果可靠,安全性和耐受性好,不增加低血糖发生风险[20]。PROactive 研究评估了吡格列酮在2 型糖尿病伴ASCVD 患者中应用的心血管结局效应,结果显示,在4 年研究期间,与安慰剂相比,虽然吡格列酮未能显著降低主要复合终点事件发生风险,但将全因死亡、非致死性心肌梗死或脑卒中风险降低了16%[21]。
2.3.3 心血管安全性良好但心血管获益不明确的降糖药物
涉及DPP-4i[22-24]、磺脲类药物(格列美脲、格列齐特)[24-26]、甘精胰岛素或德谷胰岛素[27-28]、α-糖苷酶抑制剂(阿卡波糖)[29]以及其他GLP-1 RA(利司那肽、艾塞那肽)[30-31]的相关研究表明,这些药物虽然具有良好的心血管安全性,但未能显著改善心血管结局。
2.3.4 未进行心血管安全性评估的降糖药物
对于短效胰岛素以及除格列美脲和格列齐特外的其他磺脲类药物,目前尚未开展专门的心血管安全性评估试验。
2.4 不同类型冠心病合并2 型糖尿病患者的血糖管理
要点
(1)ACS 患者住院期间应检测HbA1c,并密切监测血糖。
(2)ACS 患者如临床状况比较稳定、进食规律且无使用药物的禁忌证,入院后可考虑继续应用既往使用的口服降糖药物或GLP-1 RA,其他情况建议以皮下注射胰岛素为主。
(3)对于CCS 合并2 型糖尿病患者,不论其HbA1c是否达标,若无禁忌证,应启动具有明确心血管获益的GLP-1 RA(利拉鲁肽、司美格鲁肽和度拉糖肽)和(或)SGLT2i(恩格列净、达格列净和卡格列净)治疗。合并心力衰竭的患者应优先考虑SGLT2i,合并超重或肥胖的患者应优先考虑GLP-1 RA。
(4)胰岛素是PCI 围术期控制血糖的首选方案。对于择期手术患者,在时间允许的情况下,可根据患者情况调整其他降糖药物。
(5)对于有特殊情况(如妊娠)或诊断、治疗和管理存在困难的冠心病合并2 型糖尿病患者,应及时启动多学科会诊。
2.4.1 基本原则和路径图
2.4.1.1 ACS 患者
ACS 患者急性期血糖管理的基本原则是控制高血糖,同时避免低血糖。住院期间检测HbA1c并密切监测血糖,以便区分糖尿病和应激性高血糖;如血糖水平>13.9 mmol/L,要注意检测尿糖和尿酮体[7]。
ACS 患者急性期血糖受多种因素的影响,存在巨大的个体差异。在临床实践中,应结合患者具体情况来综合判断和选择治疗方案。如患者临床状况比较稳定、进食规律且无使用药物的禁忌证,入院后可考虑继续应用其入院前已经使用的口服降糖药物或GLP-1 RA,其他情况建议以皮下注射胰岛素为主[32]。
待患者血液动力学和病情稳定后,如已确诊合并2 型糖尿病且无药物禁忌证,应接受生活方式干预以及具有明确心血管获益的GLP-1 RA(利拉鲁肽、司美格鲁肽和度拉糖肽)和(或)SGLT2i(恩格列净、达格列净和卡格列净)治疗,依据血糖水平联用其他降糖药物,定期监测血糖,预防低血糖。如患者仅合并应激性高血糖或既往未诊断2 型糖尿病,建议病情稳定后2 周再次评估血糖和HbA1c,以明确是否存在2 型糖尿病。
ACS 患者血糖管理流程见图1。
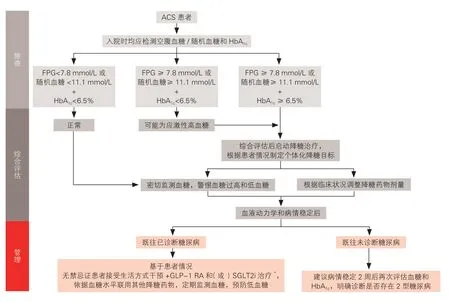
图1 ACS 患者血糖管理流程
2.4.1.2 CCS 患者
建议CCS 合并2 型糖尿病患者,不论其 HbA1c是否达标,若无禁忌证,应启动具有明确心血管获益的GLP-1 RA(利拉鲁肽、司美格鲁肽和度拉糖肽)和(或)SGLT2i(恩格列净、达格列净和卡格列净)治疗。其中,GLP-1 RA 兼具降糖、减重、改善血脂谱和降压的作用。此后如需额外控制血糖,在充分评估药物特异性和患者因素(包括血糖、合并症、体重、低血糖风险、肝肾功能等)后,可个体化选择联用其他降糖药物。
对不同患者的降糖治疗建议如下:(1)对于合并心力衰竭的患者,应优先考虑使用SGLT2i,包括达格列净、恩格列净、卡格列净,以降低心力衰竭住院风险。若SGLT2i 治疗后需额外控制血糖,可考虑联用GLP-1 RA[6,20]。(2)对于合并慢性肾脏病(定义为肾脏结构或功能异常>3 个月)的患者,应优先考虑有心、肾获益证据的SGLT2i(如恩格列净、达格列净和卡格列净)或GLP-1 RA(如利拉鲁肽、司美格鲁肽和度拉糖肽)[20]。(3)对于合并超重或肥胖的患者,应优先考虑具有明确减重效应的GLP-1 RA[20]。不同的GLP-1 RA 减重效果不同。研究显示,1.0 mg 司美格鲁肽(1 次/周)治疗40 周,患者体重降幅高达6.5 kg[33];利拉鲁肽1.8 mg(1 次/d)治疗26 周,患者平均体重较基线下降3.5 kg[34];度拉糖肽1.5 mg(1 次/周)单药治疗26 周,患者平均体重较基线下降1.5 kg[35]。2024 年美国糖尿病学会发布的糖尿病诊疗标准根据GLP-1 RA 的减重效果,推荐优先选择顺序为司美格鲁肽>利拉鲁肽>度拉糖肽>艾塞那肽>利司那肽[20]。
CCS 患者血糖管理流程见图2。
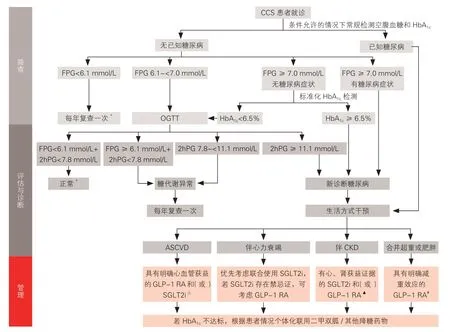
图2 CCS 患者血糖管理流程
2.4.1.3 PCI 围术期患者
在行择期PCI 时,口服降糖治疗下血糖控制良好的患者无需换用胰岛素。如术前血糖控制不良(如空腹血糖>7.8 mmol/L),可考虑换用胰岛素,皮下注射胰岛素是术前控制血糖的首选方案,可选基础-餐时胰岛素(睡前中效/长效胰岛素联合三餐前短效/速效胰岛素)、预混胰岛素皮下注射或胰岛素泵皮下注射方案。术中选择胰岛素持续静脉输注方案,同时密切监测血糖,并根据血糖结果动态调整静脉输注胰岛素的速度[36]。
对于正在使用降糖药物的患者,在时间允许的情况下,手术当日应停用部分口服降糖药和非胰岛素注射剂。对于接受静脉注射碘对比剂的患者,在检查前或检查时必须停止服用二甲双胍,在检查完成至少48 h 后且仅在再次检查肾功能稳定的情况下才可以恢复用药[37]。降糖药物DPP-4i 和GLP-1 RA的降糖作用具有血糖依赖性,低血糖发生风险低,围术期可以考虑继续使用。SGLT2i 容易导致低血容量和尿路感染,PCI 术前需停药48 h。对于术后当日即能恢复正常饮食的短小日间手术,可保留使用部分口服降糖药,但促进胰岛素分泌的磺脲类和格列奈类降糖药在禁食后容易造成低血糖,应一律停用[36]。
急诊手术由于情况危急,很难在术前对血糖水平进行理想干预,但对术中及术后的高血糖应予以控制,而且血糖监测应更加密切,以避免低血糖的发生。如患者合并酮症酸中毒,应积极进行处理,同时基于患者的总体生理情况和手术紧急程度,个体化决定是否推迟手术。
2.4.2 多学科会诊[38]
当冠心病患者存在以下情况时,可考虑多学科会诊和管理:(1)诊断困难和特殊情况:初次发现血糖异常,临床分型不明确;妊娠和哺乳期女性血糖异常。(2)治疗困难:原因不明或经心内科医师处理后仍反复发生低血糖;血糖波动较大、心内科医师处理困难、无法平稳控制;出现严重降糖药物不良反应且难处理;血糖、血压、血脂长期治疗不达标。(3)严重并发症:①糖尿病急性并发症:严重低血糖或高血糖,伴或不伴意识障碍(糖尿病酮症;疑似为糖尿病酮症酸中毒、高渗性高血糖状态或乳酸性酸中毒);②糖尿病慢性并发症(视网膜病变、肾病、神经病变、糖尿病足或外周血管病变)筛查、治疗方案的制定和疗效评估存在困难;糖尿病慢性并发症恶化需紧急救治:急性心脑血管疾病;糖尿病肾病导致的肾功能不全[估算肾小球滤过率(eGFR)<60 ml/(min·1.73 m2)]或大量蛋白尿;糖尿病视网膜病变导致的严重视力下降;糖尿病外周血管病变导致的间歇性跛行和缺血性疼痛、糖尿病足溃疡或严重足畸形等。(4) 判断患者需内分泌科医师处理的其他情况或疾病。
2.4.3 长期随访
在对冠心病合并2 型糖尿病患者进行随访时,除应关注血压、血脂等指标外,也应关注血糖的长期随访,每次随访都应复查空腹/餐后血糖,HbA1c至少每3 个月复查一次。
2.5 具有明确心血管获益的降糖药物应用实践
要点
(1)具有明确心血管获益的GLP-1 RA(利拉鲁肽、司美格鲁肽和度拉糖肽)和SGLT2i(恩格列净、达格列净和卡格列净)在用于临床时,应排除禁忌证,注意剂量的滴定,起始治疗时调整其他药物,并长期监测和随访,积极处理治疗过程中的不良反应。
(2)GLP-1 RA 和SGLT2i 联用时有协同增效作用,可降低心血管事件风险,不增加严重低血糖风险。
2.5.1 GLP-1 RA
2.5.1.1 禁忌证
GLP-1 RA 禁用于对GLP-1 RA 过敏的患者、妊娠或哺乳期患者以及有甲状腺髓样癌或2 型多发性内分泌腺瘤综合征病史或家族史的患者。此外,对于伴胃轻瘫或既往接受过胃部手术者、有胰腺炎病史或伴增殖性糖尿病视网膜病变者,应评估治疗的获益和风险,谨慎使用GLP-1 RA[39]。
2.5.1.2 GLP-1 RA 剂量的滴定
国内上市的 GLP-1 RA(除贝那鲁肽和艾塞那肽微球)均可用于轻、中度肾功能不全(肌酐清除率≥30 ml/min)患者;重度肾功能不全(肌酐清除率为15~<30 ml/min)患者可以使用司美格鲁肽、度拉糖肽和利拉鲁肽,但终末期肾病(肌酐清除率<15 ml/min)患者不推荐使用[40]。
在用药过程中,建议在患者可耐受的情况下,将GLP-1 RA 逐渐增加至心血管获益剂量。LEADER研究证实,利拉鲁肽1.8 mg(1 次/d)具有心血管获益[12];SUSTAIN-6 研究显示,司美格鲁肽0.5 mg或1.0 mg(1 次/周)治疗对主要不良心血管事件及其各组分发生风险的下降幅度相似[14]。REWIND 研究证实,度拉糖肽1.5 mg(1 次/周)具有心血管获益[16]。
2.5.1.3 起始治疗时其他药物的调整
(1)其他降糖药物调整:GLP-1RA 和DPP-4i在作用机制上存在重叠,不建议二者联用,在启动GLP-1 RA 治疗之前应停用DPP-4i。其他需调整的降糖药物主要为磺脲类药物和胰岛素。对于使用磺脲类药物的患者,应考虑在启动GLP-1 RA治疗时停药,尤其是当基线HbA1c≤7.5%或患者在任何HbA1c水平出现低血糖时。如HbA1c介于7.6%~8.5%之间,则先将磺脲类药物剂量减少50%;如HbA1c>8.5%,则维持当前剂量的磺脲类药物治疗;之后随着患者HbA1c水平接近个体化目标值,有可能停用磺脲类药物[39]。对于使用胰岛素治疗的患者,如在启动GLP-1 RA 治疗前基线HbA1c不超过目标值或出现低血糖,建议将基础胰岛素剂量减少20%~30%。对于使用较高剂量胰岛素或每日多次注射胰岛素的患者,心内科医师可考虑推迟启动GLP-1 RA 治疗,将患者转诊至内分泌科医师,由其考虑治疗转换[39]。
(2)心血管药物调整:司美格鲁肽和利拉鲁肽主要代谢途径是蛋白质降解,体外研究已证实,它们和其他活性物质之间发生与细胞色素P450 和血浆蛋白结合有关的药代动力学相互作用的可能性极低,与常用心血管药物(如地高辛、华法林、阿托伐他汀等)联用并未出现任何与临床相关的吸收延迟,因此无需调整剂量。
2.5.1.4 常见不良反应及处理原则
GLP-1 RA 极少发生低血糖,除非与磺脲类药物或胰岛素同时使用。GLP-1 RA 最常见的不良反应为胃肠道不适,呈剂量依赖性,可随治疗时间延长而减轻。当患者出现胃肠道症状后,应进行综合评估:对于短期或轻度胃肠道不良反应,可通过少量多餐和避免油炸或油腻食物来减轻症状;对于持续存在或更严重的胃肠道不良反应,应暂停GLP-1 RA剂量递增,并根据患者情况减少GLP-1 RA 剂量或换用其他GLP-1 RA,甚至停用GLP-1 RA,直至不良反应消失,然后考虑恢复GLP-1 RA 治疗。应用GLP-1 RA 时可能会出现的注射部位不良反应包括红斑、皮疹和皮下结节,可通过轮换注射部位来预防[39]。
2.5.1.5 患者监测和随访
对于接受GLP-1 RA 治疗的患者,在随访时应注意监测胃肠道不良反应,评估患者长期治疗的依从性。在启动治疗后,如患者可以耐受,无论血糖控制情况如何,可考虑将GLP-1 RA 调整至证实可改善心血管结局的剂量水平[39]。
2.5.2 SGLT2i
2.5.2.1 禁忌证
SGLT2i 的禁忌证包括:有已知过敏反应或其他不良反应;妊娠和哺乳;eGFR<20 ml/(min·1.73 m2);症状性低血压或收缩压<95 mmHg(1 mmHg=0.133 kPa)[41]。
2.5.2.2 SGLT2i 的目标使用剂量
SGLT2i 的目标剂量为:达格列净10 mg/d、恩格列净10 mg/d、卡格列净100 mg/d、索格列净200 mg/d、艾托格列净5 mg/d。根据患者的基线血压、血容量、血糖、肾功能等因素,起始治疗时药物剂量可酌情减半。
2.5.2.3 起始治疗时其他药物的调整
(1)其他降糖药物调整:磺脲类药物和胰岛素增加低血糖风险,因此,在启用SGLT2i 时,建议减少磺脲类药物剂量或停用磺脲类药物,减少胰岛素剂量[42]。
(2)心血管药物调整:SGLT2i 可诱导渗透性利尿,并可导致易感患者出现低血压,因此建议在用药过程中根据血压/肾功能调整肾素-血管紧张素-醛固酮系统阻滞剂剂量,减少利尿剂剂量[42]。药代动力学研究提示,卡格列净和索格列净可能会增加地高辛血药浓度,联合用药时需注意监测。
2.5.2.4 常见不良反应及处理原则[42]
(1)泌尿生殖道感染:多为轻至中度细菌或真菌感染,常规抗感染治疗有效。建议患者注意个人外阴部卫生,适量饮水,保持排尿通畅。(2)非高血糖性糖尿病酮症酸中毒:少见,建议启用此类药物前综合评估病情,加强用药指导及治疗后的监测。如出现腹痛、恶心、呕吐、乏力、呼吸困难,需立即检测血酮体和动脉血酸碱度以明确诊断。确诊后应立即停用SGLT2i,并给予对症治疗。
2.5.2.5 患者监测和随访
根据应用SGLT2i 过程中可能会出现的不良反应,建议在启动SGLT2i 治疗后监测eGFR、血容量、血压、尿常规、血糖、体重等指标以及进行下肢体检,必要时还可考虑进行动脉血气分析。
2.5.3 GLP-1 RA 与SGLT2i 联用
GLP-1 RA 和SGLT2i 具有独立于降糖作用的心血管保护作用,且机制互补,这为二者联用提供了可能。一项针对随机对照研究的Meta 分析表明,与单药治疗相比,SGLT2i 与GLP-1 RA 联合治疗可显著降低2 型糖尿病患者的HbA1c、体重,同时不增加严重低血糖发生风险[43]。针对心血管结局试验的Meta 分析表明,SGLT2i 与GLP-1 RA 联合治疗在减少主要不良心血管事件方面的累加效应虽未达到统计学意义,但与任何单药治疗相比均有更大获益[44]。近期一项真实世界研究的亚组分析显示,SGLT2i 与GLP-1 RA 联合治疗组的全因死亡风险与两个单药治疗组相比分别降低了47%和44%[45]。
2.6 冠心病合并2 型糖尿病患者的非降糖治疗
要点
对于冠心病合并2 型糖尿病患者,除降糖治疗外,也应关注冠心病的其他基础治疗,包括抗血小板、降压、降脂、抗心肌缺血治疗等。
2.6.1 抗血小板治疗
CCS 患者需长期服用小剂量阿司匹林,若不能耐受,可考虑以氯吡格雷替代;对于ACS 或PCI 术后患者,建议接受双联抗血小板治疗(阿司匹林+氯吡格雷/替格瑞洛)至少12 个月[6]。
2.6.2 降压治疗
2 型糖尿病合并心血管疾病患者的降压目标为<130/80 mmHg,若不能耐受,可放宽至<140/90 mmHg。降压药物首选血管紧张素转换酶抑制剂或血管紧张素Ⅱ受体拮抗剂。血压≥160/100 mmHg或高于目标血压20/10 mmHg 或单药治疗未达标者,应接受联合降压治疗[6]。
2.6.3 降脂治疗
冠心病合并2 型糖尿病患者的降脂药物首选中等强度他汀类药物[46],但应注意监测血糖。降脂治疗以低密度脂蛋白胆固醇<1.4 mmol/L 且较基线降低50%为首要目标、非高密度脂蛋白胆固醇<2.2 mmol/L 为次级目标[6,46]。
2.6.4 抗心肌缺血治疗[6]
(1)β 受体阻滞剂:为劳力性心绞痛、心肌梗死患者的首选一线用药,静息目标心率为55~60次/min。因该类药物可能降低患者对低血糖发作时的反应能力,因此应注意把握适应证。
(2)硝酸酯类药物:为各种类型心绞痛患者的一线用药,冠状动脉血运重建治疗后或心绞痛已稳定控制者不建议长期使用。
(3)钙拮抗剂:为单纯或合并痉挛性心绞痛患者的一线用药。非二氢吡啶类钙拮抗剂与β 受体阻滞剂联用时需注意对心率的影响,二氢吡啶类钙拮抗剂应尽可能选择长效制剂。
3 未来展望
尽管降糖药物在心血管疾病治疗中取得了突破性进展,但临床实践中仍存在诸多问题。首先,ACS患者血糖管理的循证证据较少,亟需更多临床研究来探索降糖启动时机、最佳降糖方案和治疗目标等管理策略。其次,国外已有研究证实,GLP-1 RA在非糖尿病的肥胖合并心血管疾病人群中有获益[47],但其中仅纳入了少量亚裔受试者,仍需开展大规模中国人群研究,以进一步验证其获益。此外,除GLP-1 RA 和SGLT2i 外,不同类型降糖药物和不同联合用药方案在心血管疾病患者中应用的有效性和安全性尚需明确。最后,中国不同年龄段的冠心病合并糖尿病患者尤其老年患者的相关降糖证据有限。对于上述问题,需要进一步开展临床试验和真实世界研究进行探索、积累证据。
共识专家组成员(按姓氏汉语拼音排序):宾建平(南方医科大学南方医院),卜培莉(山东大学齐鲁医院),陈莉明(天津医科大学朱宪彝纪念医院),陈燕燕(中国医学科学院阜外医院),陈韵岱(中国人民解放军总医院),陈桢玥(上海交通大学医学院附属瑞金医院),邓微(北京积水潭医院),郭彩霞(首都医科大学附属北京同仁医院),郭军(中国人民解放军总医院),贺勇(四川大学华西医院),黄恺(华中科技大学同济医学院附属协和医院),纪立农(北京大学人民医院),蒋峻(浙江大学医学院附属第二医院),孔洪(四川省人民医院),黎励文(广东省人民医院),李静(首都医科大学宣武医院),李牧蔚(阜外华中心血管病医院),李勇(复旦大学附属华山医院),刘斌(吉林大学第二医院),刘靖(北京大学人民医院),刘巍(北京积水潭医院),柳景华(首都医科大学附属北京安贞医院),鲁梅花(首都医科大学宣武医院),吕朝晖(中国人民解放军总医院),彭道泉(中南医院湘雅二医院),齐晓勇(河北省人民医院),钱菊英(复旦大学附属中山医院),曲鹏(大连医科大学附属第二医院),寿锡凌(陕西省人民医院心血管病院),苏晞(武汉亚洲心脏病医院),陶红(首都医科大学附属北京安贞医院),吴延庆(南昌大学第二附属医院),徐标(南京大学医学院附属鼓楼医院),杨清(天津医科大学总医院),杨伟宪(中国医学科学院阜外医院),殷跃辉(重庆医科大学附属第二医院),周翔海(北京大学人民医院)
共识执笔专家:刘靖(北京大学人民医院),周翔海(北京大学人民医院)
利益冲突:所有作者均声明不存在利益冲突
