原发性脾淋巴瘤误诊为脾脓肿一例
2024-05-07刘振华李月宏蔡艳刘培万黎昭君彭雄兵方兴保
刘振华,李月宏,蔡艳,刘培万,黎昭君,彭雄兵,方兴保
1.曲靖市第一人民医院 肝胆胰外科,云南 曲靖 655000;2.曲靖医学高等专科学校 病理学教研室,云南 曲靖 655000
原发性脾淋巴瘤(primary splenic lymphoma,PSL)是一种极为罕见的疾病,在所有非霍奇金淋巴瘤(non-Hodgkin’s lymphoma,NHL)中占比<1%[1]。弥漫大B细胞淋巴瘤(diffuse large B cell lymphoma,DLBCL)是PSL和NHL最常见的组织学亚型,其他亚型包括脾绒毛性淋巴瘤、脾边缘区淋巴瘤和滤泡性淋巴瘤[2]。PSL的临床症状无特异性,极易造成误诊。现将曲靖市第一人民医院肝胆胰外科收治的一例PSL误诊为脾脓肿病例诊治经过报道如下,以期提高对PSL的临床认识。
病例
患者女性,32岁,因“左侧腹痛伴发热2 d”于2022年8月27日收住曲靖市第一人民医院。患者2 d前无明显诱因感左侧腹部疼痛,呈持续性胀痛,且逐渐加剧,无缓解,向左侧背部放射,弯腰位疼痛自觉减轻,伴发热,余无不适。入院查体:左侧腹部压痛,未见反跳痛及肌紧张,左侧腹部可触及质地稍硬包块,约8.0 cm,活动度差,余未见异常。完善相关检查:白细胞数14.0×109/L,红细胞数4.15×1012/L,血红蛋白130 g/L,血小板数207×109/L,超敏C反应蛋白>5.0 mg/L,凝血、肝肾功能、肿瘤标志物等未见明显异常。全腹部CT平扫+增强扫描:脾脏肿块,考虑脓肿,肿瘤性病变不完全除外(图1)。上腹部MRI平扫+MRCP+三维动态增强:脾脏体积增大合并占位性病变、脾脏周围及左侧结肠旁沟积液及渗出,考虑感染性病变可能,肿瘤性病变待排(图2)。
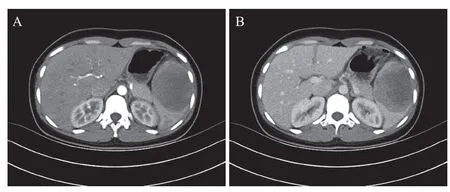
图1 腹部增强CT
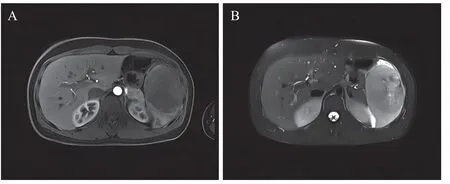
图2 腹部增强MRI
术前诊断考虑:脾肿物(脾脓肿?)。完善术前检查,排除禁忌证后于2022年8月31日行腹腔镜下全脾切除术。术中见脾肿大,约15 cm×10 cm×8 cm,脾周未见明显脓液,仅有网膜粘连,无感染征象,完整切除脾脏后送病理检查。术后标本:脾脏大小约16 cm×12 cm×8 cm,切面呈鱼白色,多结节状,质软。术后免疫组化:CD79a(+)、CD20(+)、PAX-5(-)、CD30(-)、Ki-67(70%+)、CD15(个别+)、ALK(-)、CD3(部分+)、MUM-1(+)、BCL-6(+)、EMA(-)、TDT(-)、C-myc(散在+)。病理诊断:脾脏弥漫大B细胞淋巴瘤(图3)。患者术后给予抗感染、抑酸护胃、适当止痛、止血、护肝、补液等对症治疗,恢复良好,出院后在血液科予以利妥昔单抗联合环磷酰胺、多柔比星、长春新碱、泼尼松方案(R+CHOP)化疗4 周期,后继续单用利妥昔单抗治疗4周期,每3个月复查,随访1年半未出现复发,目前仍在随访。
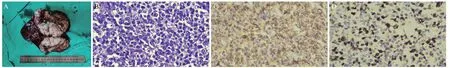
图3 手术标本及病理结果
讨论
目前将PSL定义为仅累及脾脏,无浅表淋巴结肿大[3]。PSL患者通常表现为发热寒战、左上腹疼痛、疲劳、体质量减轻、脾肿大等,也可能出现脾破裂出血。在报道的非外伤性脾破裂病例中,6.3%的脾破裂是由NHL引起[4]。PSL的检验主要是血小板减少、贫血、乳酸脱氢酶水平升高和丙型肝炎病毒感染[3]。PSL的影像学表现是脾脏内边界清楚的结节性肿块,肿块大多数是低密度影,增强后无强化或轻度强化[5]。Maglione等[6]认为,在病程中影像学检查可见脾脏逐渐增大、病灶日趋增多是PSL诊断的重要依据,但是脾切除术后的病理检查依然是确诊的金标准[7]。PSL分3期:Ⅰ期肿瘤仅限于脾脏,Ⅱ期累及脾及脾门淋巴结,Ⅲ期累及肝脏或脾外淋巴结[8]。本例患者主要累及脾脏,而血小板、血红蛋白、肿瘤标志物正常,浅表淋巴结无肿大,影像学表现为低密度影,边界清晰,可见轻度强化,结合术后病理诊断为PSL(I期)。
由于PSL罕见,无特异性临床表现,且该病与脾脓肿的影像学表现相似,导致本病例最初误诊为脾脓肿,最后通过术后病理检查才明确诊断为PSL。因此,我们在临床实践中针对此种病例术前要慎重考虑,应与以下疾病鉴别。(1)脾脏转移瘤:此种疾病有原发灶,平扫时呈多发低密度占位性病灶,增强扫描可有不同程度的强化,有“牛眼征”。(2)脾结核:此种疾病患者多有结核病史,病灶不规则、密度不均匀,可见干酪样坏死及钙化灶,增强不均匀且呈较明显强化。(3)脾血管肉瘤:此种疾病表现为边界模糊的肿块,可见坏死区或钙化,不均匀强化。
本病例诊断过程存在不足之处:(1)弥漫大B细胞淋巴瘤(DLBCL)患者通常乳酸脱氢酶升高[3],而本病例术前未行乳酸脱氢酶检测;(2)本病例以发热和左上腹疼痛为主要表现,无浅表淋巴结肿大及外周血异常,笔者因对PSL认识不足导致未能及时考虑PSL;(3)本病例最初考虑为脾脓肿,而术中探查未见明显脓液时未及时行术中冰冻检查。
DLBCL是一种侵袭性癌症,并且扩散速度很快,预后较差。因此,早发现、早干预对患者生存至关重要。Pan等[9]发现,脾切除术是一种有效的诊断和治疗手段,在PSL早期行脾切除术能显著改善患者预后。另外,辅助化疗也是重要治疗手段,目前利妥昔单抗联合环磷酰胺、多柔比星、长春新碱、泼尼松方案(R+CHOP)已成为公认的DLBCL标准化疗方案[10]。研究发现利妥昔单抗治疗、利妥昔单抗联合化疗及单纯化疗PSL患者的3 年生存率分别为95%、100%和55%[11]。Yonghao等[12]利用SEER数据库分析了347 例原发性脾淋巴瘤患者不同治疗方式的预后及复发情况,发现脾切除术后联合适当的化疗是最有效的治疗策略和预防复发的方法。
综上,我们在临床工作中发现患者不明原因的左上腹疼痛、体质量减轻和不规则发热,经抗生素治疗无效,特别是影像学提示脾占位或巨脾者时,应及时行脾切除术,通过病理检查及免疫组化明确诊断,以防延误病情导致脾破裂和肿瘤转移的发生。术后应辅以合适的化疗,改善患者的预后,预防复发。
