芬顿氧化技术处理焦化废水反渗透浓缩液探究
2024-05-04刘孟博
刘孟博,韩 颖,张 威
(维尔利环保科技集团股份有限公司,江苏 常州 213000)
引言
煤化工领域产生的废水往往具有成分复杂、毒性大、污染物种类多等特点[1]。在煤化工废水处理系统中,反渗透系统一般应用于生化处理后的高盐废水的处理流程中,由生化系统高效去除废水中的有机物。但在高盐废水处理中,因需要将废水进行浓缩除盐,进而产生了盐分较低的清液和反渗透浓液两种废水,其中反渗透浓液具有可生化性差,盐含量高的特点,且其含有较高浓度的有机污染物而无法直接排放,因而需要对其进行深度处理。
反渗透浓缩液处理的关键是去除浓缩液中难降解的有机污染物,一般采用高级氧化法进行处理,其中包括芬顿氧化法、臭氧氧化法、电化学氧化法、光催化氧化法等。这些高级氧化法处理浓缩液的效果各有利弊,其中芬顿氧化法因具有条件温和、操作简单、处理费用低、适用范围广等优点而被企业广泛采用。芬顿氧化法主要是利用过氧化氢产生的羟基自由基破坏有机污染物的组成,使其发生断链、分解、氧化等反应,再引入铁离子进行催化使得反应更加迅速和彻底。
芬顿氧化法已广泛应用于多种工业废水处理的研究中。庞悦[2]等人用芬顿氧化法处理印染废水,探索了各种反应条件对处理效果的影响;赵瑾[3]等人曾研究了芬顿氧化法对电镀废水中有机络合物的处理;孙志龙[4]等人则以芬顿氧化法作为预处理开展了对液晶显示废液的实验研究;吕丹丹[5]等人研究了芬顿氧化法对垃圾填埋场渗滤液的处理。不仅如此,许多研究还将芬顿氧化与其他水处理工艺相结合,如与紫外氧化法[6]、微电解氧化法[7-8]、超声氧化法[9]等结合进行实验研究。在诸多研究中,芬顿氧化法展示出其对有机污染物卓越的氧化处理能力,但关于其在对反渗透浓缩液中的研究较少。张正义[10]等人用催化臭氧氧化法处理了垃圾渗滤液的反渗透浓液,使污水中腐殖质的去除效率在催化剂的作用下显著提高,但仅得到有限的降解且未能完全矿化;刘恋[11]用膜生物反应器(MBR)对电镀废水处理中所产生的反渗透浓液进行处理,通过长期的污泥驯化解决了其可生化性低的问题。
针对焦化废水反渗透浓液难降解、无法达标排放的问题,本研究采用正交实验探索过氧化氢及亚铁的添加量对COD去除率真的影响,在确定了最佳的反应条件后,通过提高规模验证其稳定性。
1 实验材料与方法
1.1 实验材料与药剂
本研究所用水样来源于河北某焦化废水中水回用系统的反渗透浓液,该水样的主要水质指标如表1所示。根据水质指标显示,该水体中含有较高的盐分,且有机污染物的浓度高,依据《炼焦化学工业污染物排放标准》(GB 16171-2012)中表2的间接排放标准,该水体不能直接排放。
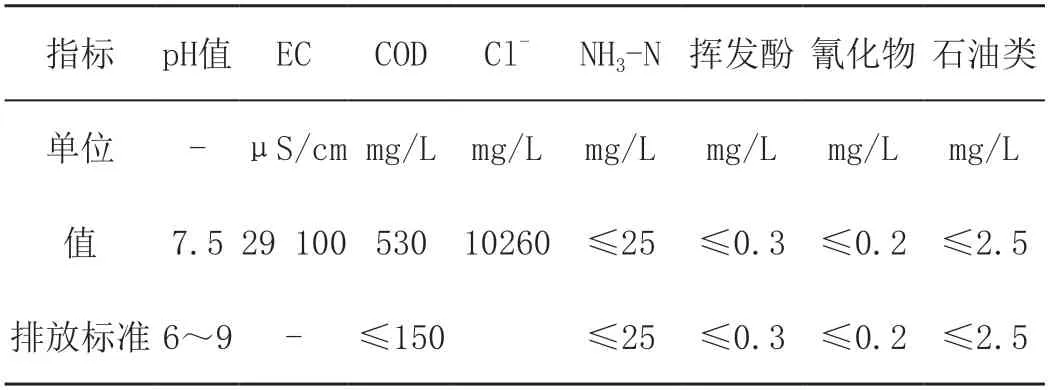
表1 反渗透出水水质

表2 正交实验因素水平表
1.2 氧化实验
1.2.1 实验设计
根据芬顿氧化原理,主要因素为过氧化氢与COD的质量比、过氧化氢与铁元素的摩尔比,根据这两点分别设置了不同水平,正交实验如表2所示。根据该表,按照两种因素不同水平的排列组合,共设置了30组实验。
1.2.2 实验步骤
根据设计量取200 mL反渗透浓缩液水样于250 mL的烧杯中,使用硫酸调节废水的pH值至设计参数;按照实验设计准确称取硫酸亚铁固体加入到溶液中,搅拌至溶解后加入一定体积的过氧化氢溶液,开始进行芬顿氧化。待反应2 h后,检测并用30%氢氧化钠溶液调节溶液pH值为7.5左右。
按照2 mg/L的投加量加入PAM,待溶液分层,用滤纸进行过滤,并检测滤液的COD和TOC浓度。
1.3 验证实验
为了保证实验结果的可重复性,提高实验的参考价值,需要重复验证正交实验结果。根据正交实验结果,按照最优的实验条件,按比例放大实验,即将初始溶液体积分别设置为200 mL、800 mL和2 000 mL,除pH设计值不变外,其余药剂的投加量均按比例放大。
1.4 二次芬顿氧化实验
由于芬顿反应可能存在反应不彻底,导致其作用并未完全发挥的问题,为探索一次芬顿氧化对溶液中有机污染物的降解程度,判断芬顿氧化是否在一次实验中达到终点,在完成一次氧化实验后,进行了二次氧化实验,其中一次和二次氧化反应的条件和药剂添加比例相同。
2 结果与讨论
2.1 芬顿氧化实验
芬顿氧化实验的结果如图1所示,其分别展示了溶液在经芬顿氧化后的COD、COD去除率、TOC和TOC去除率的变化,其中COD去除率和TOC去除率为实验后溶液中COD和TOC的降低量与实验前对应值的比例。c(H2O2):c(COD)表示设定过氧化氢的量(mg/L)与原液中COD的含量比,值越高即加入过氧化氢的量也就越高,n(H2O2):n(Fe)表示加入过氧化氢的物质量与所加入亚铁离子的物质量之比,在过氧化氢量一定时,该值越大意味着加入亚铁离子的量越高。
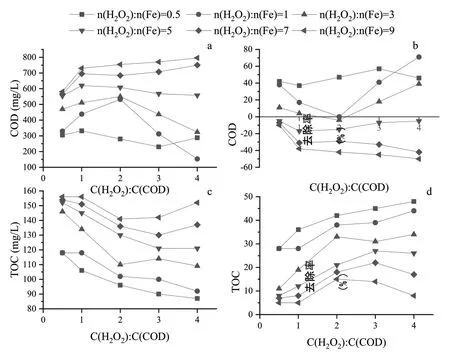
图1 芬顿氧化实验数据
根据图1中的数据,溶液COD和TOC随着过氧化氢量或亚铁离子量的添加量的不同而不断变化。在图1a中,当n(H2O2):n(Fe)>0.5时,随着过氧化氢量的提高,COD不仅没有降低,反而出现上升的趋势,这可能与过氧化氢的量有关。而在图1c中,实验后溶液TOC的下降表明COD的提高与有机物无关,而是无机物质造成的,这也印证了以上所述,另外该图还说明当存在较少亚铁离子时,投加过量的过氧化氢量还会导致TOC先降低后提高。图1b中COD去除率出现负值的原因则与过氧化氢的过量添加有直接关系。
另一方面,固定过氧化氢的添加量,提高亚铁离子的添加量,COD去除率显著降低。从芬顿氧化法原理[12]可知,这是因为加入的亚铁离子与过氧化氢发生了氧化还原反应,消耗了过量的过氧化氢,虽然亚铁离子也具有一定的还原性,但在芬顿实验结束后,溶液的pH值已调节至中性,溶液中铁离子已沉淀去除;除此之外,亚铁离子的加入会促进过氧化氢的分解,并产生羟基自由基,使得过氧化氢的利用率大大提高,也展示了亚铁离子在反应中的关键作用。然而在庞悦[2]等人的研究中,随着硫酸亚铁投加量的提高,溶液中的COD出现先上升后下降的现象,过量的亚铁离子会使过氧化氢产生的羟基自由基来不及反应而快速分解,而一味地增大亚铁离子的投加量还会提高成本,因此控制过氧化氢和亚铁离子的添加量是充分发挥芬顿氧化法作用的关键。
在本实验中,COD和TOC的去除率在c(H2O2):c(COD)=4,n(H2O2):n(Fe)=1时均达到最高,分别为71%和44%,从排放角度看,此时溶液中COD的浓度可以满足排放标准所要求的最高排放浓度。
2.2 验证实验
在得到芬顿氧化实验结果后,工作人员进行了验证实验,结果见图2。
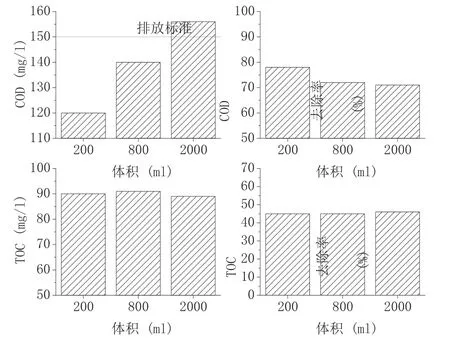
图2 重复验证实验结果
在不同体量的水中,按照c(H2O2):c(COD)=4,n(H2O2):n(Fe)=1的比例添加过氧化氢和硫酸亚铁,溶液COD含量随着体量增大而降低,并有高于最高排放标准值(150 mg/L)的风险,而所对应的TOC含量则变化不大。实际上,对于芬顿氧化法来说,搅拌速度、反应时间和温度等变量都是影响反应的因素,在仅控制体量不同的实验中,这些因素成为了影响过氧化氢分解、有机物氧化反应等的关键。从结果中我们也可以看到,有机物的去除率相差不大,造成COD偏差的直接原因可能是过氧化氢的残留。
2.3 二次芬顿实验
随机选取了c(H2O2):c(COD)=3,n(H2O2):n(Fe)=0.5作为二次芬顿药剂投加比例,在进行两次芬顿后,所得实验结果图3所示。
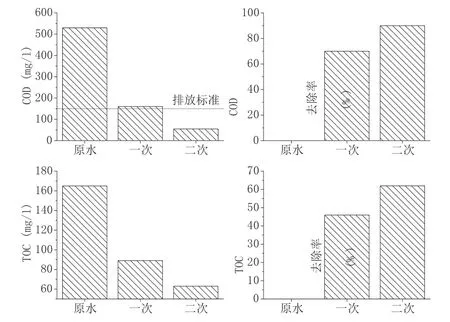
图3 二次芬顿实验结果
二次芬顿实验结果显示,在一次芬顿实验后,虽然废水中COD的去除效果很明显,且去除率已经达到70%,但是仍未达到排放标准,而在二次芬顿后COD含量再一次大幅降低,COD的去除率提升至90%。相对应地,溶液中TOC的含量也有较大幅度的变化。
3 结论
采用芬顿氧化的方式处理焦化废水中产生的RO浓液,过氧化氢的量和亚铁离子的最佳添加比例分别为c(H2O2):c(COD)=4,n(H2O2):n(Fe)=1,该比例可适用于不同规模的水量。另外,在一次芬顿氧化后,还会有大量有机污染物可以继续被氧化,因而可以采用二次芬顿氧化的方式进行更深层次的处理。
