机器人辅助、荧光腹腔镜导航保留十二指肠全胰切除术1例临床报告
2024-04-29姜改明郑凯李宇铠康强柯阳李越华
姜改明,郑凯,李宇铠,康强,柯阳,李越华
(昆明医科大学第二附属医院 肝胆胰外科二病区,云南 昆明 650101)
保留十二指肠的胰头切除术(DPPHR),由Beger 等[1]于1980 年首次报道,近来国内外多项临床研究[2-3]报道,该术式适用于慢性胰腺炎及胰头部良性肿瘤仅切除胰头,较胰十二指肠切除术其优势在于保留了远端胃、胆总管及十二指肠消化道的完整性与功能,降低营养不良等远期并发症的发生率,提高了患者的生活质量,逐渐被外科医生重视与推广。近年来,随着先进医疗器械发展和外科医师技能的提升,该术式逐渐向微创化、精准化方向发展。昆明医科大学第二附属医院肝胆胰外科于2022 年11 月为1 例终末期慢性胰腺炎伴胰管结石患者行达芬奇机器人辅助、荧光腹腔镜导航保留十二指肠全胰切除术,获得良好效果,现报告如下。
1 临床资料
患者 男,61岁,因“反复上腹部疼4年余”入院。既往饮酒史20年,2型糖尿病10年余,血糖控制欠佳。入院血糖16.27 mmol/L,余血常规、血生化、血淀粉酶、肿瘤标志物阴性。增强CT(图1A-D):慢性胰腺炎;胆总管、主胰管扩张。增强MRI(图1E-F):慢性胰腺炎急性发作,胰腺萎缩,胰头段主胰管及分支胰管多发结石并全程扩张。术前诊断:慢性胰腺炎,胰管结石,胰腺钙化,胰腺萎缩,2 型糖尿病。完善术前准备后于2022 年11 月10 日行达芬奇机器人辅助、荧光腹腔镜导航保留十二指肠全胰切除术。
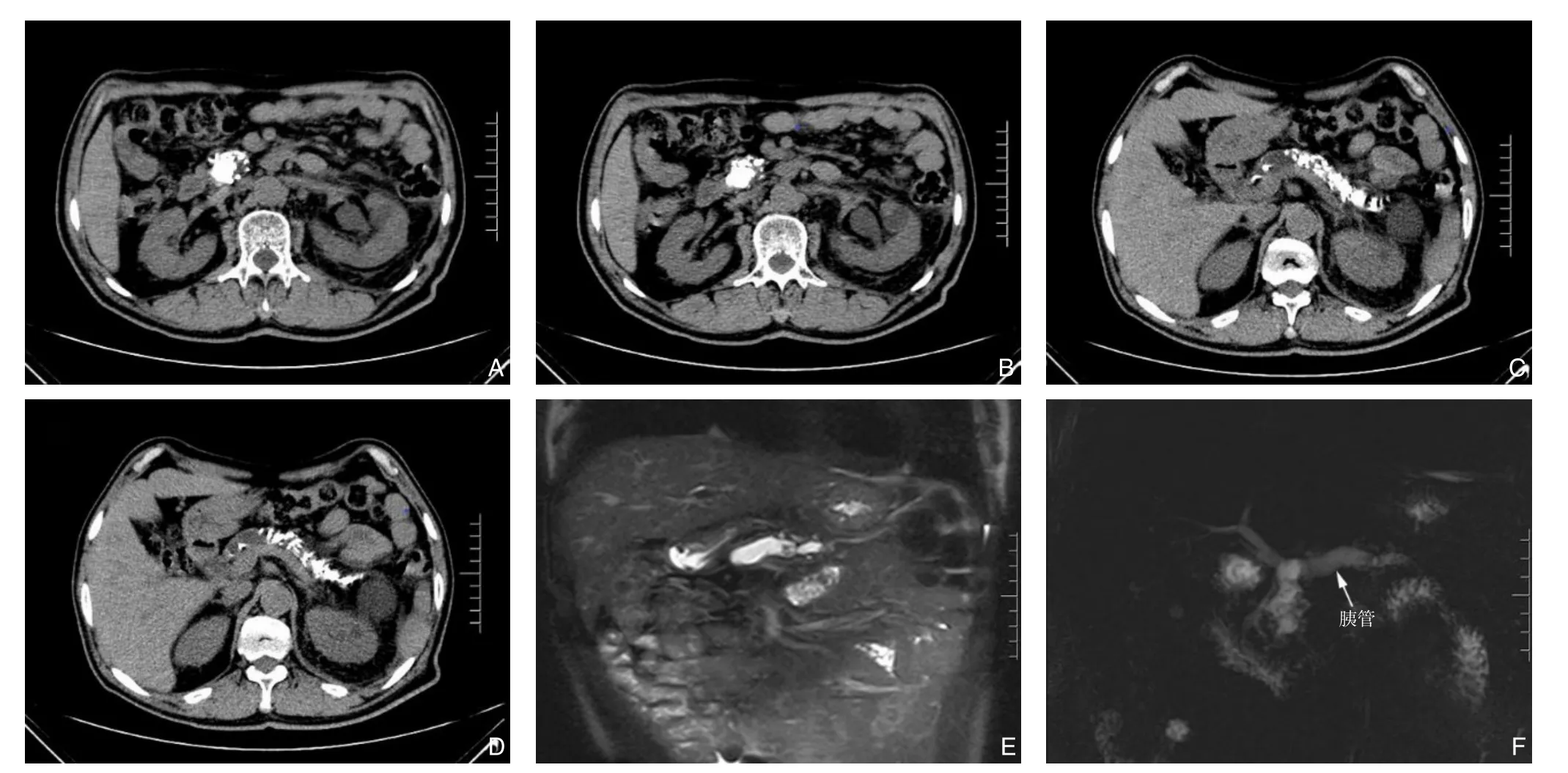
图1 患者术前影像 A-B:增强CT平扫期胰头;C-D:增强CT平扫期胰体尾;E:增强MRI胰腺冠状位;F:磁共振胆胰管水成像
手术过程:患者仰卧分腿,头抬高至30°,脐下做观察孔,建立气腹。依次建立机器人腹腔镜操作孔(图2A)。打开胃结肠韧带(图2B)及小网膜囊,使用红尿管及可吸收生物夹将胃悬吊于镰状韧带(图2C),充分显露胰腺。从胰腺颈部下缘、肠系膜上静脉前方分离胰颈与肠系膜上静脉,建立胰后隧道,用血管缝合线悬吊胰颈,超声刀横断胰颈(图2D)。考虑胰腺与脾动静脉粘连重,决定先予胰体尾联合脾切除术,从右向左沿胰腺下缘打开胰腺被膜,缝扎脾动静脉(图2E),离断脾脏周围韧带后完整切除脾脏和胰腺体尾部(图2F)。再行DPPHR:将胰颈残端向右侧牵拉,分离门静脉-肠系膜上静脉与胰头颈的间隙,离断胰十二指肠上静脉,将肠系膜上静脉向左侧牵拉,分离钩突与肠系膜上动脉,结扎胰十二指肠前下动脉(图2G),注意保护胰十二指肠后动脉弓完整(图2H),静脉推注吲哚菁绿2.5 mg,15 min 后荧光显露胆总管(图2I),分离到胆管和胰管汇合部切除胰腺头部和钩突,胰管残端血管线仔细缝扎,冲洗创面,脾窝胰头部各放置引流管1 根分别自左右侧腹引出固定。

图2 手术相关图片 A:Trocar孔分布;B:打开胃结肠韧带;C:悬吊胃于肝镰状韧带;D:横断胰颈;E:悬挂脾动静脉后横断;F:切除胰体尾和脾;G:分离钩突与肠系膜上动脉;H:显露胰十二指肠后动脉弓和胆总管;I:荧光显影胆总管
本例患者手术顺利,手术时间300 min,出血量200 mL,术后病理提示慢性胰腺炎、胰管结石。术后未出现出血、胰瘘、胆汁漏、十二指肠缺血坏死等并发症,仅出现血糖升高,予门冬胰岛素6 U三餐前皮下注射,甘精胰岛素12 U 睡前皮下注射,血糖控制良好,予复方消化酶胰腺外分泌功能替代治疗,于术后10 d 康复出院。术后7 d 复查CT 示胰腺、肝脏未见,腹腔少量积气,余未见明显异常(图3)。
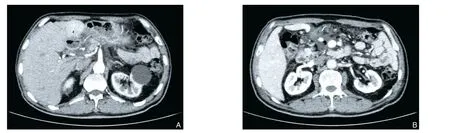
图3 患者术后影像 A:增强CT动脉期;B:增强CT门静脉期
2 讨论
慢性胰腺炎是一种多因素的纤维炎症综合征,其中胰腺炎症的反复发作导致广泛的纤维化组织替代,导致慢性疼痛、胰腺外分泌和内分泌功能不全、生活质量降低和预期寿命缩短[4]。慢性胰腺炎患者发生胰腺导管腺癌的风险增加,且发病率随着慢性胰腺炎持续时间的增加而增加[5]。目前普遍认为对于终末期全胰慢性炎性改变、胰管扩张不明显或多发分支胰管结石、其他切除术式不能缓解疼痛者,可行全胰腺切除术[6-8]。本例患者胰头段主胰管及分支胰管多发结石并全程扩张,胰腺实质广泛钙化,胰腺萎缩,符合保留十二指肠全胰切除的手术指征。
21 世纪是微创外科的世纪,与传统腹腔镜相比,达芬奇机器人具有精细稳定的操作、自动过滤手的颤抖、7 个自由度操作手臂和3D 高清稳定放大和眼手协同的手术视野等优势[9-10]。Giulianotti等[11]在2003 年发表了首例机器人胰腺切除术病例,近年来越来越多的研究[12-14]证明了机器人胰腺手术的安全性和可行性。机器人辅助手术可在胰腺所处的腹膜后微小空间内操作,使解剖、切除及缝合更确切、可靠、简便,在行保留器官功能的胰腺切除术中存在较为明显的微创优势,但同时也存在手术器械和耗材费用高等缺点[15-16]。笔者近期检索国内外数据库尚未见达芬奇机器人辅助、荧光腹腔镜导航保留十二指肠全胰切除案例的报道,考虑本例为首次采用达芬奇机器人辅助、荧光腹腔镜下荧光显影导航保留十二指肠全胰切除术。
保留十二指肠术中保留胰十二指肠血管弓的完整性是手术关键,目的是为保留的十二指肠、下段胆管提供良好血运。十二指肠的血供主要由胰十二指肠前动脉弓和胰十二指肠后动脉弓供应,其中胰十二指肠后动脉弓走行于胰腺后包膜,是营养十二指肠的主要血供,Takada 等[17-18]发现仅保留胰十二指肠后血管弓就足以维持十二指肠及胆总管血供。达芬奇机器人有助于精细操作,清晰辨认胆道、胰头及十二指肠区域的血供[19],本例很好地保留十二指肠后动脉弓,术后无十二指肠缺血、胆总管缺血坏死发生。
保留十二指肠术中对于胰腺段胆总管的显露与血供保护是此手术的一大难点。解剖胰腺段胆总管时,因胰腺段胆总管与胰腺实质紧密贴合,定位困难,游离时极易出现胆管损伤,术后易发生严重的胆汁漏。一些研究[20-22]报道,LDPPHR 术后胆汁漏的发生率为4.5%~16.7%。对此,Ishizawa等[23]引入了吲哚菁绿荧光成像在术中显露胆管,实时识别胆道解剖,避免胆道损伤。近年来,多项研究[24-25]表明,吲哚菁绿荧光导航技术对降低LDPPHR 术中胆管损伤和术后胆汁漏方面具有重要作用。本例通过术中经静脉注射吲哚菁绿、荧光显影导航使胆管显像,识别并防止误伤,术中胆总管显影效果好,胆管壁保护完好,术后未发生胆汁漏等并发症。
目前,保留脾脏胰腺远端切除术(SPDP)主要有Kimura 法(保留脾动静脉)[26]和Warshaw 法(切除脾动静脉主干、保留胃网膜左血管等侧支循环)[27]两种手术方式。其中,Kimura 法作为SPDP的首选方法,其优势在于保留了脾动、静脉,避免术后脾脏血供障碍或区域性门静脉高压[28]。虽然有多项研究[29-30]表明机器人胰体尾切除术与传统腹腔镜胰体尾切除术相比保脾率显著升高,但本例患者因慢性胰腺炎病史,术中发现胰腺与脾血管粘连明显,分离困难,出血风险高,故未行保脾治疗。
Beger 等[31]回顾性分析了1998—2012 年保留十二指肠胰头次全切和胰头全切除术382 例患者资料,总结出胰瘘为次全切除最主要并发症。在本研究中,在尽量切除胰头部胰腺组织的同时,用血管缝合线仔细缝扎了胆胰管汇合部的胰管残端,患者术后未发生胰瘘并发症。
总之,在严格掌握手术适应证前提下,达芬奇机器人辅助、荧光腹腔镜导航保留十二指肠全胰切除术是一种安全、可行、保留功能、新颖的术式,实施该术式的外科医生应熟练掌握机器人辅助腹腔镜下胰体尾切除术和LDPPHR。然而,本研究样本量仅有1 例,其临床远期疗效有待进一步的观察。
利益冲突:所有作者均声明不存在利益冲突。
作者贡献声明:姜改明负责论文撰写及投稿;郑凯负责辅助文稿的撰写、辅助分析临床及影像学资料;李宇铠负责数据收集整理、查阅文献;康强、柯阳负责文章修改;李越华、康强为手术实施者。
