苯氧威·噻嗪酮悬浮剂的高效液相色谱分析方法
2024-04-18杜秀利王广成高立明吴春先许艳秋
杜秀利,王广成,李 婷,高立明,吴春先,许艳秋*
(1.泸定县农产品质量安全(质量检测)中心,四川 甘孜 626100;2.四川省农业农村厅植物保护站,四川 成都 610045)
苯氧威(Fenoxycarb),又名双氧威、苯醚威,CAS登记号79127-80-3,是一种非萜烯类氨基甲酸酯类化合物。苯氧威既能破坏昆虫的内分泌激素,干扰昆虫发育和变态的过程,杀灭虫卵,又有胃毒和触杀作用,对鳞翅目、双翅目等害虫有特效,是一种广谱、低毒的昆虫生长调节剂和杀虫剂[1-2]。噻嗪酮(Buprofezin),CAS登记号69327-76-0,是一种噻二嗪类昆虫生长调节剂,属昆虫蜕皮抑制剂,同时也具有触杀和胃毒作用,对鞘翅目,部分同翅目及蜱螨目害虫具有持效杀幼虫活性[3]。目前我国登记的苯氧威与噻嗪酮的混配制剂主要用于柑橘树上蚧壳虫的防治。
目前公开报道的文献和标准中已有苯氧威[1-2]和噻嗪酮[4-5]相关的检测方法,但未查见二者混配制剂或苯氧威悬浮剂单制剂检测方法的相关报道,因此,本文采用高效液相色谱仪建立了一种同时测定产品中苯氧威和噻嗪酮有效成分含量的方法,该方法方便、高效、准确,是一种理想的分析方法,可用于苯氧威·噻嗪酮混配制剂,及苯氧威悬浮剂、噻嗪酮悬浮剂等相关产品的质量控制和检测。
1 材料与方法
1.1 供试药剂和试剂 苯氧威标准品,99.71%;噻嗪酮标准品,99.0%;苯氧威·噻嗪酮悬浮剂,25%;甲醇,色谱纯;超纯水。
1.2 仪器条件 高效液相色谱仪:Agilent 1260,配DAD检测器,美国安捷伦科技有限公司;电子天平:AB204-S,瑞士梅特勒-托利多集团;过滤器:滤膜孔径0.45 μm。
色谱柱:Eclipse plus C18,5.0 μm,250 mm×4.6 mm(i.d.)不锈钢柱;流动相:Ψ(甲醇+水)=80+20;流速:1.0 mL/min;柱温:30 ℃;检测波长:230 nm;进样体积:3.0 μL。采用外标法,峰面积定量。在该色谱条件下,苯氧威的保留时间约为5.3 min,噻嗪酮的保留时间约为11.3 min。典型色谱图(图1)。
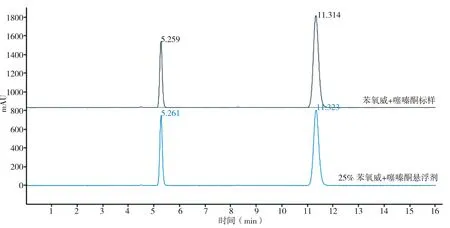
图1 相同条件下苯氧威+噻嗪酮标样和悬浮剂样品的液相色谱图
1.3 检测步骤
1.3.1 标准溶液配制 准确称取苯氧威标准品约0.03 g(精确至0.000 2 g),噻嗪酮标准品约0.12 g(精确至0.000 2 g),置于50 mL的容量瓶,加入适量甲醇超声至完全溶解后,放置至恢复室温,用甲醇稀释至刻度,摇匀备用。
1.3.2 试样溶液配置 准确称取含苯氧威约0.03 g的苯氧威·噻嗪酮样品(精确至0.000 2 g),置于50 mL的容量瓶,用水分散后用甲醇溶解,超声至完全溶解后,放置至恢复室温,用甲醇稀释至刻度,用0.45 μm孔径滤膜过滤,收集滤液备用。
1.3.3 进样分析 按前文所述的仪器条件运行液相色谱仪,待仪器完全稳定,既基线平稳且无明显波动,且连续2次进样的标准溶液苯氧威(噻嗪酮)响应值变化<1.5%后,进行样品的测定。按照标准溶液、试样溶液、试样溶液、标准溶液的顺序检测苯氧威和噻嗪酮的含量。
1.3.4 结果计算 利用工作站对苯氧威(噻嗪酮)积分,并分别将标准溶液和试样溶液的峰面积平均,待测样中苯氧威(噻嗪酮)的质量分数ω(%)的计算公式如下:
式中:A1为苯氧威(噻嗪酮)标准溶液峰面积平均值;A2为苯氧威(噻嗪酮)试样溶液峰面积平均值;m1为称取苯氧威(噻嗪酮)标准品的质量,g;m2为称取苯氧威(噻嗪酮)待测样品的质量,g;ωs为标准品中苯氧威(噻嗪酮)的纯度,%。
2 结果与讨论
2.1 流动相和检测波长的选择 本文优化了检测体系的流动相比例和检测波长。试验采用甲醇+水体系作为流动相,经优化发现当甲醇+水的比例为80+20时,苯氧威和噻嗪酮能够很好地分离,且无杂质干扰,保留时间适中,因此选择该比例为试验的流动相。采用二极管阵列检测器(DAD)在190~400 nm吸收波长范围内观察苯氧威和噻嗪酮的紫外吸收曲线,扫描结果(图2),从图可知苯氧威的最大吸收波长约在202 nm,次大吸收在228 nm,噻嗪酮最大吸收约在202 nm,次大吸收在在244 nm。由于在202 nm附近有紫外吸收的成分较多,容易出现杂质干扰,结合样品中各组分的含量、出峰峰形及干扰峰情况,最终选择230 nm为该方法的检测波长。

图2 苯氧威+噻嗪酮的紫外吸收光谱图
2.2 分析方法特异性 试验分别对苯氧威·噻嗪酮混合标样和制剂样品中苯氧威和噻嗪酮的纯度进行检测,采用HPLC-DAD 峰纯度分析法来鉴别苯氧威和噻嗪酮(样品中苯氧威和噻嗪酮的纯度图(图3、4)。试验结果显示混合标准溶液中苯氧威和噻嗪酮的纯度分别为993.470和999.922,样品中苯氧威和噻嗪酮的纯度分别为991.022和999.986,峰纯度结果均>990,有效成分出无其他物质干扰,符合定量分析要求。

图3 苯氧威·噻嗪酮悬浮剂样品中苯氧威的HPLC-DAD峰纯度色谱图

图4 苯氧威·噻嗪酮悬浮剂样品中噻嗪酮的HPLC-DAD峰纯度色谱图
2.3 非分析物干扰 用以上方法分别对空白样品、苯氧威原药和噻嗪酮原药进行色谱分析结果(图5),由图可知空白样品在苯氧威和噻嗪酮的出峰位置无干扰峰,苯氧威原药与噻嗪酮原药之间互相没有其他未分离物质的干扰。
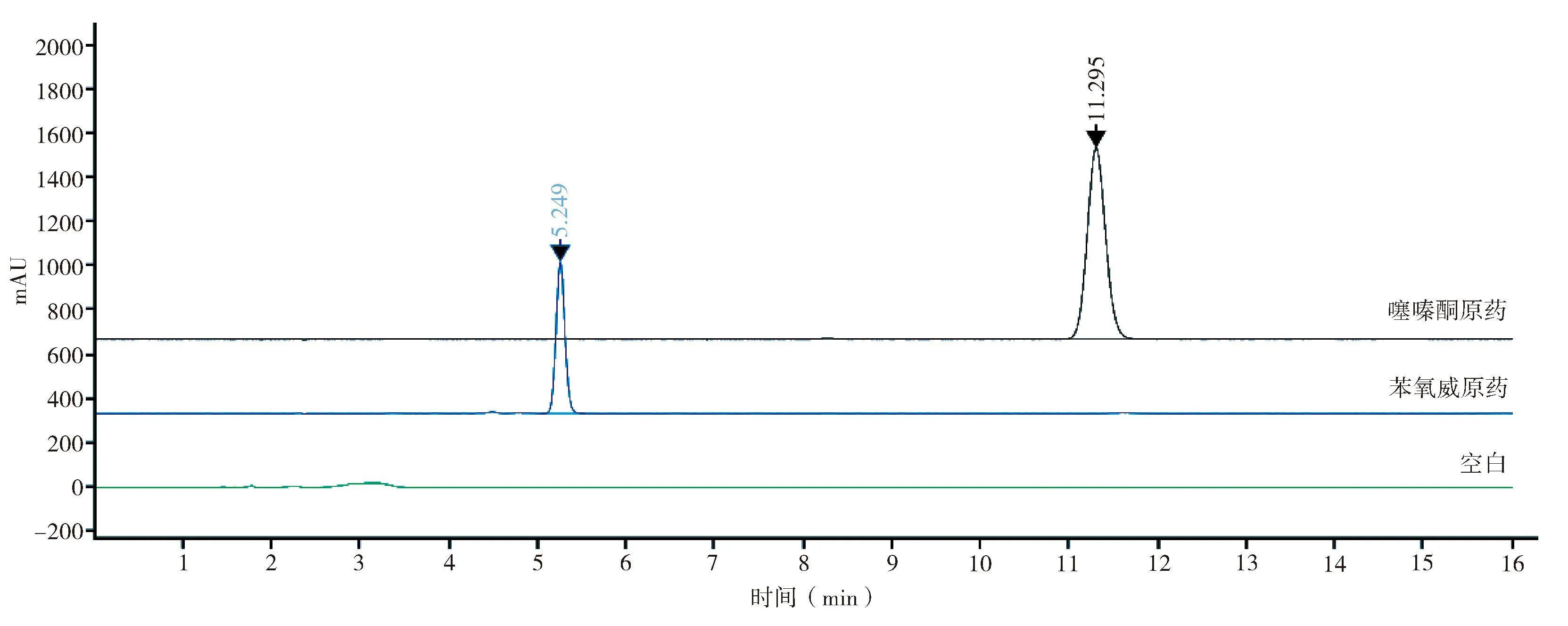
图5 非分析物干扰
2.4 分析方法的线性相关性 配制一系列不同浓度的标准溶液,苯氧威标准溶液浓度分别为0.188 1、0.408 2、0.592 4 、0.913 8、1.881 0 mg/mL,噻嗪酮浓度分别为0.623 7、1.927 5、2.346 3、2.924 0、5.316 3 mg/mL,分别对苯氧威(噻嗪酮)的进行检测。以苯氧威(噻嗪酮)的质量浓度为横坐标,峰面积为纵坐标,分别拟合线性回归方程并作线性相关图,所得结果(图6),在给定质量浓度范围内,苯氧威和噻嗪酮的质量浓度与峰面积均呈良好的线性关系。苯氧威的线性方程为Y=9 015.9X-132.2,相关系数(R2)为0.999 5;噻嗪酮的线性方程为Y=5 275.4X+170.04,相关系数(R2)为0.999 7。
2.5 分析方法精密度 对同一25%苯氧威·噻嗪酮悬浮剂样品按照本方法进行5次平行测定,计算苯氧威和噻嗪酮的质量分数,用以考察方法的精密度,试验结果(表1)。由表可见,苯氧威的标准偏差为0.002 3,变异系数为0.044%,噻嗪酮的标准偏差为0.005 2,变异系数为0.025%,该结果明显低于horwitz公式计算的理论变异系数,证明该方法的精密度符合检测要求。

表1 方法精密度数据表
2.6 方法准确度 称取一定量的悬浮剂空白样品5份,分别加入一定量的苯氧威和噻嗪酮标准品,混匀配置成试验样品,按照前文所述方法检测溶液中苯氧威和噻嗪酮的含量,计算回收率,结果(表2)。由表可知,将该方法用于测定苯氧威和噻嗪酮悬浮剂的平均回收率分别为100.03%和100.08%,符合CIPAC的基本要求。
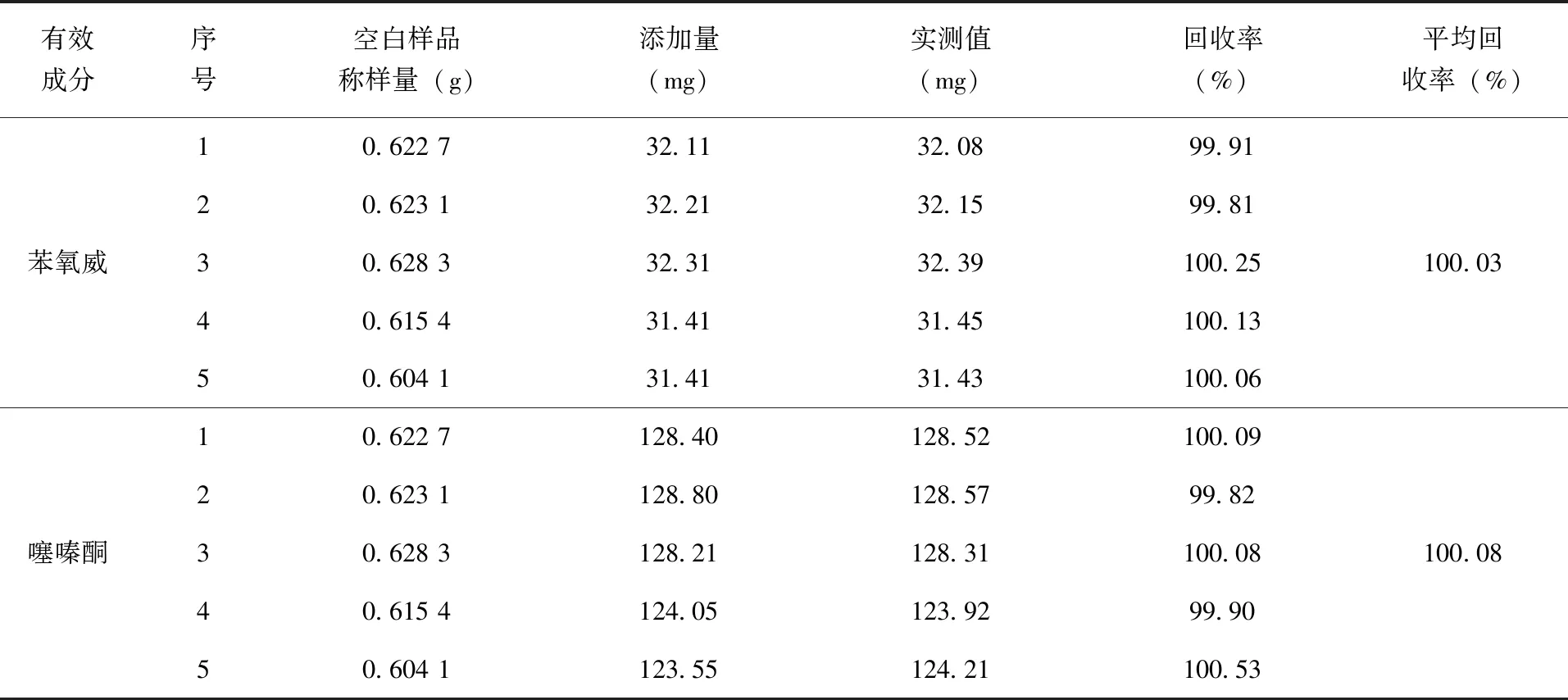
表2 方法准确度数据表
3 结论
实验结果表明,将本方法用于苯氧威和噻嗪酮悬浮剂中有效成分含量的测定,重现性好,准确度高,线性关系良好,具有简便、快速、准确及分离效果好的优点,是此类产品的质量控制有效可行的检测方法。
