基于MRI 影像组学模型预测肺癌脑转移瘤EGFR基因突变
2024-04-12李保勋彭雨琴覃尉峰肖芳黎浩江陈俊伟李佳凝胡芷瑄毛家骥沈君
李保勋,彭雨琴,覃尉峰,肖芳,黎浩江,陈俊伟,李佳凝,胡芷瑄,毛家骥,沈君*
0 引言
脑转移瘤是最常见的颅内恶性肿瘤[1-2],其发生率是颅内原发恶性脑肿瘤的10倍[3],且发病率随着影像检查手段的发展与患者生存期的延长仍在持续上升[4]。肺癌是脑转移瘤最常见的原发肿瘤来源[5]。肺癌脑转移患者预后很差,接受放疗、化疗、手术治疗等常规疗法后的无进展生存期为4~5个月[6-7]、总生存期仅为4~15 个月[8]。针对存在表皮生长因子受体(epidermal growth factor receptor, EGFR)基因突变的肺癌脑转移患者,采用表皮生长因子受体酪氨酸激酶抑制剂(epidermal growth factor receptor-tyrosine kinase inhibitor, EGFR-TKI)进行靶向治疗能够显著改善患者的预后及生存[9-11],将患者无进展生存期延长至10.0~16.5 个月[6,12],总生存期延长至25 个月[13]。然而,明确脑转移瘤的EGFR 基因突变状态需要对脑转移瘤进行活检或手术切除后病理学检测,这对患者创伤很大,可能会导致术后出血、肺栓塞和脑脊液漏等严重并发症[14-15]。另一种替代方案是直接根据肺癌原发灶的EGFR 基因突变状态判断脑转移瘤的EGFR 基因突变状态。然而,既往研究发现,高达63%肺癌原发灶与脑转移瘤之间的EGFR 基因突变状态并不一致[16-18]。目前有数项利用头颅MRI 图像的人工智能手段预测肺癌脑转移瘤EGFR 基因突变状态的研究,但是部分研究默认脑转移瘤EGFR 基因突变状态与肺癌的EGFR 基因突变状态一致,并未对脑转移瘤进行基因检测[19-20],这将极大地影响模型构建的准确性。还有部分研究为单中心研究,没有对模型进行外部测试[21-22],导致模型的泛化能力存疑。如何无创、精准预测肺癌脑转移瘤的EGFR 基因突变状态,对于筛选EGFR-TKI 靶向治疗的潜在受益患者,改善肺癌脑转移瘤患者的预后具有重要价值,仍有待进一步研究。本研究旨在开发和验证基于肺癌脑转移瘤多参数MRI 影像组学预测模型,探索模型在无创预测肺癌脑转移瘤EGFR 基因突变状态的价值,为肺癌脑转移患者提供个体化治疗管理。
1 材料与方法
1.1 研究对象
本研究为多中心回顾性研究,本研究遵循《赫尔辛基宣言》对伦理学的要求,经中山大学孙逸仙纪念医院医学伦理委员会、中国科学技术大学附属第一医院(安徽省立医院)医学研究伦理委员会和中山大学肿瘤防治中心伦理委员会批准,免除受试者知情同意,批准文号:SYSKY-2022-314-01、2022-RE-283、B2002-520-01。回顾性分析2016 年12 月至2021 年10 月在中山大学孙逸仙纪念医院、中山大学肿瘤防治中心、安徽省立医院接收诊治的肺癌脑转移患者临床及影像资料。纳入标准:(1)原发肿瘤经手术或活检病理证实为肺癌;(2)脑肿瘤经手术病理证实为肺癌脑转移瘤;(3)脑转移瘤进行了EGFR基因学检测;(4)在脑转移瘤手术前2 周内进行了头颅MRI 检查,包括T2WI 及增强T1WI(contrast enhanced T1WI, CE-T1WI)图像。排除标准:(1)患者临床、病理或影像资料不全;(2)既往存在其他恶性肿瘤;(3)由于运动伪影导致MRI图像质量差。最终纳入103例肺癌脑转移患者,共118个脑转移瘤,以中山大学肿瘤防治中心和安徽省立医院80 例患者为训练集,共89 个脑转移瘤(EGFR突变型49个,EGFR野生型40个),中山大学孙逸仙纪念医院23 例患者为测试集,共29 个脑转移瘤(EGFR突变型23个,EGFR野生型6个)。
1.2 EGFR检测方法
采用突变扩增系统(amplification refractory mutation system, ARMS)和第二代DNA 测序技术(next-generation sequencing, NGS)对脑转移瘤组织病理切片进行EGFR基因突变状态检测。
1.3 仪器与方法
中山大学孙逸仙纪念医院入组患者检查设备采用Philips Intera 1.5 T(荷兰)、Philips Achieva 3.0 T(荷兰)、Siemens Avanto 1.5 T(德国)磁共振扫描仪,安徽省立医院入组患者检查设备采用Philips Achieva 3.0 T(荷兰)、Genetic electric Discover 750w 3.0 T(美国)、Siemens Avanto 1.5 T(德国),中山大学肿瘤防治中心入组患者检查设备采用Philips Achieva 3.0 T(荷兰)、Siemens Triotim 3.0 T(德国)、Siemens Prisma 3.0 T(德国)、Genetic electric Discover 750w 3.0 T(美国)、Genetic electric Signa HDxt 3.0 T(美国)、United imaging uMR 790 3.0 T(中国)。中山大学孙逸仙纪念医院扫描序列及参数:CE-T1WI(TR 260 ms,TE 6 ms,矩阵480×480,FOV 230 mm×230 mm);T2WI(TR 3 000 ms,TE 105 ms,矩阵672×672,FOV 230 mm×230 mm)。安徽省立医院扫描序列及参数:CE-T1WI(TR 250 ms,TE 2.3 ms,矩阵512×512,FOV 230 mm×230 mm);T2WI(TR 3 280 ms,TE 80 ms,矩阵672×672,FOV 240 mm×240 mm)。中山大学肿瘤防治中心扫描序列及参数:CE-T1WI(TR 270 ms,TE 2.5、105 ms,矩 阵480×480,FOV 210 mm×210 mm);T2WI(TR 4 000 ms,TE 100、105 ms,矩阵352×352,FOV 220 mm×220 mm)。扫描层厚均为5.0 mm,层间距均为1.0 mm。采用的对比剂包括钆双胺注射液(欧乃影,通用电气药业有限公司,美国)、钆喷酸葡胺注射液(马根维显,拜耳医药保健有限公司,德国)、钆喷酸葡胺注射液(广州康臣药业有限公司,中国)和钆布醇注射液(加乐显,拜耳医药保健有限公司,德国),使用高压注射器经肘正中静脉注射对比剂,注射剂量0.2 mL/kg(0.1 mmol/kg),注射速率2.5 mL/s,5 min 后采集CE-T1WI图像。
1.4 临床资料收集及影像特征分析
通过电子病历系统获取患者临床资料,包括患者年龄、性别、肺癌病理类型。通过患者影像报告获取患者影像特征,包括脑转移瘤数目、脑转移瘤直径。当脑转移瘤数目≥2时记为多发。
1.5 图像感兴趣区勾画
头颅MRI图像均从各中心的影像归档和通信系统(picture archiving and communication system, PACS)导出,图像数据以DICOM 格式保存。将数据导入ITK-SNAP 3.6.0 软件,使用Elastix 软件(http://elastix.isi.uu.nl/)对T2WI 和CE-T1WI 图像进行配准。由具有3年神经影像诊断的放射科住院医师(医师1)在不知患者临床资料的情况下在CE-T1WI图像横断位上逐层沿脑转移瘤强化边缘勾画脑转移瘤感兴趣体积(volume of interest, VOI)并标注,将基于CE-T1WI图像勾画的脑转移瘤VOI 复制并与T2WI 图像的脑转移瘤配准,获得基于T2WI 图像的脑转移瘤VOI。两周后,医师1 随机选择数据集中30 个脑转移瘤进行勾画并标注,由具有11 年神经影像诊断的放射科副主任医师(医师2)采用相同的方法对该30 个脑转移瘤进行勾画并标注。脑转移瘤VOI 勾画示意图如图1所示。
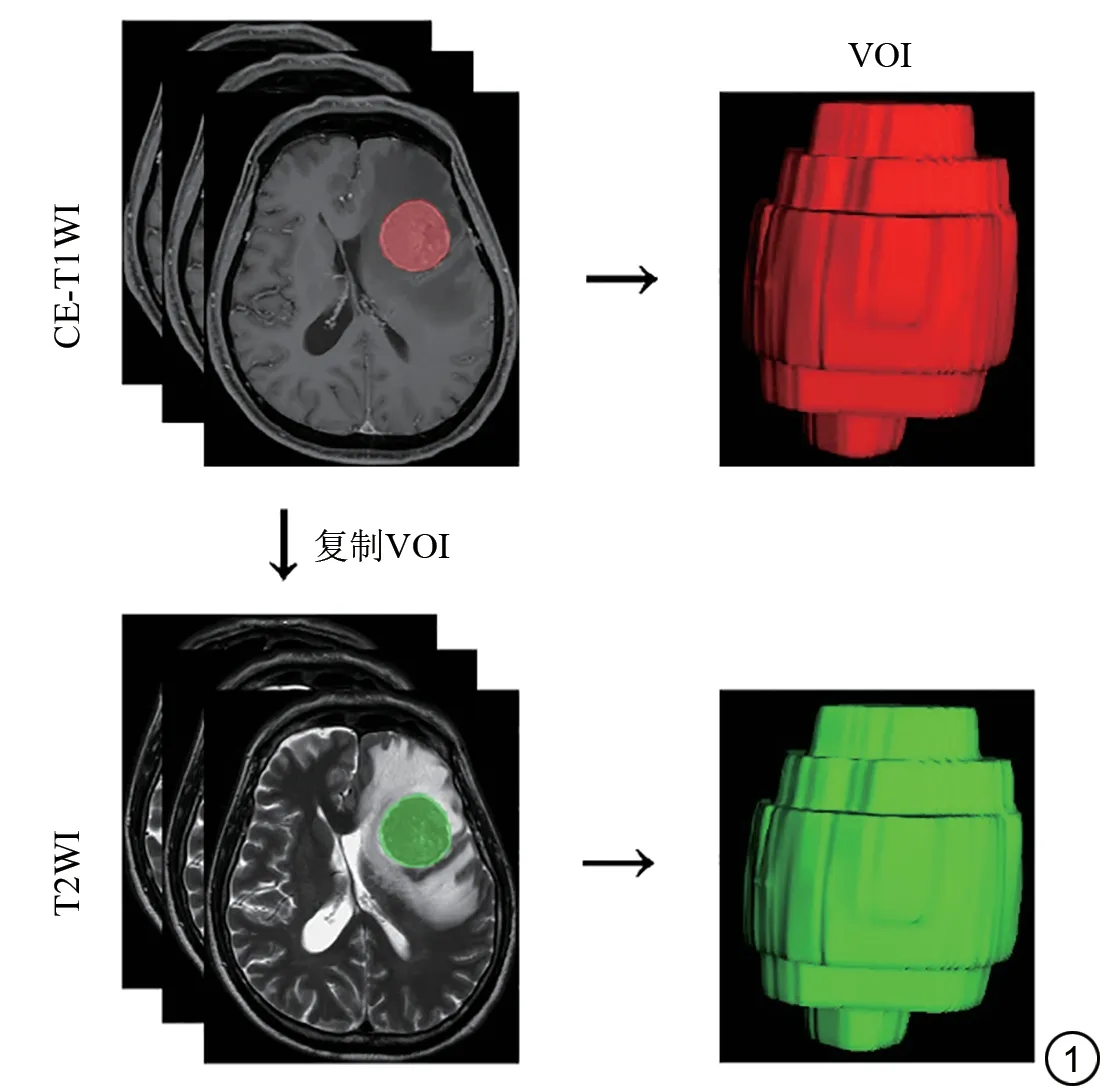
图1 脑转移瘤感兴趣体积勾画示意图。CE-T1WI:增强T1WI;VOI:感兴趣体积。Fig.1 Schematic diagram of volume of interest selection.CE-T1WI:contrast enhanced T1WI; VOI: volume of interest.
1.6 图像预处理及影像组学特征提取
首先采用N4ITK 偏差校正算法,消除不同磁共振扫描仪可能存在的非生物差异,以实现图像强度的标准正态分布。然后对所有图像进行1 mm×1 mm×1 mm 体素重采样,保证在提取三维特征时保持所有方向的均匀缩放。使用HD-BET 工具剔除颅骨后[23],采用Z-score 算法对图像强度进行归一化处理。使用Python 3.8.3 编写的开源PyRadiomics 3.0.1 软件包对图像进行影像组学特征提取。影像组学特征包括306个一阶特征,14个形态特征,1 275个二阶及高阶纹理特征,每位患者共提取3 190 个影像组学特征。
1.7 特征筛选及建模
计算医师自身(医师1 第一次勾画与医师1 第二次勾画)与两名医师间(医师1 第二次勾画与医师2 第一次勾画)影像组学特征的组内相关系数(intra-class correlation coefficient, ICC),保留ICC>0.75的特征。然后采用最大相关最小冗余(maximum relevance minimum redundancy, mRMR)算法对特征进行降维。随后,采用最小绝对收缩和选择算子(least absolute shrinkage and selection operator,LASSO)-logistics回归算法联合5 折交叉验证方法筛选出具有预测EGFR 基因突变状态价值的特征并进行建模。根据最终筛选所得特征及其系数加权求和计算影像组学评分(radiomics score, Rad-score)。
1.8 统计学分析
估算影像组学模型构建所需样本量,根据隋莲玉等[19]的研究,将预计曲线下面积(area under the curve, AUC)设置为0.823,并且设置犯Ⅰ类错误的概率不超过5%,犯Ⅱ类错误的概率不超过10%,假阳性率的下界设置为0,假阳性率的上界设置为1,EGFR 突变型与野生型脑转移瘤的样本量比例设置为1∶1,根据PASS 15 软件样本量估算的结果,总计需要纳入30 个脑转移瘤,其中15 个EGFR 突变型脑转移瘤,15个EGFR野生型脑转移瘤。统计学分析采用SPSS 26.0及R 4.2.2软件进行分析。使用ICC描述VOI勾画结果的一致性,ICC>0.75表示特征具有良好的一致性。符合正态分布的计量资料采用均数±标准差表示,采用独立样本t检验对组间差异进行评估,不符合正态分布的定量资料采用中位数(上四分位数,下四分位数)表示,采用Mann-WhitneyU检验对组间差异进行评估,定性资料采用卡方检验及Fisher精确检验对组间差异进行评估。采用受试者工作特征(receiver operating characteristic, ROC)曲线的AUC评价影像组学模型对EGFR 基因突变状态的预测效能。采用校准曲线和Hosmer-Lemeshow(HL)检验评价模型校准度。采用决策曲线(decision curve analysis,DCA)对预测EGFR基因突变状态不同阈值概率下的净获益进行量化,评估预测模型的临床应用价值。P<0.05认为差异有统计学意义。
2 结果
2.1 患者临床资料及影像特征分析
本研究最终纳入103例患者,共118个脑转移瘤病灶,其中训练集肺腺癌患者79 例,小细胞肺癌患者1例;测试集肺腺癌患者17例,小细胞肺癌患者3例,肺鳞癌患者3例。训练集和测试集的年龄、性别、病理类型、脑转移瘤数目、脑转移瘤直径在EGFR突变型及野生型组间差异均无统计学意义(P>0.05),详见表1。
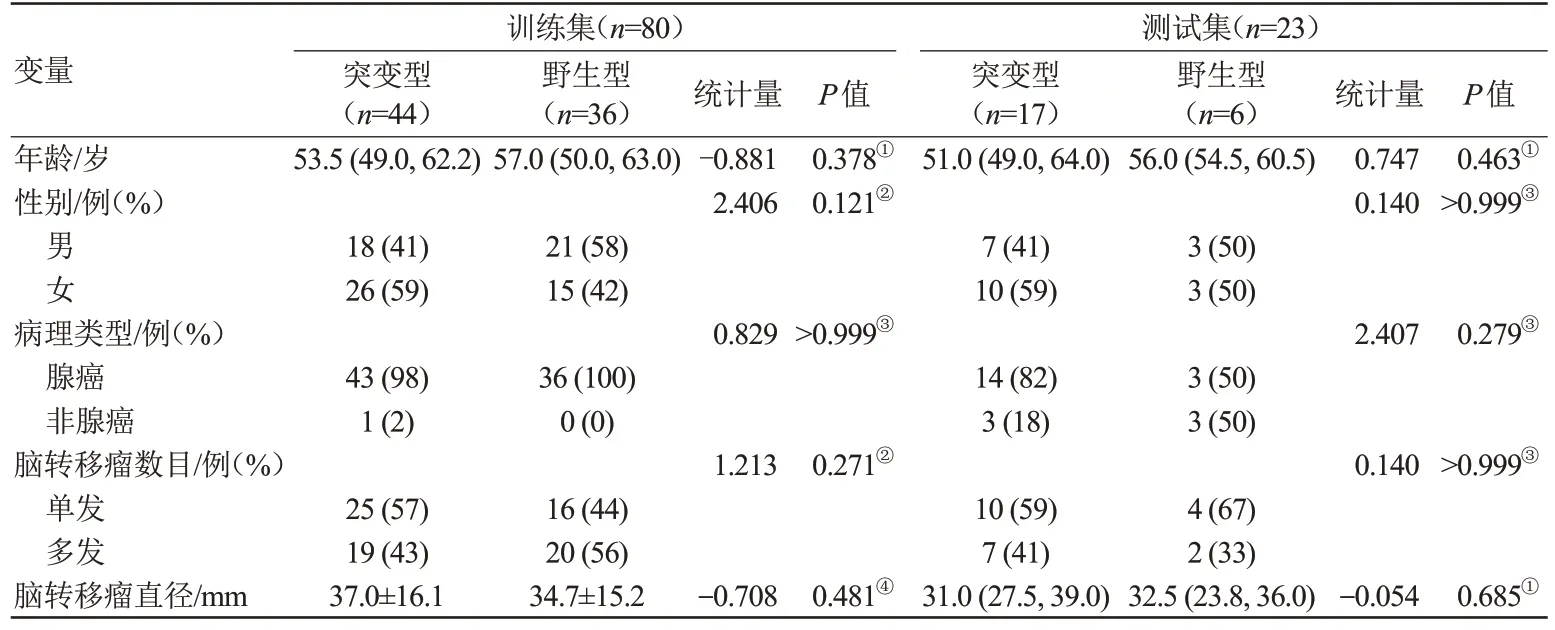
表1 肺癌脑转移患者基本临床资料及影像特征Tab.1 Clinical characteristics and MRI features of lung cancer patients with brain metastases
2.2 影像组学模型分析
每位患者在T2WI 及CE-T1WI 图像上共提取3 190个影像组学特征,这些影像组学特征的医师内部及医师之间ICC分别为0.798~0.981、0.776~0.961。对训练集影像组学特征进行mRMR 及LASSO-logistics回归分析筛选出9个影像组学特征并构建模型,筛选出的影像组学特征包括了基于CE-T1WI序列筛选出4 个组学特征和基于T2WI 序列筛选出5 个组学特征。LASSO 回归分析过程如图2 所示。通过对最终筛选所得特征及其系数加权求和计算Rad-score,计算公式见式(1)。

图2 影像组学特征筛选示意图。黑色虚线定义为最佳λ,通过5折交叉验证方法筛选出9个系数非0的影像组学特征。AUC:曲线下面积。Fig.2 Illustration of radiomics feature selection.The black dotted line is defined as the optimal λ, and 9 radiomics features with non-zero coefficients are selected by the 5-fold cross-validation via minimum criteria.AUC: area under the curve.
训练集及验证集中每例肺癌脑转移患者的Rad-score如图3所示。
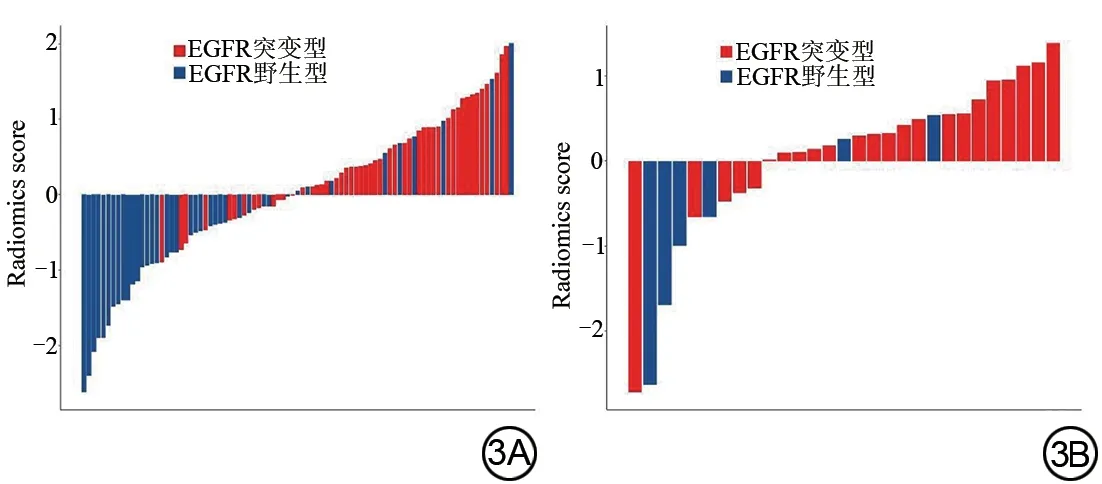
图3 训练集(3A)及测试集(3B)中肺癌脑转移患者的Rad-score。EGFR:表皮生长因子受体。Fig.3 The radiomics score of lung cancer patients with brain metastases in the training (3A) and test (3B) sets.EGFR: epidermal growth factor receptor.
2.3 影像组学模型的预测效能分析
影像组学模型的预测效能如图4所示。影像组学模型在训练集中预测EGFR 基因突变状态的AUC 值为0.828,准确度为76.4%,敏感度为81.6%,特异度为70.0%。影像组学模型在测试集中预测EGFR基因突变状态的AUC值为0.783,准确度为82.8%,敏感度为95.7%,特异度为33.3%。通过校准曲线验证模型效能,组学模型训练集和测试集的校准曲线显示EGFR基因突变状态的预测概率与实际概率具有较好的一致性(HL>0.05),组学模型具有较好的校准度(图5A)。临床决策曲线显示组学模型在13.8%~87.2%的阈值范围内具有较强的临床适用性(图5B)。
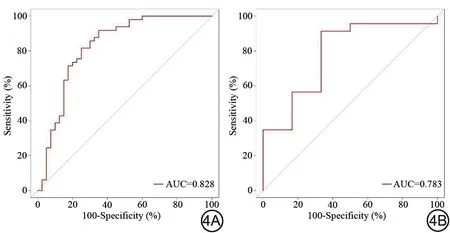
图4 训练集(4A)及测试集(4B)组学模型的受试者工作特征(ROC)曲线及曲线下面积(AUC)。Fig.4 The receiver operating characteristic (ROC) curve and the area under the curve (AUC) of the radiomics model in the training (4A) and test (4B) sets.
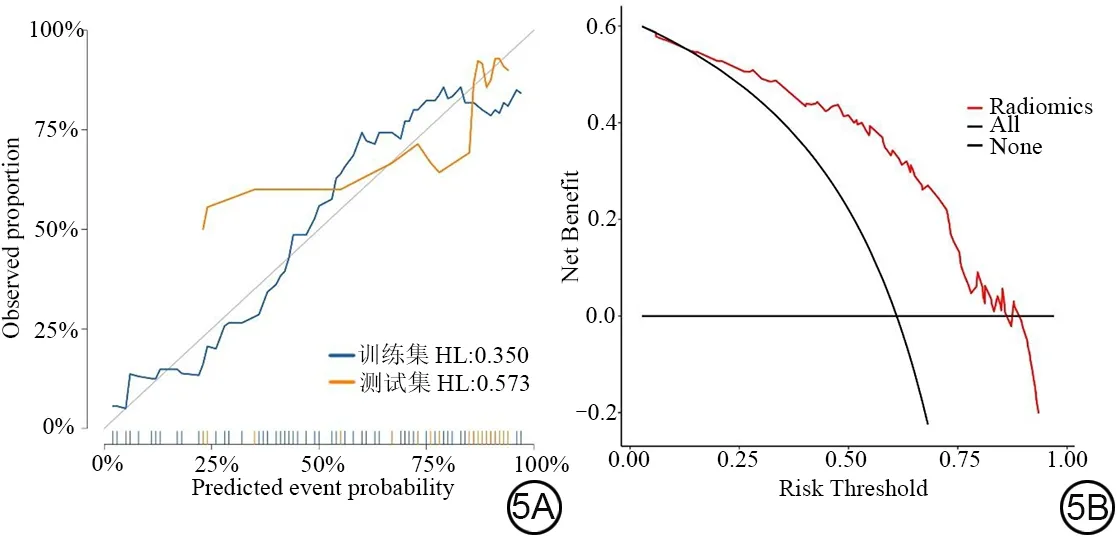
图5 组学模型的校准曲线(5A)和临床决策曲线(5B)。HL:Hosmer-Lemeshow检验。Fig.5 The calibration curve (5A) and decision curve analysis (5B) of the radiomics model.HL: Hosmer-Lemeshow test.
3 讨论
本研究为多中心回顾性研究,基于MRI T2WI及CE-T1WI 图像提取了3 190 个影像组学特征,采用mRMR 和LASSO-logistics 回归算法筛选出9 个影像组学特征并构建模型,并通过外部测试集验证模型的预测效能,明确了该模型在预测脑转移瘤EGFR基因突变情况的价值。研究结果表明,该模型可以良好地区分EGFR突变型与野生型的脑转移瘤,可成为肺癌脑转移患者脑转移瘤EGFR 基因突变状态的无创评估手段。
3.1 无创预测肺癌脑转移瘤EGFR基因突变状态的重要意义
EGFR-TKI在治疗EGFR突变型的肺癌脑转移患者领域取得了令人瞩目的效果[24-26],及时、准确地判断肺癌脑转移瘤EGFR基因突变状态对患者后续制订个性化治疗方案至关重要[27-29]。目前在临床上通常需要对脑转移瘤进行侵入性活检或手术切除才能明确脑转移瘤的基因突变状态,但是侵入性检查可能会导致术后出血、脑脊液漏等严重并发症,对于部分无法耐受手术的患者,难以获得准确的脑转移瘤EGFR基因突变状态。本研究构建的影像组学模型预测EGFR突变型脑转移瘤的准确率达到86.1%,取得了良好的预测效能。因此,本研究为无创预测肺癌脑转移瘤的EGFR 基因突变状态,筛选EGFR-TKI 靶向治疗的潜在受益患者提供了有力工具,对于改善肺癌脑转移瘤患者的预后具有重要价值。
3.2 基于头颅MRI 无创预测脑转移瘤EGFR 基因突变状态的研究
本研究开发的影像组学模型是根据多中心数据构建并验证,为了获得准确的脑转移瘤EGFR基因突变状态,本研究纳入的患者均接受了肺癌脑转移瘤手术切除并进行基因检测,为脑转移瘤本身的EGFR基因突变状态提供了精确的数据,保证了本研究构建模型的可靠性。此外,本研究纳入了所有病理类型的肺癌患者,增加了预测模型在不同病理亚型肺癌脑转移瘤中的泛用性。
既往亦有一些利用头颅MRI无创预测脑转移瘤EGFR基因突变状态的研究。隋莲玉等[19]从146例肺腺癌患者脑转移瘤的CE-T1WI、FLAIR和扩散加权成像(diffusion weighted imaging, DWI)图像提取影像组学特征,采用多因素逐步回归方法构建模型,其中多序列组合模型效能最高,验证集AUC为0.823。CHEN等[20]从110 例肺癌患者脑转移瘤的T2WI-FLAIR 和CE-T1WI 图像提取影像组学特征,采用随机森林的方法构建模型,预测EGFR 基因突变状态的AUC 为0.912。然而,以上两项研究均为单中心研究,缺乏对模型的外部测试,构建模型的泛化能力及对于其他数据集的应用效能难以确定。
WANG 等[21]从52 例肺腺癌患者脑转移瘤的CE-T1WI、T2WI、T2WI-FLAIR和DWI图像提取影像组学特征并构建模型,其中T2-FLAIR 模型效能最好,测试集AUC 值为0.871。JUNG 等[22]通过对74 例肺癌患者脑转移瘤的最小ADC 值与标准化ADC 值的比值预测肺癌脑转移瘤的基因突变状态。以上两项研究均只检测了肺癌原发灶的基因突变状态,并假设肺癌原发灶与脑转移瘤的基因突变状态一致。既往有研究[30-31]表明,高达63%的原发性肺癌和脑转移瘤的基因突变状态并不一致,这可能会极大地影响以上两项研究构建模型的准确性。
3.3 本研究的局限性
本研究具有以下局限性:(1)本研究为回顾性研究,可能会导致选择偏倚;(2)本研究的样本量相对较小,尤其是非肺腺癌脑转移瘤的患者较少,模型的效能需要更大样本量的数据集进行验证;(3)由于部分中心并未将DWI检查作为脑转移瘤的常规检查项目,因此本研究仅从T2WI 及CE-T1WI 图像中提取了影像组学特征。未来将基于DWI提取的影像组学特征纳入预测模型,这可能会进一步提高模型的预测能力。
4 结论
综上所述,基于T2WI 及CE-T1WI MRI 影像组学特征构建的影像组学模型在预测肺癌患者脑转移瘤EGFR基因突变状态中具有较高的预测效能,为肺癌脑转移瘤患者提供一种无创评估脑转移瘤EGFR基因状态的方法,为肺癌脑转移瘤患者个体化治疗方案的选择及临床医生的决策提供科学依据。
作者利益冲突声明:全体作者均声明无利益冲突。
作者贡献声明:沈君设计本研究方案,对稿件重要的智力内容进行了修改并最后定稿,获得了国家自然科学基金项目资助;李保勋起草和撰写稿件,勾画图像VOI并提取影像组学特征,获取、分析和解释本研究的数据;彭雨琴、覃尉峰、肖芳、黎浩江、陈俊伟、李佳凝、胡芷瑄获取、分析或解释本研究的数据,对稿件重要的智力内容进行了修改;毛家骥勾画图像VOI,分析及解释本研究的数据,对稿件重要的智力内容进行了修改;全体作者都同意发表最后的修改稿,同意对本研究的所有方面负责,确保本研究的准确性和诚信。
