前列腺癌诊断及预后评估中MRI影像组学的应用分析
2024-03-20黄惠娟福建省漳州市医院影像科福建漳州363000
黄惠娟 福建省漳州市医院影像科 (福建 漳州 363000)
内容提要: 目的:分析应用MRI影像组学诊断和预后评估前列腺癌的技术要点和临床价值。方法:选取2021年1月~2022年12月疑似前列腺癌患者120例,采用MRI影像组学方法和病理检查,提取影像纹理特征和构建模型,分析病理检查结果、主要纹理特征,评价模型应用价值。结果:病理检查显示,前列腺癌61例,前列腺增生59例;影像纹理特征显示,共6类1129个;模型分析显示,前列腺病灶预测模型应用效能良好,训练组AUC 0.87,95%可信任区间(0.72~1.00),敏感度81.0%,特异度90.0%,模型准确率100.0%,阳性预测值100.0%,阴性预测值85.00%,验证组AUC 0.98,95%可信任区间(0.93~1.00),敏感度85.0%,特异度85.0%,模型准确率85.0%,阳性预测值85.0%,阴性预测值85.0%。结论:MRI影像组学可辅助医师有效检出前列腺病变,促进病灶识别,以ADC图像为基础确定影像组学特征搭建模型,可比较准确地判别前列腺癌与前列腺增生,指导临床医师科学治疗疾病。
前列腺癌属于上皮性恶性肿瘤,发病位置为前列腺区域,在泌尿系统恶性肿瘤中具有高发性,中老年发病率高于其他年龄段,严重威胁男性生命安全[1]。活检进行病理学分析是局限性前列腺癌的主要危险分层方法,但是前列腺解剖结构复杂,病理组织采集受限,取样部位不同较易影响活检结果。前列腺癌病变形态具有空间异质性,随机活检病理分级准确度较低,影像学靶向活检可显著降低误诊率[2]。DWI等常规磁共振检查时,前列腺增生可能误诊为前列腺癌,导致诊断结果不准确。进行MRI影像组学研究,联合抗体偶联药物(antibody-drug conjugate,ADC)等定量分析前列腺区域病灶,有利于提高前列腺癌诊断准确性[3]。本文从2021年1月~2022年12月接诊的疑似前列腺癌患者中选取120例,说明MRI影像组学方法,分析应用价值。
1.资料与方法
1.1 临床资料
选取2021年1月~2022年12月120例疑似前列腺癌病例,年龄49~84岁,平均(63.04±9.10)岁。
纳入标准:①直肠指检显示前列腺增大,无显著中间沟,患者出现尿频、急性尿潴留、排尿困难、血尿或者膀胱刺激征等临床表现;②实施前列腺区域MRI T2WI、DWI、T1WI和DCE检查;③MRI检查后1个月内实施穿刺活检;④患者及家属知情同意。
排除标准:①MRI检查前前列腺区域穿刺史;②内分泌治疗史;③放射性治疗史;④认知功能异常;⑤精神、智力障碍;⑥资料不全。
1.2 方法
1.2.1 常规MRI检查
全部患者实施前列腺常规MRI扫查,其中DWI为轴位单次激发平面回波序列扫描。参数设置见表1。
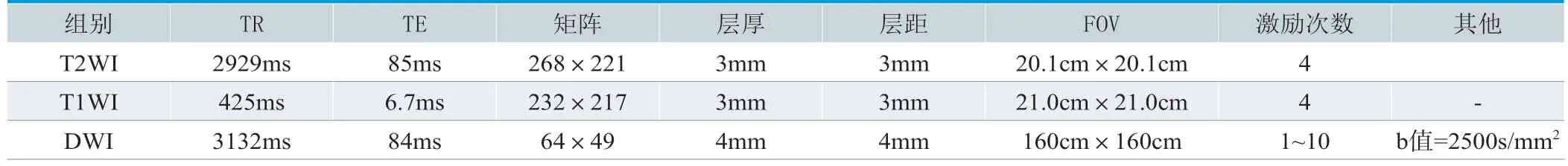
表1.MRI前列腺扫查参数
1.2.2 图像分析
使用PACS系统导出患者MRI影像,资料格式设置为DICOM。两位高年资泌尿系统影像科医师分别阅片后形成一致性意见。在ITK-Snap软件中输入ADC图,使用软件针对轴位图像手动勾画ROI曲线。勾画时,定位面积最大病灶,按照其最大层面,勾画出病灶边缘曲线。在此过程中避免覆盖血管、尿道、钙化区域、出血部位以及精囊根部。完成ROI勾画后,在A.K.软件中输入原始图像与ROI图像,然后从中提取病灶纹理特征。
1.3 观察指标
①病理检查结果:实施穿刺活检,统计病理检查结果,分析前列腺癌、前列腺增生病例数和年龄分布情况。②影像纹理特征:进行影像特征参数筛选,采用Lasso回归方法选取特征参数,并且构建生物学标志。对比前列腺癌患者和前列腺增生患者在训练组与验证组中的影像学标签。③模型分析:构建模型,获取训练组、验证组AUC值,比较两组诊断和预测准确性、阴性与阳性预测可靠性。
1.4 统计学分析
以R语言软件分析数据,回归模型降维提取影像学组特征,线性分析构建前列腺癌模型和前列腺增生模型,评价诊断准确性。对比ROI曲线下面积(即AUC数据),病灶分类效果与AUC呈正相关。
2.结果
2.1 病理检查结果
穿刺活检结果显示,120例患者中前列腺癌61例,年龄52~84岁,平均(66.27±7.40)岁;前列腺增生59例,年龄49~81岁,平均(60.12±7.26)岁。
2.2 影像纹理特征
病灶纹理特征共6类1129个,主要分为形态学特征、直方图特征、游程矩阵特征、灰度共生矩阵特征和以其为基础的Haralick特征,此外还有灰度连通区域矩阵特征。筛选影像特征参数,Lasso回归分析选择特征参数,筛选出参数后构建生物学标志。回归选择纹理参数6个,常数项系数-0.0271。分别赋予训练组和验证组影像组学标签。在训练组和验证组中,前列腺组影像学标签均高于前列腺增生组,差异有统计学意义(P<0.05),见表2。
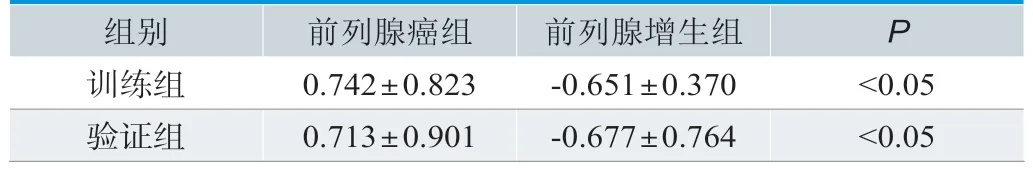
表2.影像学标签
2.3 模型分析
鉴别模型AUC、敏感度、特异度、模型准确率、阴性和阳性预测值见表3。
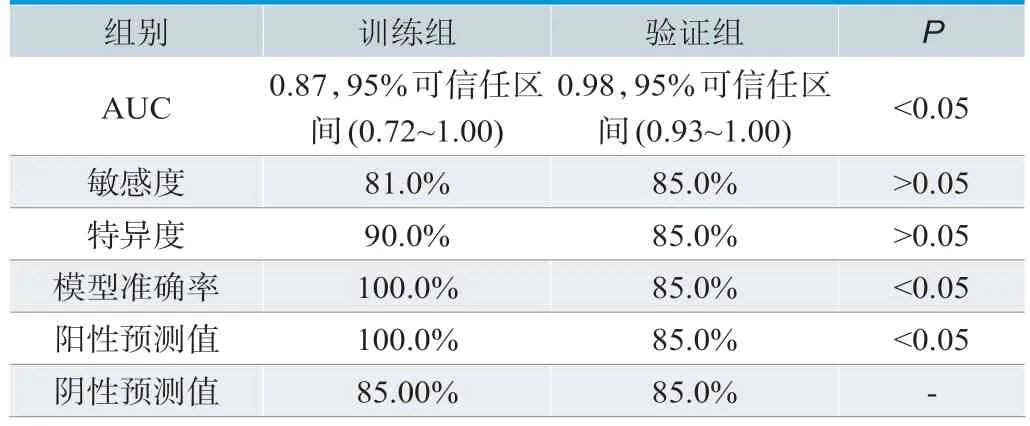
表3.模型分析结果
3.讨论
3.1 MRI影像组学的主要特点
影像组学是计算机技术与医学深度融合的产物,是先进的现代医疗技术。影像组学以临床数据为依据,分析疾病图像特征,进而分析疾病异质性。影像组学的优点是对患者无创伤,可行多次检查,而且应用成本较低。在传统MRI检查中,医师通过观察MRI图像针对检查结果做出解释,小病灶较易漏诊误诊。MRI影像组学不仅可定性疾病,而且可进行定量分析,技术方法获取的结果与传统MRI相比可靠性和精准度更高。MRI影像组学检查中,主要步骤为采集和分割MRI图像,从中提取特征信息,然后建模分析[4]。
3.2 前列腺癌诊疗和预后评估中应用MRI影像组学的价值
MRI影像组学研究利用病变区域图像纹理改变等变化,辅助医师精准分析疾病。前列腺癌MRI影像组学分析中,通过分析图像纹理提取图像像素、体素灰度值特征,提取分布状态数据以及变化趋势等,定量分析前列腺癌异质性[5]。
MRI影像组学属于新型定量分析方法,应用此种方法时,主要是深度挖掘高通量图像数据,从而对疾病结构特征进行量化描述,得出疾病的定量生物学指标。MRI影像组学方法弥补了传统MRI检查的不足。在诊断前列腺癌以及该类疾病预后评估时,MRI影像组学获取的信息更准确,应用价值更高。在此过程中,应结合临床因素分析和诊断疾病。
在诊断和预后评估前列腺癌活动中,MRI影像组学具有重要应用价值。MRI影像组学未来发展中,应积极积累临床经验,加强实践验证,进一步完善技术。在疾病预后评估中,预测模型中样本丰富性与预测准确性通常呈正相关。在MRI影像组学应用中,应统一数据获取标准,拓宽样本采集范围,完善数据库,从而提高MRI影像组学模型应用可靠性。应构建标准化工作流程,强化质量控制,提高技术可重复性。MRI影像组学分析与临床因素结合,同时充分利用医疗大数据与人工智能技术,有利于科学诊断和预后评估疾病,促进精准医疗[6]。
3.3 MRI影像组学应用方法
3.3.1 采集图像信息
在图像采集环节中,通过MRI设备扫描采集标准化图像数据,进行数据分析。图像特征分析质量受到多种因素影响,包括设备质量、参数设置科学性以及临床实践因素等。为提高结果可靠性,在采集图像时应设计执行标准化采集和重建图像方案。通过重采样、归一化预处理图像,统一像素、灰度与分辨率。采集信息构建数据库,联合前列腺肿瘤影像学检查数据库与相关医疗数据库,形成磁电流成像(Magnetic Current Imaging,MCI)图像。
根据前列腺癌临床研究需求采集影像数据,结合患者临床表现,使用标签标记获取的数据。影像组学研究要求样本量≥100个,保证样本规模有利于适度拟合。为保证科学提取图像特征,应标准化设置像素规模和层厚参数,统一图像采集设备。并且在提取图像特征前,针对图像进行标准化计算机算法处理。当层厚、图像分辨率不同时,应针对图像重采样,后续归一处理像素[7]。
3.3.2 科学分割图像
分割前列腺图像时,ROI分别选取肿瘤和前列腺腺体区域,实施分割。在图像分割环节,可采用手动、半自动与多重分割方法[8]。其中手动分割的优点是精度较高,主要是因为手动分割时影像学医师需要手动操作进行ROI勾画,通过人工手动操作可精准勾画边缘信息;缺点是效率较低,操作时间较长,适宜处理小规模数据,难以高效率处理大规模数据[9]。不仅如此,手动分割时,医师技术水平、经验、操作熟练度等均会直接影响ROI勾画效果,病灶ROI较易出现显著差异,可疑病灶识别时,医师可能做出错误判断,得出错误ROI,导致提取不准确的图像特征。在进行手动分割时,应由高年资医师操作,并且适用于小规模样本[10]。
也可在计算机算法辅助下自动分割ROI。半自动、自动分割方法应用效率较高,应用计算机算法和开源软件分割图像。自动分割显著提高了工作效率,但是自动分割较易受到图像噪声干扰,导致准确度较低[11]。应用U-Net算法等算法可提高自动分割准确性,例如,应用此种算法在前列腺T2WI图像中可自动分割前列腺轮廓,还可自动测量前列腺径线。MRI影像组学分析前列腺癌过程中,应科学选择ROI,促进精准研究[12]。
3.3.3 提取图像特征
完成ROI分割后是提取图像特征环节,提取图像特征是核心环节[13]。选择有价值的信息提取正常与异常图像。在此环节中,基于特征信息分类和预测疾病[14]。图像特征包括两类,其一是数学定量描述,主要针对病变不可见特征,包括形态学特征、一阶特征、二阶特征与高阶特征;其二是提取定性特征[15]。数学定量描述中,形态学特征描述方法是统计学数值;一阶特征也称直方图特征,含有偏差、方差、标准差等;二阶特征为病变异质性信息,利用灰度游程矩阵、灰度共生矩阵等方法使像素、体素形成合理的空间关系;高阶特征是使用拉普拉斯滤波器等提取图像特征[16]。
在此过程中,应积极提高模型鲁棒性与精准度,促进适度拟合,应从诸多特征信息中提取核心特征,核心特征信息量最丰富、应用价值最高[17]。通过算法和机器学习进行嵌入,通过MRI影像组学分析提取纹理、强度、形状等图像特征[18]。
3.3.4 建模分析
完成上述步骤后,构建分析模型。在建模环节,重点是合理选择特征,应用科学建模方法,并且在建模后验证模型[19]。综合临床数据、生物学数据、遗传信息、患者治疗史信息与影像学特征信息,数据驱动选择特征,从而保证模型具有良好效能[20]。为保证模型稳定性,应纳入多种机器学习法,全周期记录学习过程与结果信息,并且进行内部、外部验证[21]。随机森林、卷积神经网络、支持向量机是常用模型[22]。在模型效能评价中,主要方法为ROC曲线分析和评估诊断特异度、灵敏度和准确度[23]。
本次研究中,病理检查检出前列腺癌61例、前列腺增生59例,影像纹理特征6类1129个。本次研究结果表明,MRI影像组学模型预测前列腺病灶效能良好,训练组、验证组AUC值、敏感度、特异度均较好,模型准确率较高,阴性与阳性预测值较高。构建预测模型并且进行学习后,病灶鉴别模型下ROI曲线下面积较好,显示模型诊断效能较高。该结果表明,在临床诊疗前列腺癌时,可采用MRI影像组学方法,病灶分析结果准确性较好,分析结果比较科学,可准确分类病灶,指导临床治疗[24]。
综上所述,前列腺癌临床诊断中,MRI影像组学具有显著应用价值。通过MRI影像组学可挖掘标准图像的图像特征,进行定量分析,辅助医师临床诊断疾病和预测疾病未来发展趋势。应用此种方法,可提高疾病诊断准确性,促进前列腺癌科学诊断和治疗。
