酸性含锑溶液中除铜的探索与研究
2024-03-19康钦科
康钦科,刘 娜
(新邵辰州锑业有限责任公司,湖南 新邵 422900)
锑的湿法冶金自1965年在我国开始进行探索[1],但由于生产成本偏高、废水处理困难及难以规模化应用等问题,多年来一直停留在试验阶段,能够成功应用于工业生产实践的湿法炼锑工艺少之极少。新邵辰州锑业有限责任公司经过近十年的研究探索,先后进行了小型试验、连续扩大试验、工业试验及工业优化试验,开发了一套完整的高砷锑金精矿酸性湿法提锑技术,并成功实现工业化与规模化,成为行业新标杆,引领锑冶金走向绿色清洁生产之路。
采用酸性湿法提锑工艺处理高砷高硫复杂难冶的锑金精矿,有效解决了锑、砷选择性分离难题,该工艺具有流程短、能耗低、试剂消耗量少、原料适用性强、金属回收率高等优点,且避免了传统火法工艺中废气、废水、废渣的产生,为湿法炼锑技术开辟了一条新途径。但由于锑金精矿中的铜也会有少量浸出并在溶液中富集,会导致锑产品因铜元素超标影响品级,因此,采取一种能将含锑溶液中的铜离子除去的方法很有必要。
1 金属离子主要分离富集方法
金属分离根据工艺类型可以分为火法和湿法[2],在新邵辰州酸性湿法提锑工艺中选择火法除铜需要加开火法精炼,短期内无法实现。因此,主要考虑采用湿法工艺进行溶液除铜。
通过查阅相关文献[3],金属离子主要分离富集方法大致有以下几种:离子沉淀法、置换沉淀法、离子交换法、有机溶剂萃取法、共沉淀法。
1.1 离子沉淀法
离子沉淀是指溶液中的某种离子在沉淀剂的作用下,形成难溶化合物而沉淀的过程,沉淀法处理含铜废水此前也有文献报道[4],下面对新邵辰州酸性湿法提锑工艺中除铜的具体条件和情况进行分析。
1.1.1 氢氧化物沉淀法
在新邵辰州酸性湿法提锑工艺中,如果选择使用氢氧化物离子沉淀法进行铜离子的分离,可能会发生的反应见表1[3]。

表1 298K及aMez+=1时金属氢氧化物沉淀的pH值
从表1可以看出选择氢氧化物沉淀法来去除含锑溶液中的铜离子,理论上可以通过调节pH 将Sb3+、Fe3+、Cu2+、Fe2+依次沉淀出来,但在实际操作过程中却把我们所需的大量锑离子沉淀出来,反而使得工艺更加复杂了,因此,此法并不适用于酸性湿法提锑工艺含锑溶液(溶液pH<0)的除铜。
1.1.2 硫化物沉淀法
由于硫化锑在含锑溶液中的稳定性较差,很容易被氧化,结合表2可以看出来选择硫化物沉淀法来去除含锑溶液中的铜离子,不需要调节pH值、不影响溶液中原有的锑离子,就可以控制含锑溶液中的铜离子达到理想水平,非常适合酸性湿法提锑工艺含锑溶液(溶液pH<0)的除铜。

表2 某些金属硫化物在298 K时的溶度积与平衡pH值
因此,采用硫化物沉淀法进行含锑溶液的除铜研究是本试验的主要研究内容。
1.2 置换沉淀法
置换沉淀是指用较负电性的金属从溶液中取代出较正电性金属的过程。其在冶金应用中有以下两个用途:(1)用主体金属除去浸出液中的较正电性金属;(2)用较负电性的金属从浸出液中提取较正电性金属。
在新邵辰州酸性湿法提锑工艺中,电负性从大到小:Fe>Sb>Cu,可以使用金属铁将溶液中的铜置换出来[5],但同时锑离子也会被置换出来,因此选择金属锑来置换铜离子作为含锑溶液除铜的备选方案[6],我们也进行了探索。
1.3 离子交换法
离子交换法是指利用溶液通过离子交换剂(离子交换树脂)时发生在溶液和离子交换剂之间的相同符号的离子交换作用而使离子分离的方法。
各种离子交换树脂的交换能力和选择性不同,选择合适成型的离子交换剂对金属离子的分离至关重要,由于强酸性含锑溶液中的锑在pH≈1时即可发生水解,因此,要找到能将铜离子吸附除去而不影响锑离子的离子交换剂目前来说还有一定难度,且离子交换剂容易受污染或氧化失效,需要频繁再生,成本难以控制。
1.4 电解法
电解法基本原理是当电流通过电解质溶液时,溶液中的阳离子产生离子迁移和电极反应,即溶液中的阳离子向阴极迁移,并在阴极上产生还原反应,使金属沉积。
电解法处理含重金属离子溶液,是采用电能代替化学试剂去除水中的重金属离子。电解法在去除铜离子中的应用,主要应用于含铜废水的处理[7-8]。电解法处理含铜废水能直接回收金属铜,处理设备投资和经营费用均不高,管理操作简单,但在处理低浓度废水时电流效率较低,并且电解过程中含锑溶液中的锑离子也会优先于铜离子先沉积,难以实现分离。
1.5 其他方法
其他方法如萃取法、膜分离法虽然可以实现铜的分离和富集,但其分离效果受到溶液中其它离子和物质的影响较大,并且存在成本较高且分离效果难以保证的缺点。
综上所述,试验部分选用对该公司酸性湿法提锑工艺影响不大的试剂(不新增其它杂质离子)进行试验,采用离子沉淀法和置换沉淀法对含锑溶液进行除铜试验探讨。
2 试验部分
1.硫化物沉淀法:(1)准备并调试各类仪器设备,确保能正常工作;(2)取烧杯,分别向含锑溶液(生产工艺上现取溶液)加入硫化锑(锑块矿研磨后使用)、硫化钠(Na2S·9H2O)、锑硫(硫化铁混合物,研磨后使用)、硫化氢(现场制备),调节搅拌器至合适强度搅拌溶液;(3)搅拌一段时间后静置澄清过滤,取液样测铜和其它元素。反应后的渣样烘干后计量并检测铜和其它元素;(4)原含锑溶液取样检测铜和其它元素。
2.置换沉淀法:(1)准备并调试各类仪器设备,确保能正常工作;(2)称取一定量锑粉(阴极锑研磨后使用),记重,量取一定量含锑溶液。将锑粉加入含锑溶液中恒温搅拌,待反应一段时间之后过滤;(3)取液样测铜、锑。反应后的锑粉烘干后计量并检测铜、锑;(4)检测原锑粉中的锑和铜;原含锑溶液取样检测铜、锑。
3 结果与讨论
3.1 硫化物沉淀法
3.1.1 定性试验及反应时间对硫化物除铜的影响
分别使用硫化锑(块矿研磨后取-0.147 mm用于试验)、硫化钠(Na2S·9H2O)、硫化铁(锑硫研磨后取-0.147 mm用于试验)、硫化氢进行试验,硫化物用量为理论用量的50倍(含锑溶液中锑含量为50 g/L,铜含量为23.52 mg/L),反应温度为30℃,分别取反应5、10、20、30、40 min后溶液分析其铜含量,如图1所示。

图1 溶液铜沉淀率随时间变化图
从图1中可以看出,使用硫化锑(锑块矿研磨后取-0.147 mm用于试验)、硫化钠(Na2S·9H2O)除含锑溶液中的铜,除铜率可以达到95%以上,且在反应10 min左右基本完成沉淀。使用硫化氢反应40 min后的除铜率为91.41%,但硫化氢制备过程略复杂。而硫化铁(锑硫)反应40 min的除铜率只有39.33%,不适用于本体系除铜。故后续只考察硫化钠且重点考察硫化锑的试验情况。
3.1.2 硫化物用量对除铜的影响
分别使用硫化锑(锑块矿研磨后取-0.147 mm用于试验)、硫化钠(Na2S·9H2O)进行试验,硫化物用量为理论用量的10、20、30、40、50倍(含锑溶液中锑含量为50 g/L,铜含量为23.52 mg/L),反应温度为30℃,搅拌反应40 min后取溶液分析其铜含量,如图2所示。

图2 溶液铜沉淀率随沉淀剂理论用量变化图
从图2中可以看出,使用硫化锑(锑块矿研磨后取-0.147 mm用于试验)、硫化钠(Na2S·9H2O)除含锑溶液中的铜,除铜率基本相差不大,沉淀剂用量为理论用量的50倍左右,除铜率可达98%左右。考虑到硫化钠(Na2S·9H2O)在酸性体系下可能会产生一定量的H2S有毒有害气体且增加成本,工业应用难度较大,而硫化锑(锑块矿)本身可做为生产原料,在增加生产处理量的同时,又能去除溶液中的铜,更具可行性与实际操作性。故本节重点考察硫化锑在溶液中除铜的效果。
3.1.3 反应温度对硫化锑除铜的影响
使用硫化锑(锑块矿研磨后取-0.147 mm用于试验)进行温度试验,硫化物用量为理论用量的50倍(含锑溶液中锑含量为50 g/L,铜含量为23.52 mg/L),反应温度为20、30、40、50、60℃,搅拌反应40 min后取溶液分析其铜含量,如图3所示。

图3 溶液铜沉淀率随温度变化图
从图3中可以看出,使用硫化锑除含锑溶液中的铜,除铜率在试验温度范围内,无明显变化。
3.1.4 沉淀剂粒度对硫化锑除铜的影响
使用硫化锑(锑块矿研磨后取 -0.365、-0.246、-0.175、-0.147、-0.121 mm)进行粒度试验,硫化物用量为理论用量的50倍(含锑溶液中锑含量为50g/L,铜含量为23.52 mg/L),反应温度为30℃,搅拌反应40 min后取溶液分析其铜含量,如图4所示。
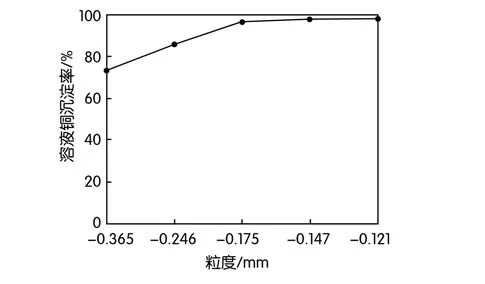
图4 溶液铜沉淀率随沉淀剂粒度变化图
从图4中可以看出,沉淀剂颗粒越细小,铜沉淀得越完全,在目粒径小于0.180 mm,铜的沉淀率能达到95%以上,但是沉淀剂颗粒越细,反应过程中的沉淀剂粉末会浮在液面影响操作。
3.2 置换沉淀法
3.2.1 反应时间对锑粉置换除铜的影响
使用锑粉(阴极锑研磨后取-0.147 mm)进行试验,锑粉用量为理论用量的10倍(含锑溶液中锑含量为50 g/L,铜含量为23.52 mg/L),反应温度为30℃,搅拌反应5、10、20、30、40 min后取溶液分析其铜含量,如图5所示。

图5 溶液铜置换随时间变化图
从图5中可以看出,使用锑粉(阴极锑研磨后取-0.147 mm用于试验)置换含锑溶液中的铜,铜置换率可以达到80%以上,开始反应速度较快,5 min置换率就可以达到70.23%,后期随着时间的增加铜置换率缓慢增加。
3.2.2 锑粉用量对置换除铜的影响
使用锑粉(阴极锑研磨后取-0.147 mm)进行试验,锑粉用量为理论用量的2、5、10、20、40倍(含锑溶液中锑含量为50 g/L,铜含量为23.52 mg/L),反应温度为30℃,搅拌反应40 min后取溶液分析其铜含量,如图6所示。
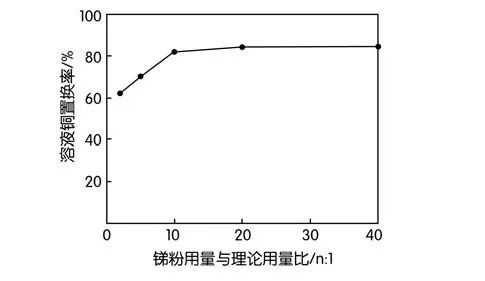
图6 锑粉理论用量对铜置换率的影响
从图6中可以看出,锑粉用量达到10倍理论值后,铜置换率受锑粉用量的影响大大减少。
3.2.3 温度对锑粉置换除铜的影响
使用阴极锑粉(研磨后取-0.147 mm用于试验)进行温度试验,锑粉用量为理论用量的10倍(含锑溶液中锑含量为50 g/L,铜含量为23.52 mg/L),反应温度为20、30、40、50、60℃,搅拌反应40 min后取溶液分析其铜含量,如图7所示。

图7 溶液铜置换率随温度变化图
从图7中可以看出,在考察条件内温度对铜置换率影响不大,且温度超过45℃以后,铜置换率还略有下降。
3.2.4 锑粉粒度对除铜的影响
使用锑粉(阴极锑研磨后取-0.365、-0.246、-0.175、-0.147、-0.121 mm)进行粒度试验,锑粉用量为理论用量的10倍(含锑溶液中锑含量为50 g/L,铜含量为23.52 mg/L),反应温度为30℃,搅拌反应40 min后取溶液分析其铜含量,如图8所示。
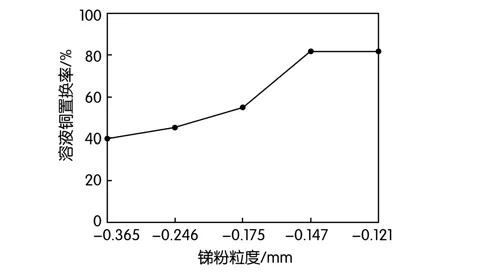
图8 溶液铜置换率随锑粉粒度变化图
从图8中可以看出,置换剂阴极锑粉的颗粒大小对铜置换率的影响较大,阴极锑粉颗粒越细小,铜置换率越高,在阴极锑粉粒径小于0.150 mm,铜的置换率能达到80%以上,但是和硫化锑沉淀法除铜一样颗粒越细,反应过程中的阴极锑粉末会浮在液面影响操作。
4 总结
从试验结果来看,硫化锑、硫化钠、锑粉都可以用来去除酸性含锑溶液中的铜离子,且不会影响原生产工艺。使用硫化物(硫化锑和硫化钠)除铜效率较高,试验中可达95%以上,铜离子可以降至1 mg/L以下。而使用阴极锑粉置换除铜效率不如硫化物,在试验条件相同的情况下,铜置换率最高不到85%,但是用量相对要少,且置换后静置沉淀的效果比硫化物沉淀法除铜操作更为理想。实际生产中,可根据溶液中铜离子的含量高低,确定采取何种方式,或者采用联合处理工艺去除含锑溶液中的铜离子。
