基于网络药理学和动物实验探讨芪遂逐水膏敷贴剂抗肝硬化腹水的作用机制
2024-03-10毛德文王明刚余钰娟宋振恒周晓云黄永林
刘 茵,邱 华,毛德文,王明刚,余钰娟,宋振恒,周晓云,黄永林
(1.广西中医药大学第一附属医院肝病科,广西 南宁 530023; 2.广西医科大学附属肿瘤医院中医科,广西 南宁 530000; 3.广西中医药大学研究生院,广西 南宁 530001)
肝硬化是一种以弥漫性纤维化、肝内静脉血流严重中断、门脉高压和肝衰竭为特征的进行性慢性肝病。当出现腹水、静脉曲张出血时,会出现失代偿性肝硬化[1],其发病率高,能诱发许多自发性腹膜炎、肝肾综合征等致命的并发症[2]。目前,治疗肝硬化腹水方法包括控制水和钠盐的摄入、利尿剂、腹腔穿刺放液配合静脉输注白蛋白、生长抑素及肝移植等,但远期疗效欠佳,且复发率高,需要巨额的医疗费用[3]。近年来,中药具有多成分、多靶点、多途径的特点,在肝病治疗中协同作用好且副作用低[4]。芪遂逐水膏由黄芪、甘遂、木香、茯苓、丹参、益母草和大腹皮组成,具有益气健脾、活血柔肝、温阳暖肾、利水消肿等功效[5],能有效促进肝硬化顽固性腹水患者腹水消退,改善肝功能[6]。本研究利用网络药理学分析芪遂逐水膏敷贴有效活性成分及其可能作用通路,构建复方中药-单体化合物-药物作用靶点-通路的作用网络,并通过动物实验验证,为临床更好地利用芪遂逐水膏敷贴提供理论基础。
1 材料
1.1 药物 芪遂逐水膏由黄芪、甘遂、木香、茯苓、益母草、丹参、大腹皮7 味中药组成,由广西中医药大学第一附属医院药房提供,经广西中医药大学何报作教授鉴定为正品,按照前期确定的药物提取方法、制剂基质配方、制剂工艺及质量标准制备芪遂逐水膏的凝胶膏剂型[7-9]。黄芪、茯苓、益母草加12 倍量水浸泡30 min,回流提取3次,每次1.5 h,合并提取液; 取甘遂、木香、丹参、大腹皮加6 倍量85%乙醇浸泡30 min,加水回流提取2 次,每次1.5 h,合并提取液,过滤,将水煎液与乙醇回流提取液合并,浓缩得到浸膏,真空干燥,粉碎,制成干膏粉。在凝胶膏基质和透皮促渗剂中加入制备好的中药干膏粉搅拌混匀,制备芪遂逐水凝胶膏,每片规格为6 cm×8 cm。本品每片含黄芪以黄芪甲苷计不低于0.693 2 mg,含甘遂以大戟二烯醇计不低于1.476 6 mg[8]。按成人与大鼠体表面积比例换算,统一裁制成1 cm×1 cm、2 cm×2 cm 2 种规格,在4 ℃下保存。
1.2 试剂与仪器 谷丙转氨酶 (ALT)、谷草转氨酶(AST)、总胆红素(TBIL)、白蛋白(ALB) 试剂盒购自深圳迈瑞生物医疗电子股份有限公司; 伊红、中性树脂、RIPA (强) 组织细胞快速裂解液、BCA 蛋白浓度测定试剂盒购自北京索莱宝科技有限公司(货号E8090、G8590、R0010、PC0020); 苏木素购自武汉赛维尔生物科技有限公司(货号G1004); 血管内皮生长因子A (VEGFA)、丝裂原活化蛋白激酶8 (MAPK8)、蛋白激酶B1 (AKT1)、TP53、GAPDH、Goat anti-Rabbit IgG 购自武汉贝茵莱生物科技有限公司(货号PAB30096、PAB33334、PAB30596、PAB34226、PAB36269、SAB43714); PVDF 转移膜、化学发光试剂购自美国Millipore 公司 (货号IPVH00010、WBKLS0500)。mini protean 3 cell 电泳仪购自美国Bio-Rad公司; iCEN-24R 高速冷冻离心机购自杭州奥盛仪器有限公司; Tanon-5200 全自动化学发光分析仪购自上海天能科技有限公司。
1.3 动物 SPF 级雄性SD 大鼠24 只,体质量200~250 g,来源于三峡大学(质量合格证号42010200005069),饲养于武汉华联科生物技术有限公司,实验动物使用许可证号SYXK (鄂) 2018-0104。研究符合武汉华联科生物技术有限公司伦理审查委员会有关动物研究指导原则(伦理审查号HLK-20210930-01)。
2 方法
2.1 芪遂逐水膏活性成分及靶点筛选 通过中药系统药理学数据库与分析平台(TCMSP,http: //tcmspw.com/tcmsp.php,version 2.3) 进行数据挖掘,收集有效成分与作用靶点。通过对既往外敷型药物有效成分的研究结果[10-11],将化合物相对分子质量(MW) ≤500、辛醇与水分配系数(AlogP) <5、氢键供体数 (Hdon) <5、氢键受体数(Hacc) <10、可旋转键(RBN) <10 设置为筛选参数,在TCMSP 数据库检索活性成分对应的靶点,通过UniProt 数据库将其名称转换为基因简称。
2.2 芪遂逐水膏预测靶点功能分析 通过构建蛋白质-蛋白质交互作用网络(PPI),可清晰呈现靶点与靶点之间直接、间接的调控关系。使用STRING 数据库分析靶点之间蛋白互作关系,DAVID 分析工具对获得的靶蛋白进行基因本体(GO) 分析[12],包括生物学过程(BP)、细胞定位(CC) 和分子功能(MF),各自描述了基因产物可能行使的分子功能、所处的细胞环境、参与的生物学过程,将P≤0.05 设定为显著性基因富集的临界值,使用R 软件进行作图。再采用京都基因与基因组百科全书(KEGG)[13-14]分析,物种设置为人(Homosapiens),以P<0.05 为标准确定功能及重要通路,并对通路进行注释和分析。
2.3 芪遂逐水膏及肝硬化腹水共有靶点分析 采用GeneCards[15](https: //www.genecards.org/) 数据库中查找肝硬化腹水相关靶点,取活性成分预测靶点与疾病预测靶点交集,绘制韦恩图。采用DAVID 分析工具对获得的靶蛋白进行GO和KEGG 分析,以P<0.05 为标准确定功能及重要通路,并对后者进行注释和分析。
2.4 网络药理学网络构建 选择共有靶点中与肝硬化腹水相关的通路,使用Cytoscape 3.7.0 软件绘制“靶基因-通路” 网络图。
2.5 动物实验 大鼠适应性喂养1 周后,随机分为正常组、模型组与芪遂逐水膏敷贴高、低剂量组,每组6 只。除正常组外,其余各组大鼠第1 周给予35%苯巴比妥CMCNa 混悬液,然后背部皮下注射CCl4油溶液建立肝硬化腹水模型,14 周后芪遂逐水膏敷贴高、低剂量组分别给予2 cm×2 cm、1 cm×1 cm 规格敷贴于脱毛大鼠的腹部皮肤上,每天1 次,每次6 h,连续4 周。
常规乙醚麻醉大鼠后腹主动脉采血,离心,收集血清,全自动生化分析仪检测ALT、AST 活性及TBIL、ALB 水平,收集肝组织,HE 染色观察肝脏病理变化。
Western Blot 法检测VEGFA、CASP3、MAPK8、AKT1、TP53 蛋白表达,将大鼠肝脏剪碎,按比例加入裂解液(含蛋白酶和磷酸酶抑制剂),匀浆器匀浆直至完全裂解。4 ℃、12 000×g离心10 min,取上清进行蛋白质浓度检测,加入适量上样缓冲液,沸水浴10 min 使蛋白变性,将配制好的PAGE 胶放入电泳槽中,上样后电泳,湿转转膜,5%脱脂奶粉室温封闭4 ℃过夜,加入一抗VEGFA、CASP3、MAPK8、AKT1、TP53 (1 ∶1 000),室温孵育1 h,TBST洗涤3 次,再加入二抗(1 ∶20 000) 室温孵育1 h,TBST洗涤3 次,滴加ECL 化学发光液,以GAPDH 为内参,Image J 软件计算相关条带灰度值。
2.6 统计学分析 通过SPSS 20.0 软件进行处理,数据以(±s) 表示,2 组间比较采用t检验,多组间比较采用单因素方差分析。P<0.05 表示差异具有统计学意义。
3 结果
3.1 芪遂逐水膏活性成分及靶点筛选 共得到13 种活性成分和240 个预测靶点,见图1。
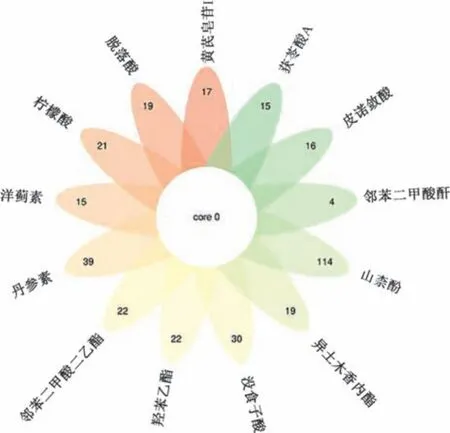
图1 “化合物-预测靶点个数” 花瓣图
3.2 芪遂逐水膏靶蛋白PPI 分析 蛋白互作网络图见图2,包含240 个节点、2 674条边,平均节点度为22.3,PPI富集P<1.0 × 10-16。使用Cytoscape 软件中的network analyzer 工具对预测靶蛋白互作结果进行可视化分析,其中节点的大小和颜色的明暗与靶蛋白的节点度呈正比,节点越大,靶蛋白与其他蛋白的关联度越大,结果见图3。由此可知,AKT1、TP53、VEGFA、TNF、SRC、PTGS2、EGFR、CASP3、JUN、ESR1 等蛋白之间的相互作用具有重要地位,其中AKT1、TP53、VEGFA、TNF 邻接靶标数目最多。
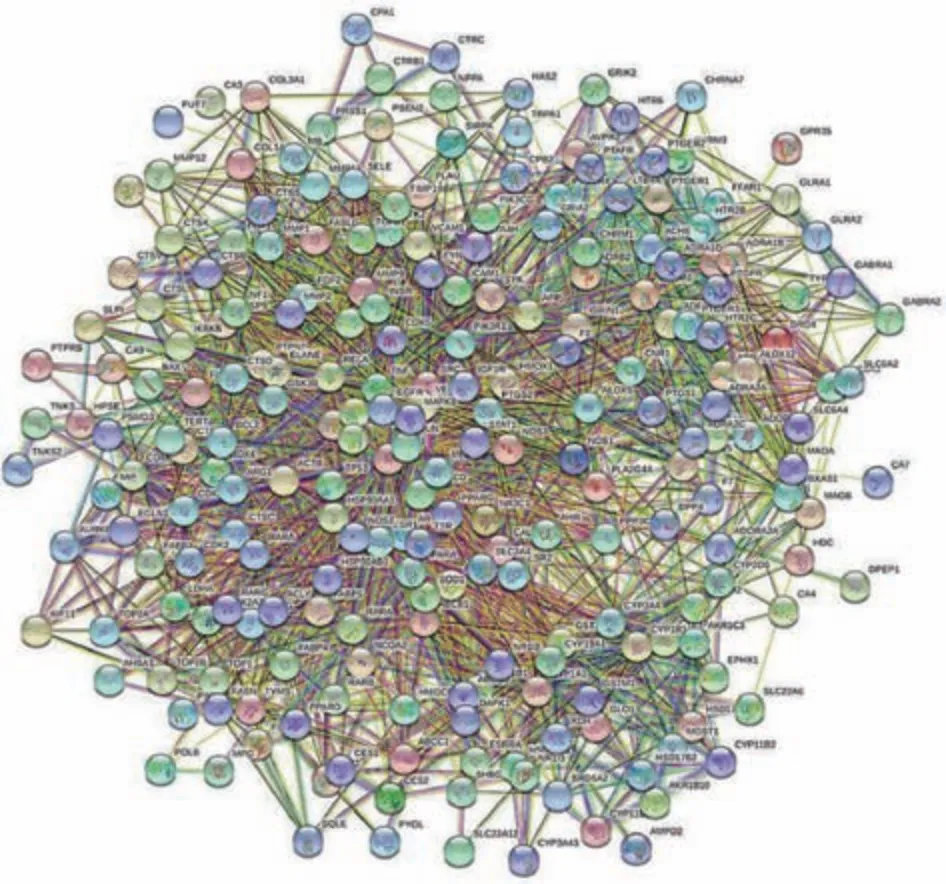
图2 芪遂逐水膏活性成分预测靶点PPI 蛋白互作图

图3 芪遂逐水膏预测靶点蛋白互作可视化图
3.3 芪遂逐水膏预测靶点功能分析 GO 分析显示,芪遂逐水膏活性成分参与的生物学过程最多的为药物反应、氧化应激、活性氧代谢过程等,主要涉及的细胞定位为膜筏、膜微域、囊腔等,分子功能主要有血红素结合、四吡咯结合、氧化还原酶活性,作用于成对供体,结合或还原分子氧,见图4。KEGG 分析显示,芪遂逐水膏活性成分主要参与神经活性配体-受体相互作用、化学致癌作用-受体激活、流体剪切应力和动脉粥样硬化、脂质和动脉粥样硬化等通路,见图5。
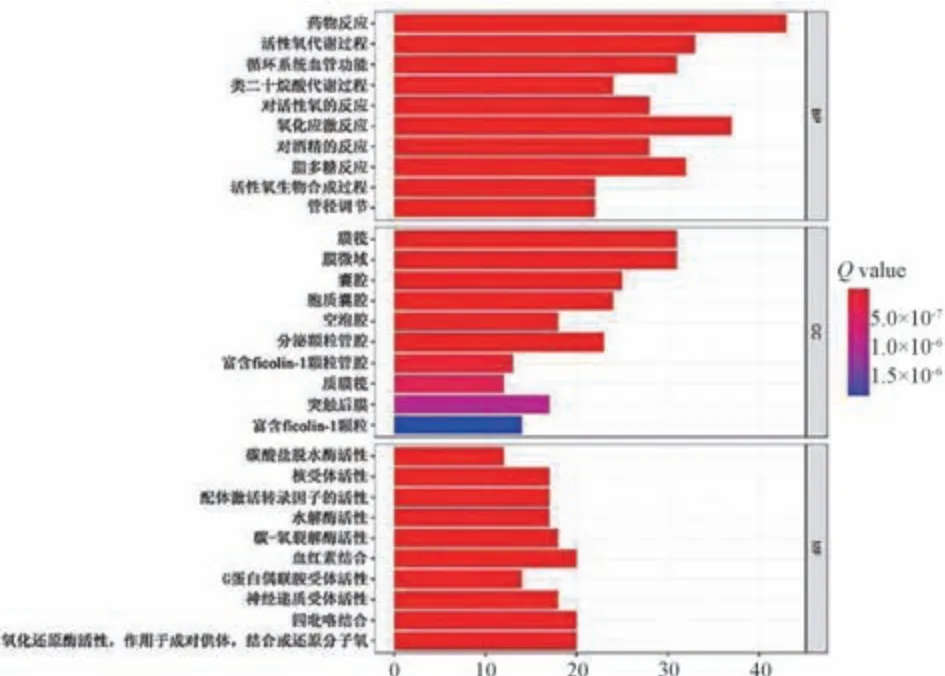
图4 芪遂逐水膏预测靶点的GO 功能分析柱状图

图5 芪遂逐水膏预测靶点的KEGG 通路分析柱状图
3.4 芪遂逐水膏与肝硬化腹水共有靶点分析 在GeneCard数据库(https: //www.genecards.org/) 查找肝硬化腹水相关靶点作为预测靶点,共得到1 108 个。活性成分预测靶点与肝硬化腹水预测靶点取交集,绘制韦恩图,见图6,得到共有靶点86 个,PPI 蛋白互作图见图7,包含86 个节点、1 083 条边,平均节点度为25.2,PPI 富集P<1.0×10-16。其中,共有靶点中的核心基因为AKT1、VEGFA、TNF、TP53、CASP3、MMP9 等。

图6 芪遂逐水膏与肝硬化腹水共有靶点

图7 芪遂逐水膏与肝硬化腹水共有靶点PPI 蛋白互作图
3.5 芪遂逐水膏及肝硬化腹水共有靶点功能分析 GO 分析显示,参与最多的生物学过程为药物反应、氧含量反应等,主要涉及的细胞定位为膜筏、膜微域等,分子功能主要有DNA 转录因子结合、血红素结合、四吡咯结合,见图8。KEGG 分析显示,其主要参与脂质和动脉粥样硬化、流体剪切应力和动脉粥样化等通路,见图9。
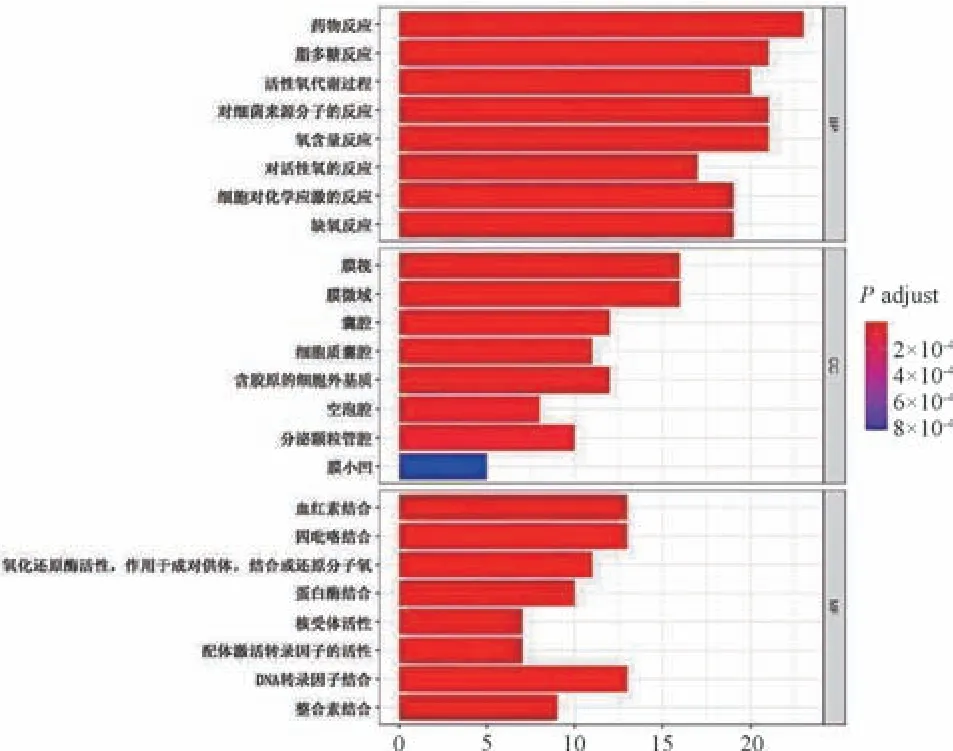
图8 芪遂逐水膏及肝硬化腹水共有靶点的GO 功能分析柱状图
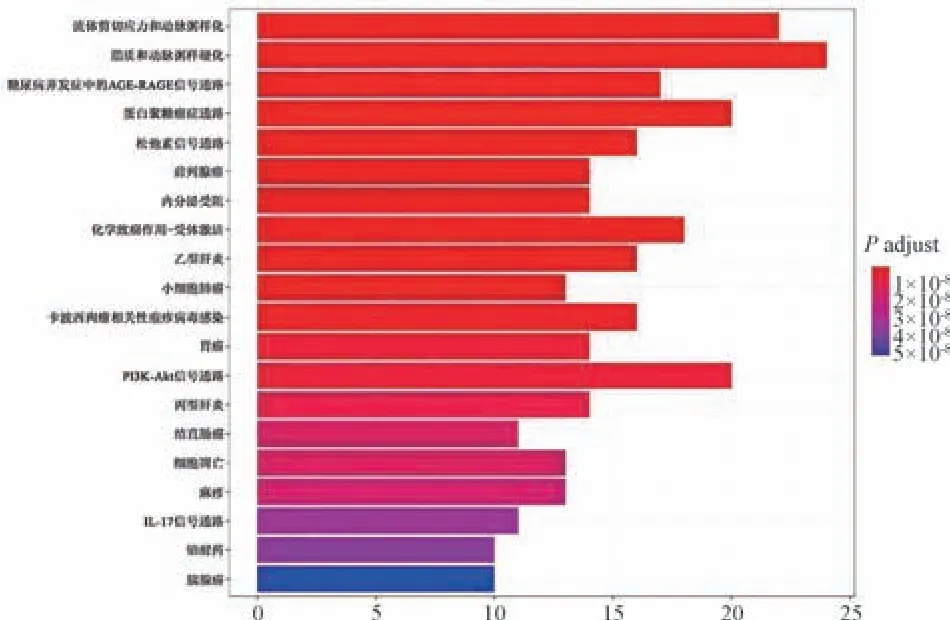
图9 芪遂逐水膏及肝硬化腹水共有靶点的KEGG 通路分析柱状图
3.6 靶点-通路的网络分析 基于共有靶点-通路关系使用Cytoscape 软件构建靶点-通路网络,可直观地体现芪遂逐水膏通过多靶点和多通路治疗肝硬化腹水的作用机制,见图10。

图10 芪遂逐水膏与肝硬化腹水共有靶点-KEGG 通路网络图
3.7 肝脏病理学观察 正常组肝脏结构清晰完整,肝细胞呈放射状整齐排列,无炎症细胞浸润; 模型组肝脏结构明显破坏,肝细胞排列紊乱,出现变性肿胀及坏死,伴有大量炎性细胞浸润,纤维组织增生形成假小叶; 芪遂逐水膏低剂量组肝脏结构基本完整,轻微纤维组织增生,可见少量炎性细胞浸润,较模型组有改善; 芪遂逐水膏高剂量组肝脏结构基本恢复正常,肝细胞索排列较整齐,可见散在的炎性细胞浸润,见图11。
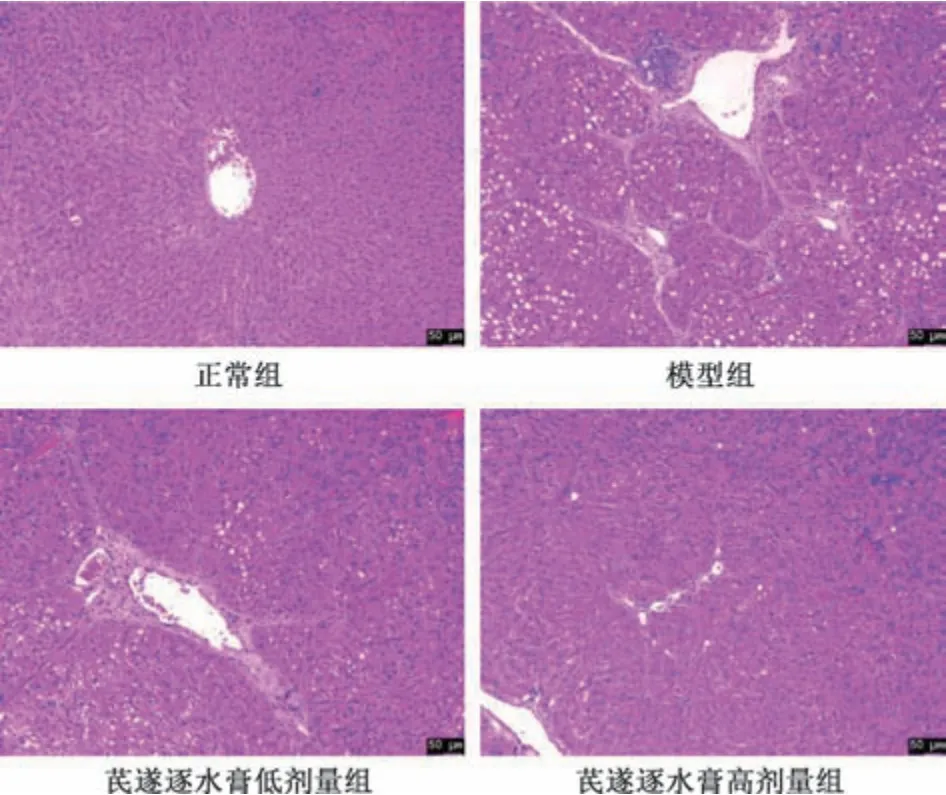
图11 各组大鼠肝组织染色(HE,×100)
3.8 芪遂逐水膏对ALT、AST 活性及TBIL、ALB 水平的影响 与正常组比较,模型组血清ALT、AST 活性及TBIL 水平升高,ALB 水平降低(P<0.01),表明模型制备成功;与模型组比较,芪遂逐水膏低剂量组血清ALT、AST 活性降低(P<0.05),TBIL、ALB 水平无明显变化(P>0.05),芪遂逐水膏高剂量组血清ALT、AST 活性及TBIL 水平降低(P<0.01),ALB 水平升高(P<0.01),见图12。
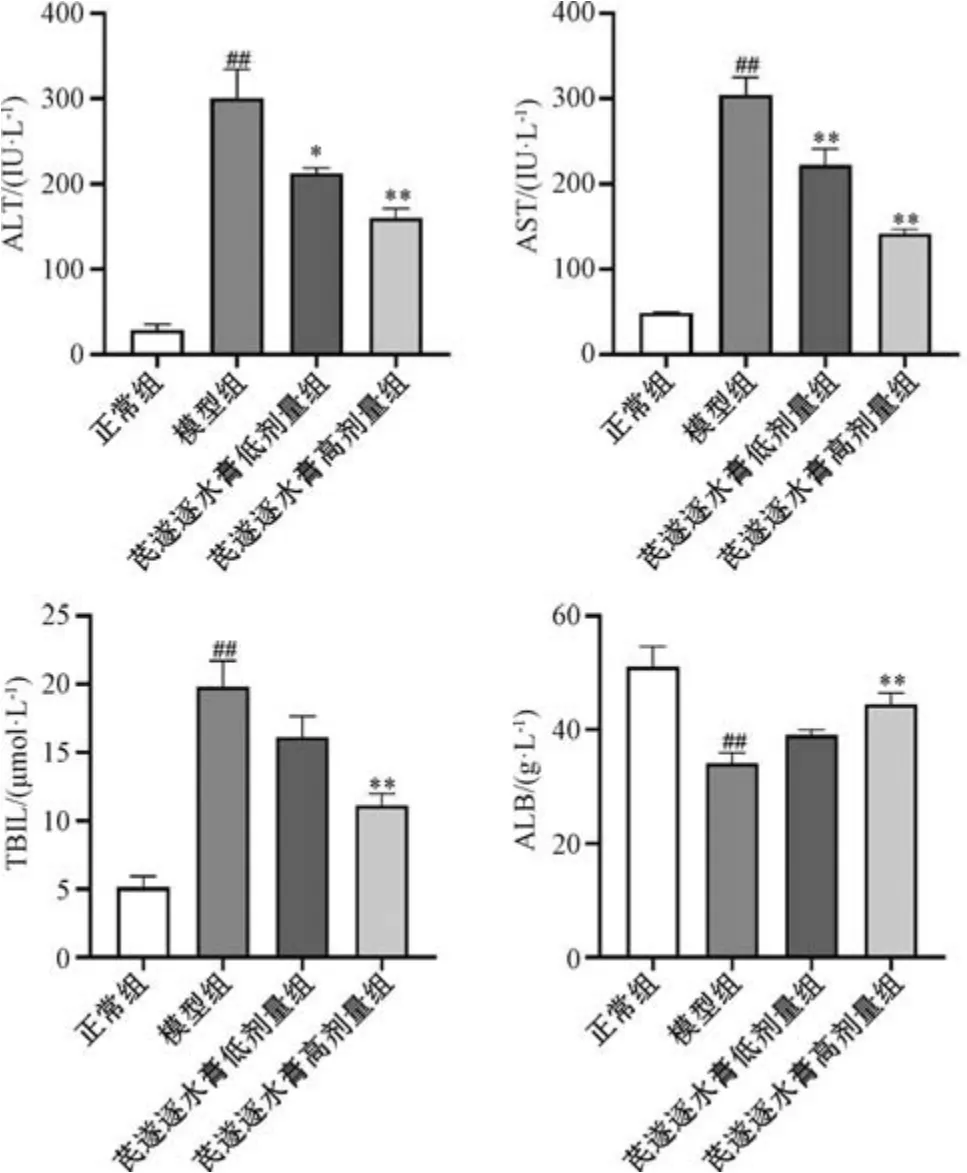
图12 芪遂逐水膏对ALT、AST 活性及TBIL、ALB 水平的影响(±s,n=3)
3.9 芪遂逐水膏对VEGFA、CASP3、MAPK8、AKT1、TP53表达的影响 与正常组比较,模型组肝脏组织VEGFA、CASP3、MAPK8、AKT1、TP53 蛋白表达升高(P<0.01);与模型组比较,芪遂逐水膏各剂量组肝脏组织VEGFA、CASP3、MAPK8、AKT1、TP53 蛋白表达表达降低(P<0.05,P<0.01),见图13。

图13 芪遂逐水膏对VEGFA、CASP3、MAPK8、AKT1、TP53 表达的影响(±s,n=3)
4 讨论
腹水是肝硬化最突出的临床表现,肝硬化腹水的发生严重影响了肝硬化患者的生命质量与生存率,目前尚无特效疗法[16]。中药方剂具有多成分、多靶点、多途径的特点,在治疗肝硬化腹水方面具有独特的优势,但难以解释其药理作用机制。
TCMSP 发现,芪遂逐水膏组方13 种活性成分,其对应的靶点共有240 个,其中AKT1、TP53、VEGFA、TNF、SRC、PTGS2、EGFR、CASP3、JUN、ESR1 等蛋白具有重要地位。AKT 参与多种细胞功能,如生存、代谢、转录和翻译等过程,在癌症和炎症性疾病中起调节作用[17-18]。VEGFA 是生理和病理状态下最重要的血管内皮生长因子,参与肿瘤新生血管的形成,在肿瘤的形成、增殖和转移中起着重要的作用[19]。caspase-3 是半胱氨酸天冬氨酸蛋白酶家族的成员之一,有证据表明它可促进癌细胞生长、细胞迁移和侵袭性,为疾病治疗提供新靶点[20-21]。
PPI 蛋白互作图分析发现,芪遂逐水膏和肝硬化腹水共有靶点中的核心基因为AKT1、VEGFA、TNF、TP53、CASP3、MMP9。GO 和KEGG 功能分析发现主要参与药物反应和氧含量反应,具有DNA 转录因子结合、血红素结合、四吡咯结合等分子功能,参与脂质和动脉粥样硬化、流体剪切应力和动脉粥样化等通路,结果表明芪遂逐水膏对肝硬化腹水的治疗是多靶点的。根据共有靶点-通路网络图分析发现,VEGFA、CASP3、MAPK8、AKT1、TP53 与芪遂逐水膏治疗肝硬化腹水密切相关。VEGFA 和CASP3 参与细胞凋亡和增殖等生物过程,与线粒体功能和凋亡密切相关,AKT1 磷酸化会降低氧化应激刺激的MAPK 激酶活性,从而防止细胞凋亡。MAPK 信号通路参与炎症反应、细胞分化、细胞凋亡和肿瘤侵袭等多种生物学过程[22]。本研究构建肝硬化腹水动物模型后检测血清肝功能指标,结果显示模型组血清中ALT、AST 活性和TBIL 水平高于正常组,ALB 水平降低。肝脏病理组织检查发现模型组肝脏结构破坏,纤维组织增生形成假小叶,有大量炎性细胞浸润,表明模型制备成功。本研究进一步检测肝脏中VEGFA、CASP3、MAPK8、AKT1、TP53 的表达,结果显示在肝硬化腹水模型中,VEGFA、CASP3、MAPK8、AKT1、TP53 蛋白表达增加,给予芪遂逐水膏后蛋白表达降低。
综上所述,芪遂逐水膏治疗肝硬化腹水的可能机制是多成分、多靶点、多途径的协同作用,可能与VEGFA、CASP3、MAPK8、AKT1、TP53 有关,为临床更好的利用芪遂逐水膏敷贴提供理论基础。
