UPLC 法同时测定护肝片中8 种五味子木脂素的含量
2024-03-10赵志远张金朋刘媛媛
赵志远,张金朋,赵 硕,刘媛媛
[山东第一医科大学(山东省医学科学院) 药学院,山东 泰安 271016]
护肝片收载于2020 年版 《中国药典》 一部[1],由柴胡、五味子、板蓝根等多味中药组成[2],主要用于治疗各种原因导致的肝功能受损,方中五味子是其发挥养肝作用的主要药味,物质基础是木脂素类化合物,对于神经系统具有抗癫痫[3]、提高学习记忆能力[4]、镇静催眠[5]功能,对于消化系统具有保肝护胆[6]功效,此外还有着抗肿瘤[7]、延缓衰老[8]、抗病毒[9]、抗炎、免疫调节[10]作用。
现行药典中护肝片“含量测定” 项下以五味子醇甲为评价指标,而同一类化合物药理作用相似,临床使用时容易产生叠加效应[11-12]。目前,木脂素含量测定方法主要包括HPLC 法、UPLC法、LC-MS 法等[13],本实验采用UPLC 法,与HPLC 法相比分离效率更高,耗时更短[14],更适合中药复杂成分的分离[15],在提高效率的前提下,同时测定五味子醇甲、戈米辛J、五味子醇乙、当归酰戈米辛H、当归酰戈米辛Q、五味子酚、五味子甲素、五味子丙素的含量,以期为该制剂质量控制、临床用药等效性研究提供依据。
1 材料
1.1 仪器 Nexera X2 型超高效液相色谱仪,配置LC-30AD 型溶液输送单元、SIL-30AC 型高效液相色谱仪自动进样器、SPD-M30A 型光电二极管阵列紫外可见光检测器、CTO-20AC 型柱温箱(日本岛津公司); Direct-Q®8UV-R 型超纯水系统(德国Merck 公司); ES-E120A 型电子分析天平(天津德安特传感技术有限公司); KQ-600DB 型超声波清洗器(昆山市超声仪器有限公司); Fresco21 型高速冷冻离心机 [赛默飞世尔科技 (中国) 有限公司]。
1.2 试剂与药物 五味子醇甲(批号D1827017,纯度≥98.00%)、五味子醇乙(批号F1508140,纯度≥98.00%)、五味子甲素(批号D1911039,纯度≥98.00%)、五味子丙素(批号D1608128,纯度≥98.00%) 对照品均购自上海阿拉丁生化科技股份有限公司; 戈米辛J (批号G99633663,纯度≥98.00%)、当归酰戈米辛 H ( 批号A43133661,纯度≥98.00%) 对照品均购自上海吉至生化科技有限公司; 当归酰戈米辛Q 对照品(批号PCS-210329,纯度≥98.00%) 购自北京中科质检生物技术有限公司; 五味子酚对照品(批号C12256480,纯度≥98.00%) 购自上海麦克林生化科技有限公司。护肝片 (批号202106114、202111015、202105212,糖衣片,片心重0.35 g)购自黑龙江葵花药业股份有限公司。甲醇、甲酸、乙腈均为色谱纯; 其余试剂均为分析纯; 水为纯化水(由Direct-Q®8UV-R 型超纯水系统制备)。
2 方法与结果
2.1 色谱条件 WELCH Ultimate ®-C18色谱柱(100 mm×2.1 mm,1.8 μm); 流动相0.1% 甲酸(A) -乙腈(B),梯度洗脱(0 ~0.01 min,45%B; 0.01 ~1.2 min,45% ~53% B; 1.2 ~3 min,53% ~53.5% B; 3 ~10 min,53.5% ~55% B; 10 ~13 min,55% ~95%B; 13 ~15 min,95%B; 15 ~17 min,95% ~45%B; 17 ~21 min,45% B); 体积流量0.3 mL/min; 柱温40 ℃; 检测波长267 nm; 进样量6 μL。
2.2 溶液制备
2.2.1 对照品溶液 精密称取对照品五味子醇甲5 mg、五味子醇乙和五味子甲素各1.5 mg、当归酰戈米辛Q 和五味子丙素各0.5 mg、五味子酚0.2 mg、戈米辛J 0.3 mg、当归酰戈米辛H 1 mg,置于10 mL 量瓶中,甲醇定容至刻度,摇匀,过0.22 μm 微孔滤膜,取续滤液,即得(各成分质量浓度分别为五味子醇甲500 μg/mL、戈米辛J 30 μg/mL、五味子醇乙150 μg/mL、当归酰戈米辛Q 50 μg/mL、当归酰戈米辛H 100 μg/mL、五味子酚20 μg/mL、五味子甲素150 μg/mL、五味子丙素50 μg/mL)。
2.2.2 供试品溶液 取本品3 片,除去包衣,研细,精密称取0.4 g,加入乙酸乙酯16 mL,超声(功率600 W,温度30 ℃) 提取30 min,放冷,4 000 r/min 离心10 min,取上清液,在蒸发皿上75 ℃水浴蒸干,10 mL 甲醇超声溶解,反复清洗蒸发皿,摇匀,12 000 r/min 离心10 min,取上清液,过0.22 μm 微孔滤膜,取续滤液,即得。
2.3 专属性试验 精密吸取“2.2” 项下对照品、供试品溶液及空白溶剂(甲醇) 适量,在“2.1”项色谱条件下各进样6 μL 测定,结果见图1。由此可知,各成分色谱峰峰形较好,均能达到基线分离(分离度均大于1.5),理论塔板数均不低于8 000,空白溶剂无干扰,表明该方法专属性良好。

图1 各成分UPLC 色谱图Fig.1 UPLC chromatograms of various constituents
2.4 线性关系考察 分别取“2.2.1” 项下对照品溶液2.5、1、0.71、0.5、0.05 mL,置于5 mL量瓶中,甲醇稀释定容至刻度,摇匀,过0.22 μm微孔滤膜,取续滤液,即得稀释0、2、5、7、10、100 倍的线性工作液,取适量,在“2.1” 项色谱条件下进样测定。以对照品峰面积(Y) 对其质量浓度(X) 进行回归,结果见表1,可知各成分在各自范围内线性关系良好。
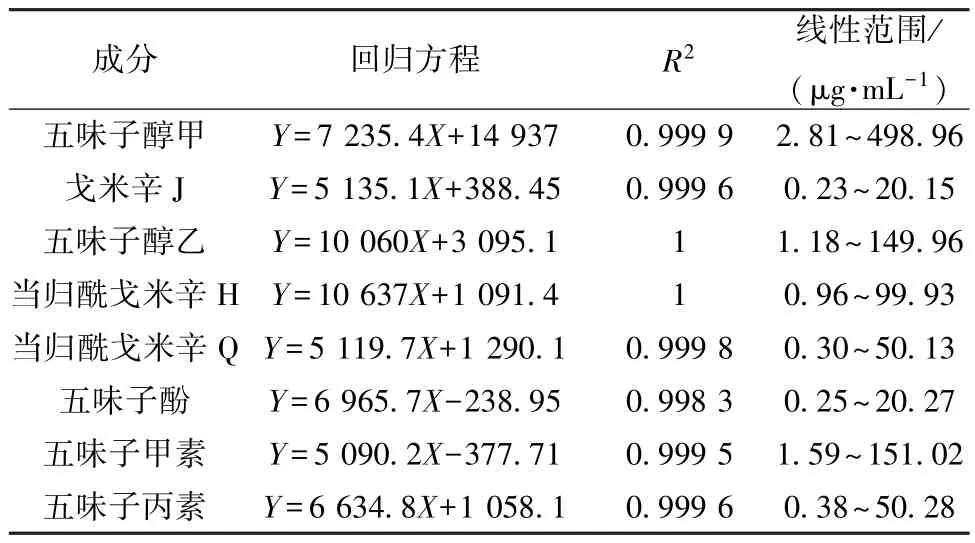
表1 各成分线性关系Tab.1 Linear relationships of various constituents
2.5 精密度试验 取“2.4” 项下稀释2 倍的线性工作液适量,在“2.1” 项色谱条件下进样测定6 次,测得五味子醇甲、戈米辛J、五味子醇乙、当归酰戈米辛H、当归酰戈米辛Q、五味子酚、五味子甲素、五味子丙素峰面积RSD 分别为0.28%、0.49%、0.31%、0.30%、0.39%、0.62%、1.04%、1.04%,表明仪器精密度良好。
2.6 稳定性试验 取本品(批号202106114) 适量,按“2.2.2” 项下方法制备供试品溶液,室温下于0、2、4、8、12、24 h 在“2.1” 项色谱条件下进样测定6 次,测得五味子醇甲、戈米辛J、五味子醇乙、当归酰戈米辛H、当归酰戈米辛Q、五味子酚、五味子甲素、五味子丙素峰面积RSD 分别为0.51%、0.80%、0.48%、0.53%、1.27%、1.26%、0.35%、1.19%,表明溶液在24 h 内稳定性良好。
2.7 重复性试验 精密称取本品 (批号202106114) 粉末6 份,每份0.4 g,按“2.2.2”项下方法制备供试品溶液,在“2.1” 项色谱条件下进样测定,测得五味子醇甲、戈米辛J、五味子醇乙、当归酰戈米辛H、当归酰戈米辛Q、五味子酚、五味子甲素、五味子丙素峰面积RSD 分别为0.63%、1.05%、0.65%、0.36%、0.73%、0.90%、1.41%、1.30%,表明该方法重复性良好。
2.8 加样回收率试验 精密称取本品 (批号202106114) 粉末0.2 g,按“2.2.2” 项下方法制备供试品溶液,精密量取1 mL,置于5 mL 量瓶中,甲醇定容至刻度,过0.22 μm 微孔滤膜,取续滤液,在“2.1” 项色谱条件下进样测定,测得各成分原有量分别为五味子醇甲23.24 μg、戈米辛J 2.63 μg、五味子醇乙5.85 μg、当归酰戈米辛H 3.95 μg、当归酰戈米辛Q 1.15 μg、五味子酚1.04 μg、五味子甲素9.82 μg、五味子丙素2.60 μg。精密量取上述供试品溶液9 份,每份1 mL,置于9 个5 mL 量瓶中,分别按50%、100%、150%水平加入对照品溶液各10 mL,平行3 份,分别取1 mL,置于9 个5 mL 量瓶中,甲醇定容至刻度,在“2.1”项色谱条件下进样测定,计算回收率。结果,五味子醇甲、戈米辛J、五味子醇乙、当归酰戈米辛H、当归酰戈米辛Q、五味子酚、五味子甲素、五味子丙素平均加样回收率分别为101.94%、97.56%、102.67%、101.58%、99.14%、96.84%、98.07%、96.02%,RSD 分别为0.62%、1.30%、1.45%、0.86%、0.76%、1.28%、1.14%、1.60%。
2.9 样品含量测定 取3 批样品(批号202106114、202111015、202105212,编号1 ~3) 粉末,每批0.4 g,按“2.2.2” 项下平行制备3 份供试品溶液,在“2.1” 项色谱条件下进样测定,计算含量,结果见表2,可知各成分含量由高到低依次为五味子醇甲、五味子甲素、五味子醇乙、当归酰戈米辛H、五味子丙素、戈米辛J、当归酰戈米辛Q、五味子酚。在中药质量控制评价模式中,五味子醇甲作为五味子糖浆质量控制指标,符合2020 年版《中国药典》 标准(RSD<2%)。
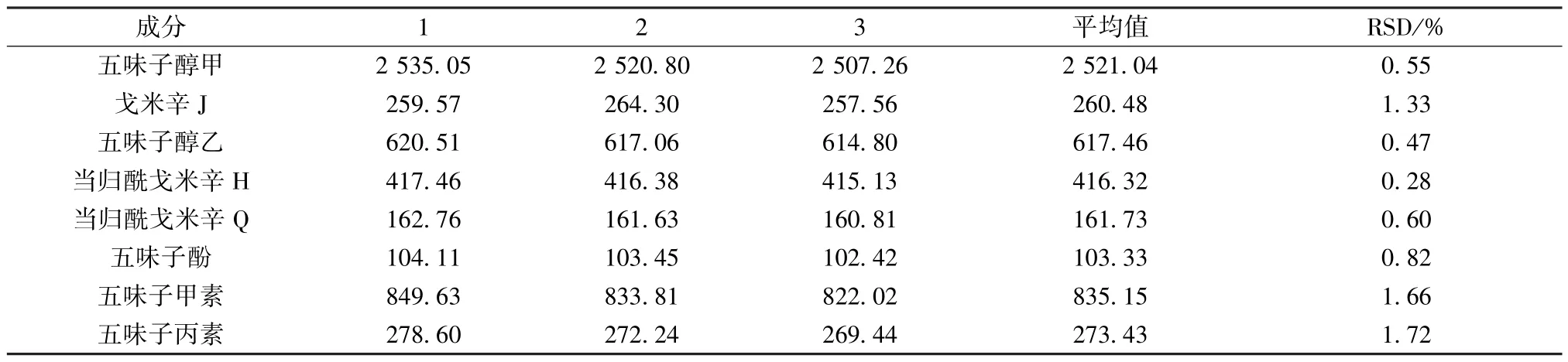
表2 各成分含量测定结果(μg/g,n=3)Tab.2 Results for content determination of various constituents (μg/g,n=3)
3 讨论
3.1 提取方法选择 本实验分别考察了80% 甲醇[16]、甲醇[17]超声提取10、20、30 min,发现色谱图中杂质峰太多,无法对五味子木脂素进行定量分析。综合提取率等多种指标,最终确定乙酸乙酯超声提取30 min,挥干后甲醇溶解作为提取方法。
3.2 色谱条件选择 本实验参考文献[18] 报道,分别考察了WELCH Ultimate®-C18(100 mm×2.1 mm,1.8 μm)、ACQUITY UPLC ® BEH-C18(100 mm×2.1 mm,1.7 μm) 色谱柱,发现各五味子木脂素在WELCH Ultimate®-C18色谱柱上色谱峰峰形、分离度均良好。再考察了流动相甲醇-水,发现各五味子木脂素出峰不完全,分离度不符合要求,而改用乙腈-水洗脱后出峰良好。然后,分别考察了0.1% 甲酸、0.1% 乙酸、0.1% 磷酸,发现加入0.1%甲酸后各五味子木脂素分离度良好,峰形对称。
前期报道,木脂素检测波长主要包括220 nm[19]、250 nm[20]、254 nm[21]。本实验在200 ~400 nm 波长处对对照品溶液进行扫描,发现各五味子木脂素在267 nm 处基线平稳,吸收最好,杂质峰最少。再分别考察了柱温(35、40、45 ℃)、体积流量 (0.28、0.3、0.32 mL/min)、进样量(4、6、8 μL),发现在柱温40 ℃、体积流量0.3 mL/min,进样量6 μL 下各五味子木脂素色谱峰峰形理想,可与周围干扰物质达到良好的分离效果。
4 结论
本实验建立UPLC 法同时测定护肝片中五味子醇甲、戈米辛J、五味子醇乙、当归酰戈米辛H、当归酰戈米辛Q、五味子酚、五味子甲素、五味子丙素的含量,该方法简便、快速、准确,而且专属性强,精密度好,可为后续该制剂及其所含木脂素类化合物的研究奠定基础。
