宏观非平衡超分子自组装综合实验
2024-03-04赵婷李盼盼王旭
赵婷,李盼盼,王旭
山东大学化学与化工学院,国家胶体材料工程技术研究中心,济南 250100
自然界中的非平衡组装是一个常见且重要的过程[1,2]。这种动态的非平衡组装体系受控于耗散热力学,通常运行在高能量状态下,并通过消耗能量或者化学燃料来维持活性结构以实现复杂功能[3–5]。不管是微观还是宏观层面,都存在多种多样的非平衡组装过程。模拟这种能量驱动的非平衡组装是构造仿生组装体的基础[6–8]。基于此,研究者们设计出了一系列化学燃料驱动的诸如合成小分子[9]、聚合物[10,11]、生物大分子[12]以及纳米颗粒[13]等微观基元的非平衡组装体系,并将其应用在可控药物释放[14]以及自修复[15]等领域。在宏观组装领域,尺寸大于十微米的组装基元通过长程力[16]、共价键[17]或者超分子相互作用[18–20]实现组装,但当前的宏观组装体系多处于能量稳定的状态,导致解组装过程难以实现。因此,开发宏观超分子非平衡体系不仅可以动态调控宏观组装基元的组装和解组装,而且在设计和开发精准组装以及自适应的智能材料领域中发挥重要作用。
水凝胶是一种具有三维交联聚合物网络结构的亲水性高分子材料[21,22],因其表面具有良好的变形性而被广泛应用在宏观组装领域。通过制备聚电解质水凝胶,并结合脲酶(urease)分解尿素的酶促反应可实现基于静电相互作用的宏观非平衡超分子自组装。通过设计相关实验,可以激发本科生从事科学研究的热情,增加学习兴趣,坚定学习信心,提升学生的实验操作水平。
在本实验中,我们将具有pH响应性的单体引入到聚电解质水凝胶中,并通过时钟反应自发改变非平衡组装体系的pH,进而实现水凝胶组装基元的组装或解组装。本实验具有实验危险系数低、实验操作方法简单易行、实验现象明显等特征,因此非常适合用于教学实践活动。实验过程中涉及偏光显微镜、质构分析仪以及pH计等仪器的使用,促使学生加深对基础知识的理解,同时增强实验操作能力以及学习相应的表征技术及分析方法。
1 实验目的
(1) 了解超分子化学、非平衡体系以及宏观组装的基础知识;
(2) 掌握聚电解质水凝胶的基本制备方法以及基于静电相互作用的非平衡体系的构建方法;
(3) 掌握偏光显微镜和质构分析仪用于非平衡组装体系研究的分析方法。
2 实验原理
4-乙烯基吡啶(4VP)是一种含有氨基的单体,其在高pH (碱性或中性)条件下不带电荷,在低pH(酸性)条件下发生季铵化反应而带正电(图1)[23]。因此,将其作为一种功能单体可制备出具有pH响应性的聚电解质水凝胶,这种凝胶在酸性条件下显电正性,在碱性条件下不带电。另一种凝胶则选择对苯乙烯磺酸钠(SSNa)作为功能单体,其不具有响应性,在各种条件下均显电负性。因此,在酸性条件下,两种凝胶因静电相互作用而实现组装,而在碱性条件下则由于静电相互作用的消失而实现解组装。尿素-脲酶计时反应[24]在反应过程中可以改变体系的pH (图2)。因此,将两种水凝胶与化学燃料驱动的pH计时反应合理地结合在一起,即可构建宏观非平衡超分子组装体系。在本实验中,初始pH为8的体系中两种凝胶呈现解组装的状态,加入化学燃料(酸性尿素缓冲液)后,体系pH迅速下降至3.8左右,此时,正电凝胶表面发生季铵化反应而显正电,两种凝胶实现组装;与此同时,体系中的脲酶催化分解尿素产生氨,使得体系pH缓慢上升,达到一定pH后,组装体实现解组装,进而实现了凝胶解组装→组装→解组装的动态转换,即宏观非平衡超分子组装过程(图3)。反复添加燃料可以实现凝胶之间的循环组装过程,但由于体系内存在废物累积以及脲酶失活的问题,此非平衡组装过程不能够无限循环。

图1 4VP的化学结构式

图2 脲酶分解尿素的反应方程式

图3 非平衡体系中组装体燃料耗散过程中组装状态变化及原理示意图
3 实验仪器与试剂
实验所用仪器和实验所用试剂详见表1、表2。
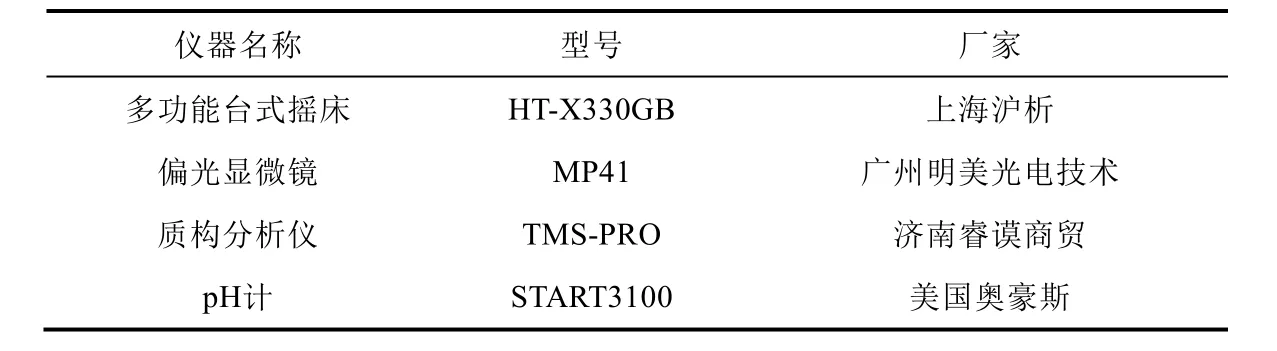
表1 主要实验仪器
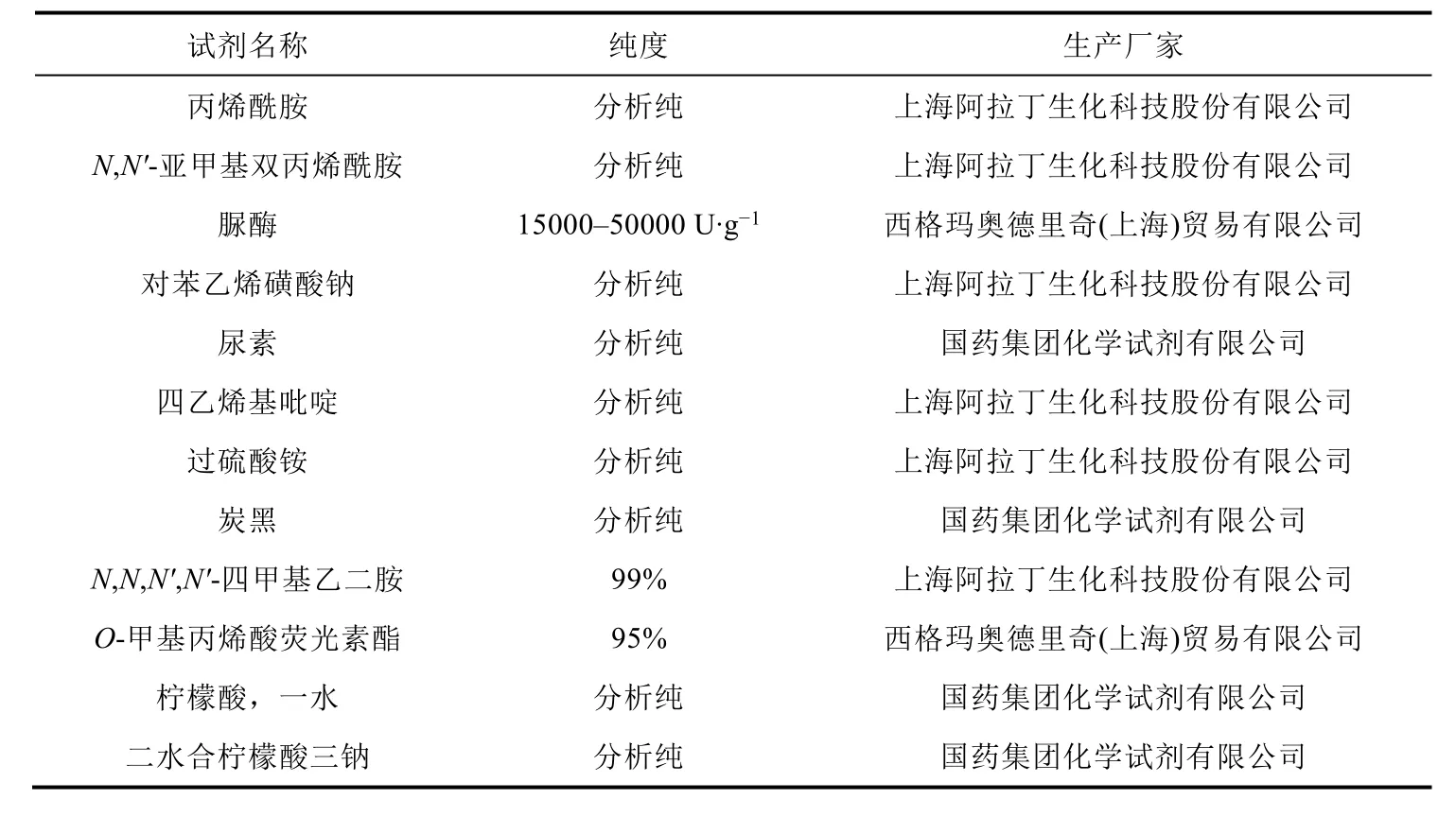
表2 主要实验药品
4 实验步骤
4.1 两种聚电解质水凝胶的制备
两种凝胶均采用均相自由基聚合的方式合成,合成所用原料以及合成过程如图4所示。

图4 正电凝胶和负电凝胶的合成示意图
具有pH响应性的正电凝胶(PCgel)的制备:称取306.0 mg丙烯酰胺(AAm),15.5 mgN,N'-亚甲基双丙烯酰胺(MBAAm),6.0 mg脲酶(urease),5.0 mgO-甲基丙烯酸荧光素酯(FM)溶解于5.0 mL去离子水中,充分溶解以后,再加入70.0 μL 4VP以及10.0 µLN,N,N',N'-四甲基乙二胺(TEMED),经超声充分混合后,在体系中加入11.5 mg过硫酸铵(APS)。接着将混合均匀的溶液倒入相应的模具中,在室温条件下,溶液在30 min内变成水凝胶,用去离子水反复洗涤水凝胶,将黄色的正电凝胶切成棱长为5.0 mm的正方体小块备用。
负电凝胶(PAgel)的制备:称取306.0 mg AAm,15.5 mg MBAAm,6.0 mg脲酶,5.0 mg炭黑(CB)溶解于5.0 mL去离子水中,充分溶解以后,再加入25.2 mg SSNa以及10.0 µL TEMED,经超声充分混合后,在体系中加入11.5 mg APS。接着将混合均匀的溶液倒入相应的模具中,在室温条件下,溶液在30 min内变成水凝胶,用去离子水反复洗涤水凝胶,将黑色的负电凝胶切成棱长为5.0 mm的正方体小块备用。
4.2 宏观非平衡超分子自组装体系的构建
(1) 配制0.1 mol·L−1的缓冲液:分别配制好0.1 mol·L−1的柠檬酸溶液以及0.1 mol·L−1的柠檬酸三钠溶液备用,再用两种溶液调pH,得到pH = 8的0.1 mol·L−1碱性缓冲液以及pH = 3的0.1 mol·L−1酸性缓冲液。
(2) 配制化学燃料:称取5 g尿素,用浓度为0.1 mol·L−1的酸性缓冲液(pH = 3)溶解并定容至100 mL。
(3) 非平衡组装体系的构建:分别取两块正电凝胶和两块负电凝胶放入含有1.5 mL pH = 8的0.1 mol·L−1碱性缓冲液的称量瓶中,将称量瓶放置在摇床上,并以180 r·min−1的速度进行摇晃旋转使得凝胶小块可以相互碰撞,此时凝胶不组装。向该体系中加入3.5 mL化学燃料(酸性尿素溶液),混合均匀,摇晃2 min左右,观察到凝胶块的组装现象。接下来保持180 r·min−1的转速,观察两种凝胶之间组装状态的变化并定时拍摄照片、测定pH、研究组装体之间的粘接强度变化。
5 结果与讨论
5.1 加入化学燃料后,正电凝胶和负电凝胶组装状态随时间的变化
如图5所示,初始pH = 8的体系中,正电凝胶和负电凝胶不组装,加入化学燃料(最终浓度为:50 mg·mL−1尿素,0.1 mol·L−1柠檬酸/柠檬酸三钠缓冲液,pH = 3)后,非平衡组装体系的pH迅速下降,两种凝胶实现组装。与此同时,化学燃料中的尿素在体系中脲酶的催化下会缓慢分解产生氨,使得体系pH升高,两种凝胶再次实现解组装。以上解组装→组装→解组装动态变化的结果说明正电凝胶会随着体系pH的变化而表现出不同的带电性质,在碱性条件下,正电凝胶不显电性,此时两种凝胶之间没有静电相互作用,因而表现出解组装的状态;而在酸性条件下,正电凝胶的表面因发生季铵化反应而显正电,此时两种凝胶的表面电荷之间存在静电相互作用,因而表现出组装的状态。
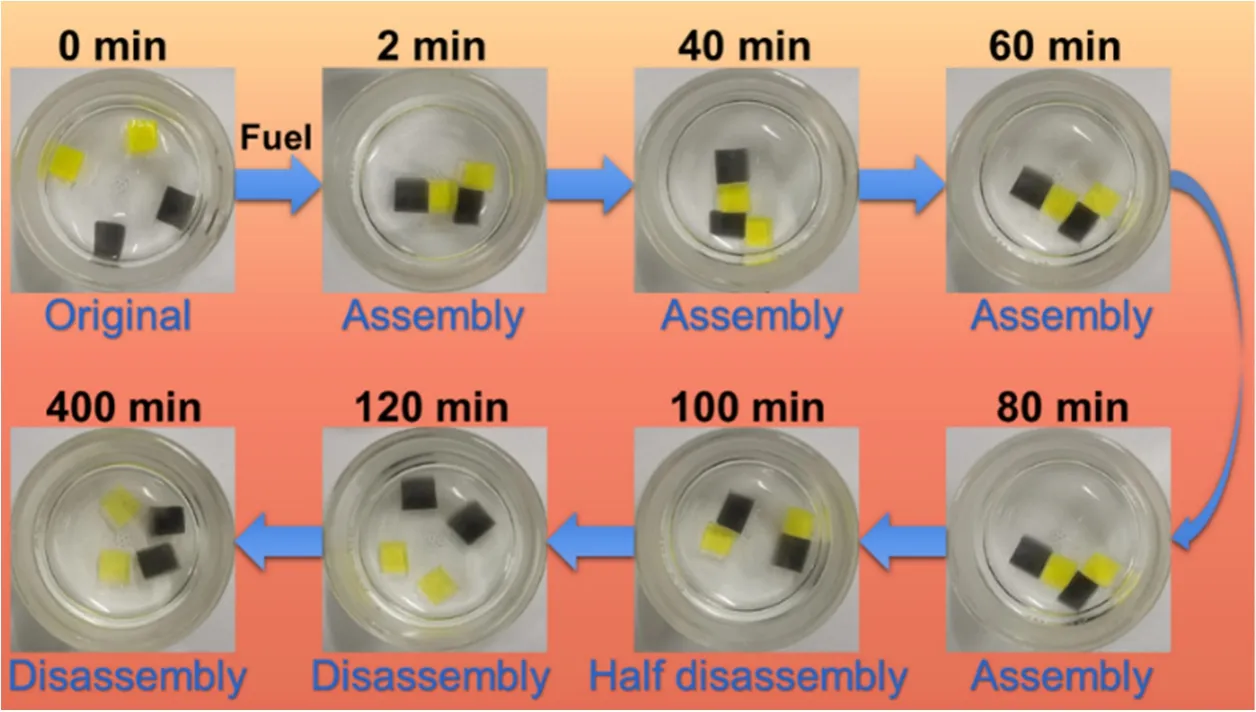
图5 加入化学燃料后,非平衡组装体系中组装基元的组装状态变化
5.2 两种凝胶在酸性条件下形成的组装体界面表征
本实验除了可以直接观察到宏观的组装现象外,还可以利用偏光显微镜来进一步观察组装界面,结果如图6所示。从图中可看出,两种凝胶在酸性条件下可以形成致密的组装体,组装体的界面接触良好。

图6 凝胶组装体的数码照片(左)和光学显微镜照片(右)
5.3 加入化学燃料后,体系pH随时间的变化
向宏观非平衡超分子组装体系中加入化学燃料后,体系的pH会随时间的变化而发生变化,结果如图7所示。体系的初始pH为8,化学燃料的加入使得体系的pH迅速降到3.8左右,而后又不断增加,整体呈现出一个先降后升的趋势,这主要是由于化学燃料中的酸性缓冲液使得体系的pH快速下降,而后凝胶中的脲酶可以分解缓冲液中的尿素,这个过程中产生的氨使得体系的pH缓慢上升。体系pH的变化是正电凝胶和负电凝胶组装状态发生变化的主要原因。
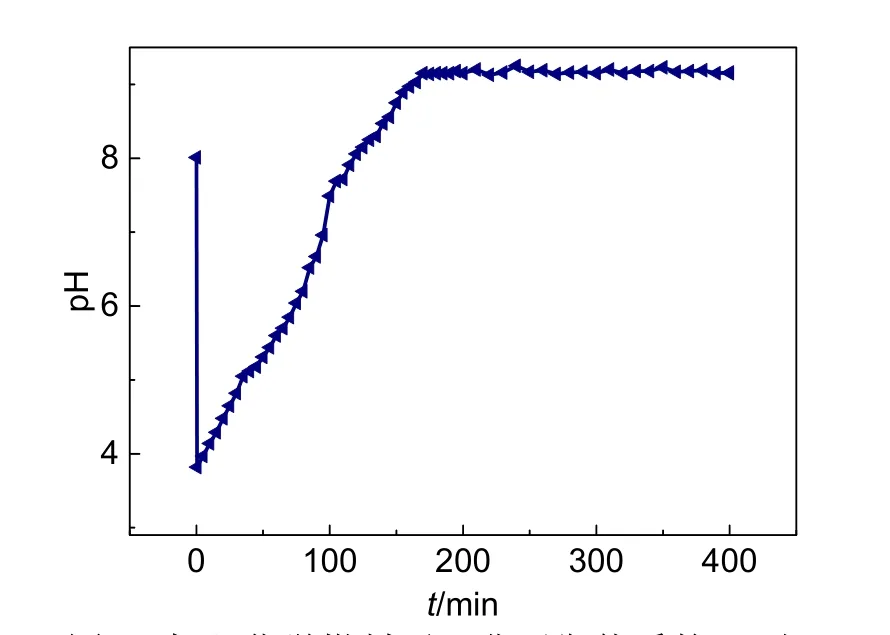
图7 加入化学燃料后,非平衡体系的pH随时间变化图
5.4 正电凝胶和负电凝胶形成的组装体在非平衡组装过程中拉伸曲线的测定
本实验采取拉伸的测试方法来进一步探索凝胶组装体之间的粘接程度,用到的仪器为质构分析仪。将粘接到一起的两种凝胶组装体固定在夹具两端,以60 mm min−1的拉伸速度分别拉向相反的位置,即可得到组装体的应力-应变曲线。上诉非平衡组装实验过程中,不同时间下测得的凝胶组装体之间的拉伸应力-应变曲线如图8所示。从图中可知,组装体在0 min的时候基本没有粘接力;2 min时由于体系内的pH迅速由碱性变为酸性,此时拉伸曲线可达到最大的断裂应力;而随着脲酶分解尿素反应的进行,体系的pH不断恢复为碱性,此时组装体的组装强度逐渐下降,120 min后恢复到初始状态。需要注意的是,凝胶组装体之间的超分子相互作用是较弱的,因此在实验过程中需使用合适的测试量程。
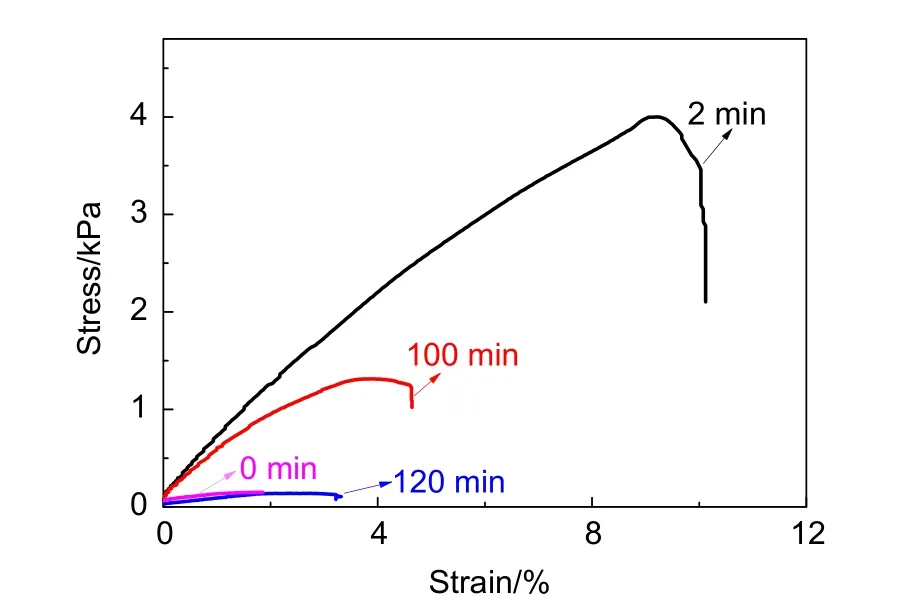
图8 体系中的凝胶组装体在不同时间的拉伸曲线
5.5 正电凝胶和负电凝胶形成的组装体在非平衡组装过程中粘接强度的变化
两种凝胶之间形成的组装体的粘接强度可以用拉伸曲线中的断裂应力来表示。非平衡组装过程中,凝胶组装体的粘接强度随时间而变化,由图9可知,在初始的碱性缓冲溶液中,两种凝胶之间不组装,因此组装体的粘接强度为0;而向体系中加入化学燃料以后,两种凝胶发生组装,组装体的粘接强度达到3.9 kPa;随着体系内pH的不断增加,凝胶组装体的粘接强度不断下降,到120 min时,体系的pH达到8以上,此时凝胶之间发生解组装,组装体的粘接强度又变为0。
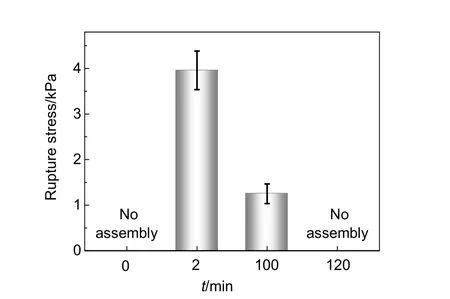
图9 体系中的凝胶组装体在不同时间的粘接强度
6 实验组织运行建议
(1) 建议本综合实验分三个模块进行教学:第一模块是两种聚电解质水凝胶的制备以及切块备用;第二模块是宏观非平衡超分子自组装体系的构建;第三模块是组装体的表征和粘接强度的测定。在教学过程中可根据三个模块的内容分三个课时进行授课。
(2) 建议教师在开始本综合实验前,采用多媒体的教学方式对本实验涉及到的实验原理、材料制备过程、仪器设备的使用方法以及各类注意事项进行讲解,使学生对实验过程有初步理解。
(3) 在实验预习阶段,学生要先通过查阅相关文献资料,了解自由基聚合的基本原理、非平衡组装的特点及其与静态自组装的区别,以便后续的实验能够顺利地开展。进行本综合实验时,要求学生根据相应的实验方案以小组的方式进行实验,要求小组成员分工合作。
(4) 在制备两种含脲酶的凝胶时,引发剂APS和促进剂TEMED的添加顺序不可调,须先加促进剂,再加引发剂,否则会导致脲酶失活。并且凝胶中的脲酶放置太长时间也容易失活,因此建议凝胶在使用时即时制备即可,以保证非平衡组装体系的成功构建。
(5) 本体系中,凝胶中脲酶的含量和化学燃料中尿素的浓度均会对单位时间内氨的产生量有较大影响,进而影响体系内pH变化的速率以及凝胶实现解组装的时间。在一定范围内,尿素的浓度固定时,脲酶的含量越高,则体系内pH升高越快,凝胶实现解组装所需要的时间越短;脲酶含量固定时,化学燃料中尿素的含量越高,则体系内pH升高越快,凝胶实现解组装所需要的时间越短。因此实验过程中教师可以根据课程时间来选择合适的脲酶含量以及尿素浓度来调节凝胶实现解组装的时间。
(6) 实验过程中用到的仪器均需要严格按照操作说明书进行,注意规范操作,并且本实验过程中会产生氨,因此耗散过程须在通风橱设备中进行。
(7) 建议每名学生在课后独立完成实验报告,对实验体系进行进一步思考,并对所得数据进行认真分析及归纳总结。
7 结语
本文介绍了一个大学化学综合实验,主要包括了聚电解质水凝胶的制备方法、宏观非平衡超分子自组装体系的构建、组装体表征方法等相关内容。聚电解质水凝胶材料的开发及应用以及非平衡组装机理研究是目前比较热门的科研方向,有助于本科生了解最前沿的科研动向。本实验综合性强,将各方面知识充分融合,可以培养学生综合运用所学知识解决问题的能力,提高学生实验操作水平,激发本科生的科研热情,从而开拓学生创新性思维,提升科学素养。另外,本实验将最新的科研成果转化为化学综合实验的教学内容,实现了超分子化学前沿研究同本科生实验教学的融合,使本科生及早接触科研,使科研育人落到实处,为学生日后升学及工作发展奠定基础,为国家和社会输送高素质的化学科学人才。
