肉桂醛纳米乳的制备及体内药动学评价
2024-02-29常格牛霞李桂玲
常格,牛霞,李桂玲
目的 构建肉桂醛纳米乳(Cin-NE),以提高肉桂醛(Cin)稳定性、溶解度以及口服生物利用度。
方法 将 Cin 同时作为药物和油相,以蓖麻油聚氧乙烯醚(EL-35)为乳化剂,构建 Cin 乳剂(Cin-E),稀释后得到具有抗稀释性的纳米递送系统—— Cin-NE,通过激光粒度仪对其粒径和 PDI 进行检测,采用 UPLC 对纳米乳中肉桂醛含量进行检测,以外观性状、粒径和含量为指标,考察长期放置的 Cin-NE 的稳定性。此外,通过对 SD 大鼠进行口服灌胃给药,研究该纳米乳的口服吸收情况以及体内药动学特征。
结果 将 Cin 载入纳米乳中,显著提高了药物在水中的溶解度;Cin-E 中 Cin 含量为 90.9 mg/ml,其制备的 Cin-NE粒径较小且分布均匀,在水、模拟胃液和模拟肠液中具有抗稀释性;4 ℃ 下放置稳定性良好。SD 大鼠口服灌胃给药的体内药动学结果表明,Cin-NE 生物利用度是 Cin 原料药的3 倍,可见纳米乳显著改善了 Cin 的口服吸收。
结论 成功构建了无需额外加入其他油相、无需助乳化剂、处方精简、工艺简单的 Cin 纳米药物递送系统 Cin-NE,其稳定性、溶解度以及口服生物利用度显著优于 Cin,为 Cin的临床应用提供了有益的探索和启示。
肉桂属于樟科植物,原产于中国,是传统的药食同源植物。肉桂中化学组分繁多,存在大量挥发油类物质,通常被称为肉桂油;此外还含有黄酮类、萜类、香豆素类、多糖等成分。肉桂油的主要成分为肉桂醛(cinnamaldehyde,Cin),含量最高可达90% 以上,是肉桂最重要的活性成分[1-2]。肉桂醛也被称为桂皮醛,天然存在的肉桂醛均为反式结构,属于天然苯并烯醛结构化合物,室温为淡黄色油状液体,并具有芳香气味。
肉桂醛来源于天然植物,易于获取,毒性极低,且已被证实具有多种显著的药理活性,包括抗炎、抗菌、抗癌以及抗糖尿病等特性[3-5]。但由于肉桂醛本身为油状液体,水中溶解度极低,导致口服生物利用度差。此外,肉桂醛长期放置易被氧化。因此,肉桂醛作为药物应用于临床仍任重而道远。通过构建肉桂醛的纳米递送系统,提高其稳定性、溶解度以及口服生物利用度,是增加肉桂醛成药性的一种可行办法。纳米乳制备简单,无需大量载体材料,载药量高,毒性低且性状稳定,可口服给药。由于其结构中同时具有亲水和亲油区域,纳米乳可显著提高药物溶解度,进而提高生物利用度[6]。由于肉桂醛室温下为油状液体,在作为药物的同时,还可作为纳米乳组分中的油相,能够进一步精简处方;且其制备方法简单,易于工业化生产。因此,本文构建肉桂醛的纳米乳递送系统,并对其抗稀释性、放置稳定性和体内药动学进行了考察。
1 材料与方法
1.1 材料
1.1.1 实验仪器 RTCbasic 磁力搅拌器为德国IKA 公司产品;ME303E 分析天平和 XS105 分析天平均为瑞士梅特勒-托利多仪器公司产品;Nano-ZS90 激光粒度及 Zeta 电位分析仪为英国马尔文仪器有限公司产品;LC-2040C 3D MT 超高效液相色谱为日本岛津公司产品;UPLC/MS/MS 系统,包括Xevo TQ-S 三重四极杆质谱仪、Acquity UPLC 均为美国 Waters 公司产品;SCI-VSv 涡旋振荡器和 D3024R 高速冷冻离心机均为美国赛洛捷克公司产品。
1.1.2 实验材料 肉桂醛、蓖麻油聚氧乙烯醚、吐温80、胃蛋白酶均购自上海麦克林生化科技股份有限公司;聚氧乙烯氢化蓖麻油购自北京华威锐科化工有限公司;胰蛋白酶购自阿拉丁生化科技股份有限公司;肉桂酸、肉桂酸甲酯、氯霉素均购自南京源植生物科技有限公司;甲醇购自美国 Thermo Fisher Scientific 公司。
1.1.3 实验动物 SPF 级 SD 大鼠18 只,8 周龄,雄性,购自北京华阜康生物科技股份有限公司,许可证号:SCXK(京)2019-0008,在昼夜交替照明、恒温恒湿环境中饲养 3 d,自由饮水进食。所有动物实验均通过中国医学科学院医药生物技术研究所动物实验中心伦理委员会批准。
1.2 方法
1.2.1 Cin-E 处方筛选及 Cin-NE 的制备 首先,对肉桂醛乳剂的乳化剂种类及含量进行筛选。室温条件下,称取 600 mg 肉桂醛,分别以吐温80、聚氧乙烯氢化蓖麻油(ethoxylated hydrogenated castor oil,RH)以及蓖麻油聚氧乙烯醚(EL-35)为乳化剂,乳化剂用量如表 1 所示,于 600 r/min转速下混合均匀,获得油相体系,然后将 5 ml 纯净水逐滴加入油相体系中,滴加过程保持转速为600 r/min,持续搅拌 3 min,使之形成分散体系,观察所得分散体系外观。对外观良好的处方进行进一步考察,取 20 μl 新制备的处方于 1.5 ml EP 管中,加入 1 ml 纯净水进行稀释,轻轻振荡混匀,后立即采用激光粒度仪进行粒径及 PDI 的测定。将制剂置于 4 ℃ 保存,于 7 d 后观察外观并再次进行粒径测定,初步筛选出可制得均匀分布的Cin-NE 的 Cin-E 最佳处方。
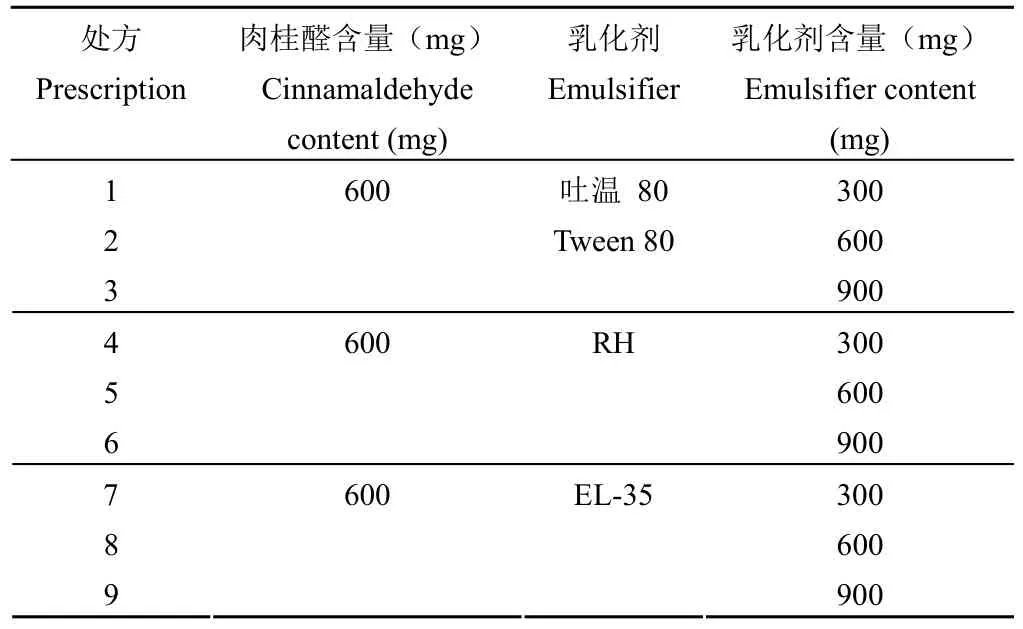
表1 肉桂醛乳剂处方筛选Table 1 Prescription screening of Cin-E
1.2.2 Cin-NE 抗稀释性研究 分别采用水、模拟胃液(SGF)以及模拟肠液(SIF)对 Cin-E 最佳处方进行抗稀释性考察,探索 Cin-E 口服给药后进入消化道形成纳米乳的可行性。
1.2.2.1 SGF 和 SIF 配制
SGF:取盐酸 384 μl 与 50 ml 水混合后,加入胃蛋白酶 1 g,混合均匀,加水稀释至 100 ml,摇匀。
SIF:称取磷酸二氢钠 0.6 g,溶解在 50 ml 水中,用氢氧化钠溶液调节 pH 至 6.8,加入胰蛋白酶 1 g,混合均匀,加水稀释至 100 ml,摇匀。
1.2.2.2 Cin-NE 对水、SGF 及 SIF 的抗稀释性研究 取 Cin-E 于 1.5 ml EP 管中,分别采用水、SGF、SIF 以 1:20、1:50、1:100、1:200、1:400、1:800、1:1600 的比例进行稀释,轻轻振荡混匀,后采用激光粒度仪进行粒径测定。
1.2.3 Cin-E 及 Cin-NE 放置稳定性考察 室温条件下,取 600 mg 肉桂醛于 5.8 ml 纯净水中,混合均匀,即得理论上总体系中 Cin 浓度与 Cin-E相同的非均相肉桂醛乳浊液(Cin-Water)。
取 20 μl 新制备的最佳处方 Cin-E 于 1.5 ml EP 管中,加入 1 ml 纯净水进行稀释,轻轻振荡混匀,即得 Cin-NE,后立即采用激光粒度及 Zeta 电位分析仪进行粒径、PDI 及 Zeta 电位的测定。
取 Cin-E 和 Cin-Water 各 10 μl,前者加水制得 Cin-NE,然后将 Cin-NE 与 Cin-Water(吸取其中水相层)分别以甲醇稀释至适宜浓度后,采用UPLC 法测定肉桂醛含量(流动相:60% 甲醇 -水,柱温:30 ℃,流速:0.2 ml/min)。
将 Cin-E 和 Cin-Water 分别避光储存于 25 ℃和 4 ℃ 条件下,考察两者在不同环境下的放置稳定性,包括粒径分布稳定性与药物含量稳定性。
1.2.4 Cin-NE 在大鼠体内药动学研究
1.2.4.1 药品配制 室温条件下,称取 600 mg肉桂醛、600 mg 蓖麻油聚氧乙烯醚,于 600 r/min转速下混合均匀,获得油相体系,然后将 5 ml 纯净水逐滴加入油相体系中,滴加过程保持转速为600 r/min,持续搅拌 3 min,使之自发形成均一分散体系,即 Cin-E。
室温条件下,称取 600 mg 肉桂醛,加入 5.8 ml橄榄油,在 600 r/min 转速下搅拌 3 min,混合均匀,制得理论上肉桂醛浓度与 Cin-E 相同的油状液体,作为肉桂醛原料药的给药形式。
1.2.4.2 分组、给药与血样采集 将雄性 SD 大鼠随机分为 3 组,每组 6 只,分别为空白组、原料药(Cin)组以及制剂(Cin-NE)组,于给药前禁食不禁水 12 h。空白组大鼠不给药,直接进行眼眶取血,置于 1.5 ml 肝素钠 EP 管中;原料药组和制剂组大鼠均以 250 mg/kg 剂量分别灌胃给予Cin 与 Cin-E(Cin-E 在消化道中被稀释产生Cin-NE),并于给药后 10、30 min、1、2、3、4、6、8、12、24 h 进行眼眶取血 200 μl,置于 1.5 ml肝素钠 EP 管中。待血样 4 ℃ 静置分层后,于3000 r/min、4 ℃ 条件下离心 15 min,取上清液,即为血浆样品,保存于 -80 ℃ 冰箱中备用,使用时于 4 ℃ 静置融化。

表2 肉桂醛及其主要代谢产物质谱条件Table 2 Mass spectrometry conditions for cinnamaldehyde and its main metabolites
1.2.4.3 液质条件 色谱柱:Waters Acquity UPLC BEH C18 色谱柱(100 mm × 2.1 mm,1.7 μm),Shim-pack GIST-HP(G) C18 预柱(2 μm);流动相:[0.02 mol/L 醋酸铵-甲醇(95:5)](A)-[0.02 mol/L醋酸铵-甲醇(5:95)](B),梯度洗脱(0 ~ 2.5 min为 100% A,2.5 ~ 5 min 线性转变为 100% B,5 ~8 min 维持 100% B,8 ~ 12 min 线性恢复为 100%A);柱温:40 ℃;流速:0.3 ml/min。采用电喷雾离子源(ESI 源);毛细管电压:3 K;脱溶剂气:500 ℃;其余质谱参数如表 2 所示。
1.2.4.4 标准曲线绘制
内标溶液:精密称取 10 mg 氯霉素于 50 ml容量瓶中,以甲醇溶解并稀释至刻度,得到内标贮备液。临用时采用甲醇将贮备液稀释 10 000 倍,得到浓度约为 20 ng/ml 的内标溶液。
对照品贮备液:精密称取 10 mg 肉桂醛、10 mg肉桂酸、50 mg 肉桂酸甲酯于同一 50 ml 容量瓶中,以甲醇溶解并稀释至刻度。采用甲醇将上述溶液稀释 5 倍作为 S1,然后倍比稀释得到 S2 ~S11,即为对照品贮备液。
系列标准溶液:分别取上述不同浓度对照品贮备液(S1 ~ S11)10 μl,向其中加入 90 μl 空白血浆,涡旋混匀。然后,分别量取上述溶液 30 μl,向其中加入 90 μl 内标溶液,涡旋 5 s,14 000 r/min、4 ℃ 下离心 10 min,取上清液,作为系列标准溶液。
空白溶液:取 30 μl 空白血浆,加入 90 μl 内标溶液,涡旋 5 s,14 000 r/min、4 ℃ 下离心 10 min。取上清液,作为空白溶液。
分别精密量取空白溶液及系列标准溶液各70 μl,进行 UPLC/MS/MS 检测,分别以肉桂醛、肉桂酸、肉桂酸甲酯的响应值对其浓度进行线性回归,得到各自的标准曲线。
1.2.4.5 样品处理及检测 分别量取 1.2.4.2 项下的血浆样品各 30 μl,向其中加入 90 μl 内标溶液,涡旋 5 s,14 000 r/min、4 ℃ 下离心 10 min。取上清液 70 μl,进行 UPLC/MS/MS 检测,记录各样品中肉桂醛、肉桂酸、肉桂酸甲酯的响应值,用标准曲线方程计算其含量。
2 结果
2.1 Cin-E 的处方筛选
肉眼观察不同乳化剂种类和用量的处方所得制剂外观,处方 1 和处方 7 可见大量白色不溶颗粒,其余处方外观良好,为均一乳白色液体。4 ℃ 放置 7 d 后,处方 4、8、9 外观无明显变化,其余处方均发生分层现象。对各处方样品进行粒径测定,结果如表 3 所示。处方 4 放置 7 d 后 PDI 过大,因此优选处方 8、9。处方 8 中 EL-35 含量更低,考虑载药量与安全性,故选择处方 8 作为Cin-E 的最佳处方,用于后续研究。
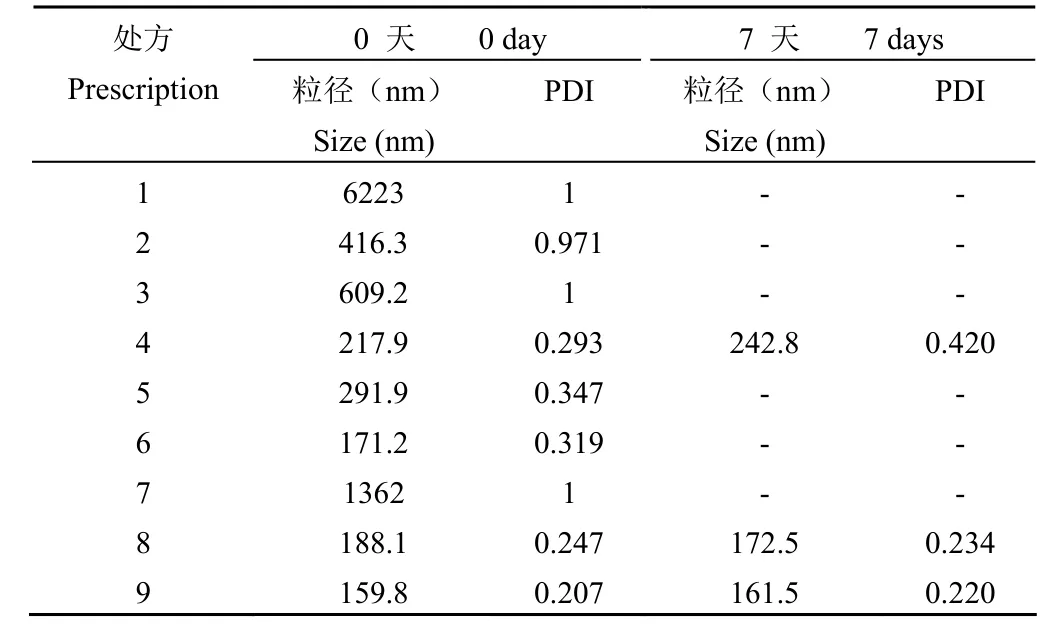
表3 肉桂醛乳剂不同处方粒径分布Table 3 Particle size distribution of various CIN-E prescription
2.2 Cin-NE 抗稀释性研究
Cin-E 在水、模拟胃液和模拟肠液中,以 1:20、1:50、1:100、1:200、1:400、1:800、1:1600 的比例稀释后,均可形成粒径分布均一的 Cin-NE(图 1),表明 Cin-E 形成 CIN-NE 的抗稀释范围大,口服后可在消化道中被稀释形成纳米乳。

图1 Cin-E 以不同比例水、模拟胃液和模拟肠液稀释后所得 Cin-NE 粒径Figure 1 The particle size of Cin-NE after dilution of Cin-E with different proportions of water, SGF and SIF
2.3 稳定性考察
新制备的 Cin-E 外观为均一的乳白色液体,加水稀释后为半透明液体,呈淡蓝色乳光,即 Cin-NE(图 2),粒径为 188.1 nm,PDI 为 0.247,说明其粒径在纳米级,且粒径分布均匀,Zeta 电位为-5.71 mV,带负电(图 3);Cin 水中饱和溶解度< 1 mg/ml,Cin-E 中 Cin 含量为 90.9 mg/ml,极大提高了 Cin 水中溶解度。Cin-Water 为非均相油水混合物,总体系中 Cin 的浓度理论上与 Cin-E相同,由稳定性考察结果可知:Cin-Water 静置后出现水油分离,水相中药物含量急剧下降;Cin-E 放置后外观良好,未见明显分层,加水稀释后制得的Cin-NE 药物含量稳定性较 Cin-Water 明显提升,且粒径分布均一。可见,与 Cin-Water 相比,Cin-NE稳定性显著提高。长期放置(365 d)后,4 ℃ 放置的 Cin-E 所得 Cin-NE 的粒径、含量均较 25 ℃更加稳定,表现出良好的放置稳定性(图 4、图 5)。需要指出的是,Cin-E 在 25 ℃ 放置 170 ~ 210 d期间,其外观性状已发生明显变化,肉眼可观察到肉桂醛析出的现象,且 PDI 也显著增大,此时的粒径结果(粒径下降)已不能准确反映体系的稳定情况。
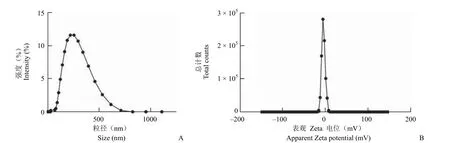
图3 Cin-NE 粒径(A)和 Zeta 电位(B)分布图Figure 3 Size (A) and Zeta potential (B) distribution of Cin-NE
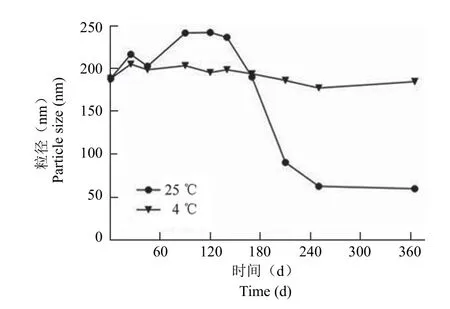
图4 25 ℃ 和 4 ℃ 贮存下 Cin-E 稀释后所得 Cin-NE的粒径变化Figure 4 Changes of particle size of Cin-NE obtained by diluting Cin-E storaged in 25 ℃ and 4 ℃ after long-term
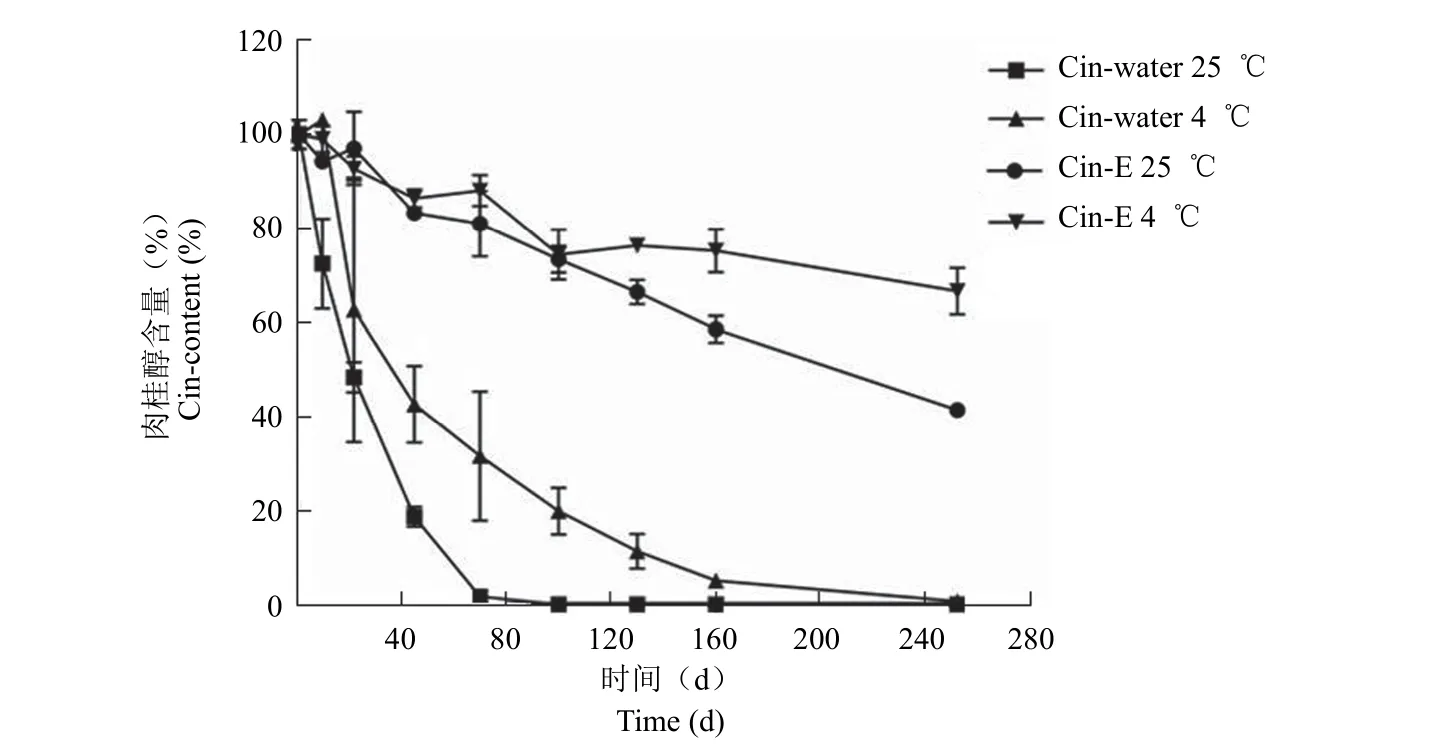
图5 25 ℃ 和 4 ℃ 贮存下 Cin-Water 和 Cin-E 中 Cin 含量变化Figure 5 Changes of Cin content of Cin-Water and Cin-NE storaged in 25 ℃ and 4 ℃ after long-term
2.4 Cin-NE 在大鼠体内药动学考察
分别以 Cin 组和 Cin-NE 组血浆样品中肉桂醛、肉桂酸、肉桂酸甲酯的浓度对时间作图,得到这几种成分的血浆浓度-时间曲线(图 6、图 7、图 8)。由结果可见,肉桂醛口服吸收入血后迅速转化为肉桂酸和肉桂酸甲酯,肉桂醛含量极低(图 6),故通过血浆中肉桂酸和肉桂酸甲酯的含量变化对体内药动学结果进行评估。
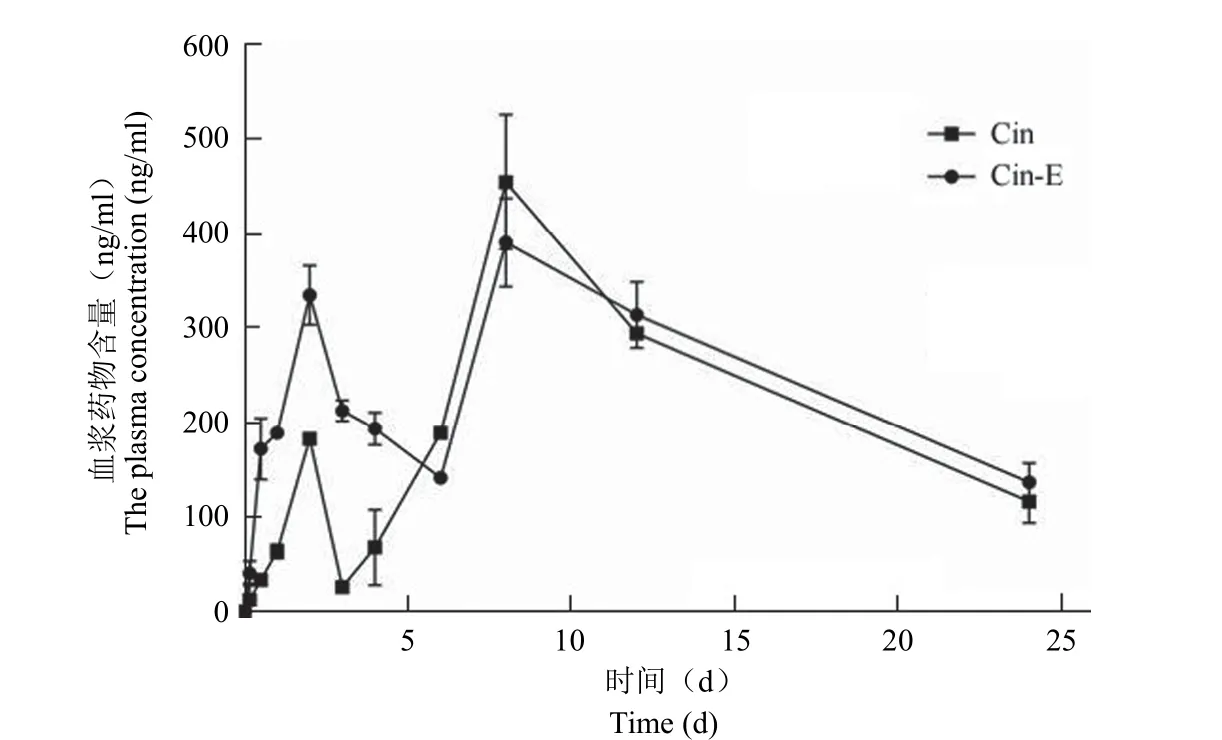
图6 大鼠血浆肉桂醛含量变化Figure 6 Changes of plasma cinnamaldehyde content in rats
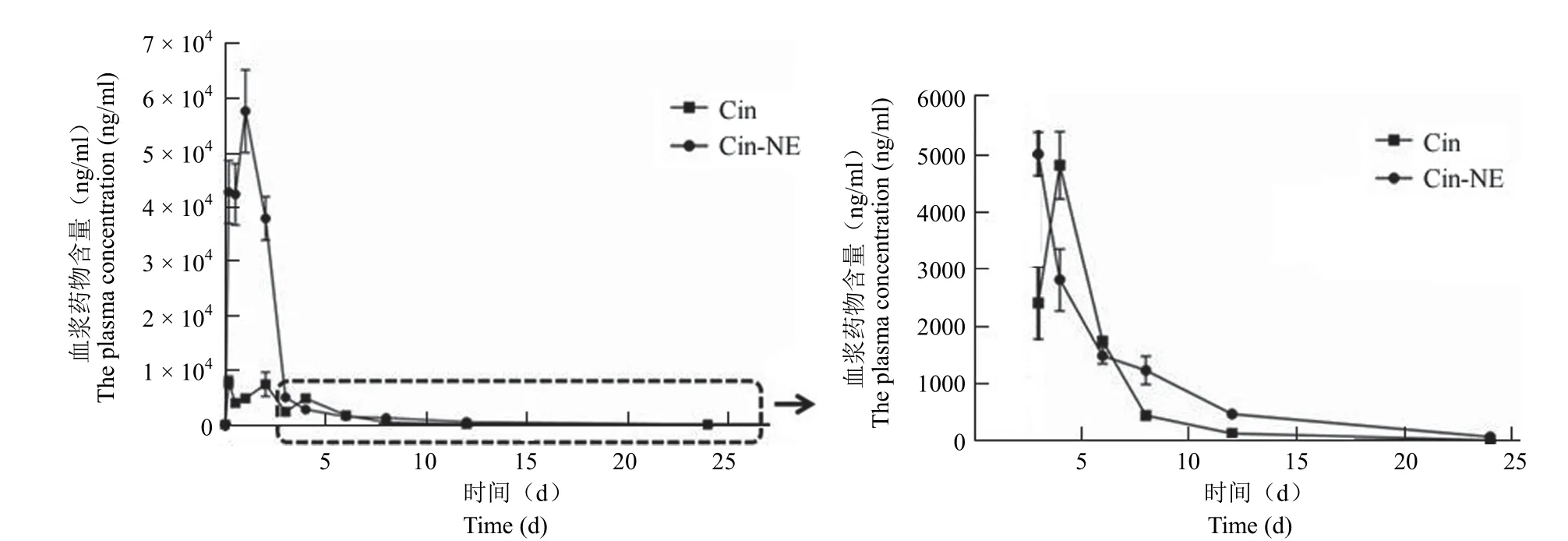
图7 大鼠血浆肉桂酸含量变化(右图为左图虚线框内的放大)Figure 7 Changes of plasma cinnamic acid content in rats (The right image is an enlargement of the left dashed box)
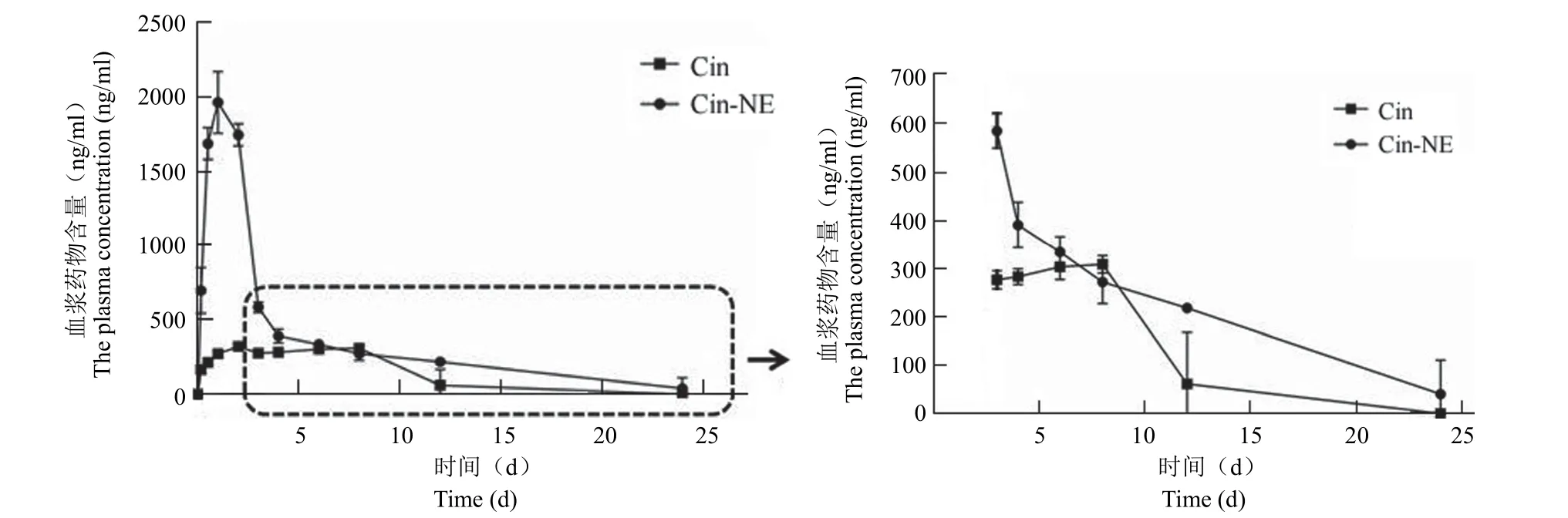
图8 大鼠血浆肉桂酸甲酯含量变化(右图为左图虚线框内的放大)Figure 8 Changes of plasma methyl cinnamic acid content in rats (The right image is an enlargement of the left dashed box)
Cin 原料药在大鼠体内口服吸收极差,而Cin-NE 显著增加了肉桂醛的口服吸收。Cin-NE 组SD 大鼠体内肉桂酸AUC是原料药的 3 倍,Cmax较原料药提高 3 倍,CLz/F 仅为原料药的 1/3(表 4);Cin-NE 组肉桂酸甲酯AUC是原料药的2 倍,Cmax接近原料药的 3 倍,CLz/F 显著下降(表 5)。

表4 大鼠体内肉桂酸药动学参数Table 4 Pharmacokinetic parameters of cinnamic acid in rats

表5 大鼠体内肉桂酸甲酯药动学参数Table 5 Pharmacokinetic parameters of methyl cinnamic acid in rats
3 讨论
Cin 作为食品中常用的天然香料成分,毒性极低且具有抗炎抗菌等多种药理活性,具有很高的药用价值。Cin 室温下为淡黄色油状液体,在水中溶解度低,口服生物利用度差,且易被氧化,长期放置稳定性差。因此,有必要通过构建 Cin 的纳米药物递送系统提高其稳定性以及口服生物利用度。
本文利用 Cin 室温为油状液体的物理性质,以 Cin 原料药自身作为油相,以 EL-35 为乳化剂,无需助乳化剂,成功制备外观呈均一乳白色的Cin 乳剂——Cin-E,该乳剂稀释后即得具有淡蓝色乳光和抗稀释性的 Cin 纳米乳递送系统——Cin-NE,经粒径测定可知其粒径在纳米级,且粒径分布良好。长期放置的 Cin-E 稀释所得的 Cin-NE外观性状无明显变化,粒径仍然保持稳定,药物含量稳定性较原料药大幅提升,且在 4 ℃ 下的放置稳定性显著优于室温,表明 Cin-NE 的构建成功提高了肉桂醛的水中溶解度与放置稳定性。此外,通过对 SD 大鼠进行口服灌胃给药,探究肉桂醛原料药及其纳米乳的体内药动学特征,可知该纳米乳显著提高了肉桂醛的口服生物利用度,具有更高的AUC,Cmax以及更小的 CLz/F。
综上可知,Cin-NE 的构建成功解决了肉桂醛原料药稳定性差、水中溶解度低以及口服生物利用度差等问题,大大增加了肉桂醛的成药性,对肉桂醛的临床应用产生一定的推进作用。
