白葡奈氏菌片联合ICS+LABA治疗中重度COPD急性发作
2024-02-28张玄陈园园张国英王静李姗姗王建春
张玄 陈园园 张国英 王静 李姗姗 王建春
慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)是呼吸科常见病,而急性发作期的中重度COPD 患者其咳嗽、咳痰、喘息及哮鸣音表现突出,严重影响到患者的生活质量。临床中针对中重度COPD急性发作的治疗研究可见,其中吸入糖皮质激素+长效β2受体激动剂(inhaled corticosteroid+longacting β2-agonist,ICS+LABA)治疗本病的效果较受肯定,但是众多相关的研究显示,其疗效仍有较大的提升空间,对于急性发作情况的控制需求仍然存在,且患者的生活质量的改善需求也较高[1-3]。临床中关于白葡奈氏菌片治疗各类呼吸系统疾病的研究均可见,其中包括在慢阻肺患者中的应用研究,但是白葡奈氏菌片对于重度急性发作患者的治疗效果研究差异较大。故本研究现探究白葡奈氏菌片联合ICS+LABA 在中重度COPD 急性发作患者中的细致应用效果及对生活质量的改善程度,报道如下。
1 资料与方法
1.1 一般资料
选取2020 年6 月—2021 年12 月山东第一医科大学附属省立医院收治的80 例中重度COPD 急性发作患者,纳入标准:20 岁及以上者;山东第一医科大学附属省立医院收治的中重度COPD,且处于急性发作阶段的患者;知情同意本研究,且临床资料完整者。排除标准:入院前接受COPD 相关的各方面治疗及干预者;存在哮喘及其他呼吸系统疾病者;合并肾、肝、肺等系统器官功能不全者;合并代谢性疾病及免疫性疾病者;沟通障碍、认知障碍及精神病史者。根据随机数字表法将患者分为2 组。2 组中重度COPD 急性发作患者的上述基线资料比较,差异无统计学意义(P>0.05),见表1。本次研究经山东第一医科大学附属省立医院医学伦理学委员会批准。

表1 2 组的一般资料比较
1.2 方法
2 组患者均进行常规抗炎、去痰解痉止咳、支气管扩张及抗氧化治疗,并进行吸氧治疗。在此基础上,对照组采用ICS 加LABA 进行治疗,以沙美特罗替卡松[Glaxo Wellcomeproduction(法国),批准文号:注册证号H20 150324;规格:50 μg :250 μg×60 泡/盒]吸入,1 吸/次,其中含有50 μg 沙美特罗与250 μg 丙酸氟替卡松,2 次/d。观察组则在上述常规的各项治疗措施基础上,口服白葡奈氏菌片(齐鲁制药有限公司;批准文号:国药准字H37 023540;规格:0.3 mg×40 片),以白葡奈氏菌片口服,4 片/ 次,3 次/d。2 组患者的治疗时间均为2 周。
1.3 观察指标
将2 组的COPD 治疗总有效率、不良反应发生率进行统计及比较,同时将2 组治疗前后的症状体征积分、疾病状态[慢性阻塞性肺疾病评分(COPD assessment test,CAT 评分)]及生活质量[世界卫生组织生存质量测定量表简表(World Health Organization on quality of life brief scale,WHOQOL-BREF 评分)]进行比较。(1)COPD 治疗效果:以患者的COPD 相关症状体征积分改善幅度在90%及以上为基本控制,以患者的COPD 相关症状体征积分改善幅度在30%~89%为有效,以患者的COPD 相关症状体征积分改善幅度不足30%则判定为无效[4]。COPD治疗总有效率=(组内基本控制例数+组内有效例数)/组内总例数×100%。(2)不良反应:将2 组COPD 患者治疗期间出现的不良反应进行统计,其包括心悸、皮疹、皮肤瘙痒等。(3)症状体征积分:对患者的咳嗽、咳痰、喘息及哮鸣音等进行评分,以《中药新药临床研究指导原则》进行评估,每个方面的评分范围为0~3 分,其中0 分为无相关表现,1 分为轻度,2 分为中度,3 分为重度[5]。(4)CAT 评分:本标准是有效评估COPD 疾病状态的标准,其包括8 个评估项目,每个方面的评分范围为0~5 分,患者得分为0~10 分、11~20 分、21~30 分及31~40 分分别判定为病情轻微、病情中度、病情严重及病情非常严重[6]。(5)WHOQOL-BREF 评分:于治疗前及治疗1、2 周后分别采用WHOQOL-BREF评分标准评估2 组COPD 患者的生活质量,其含有4 个维度,分别为生理、心理、社会关系及周围环境,上述4 个维度均换算为百分制,且每个维度换算后的得分越高表示患者的生活质量越高[7]。
1.4 统计学处理
研究中的统计学采用SPSS23.0 软件分析,计数资料的描述方式为n(%),计量资料的描述方式为(),采用上述软件对上述分类后的数据分别进行χ2检验与两独立样本均数t检验,等级资料数据则采用秩和检验,P<0.0 5 表示差异有统计学意义。
2 结果
2.1 2 组COPD 患者的治疗总有效率比较
治疗1 周、2 周后观察组患者的COPD 治疗总有效率显著高于对照组,差异有统计学意义(P<0.05),见表2。

表2 2 组COPD 患者的临床治疗总有效率比较 [例(%)]
2.2 2 组不良反应发生率比较
2 组的不良反应发生率差异无统计学意义(P>0.05),见表3。

表3 2 组不良反应发生率比较 [例(%)]
2.3 2 组治疗前后的症状体征积分比较
治疗前2 组的症状体征积分差异无统计学意义(P>0.05),治疗1、2 周后观察组的症状体征积分显著低于对照组,差异有统计学意义(P<0.05),见表4。
表4 2 组治疗前后的症状体征积分比较(分,)
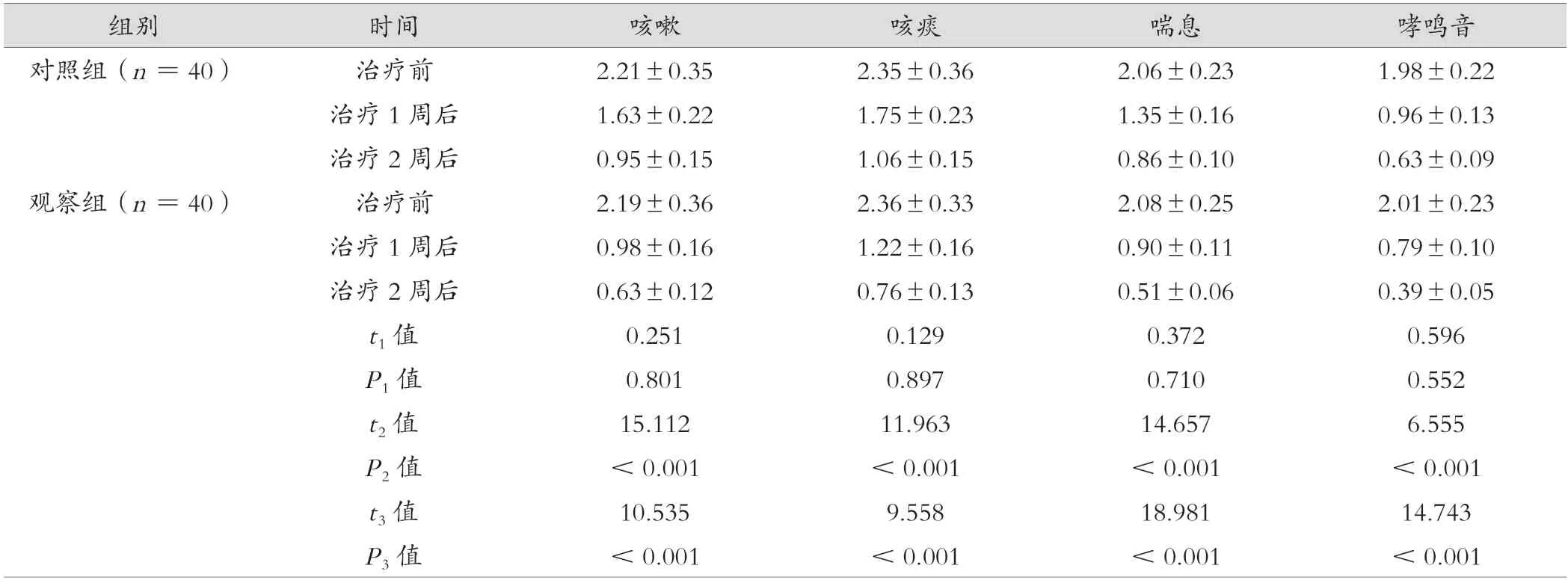
表4 2 组治疗前后的症状体征积分比较(分,)
注:t1 值、P1 值为2 组治疗前比较,t2 值、P2 值为2 组治疗1 周后比较,t3 值、P3 值为2 组治疗2 周后比较。
2.4 2 组治疗前后的CAT 评分比较
治疗前2 组的CAT 评分构成差异无统计学意义(P>0.05),治疗1、2 周后观察组的CAT 评分构成优于对照组,差异有统计学意义(P<0.05),见表5。
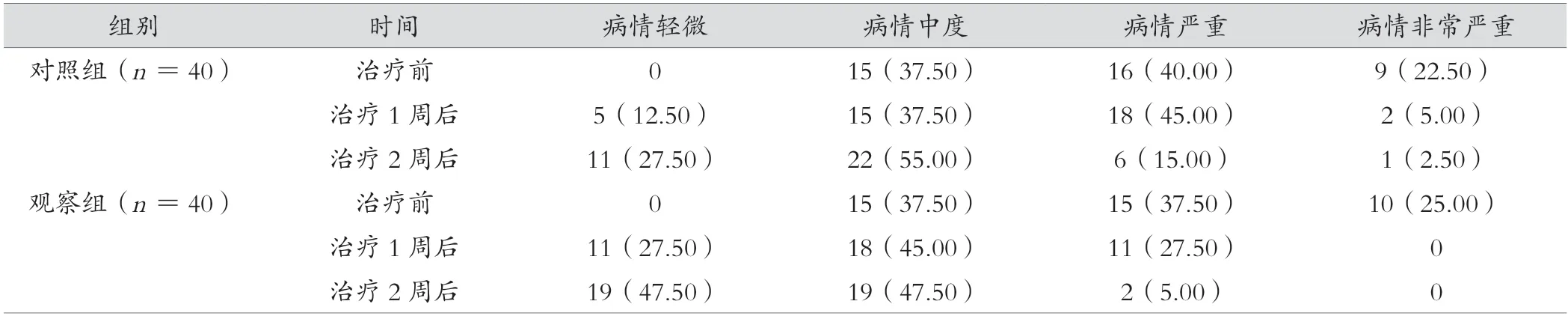
表5 2 组治疗前后的CAT 评分构成比较 [例(%)]
2.5 2 组治疗前后的WHOQOL-BREF 评分比较
治疗前2 组的WHOQOL-BREF 评分差异无统计学意义(P>0.05),治疗1、2 周后观察组的WHOQOLBREF 评分显著高于对照组,差异有统计学意义(P<0.05),见表6。
表6 2 组治疗前后的WHOQOL-BREF 评分比较(分,)
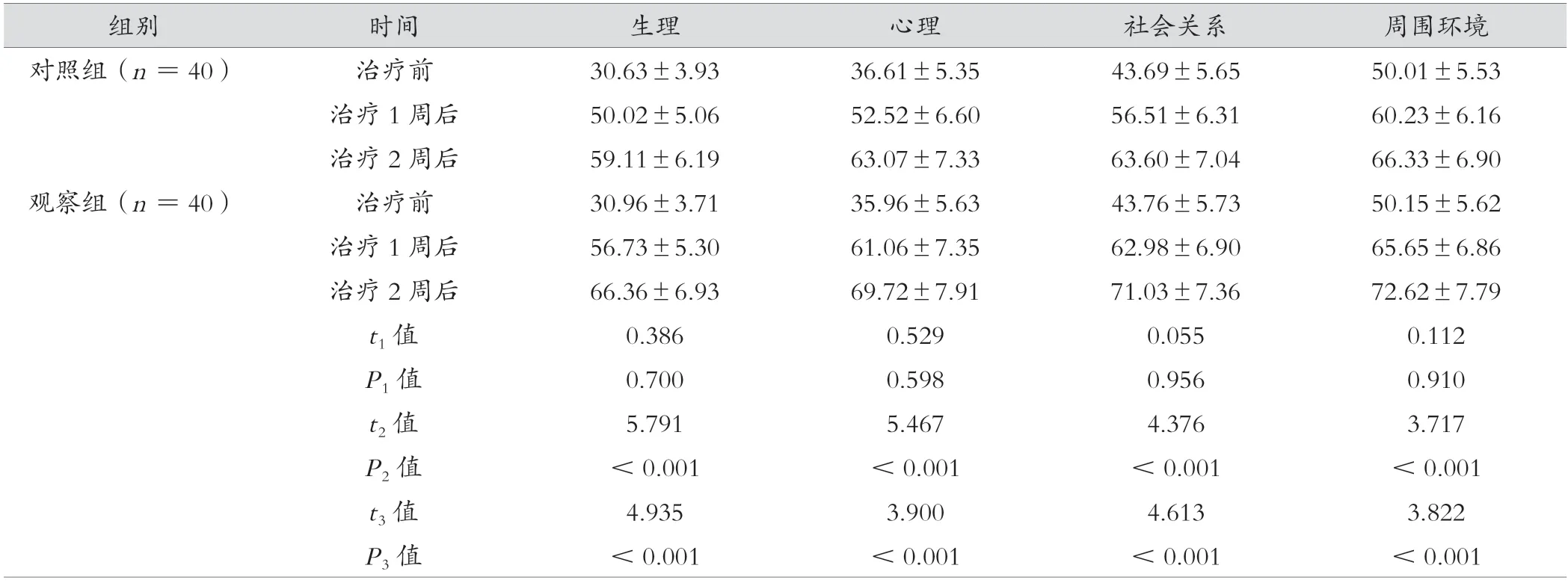
表6 2 组治疗前后的WHOQOL-BREF 评分比较(分,)
注:t1 值、P1 值为2 组治疗前比较,t2 值、P2 值为2 组治疗1 周后比较,t3 值、P3 值为2 组治疗2 周后比较。
3 讨论
COPD 患者的气流受限情况突出,严重影响到患者的健康状态、生活质量,而中重度的COPD 急性发作患者的咳嗽、咳痰、喘息等情况相对更为突出。临床中针对中重度COPD 急性发作的诊治研究多见,其中ICS+LABA 用于本类患者的研究占比较高,上述药物不仅仅对于气道炎症具有较好的控制作用[8],且对气道重塑具有调控作用,而COPD 患者的气道炎症及气道重塑等情况表现突出,尤其是急性发作患者的上述方面表达波动幅度相对更大,因此上述药物对于COPD 患者的应用效果值得肯定。但是众多相关的研究显示,本类治疗方案的治疗效果仍有一定的提升空间[9]。近年来临床中采用白葡奈氏菌片治疗呼吸系统疾病的研究不断增多,其在提高机体非特异性免疫和呼吸系统的特异性免疫功能方面均有较好的作用,同时其还可以影响到延脑的咳嗽中心,因此有助于调控咳嗽反射,在控制咳嗽及呼吸道黏液分泌方面均有较好的效果[10],其用于COPD 急性发作与诊治的研究可见,但是细致的作用研究仍不足。
本研究结果显示,加用白葡奈氏菌片的效果相对更好,优势体现在多个方面,包括COPD 治疗总有效率相对更高,症状体征积分、CAT 评分及WHOQOL-BREF 评分改善幅度更大,差异有统计学意义(P<0.05),而其不良反应发生率未见显著升高,差异无统计学意义(P>0.05),说明其在有效提升中重度COPD 急性发作疗效的基础上,安全性也值得肯定。分析原因,ICS+LABA 对COPD 的局部炎症及气道重塑进行了有效控制的基础上,白葡奈氏菌片对机体免疫及呼吸道咳嗽中枢进行了有效的调控[11-12],因此更有助于提升COPD 治疗的效果,同时对于植物神经的调控,有助于呼吸道黏膜腺体的分泌调控,因此对咳嗽、咳痰等情况也有较好的改善作用,故认为加用白葡奈氏菌片的临床优势更为突出[10]。
综上所述,白葡奈氏菌片联合ICS+LABA 在中重度COPD 急性发作阶段的应用效果更为显著,且对本类患者的生活质量具有更好的改善作用。此文的研究结果为慢阻肺相关诊治措施的后期标准制定提供了借鉴内容。
