氯化钾水溶液微观结构的分子动力学模拟研究
2024-02-01王丽娜张文惠尚洁莹赵兴宇周恒为
王丽娜, 张文惠, 尚洁莹, 赵兴宇, 周恒为
(伊犁师范大学 物理科学与技术学院 新疆凝聚态相变与微结构实验室, 伊宁 835000)
1 引 言
液体微观结构是一个被人们长期关注的问题,溶液作为一类常见的液体,也是重要的学术研究对象. 现有结果表明在一些溶液中虽然从表观上看是均匀的,但是在微观上却存在着不均匀性或团簇[1-15]. 这些现象不仅存在于电解质溶液之中,而且也存在于一些二元混合液体中. 在电解质溶液中这种不均匀性表现为离子团簇的存在[5,6,10,15];在二元混合液体中表现为两个玻璃化转变过程共存或者两个α弛豫过程共存,该现象需要在假设二元液体中存在着微观不均匀的前提下,才能得到较为合理的解释[3,4,11-14]. 总之,溶液仍然需要人们不断地开展研究[2,16-18].
近期的研究表明在氯化钠水溶液中存在着直接接触离子对、部分间隔离子对和完全间隔离子对,并且以离子对为基础形成了由离子与水分子共同构成的离子团簇,同时溶液中也存在着水分子连续分布的区域[5,7,8,15];而且二者的组成分别与氯化钠水溶液低温下所形成NaCl·2H2O晶体与冰的组成具有一致性[15,19],引发人们对溶液形成晶体机制的思考. 盐的水溶液的种类十分众多,依据所形成晶体的不同,可以将其分成两类:一类是只能形成无水盐和冰的溶液,例如氯化钾水溶液和硝酸钠水溶液等,另一类是可以形成水合盐(即盐与水发生水合反应而形成的水合物)和冰的溶液,例如氯化钠水溶液和硫酸镁水溶液等[19,20]. 因此,对不同类型盐的水溶液中离子分布和团簇情况进行研究,并与其所形成的晶体结构进行比较,将有助于认知溶液的微观结构和结晶机制.
在氯化钾水溶液的研究方面,Ahmadi等[21]在293 K和1 atm下对过饱和氯化钾水溶液的均匀成核进行了分子动力学模拟,表明晶核在氯化钾局域浓度高的区域形成. Wang等[22]在弱静磁场的作用下,通过X射线衍射和分子动力学方法对氯化钾水溶液的结构进行了考察. 结果表明磁场会影响离子的水化半径和自扩散系数,还会导致离子的结构从无序变为有序;而且钾离子更容易受到磁场的影响,但浓度越高,磁场的影响越小. Peng等[23]通过分子动力学方法对氯化钾水溶液表面处的水分子角度、表面张力和表面电位等进行了分析,结果也与实验相一致.
氯化钾水溶液作为一种降温时只形成无水盐和冰的物质[20],虽然人们已经对其进行了一些研究,但是该溶液离子与溶剂共同作用下所形成的离子团簇、水分子的空间分布情况,以及二者与此溶液在低温下所形成晶体的联系,依然有待于进一步研究. 氯化钾水溶液中离子结构简单,便于分析. 因此,本文以氯化钾水溶液为对象开展了研究工作.
2 模型建立与模拟方法
模型中的水分子是通过常用的SPC/E模型[8,24]来构建的,其氢键长度r0为0.1 nm,H-O-H的键角θ0为109.47 °. 除水分子外,模型中还包含K+和Cl-两种离子. 原子间、离子间以及原子与离子间的相互作用采用Lennard-Jones势和库仑相互作用来描述,具体见文献[15]. 每种原子或离子在Lennard-Jones势中的能量参数ε和尺寸参数σ以及在库仑相互作用中的电荷量q如表1所示[8,21,24]. 异种原子或离子之间的ε和σ按照Lorentz-Berthelot混合规则来计算.
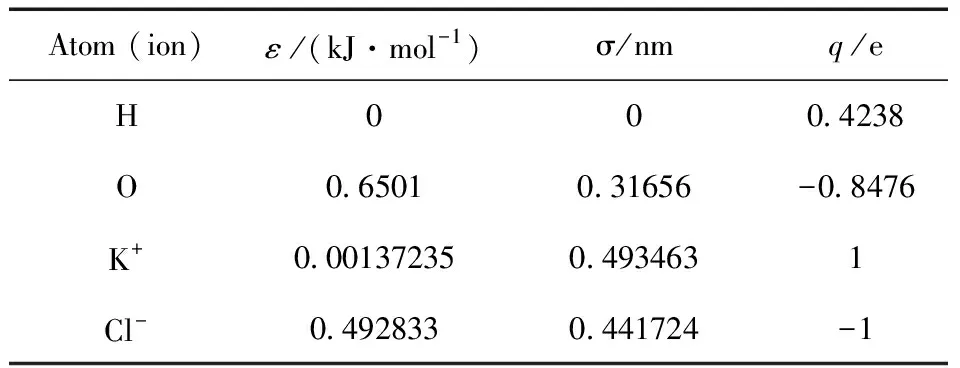
表1 原子和离子的势参数
模型的原始构型是由330个水分子以及13对K+和Cl-随机分布在立方体格点上而构成的,对应的KCl的质量分数为14.02%,摩尔分数为3.79%. 模拟过程是在300 K和1 atm的等温等压条件下通过Lammps软件[25]实施的,模拟时的边界为周期性边界,水分子为刚性分子. 时间步长为1 fs,具体模拟细节见文献[15]. 模拟工作是在原始构型弛豫1 ps之后的基础上进行的,即计时零点为该时刻. 本文的模拟时长为4 ns,为了使所获得的结果能够体现系统平衡态的性质,本文分析中所用的数据都取自2 ns之后.
3 模拟结果与讨论
图1所示的是模拟所得的氯化钾水溶液中原子或离子间的径向分布函数g(r),这里r是到中心原子或离子的距离. 从图1(a)中O-O的g(r)可以看出水分子的分布符合液体的特征,与文献[21]中的结果相符,径向分布函数上的峰的最大值分别位于r为0.275 nm、0.445 nm和0.685 nm处. 图1(b)和(c)分别是K+-K+和Cl--Cl-的径向分布函数,可以看出二者呈现出了相似的形状特征,而且峰的最大值所对应的r都分别相同,依次为0.445 nm、0.625 nm和0.835 nm. 氯化钾水溶液中的这些特征都明显不同于氯化钠水溶液的;从峰值的大小上来看,氯化钾水溶液中同种离子(K+-K+和Cl--Cl-)的径向分布函数第一峰的值比氯化钠水溶液的要大得多,第二峰的值也较大,并且第一峰的峰值要大于第二峰的[8,15].
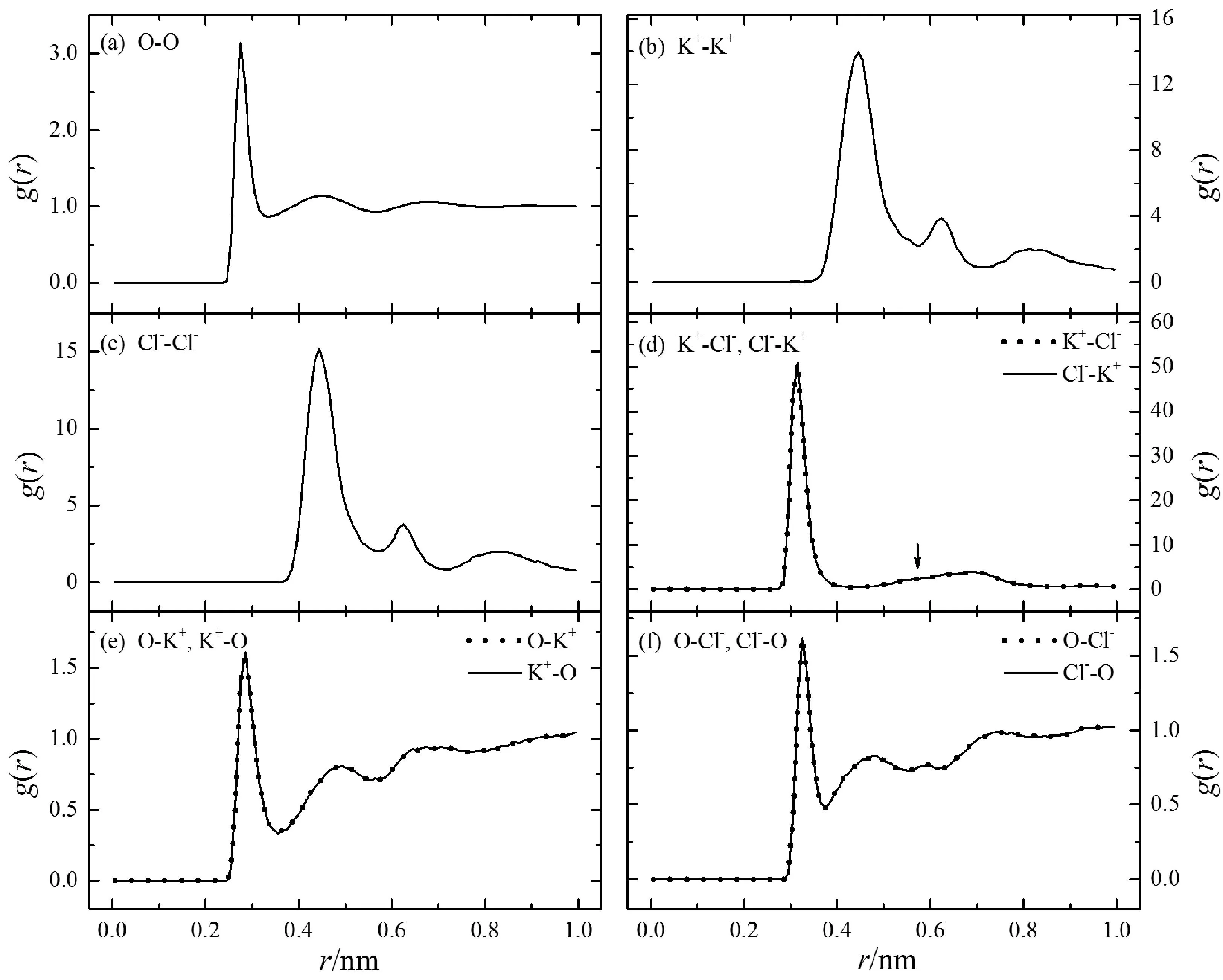
图1 氯化钾水溶液的径向分布函数g(r)Fig.1 Radial distribution functions g(r) in solution of potassium chloride.
图1(d)是K+-Cl-和Cl--K+的径向分布函数,二者之间相互重合得很好,三个峰的最大值分别位于r为0.315 nm、0.575 nm和0.695 nm处. 该径向分布函数上第一峰的峰值远大于氯化钠水溶液中Na+-Cl-和Cl--Na+的[7,8,15],并且第一峰的峰值也远大于第二峰(图1(d)箭头所示处)的,值分别为51.0和2.4;第三峰略高于第二峰. 图1(e)和(f)是K+-O与O-K+、O-Cl-与Cl--O的径向分布函数,也分别能够相互重合,但是其第一峰的峰值要比氯化钠水溶液中对应径向分布函数的值要小[7,8,15],分别约为21%和43%,说明在氯化钾水溶液中,每个离子周围有着更少的水分子分布.
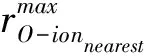
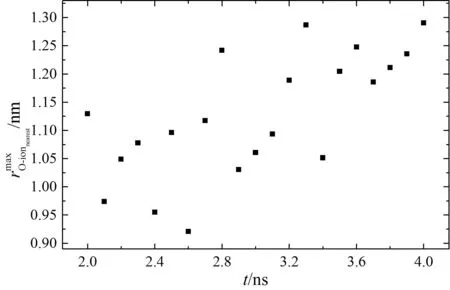
图2 系列时刻下瞬态图像中O到其最近离子间的最大距离Fig.2 Maximum distances from O to its nearest ion in transient images at a series of moments.
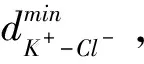
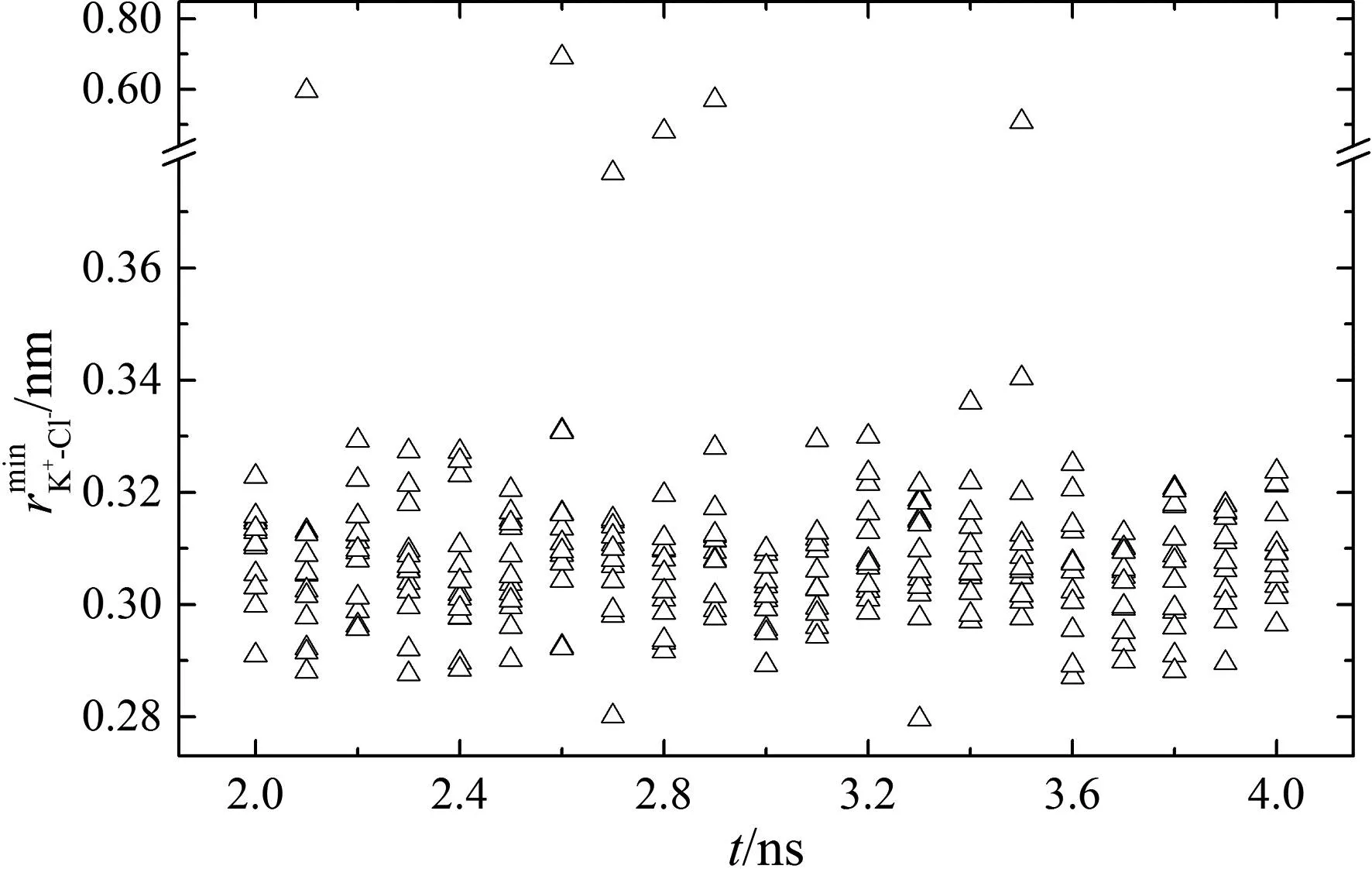
图3 系列时刻下瞬态图像中K+与其最近邻Cl-之间的距离Fig. 3 Distances between K+ and its nearest neighbor Cl- in transient images at a series of moments.
由于在氯化钾水溶液中,K+与Cl-之间主要以直接接触离子对的形式而存在,该类离子对与K+-Cl-径向分布函数上的第一峰相对应,所以为了研究以此类离子对为基础而形成的离子团簇,这里选择该径向分布函数上第一峰谷所对应r的大小(值为0.435 nm)作为判据来统计离子所形成的团簇[10,15]. 图4所示的是统计所得的每幅瞬态图像中包含的团簇数nIC以及团簇内的离子数nion,可以看出nIC最多为4,最少为1,多数在1~3之间. 从每个团簇中的离子数来看,团簇主要可以分为两类,一类是较大的团簇,离子数在22~26之间,平均值为25.0;一类是较小的团簇,离子数在1~2之间,平均值为1.2. 离子数为1的团簇,也就是以单独形式存在的离子. 结合图5中团簇大小dIC随nion的分布情况,可以看出离子数少时,dIC值较小(这里认为离子数为1的团簇的大小为0 nm),而离子数多时,其值则较大;较大团簇的尺寸分布在1.28 nm~2.60 nm的范围之内,平均值为1.73 nm. 氯化钾水溶液中较大离子团簇的存在说明K+与Cl-倾向于以团簇的形式存在,也表明氯化钾水溶液中存在着明显的自聚集效应[25-28]. 溶液中较小团簇甚至是单独离子的存在,应该是由离子和水分子的相互作用以及它们的热运动所导致的.
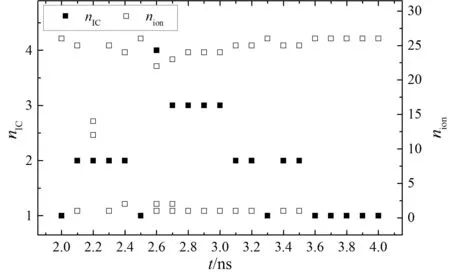
图4 系列时刻下瞬态图像中的团簇数nIC和每个团簇中的离子数nionFig.4 Cluster number nIC in transient images at a series of moments and number of ions nionin each ion cluster.
图6是瞬态图像中离子的典型分布情况,图中最大团簇之外的离子已经用虚线圈出,其余的离子都属于相应时刻下最大的离子团簇,每幅图都是以较容易观察出离子团簇结构的角度呈现地. 可以看出较大团簇内部的离子与周围离子之间呈现出了氯化钾晶体的类似结构,即一种离子填充在异种离子所形成的八面体空隙中;而且结合图7(a),可以看出这些离子之间并不存在水分子,其物质组成也与氯化钾晶体的相一致,而且绝大多数离子都存在于这类团簇中. 在较大团簇中离子按该结构分布也是导致K+-O、O-K+、O-Cl-与Cl--O的径向分布函数中第一峰的峰值要比氯化钠水溶液中对应径向分布函数上相应峰值要小的原因,也验证了前文关于氯化钾水溶液中离子对主要是直接接触离子对的推测. 在较大团簇边缘的离子会出现以K+和Cl-交替排列的链状形式向外延伸;同时可以发现离子团簇的大小和形状会随着时间的改变而变化.
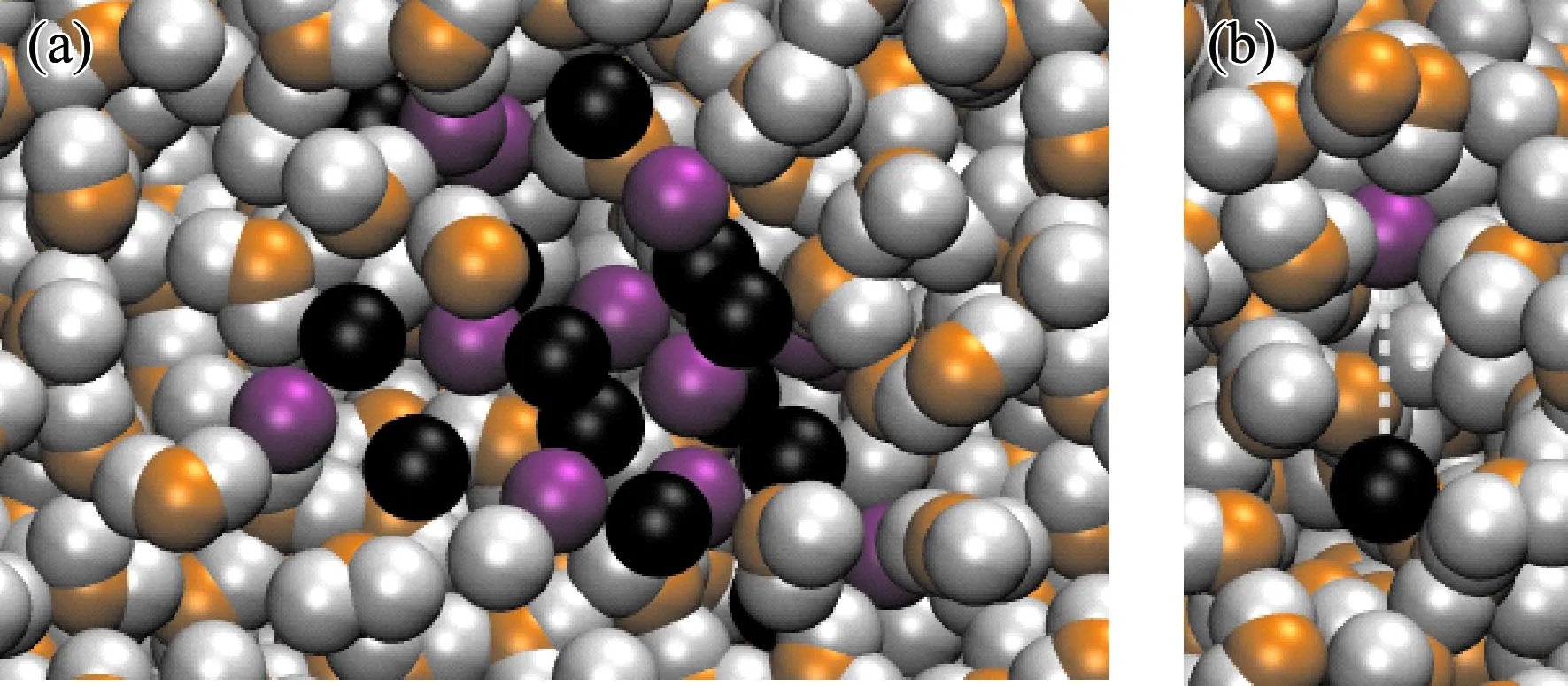
图7 最大离子团簇内部及其附近水分子的瞬态图(a)和部分间隔离子对的图像(b). 图(b)中离子对上层的水分子未显示,离子间距为0.570 nm(紫色、黑色、橘色和白色分别代表K+、Cl-、O和H). Fig. 7 Transient images of the largest ionic cluster and its nearby water molecules (a)as well as image of partially-spaced ion-pair (b). Some water molecules in the upper layer of the ion-pair are not shown in the Fig. (b)and the distance between the two ions is 0.570 nm (colors of purple,black,orange and white represent K+,Cl-,O and H,respectively).
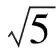

将氯化钾水溶液中原子或离子间的相互作用参数与氯化钠水溶液的进行对比,可以发现其主要差别就是K+的取值与Na+的不同. 与Na+相比,K+的ε较小,σ较大,而q则相同. 这导致在平衡时K+与O的相互作用势要弱于Na+与O的,而且水分子中还有H,而阳离子与H之间的库仑作用力为斥力,最终导致K+与水分子的结合较弱,而与Cl-之间的结合相对较强,从而使大多数K+与Cl-形成了直接接触离子对. 由此可以发现原子、离子间的相互作用对形成的团簇结构以及微观不均匀性具有重要影响,当然形成微观不均匀的机制还有待于深入研究.
在本文所研究的浓度下,氯化钾水溶液在低温下形成的固体为冰和氯化钾晶体,而上述结果所呈现出的水分子连续分布区域以及离子团簇的物质组成分别与这两种固体的组成相一致,并且离子团簇的结构和氯化钾晶体的是类似的,而氯化钠水溶液的结果也同样表明了这种对应关系. 综合考虑这两种类型的溶液,可以发现溶液所形成的晶体种类与溶液中水分子连续分布区域以及离子团簇的组成密切相关,也就是在溶液中已经存在了晶体所对应的单元. 这些结果为理解溶液中的结晶过程提供了思路,也为认知液体的结构和动力学提供基础.
4 结 论
本文通过对氯化钾水溶液的分子动力学模拟结果进行分析,获得了该溶液性质和微观结构的一些认知. K+-K+和Cl--Cl-径向分布函数的特征具有一致性,三个峰的最大值所对应的位置分别相同;K+-Cl-和Cl--K+的径向分布函数能够彼此重合,K+与其最近邻Cl-之间的距离主要分布在0.28 nm至0.38 nm之间,位于K+-Cl-径向分布函数上第一峰的范围之内;所对应的离子对为直接接触离子对,占比约为97.4%,是K+-Cl-径向分布函数上第一峰的来源.
系列时刻下瞬态图像内O到其最近离子距离中最大值的统计结果表明氯化钾水溶液中存在着水分子连续分布的区域,其平均尺寸至少为2.26 nm. 瞬态图像还表明溶液中主要存在着较大和较小两类离子团簇,包含的离子数分别在22~26之间和1~2之间,离子团簇的大小和形状会随着时间的改变而变化;较大团簇的尺寸在1.28 nm~2.60 nm的范围内. 较大的离子团簇和水分子连续分布区域的存在表明了氯化钾水溶液具有微观不均匀性和自聚集效应.
较大团簇内部的离子与周围离子之间具有氯化钾晶体的类似结构,即一种离子填充在异种离子所形成的八面体空隙中. 将K+-Cl-、Cl--K+、K+-K+和Cl--Cl-径向分布函数上各峰最大值所对应距离间的关系与氯化钾晶体中各离子间距离的几何关系进行对比,表明K+-Cl-和Cl--K+径向分布函数上第三峰应该来源于较大离子团簇内第二近邻的异号离子,K+-K+和Cl--Cl-径向分布函数上第一、第二和第三峰也来源于较大离子团簇内的相应离子. 在此基础上,结合溶液中离子的分布图像,表明K+-Cl-和Cl--K+径向分布函数上第二峰来源于部分接触离子对,但是该类离子对所占比例非常低,仅约为1.47%. 另外,结合原子、离子间的相互作用对离子对和团簇形成的原因进行了解释.
氯化钾水溶液中水分子连续分布区域以及离子团簇的物质组成分别与其低温下形成的冰和氯化钾晶体两种固体的组成具有一致性,而且离子团簇的结构和氯化钾晶体的类似. 再结合氯化钠水溶液中同样的对应关系,表明溶液所形成的晶体种类与溶液中水分子连续分布区域以及离子团簇的组成密切相关,也就是在溶液中已经形成了晶体所对应的单元,这些结果为理解溶液中的结晶过程提供了基础.
