六硼酸钡Ba3B6O9(OH)6热力学性质研究
2024-02-01岑方龙冯晓琴王万钟陈南洋武文韬黄宏升
岑方龙, 冯晓琴,2, 王万钟, 陈南洋, 武文韬, 黄宏升,2
(1.贵州理工学院 化学工程学院, 贵阳 550003; 2.贵州理工学院 贵州省普通高等学校能源化学特色重点实验室, 贵阳 550003)
1 引 言
硼酸盐种类繁多并且结构复杂多变. 硼及其化合物在如玻璃、陶瓷、纺织、冶金、航空、军工等[1]众多工业领域具有较高的应用价值,正越来越受到人们重视. 硼酸盐因具有质轻、阻燃、高强、耐热、非线性光学等[2,3]特殊性能,在通讯、阻燃剂、非线性光学 (NLO)材料等领域具有潜在应用[4,5],其中硼酸钡盐,如β-BaB2O4[6]、BaAl2B2O7[7]、Ba2Be2B2O7[8]等被用作非线性光学材料,高折射率和高电子极化率的玻璃[9]、辐射屏蔽玻璃[10]、光功率限制等[11]. 因此,对于硼酸钡盐受到越来越多的关注.
热力学性质在科学研究和工业应用中起着非常重要的作用,热力学数据可以提供有关所用分子的稳定性和反应性的信息. Bassett[12]曾系统收集了1976年以前发表的无水和水合硼酸盐热力学性质数据. 近几十年来,李军、高世扬、刘志宏和Gurevich等人[13-18]测试了KB5O8·4H2O、NaB5O8·5H2O、Ca2B6O11·5H2O、Mg2B12O20·7H2O、SrB6O10·5H2O、BaB8O11(OH)4·3H2O和Zn[B12O14(OH)10]等碱金属硼酸盐、碱土金属硼酸盐和过渡金属硼酸盐的标准摩尔生成焓等热力学性质. 此外,人们开发了一些经验和理论方法来关联和预测化合物的热力学性质,如李军、高世扬等人[15]在前人研究的基础上结合实验测定结果,提出了“Group Contribution Method” (基团贡献法),应用于硼氧酸盐热力学性质的预测,提出了关联和预测水合硼酸盐热力学性质的方程.
Yu等人[19]首次合成制备得到了Ba3B6O9(OH)6,是第一个发现硼原子均是四配位的链状结构的硼酸盐,后Li等[20]人利用水热法制备得到了纳米棒状的Ba3B6O9(OH)6,并通过焙烧它制备得到了β-BaB2O4(BBO). Feng等人[21]采用水热法制备了Ba3B6O9(OH)6∶Eu3+,并通过焙烧它制备得到了BaB2O4∶Eu3+,结果表明Ba3B6O9(OH)6是一种良好的发光材料基质,且可用于制备BaB2O4,但并未发现有关于Ba3B6O9(OH)6热力学性质的报道. 因此,本文采用水热法合成了六硼酸钡盐Ba3B6O9(OH)6并测定了它的标准摩尔生成焓,根据测试结果采用基团贡献法估算了[B6O9(OH)6]6-的标准摩尔生成焓.
2 实验部分
2.1 仪器和试剂
101-0A型电热鼓风干燥箱(天津市泰斯特仪器有限公司);78-1型磁力加热搅拌器(江苏中大仪器);FA2004B型电子天平(上海佑科仪器);SHZ-D(Ⅲ)型循环水式多用真空泵(巩义市科华仪器);Nicolet· NEXUS 670型傅里叶红外光谱仪(FI-RI,布鲁克光谱仪公司);ULtima·IV型 X-射线衍射仪(XRD,日本理学);Nova Nano SEM 450型电子扫描显微镜(SEM,美国FEI公司);TG 209 F3型综合热分析仪(TG-DSC,德国耐驰公司).
硝酸钡(Ba(NO3)2,≥99.5%)购自上海沃凯生物技术有限公司;四硼酸钠(Na2B4O7·10H2O,≥99.5%)购自天津博迪化工股份有限公司;无水乙醇(C2H5OH,≥99.7%)购自天津市富宇精细化工有限公司;高纯氯化钾(KCl,≥99.99%)购自天津市富宇精细化工有限公司;碳酸钠(Na2CO3,≥99.8%)购自天津市永大化学试剂有限公司;盐酸(HCl,质量分数为46%~48%)购自天津市富宇精细化工有限公司.
2.2 实验方法
2.2.1Ba3B6O9(OH)6的制备
合成中使用的所有试剂都是分析纯试剂. 称取1.2959 g硝酸钡溶解于40 mL蒸馏水中,然后将40 mL溶有2.2925 g硼砂的溶液加入上述溶液中,混合搅拌30分钟后,将其转移至水热反应釜中,在240 ℃中反应24 h,将产物抽滤,并分别用热水、无水乙醇洗涤,然后将其在50 ℃下干燥24小时,得到Ba3B6O9(OH)6产物.
2.2.2表征方法
合成样品分别用利用傅里叶红外分析仪(Nicolet NEXUS 670,测试波数范围为4 000~400 cm-1,分辨率4 cm-1)对其官能团进行分析;利用X射线粉末衍射仪(日本ULtima Ⅳ型,Cu靶Ka线,石墨片滤波,步长0.02 °/s,扫描范围:10 °~70 °)对其进行物相分析;利用热重差热分析(德国耐驰TG209F3Tarsus,以20 ℃/min的速率升温,升温范围25~800 ℃)对其热分解过程进行分析;利用扫描电镜(美国Nova Nano SEM 450,电子流强度为20 keV,电子加速电压为0.5~30 kV,放大倍数为10 000~50 000)对其进行形貌分析.
2.2.3标准摩尔生成焓的测量方法
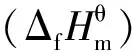
在298.15 K下参照文献[23]的方法利用量热仪测定了Ba3B6O9(OH)6在0.9995 mol ·dm-3HCl(aq)中的标准摩尔溶解焓. 根据盖斯定律,结合热力学循环其它反应的反应焓(ΔrHmθ),ΔrHmθ(5)可根据以下表达式计算:
ΔrHmθ(5)=ΔrHmθ(1)+ΔrHmθ(2)-
ΔrHmθ(3)-ΔrHmθ(4)
再结合虚拟反应中Ba(OH)2·8H2O(s)、H3BO3(s)、H2O(l)的标准摩尔生成焓,即可得到Ba3B6O9(OH)6的标准摩尔生成焓.
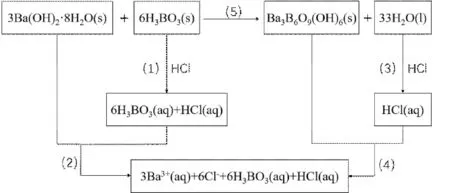
图 1 测定Ba3B6O9(OH)6标准摩尔生成焓的热力学循环 Fig. 1 Thermodynamic cycle for determining the standard molar formation enthalpy of Ba3B6O9(OH)6
2.2.4量热仪的标定
量热所用仪器为SRC100型具有恒温环境的溶解-反应量热仪. 在T=298.15 K下进行了五次量热实验.
完全溶解反应所需的总时间约为 0.5小时. 在每个量热实验中反应后没有观察到固体残留物. 为了检查热量计的性能,使用KCl(光谱纯,使用前在130 ℃下烘6 h)在去离子水中的溶解焓对量热计进行准确度测验与校正. 测量结果见表1,测量ΔsolHm(KCl)平均值为17.534±0.0063 kJ·mol-1与文献报道[24]的17.524 ± 0.028 kJ·mol-1基本一致,这表明本工作中用于测量溶解焓的量热仪可靠. 表中No为测试次数,m为溶质样品的质量,ΔsolHm为每次测定溶质的摩尔溶解焓.

表1 在25.00℃时KCl在水中的摩尔溶解焓
3 结果与讨论
3.1 样品表征与分析
3.1.1X射线粉晶衍射分析(XRD)
样品的 XRD 图如图 2 所示. 可以看出样品的衍射峰较强,表明其结晶度较好;图谱中未观察到杂质、其他硼酸盐和未反应物质的特征峰,其特征晶面间距d/nm值为0.4996、0.4638、0.4504、0.3559、0.3487、0.3449、0.3060、0.3017、0.2327、0.2205、0.1937,既不是原料单一组分的,也不是二者的加合,与Ba3B6O9(OH)6相应的JCPDS卡(File No.97-028-1231)基本一致,表明样品为Ba3B6O9(OH)6.
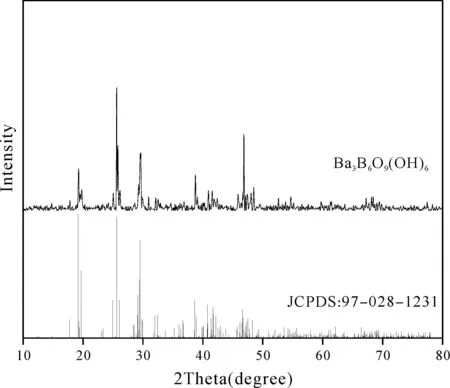
图2 Ba3B6O9(OH)6的X-射线粉晶衍射图Fig. 2 X-ray powder diffraction pattern of Ba3B6O9(OH)6
3.1.2红外光谱分析(FT-IR)
合成产物的FT-IR光谱如图3所示,结合相关文献[25],对其特征吸收波数归属如下:3464 cm-1处强吸收峰为O-H键的伸缩振动;1198 cm-1处吸收峰为B-O-H的面内伸缩振动. 1028 cm-1至875 cm-1范围的吸收峰为B(4)-O的反对称和对称伸缩振动;554 cm-1处吸收峰归属为(BO4)5-的特征吸收峰,其为Ba3B6O9(OH)6结构的基本单元. 结果表明该物质只含有BO4配位方式,与文献报道Ba3B6O9(OH)6为均是硼氧四配位一致[19].
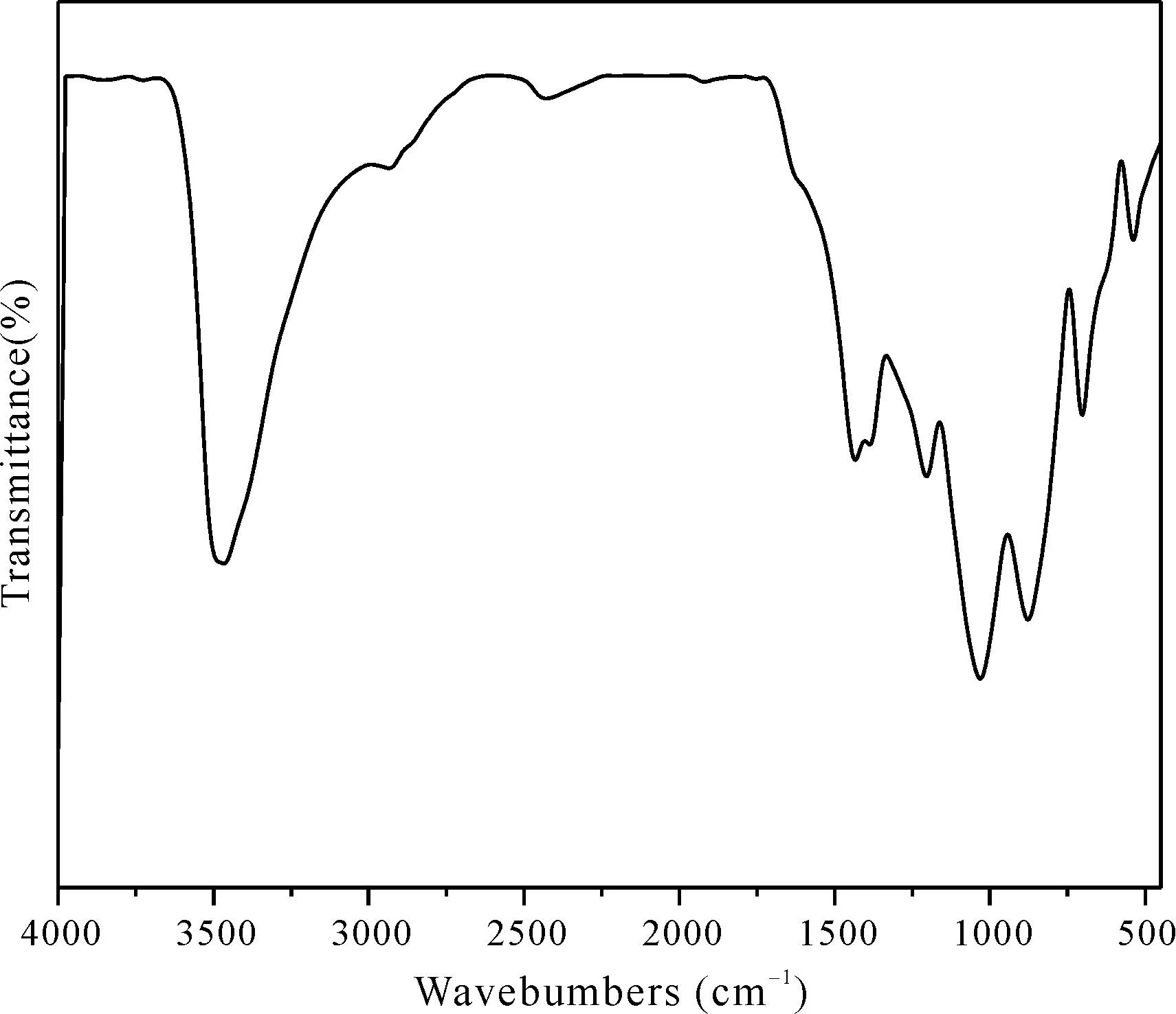
图3 Ba3B6O9(OH)6的红外光谱图Fig.3 FT-IR spectrum of Ba3B6O9(OH)6
3.1.3扫描电镜(SEM)分析
制备样品的SEM如图4所示,从低倍图中可以看出样品为大小不一、形貌较规则的块状结构,其直径大约100 μm;从高倍图中可以看到样品棱角分明,表面较光滑,有少量微孔. 由此可得出制备的样品为块状的微米结构材料.

图4 Ba3B6O9(OH)6的扫描电镜图(a)低倍图;(b)高倍图Fig. 4 SEM image of Ba3B6O9(OH)6 (a)low magnification;(b)high magnification
3.1.4综合热分析法(TG-DSC)
合成样品的TG-DSC曲线如图5所示,从TG曲线上可看出,样品在100-600 ℃之间出现两个失重段,总的失重为7.77%,这与理论上失去3个结构水的失重率7.47%基本吻合. 第一个失重段出现在100-400 ℃之间,失重为2.48%,对应于物质失去1个结构水. 第二个失重段出现在400-800 ℃之间,失重为5.29%,对应于两个结构水的失去. DSC曲线中,在337 ℃、470 ℃出现两个吸热峰分别对应一个结构水、两个结构水的脱失;在749 ℃左右出现的吸热峰对应为结晶不完整产物的熔融吸热;在650 ℃附近出现的放热峰对应于无定形转化为晶型的结晶放热.
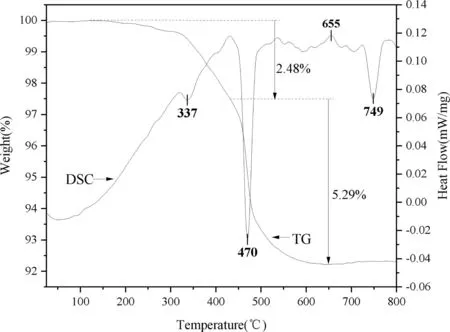
图5 Ba3B6O9(OH)6的TG-DSC曲线图Fig.5 TG-DSC curve of Ba3B6O9(OH)6
结合TG-DSC分析及文献报道[20],推测Ba3B6O9(OH)6热处理过程如下式(1-3):
(1)
(2)
(3)
当温度为130 ℃以下时该物质比较稳定;当温度升至130 ℃左右时,Ba3B6O9(OH)6开始失去结构水,温度达到600 ℃左右时,样品基本已经完全失去结构水,其晶格完全破坏,Ba3B6O9(OH)6转变为无定形Ba3B6O12(其结构式为:Ba3(B3O6)2,结构简式为:BaB2O4);当温度继续升高时,无定形BaB2O4开始转化为晶型BaB2O4.
3.2 量热实验结果
Ba3B6O9(OH)6在100 mL的0.9995 mol·dm-3HCl(aq)中298.15 K时的摩尔溶解焓见表2. 表中No为测试次数,m为溶质样品的质量,ΔsolH为每次测定的溶质溶解焓变,ΔsolHm为每次测定溶质的摩尔溶解焓.

表2 一定质量的Ba3B6O9(OH)6 (s)在 0.9995 mol·dm-3 HCl(aq)中的摩尔溶解焓 (ΔsolHm).a
表3为计算Ba3B6O9(OH)6标准摩尔生成焓(ΔfHmθ)的热力学循环中各虚拟反应的标准摩尔反应焓,表中No为虚拟反应编号,Reaction为虚拟反应的化学方程式,ΔrHmθ为标准摩尔反应焓,其中H3BO3(s)溶解于0.9995 mol·dm-3HCl(aq)的摩尔溶解焓为(21.83±0.08)kJ·mol-1取自文献[26],HCl(aq)的稀释焓由 NBS table[27]计算得出. 结合这些数据,根据热力学循环计算得到生成Ba3B6O9(OH)6的虚拟反应(5)的标准摩尔焓变为32.34±0.58 kJ·mol-1. 再结合Ba(OH)2·8H2O(s)、H3BO3(s)、H2O(l)的标准摩尔生成焓(ΔfHmθ),得到了Ba3B6O9(OH)6的标准摩尔生成焓(ΔfHmθ)为-(7130.664 ±4.2)kJ·mol-1. Ba(OH)2·8H2O(s)的标准摩尔生成焓取自NBS tables[27]为 -(3342.2±0.6)kJ·mol-1. H2O(l)、H3BO3(s)的标准摩尔生成焓取自CODATA Key Values[28]分别为- (285.830±0.040)kJ·mol-1和 -(1094.8±0.8)kJ·mol-1.
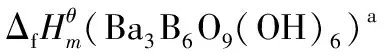
表3 计算热力学循环中各虚拟反应的标准摩尔反应焓
3.3 [B6O9(OH)6]6-的热力学性质估算结果
根据基团贡献法[15],Ba3B6O9(OH)6的标准摩尔生成焓(ΔfHmθ)可用下式表示:
其中ΔfHmθ(Ba2+,aq)为-537.64 kJ·mol-1[27],结合测量的ΔfHmθ(Ba3B6O9(OH)6,s)的数据,可计算出[B6O9(OH)6]6-的标准摩尔生成焓为-5517.744 kJ·mol-1.
4 结 论
通过水热法合成了块状形貌的六硼酸钡Ba3B6O9(OH)6,并通过 XRD、FT-IR、TG-DSC 和SEM对其进行了表征. 对其热处理过程中的物相变化进行了分析. 通过微量热仪测定了Ba3B6O9(OH)6在 0.9995mol·dm-3HCl(aq)的摩尔溶解焓为32.34±0.58 kJ·mol-1,并计算了其标准摩尔生成焓为-(7130.664±4.2)kJ·mol-1. 此外,通过基团贡献法估算了[B6O9(OH)6]6-的摩尔生成焓为-5517.744 kJ·mol-1. 研究结果进一步补充、丰富了硼酸盐的热力学数据.
