生物炭对磷石膏中磷的固化作用
2024-01-29徐冠立
敖 翔,徐冠立,李 珎,柏 涵
(成都理工大学 地球科学学院, 四川 成都 610059)
磷石膏是湿法制备磷酸过程中的副产物,其主要成分为二水硫酸钙,还含有0.5%~1.5% 的P2O5(彭家惠等, 2000)。在雨水的淋滤作用下,磷石膏中的磷浸出,会造成堆场附近的水体富营养化进而污染土壤(张柱, 2019)。
磷石膏中的磷一般是作为杂质被去除的。在工业上,一般采用水洗法、酸洗法、煅烧法和中和法等方法去除磷石膏中的磷(Wangetal., 2020)。其中,水洗法和酸洗法是以水或酸为洗剂对磷石膏进行浸洗,将磷石膏中的磷洗脱在洗液中 (李展等, 2020; 张利珍等, 2022),这种方法对洗液的消耗大,且存在洗液处理困难、易造成二次污染的问题。煅烧法则是在高温下对磷石膏进行煅烧,脱出磷石膏中的有机磷,将共晶磷转化为惰性焦磷酸盐物质(邓浩, 2020),该方法能耗和成本较高。中和法是通过向磷石膏中引入碱性改性材料(通常为石灰),与可溶磷发生反应生成惰性物质消除可溶磷的危害(Kaziliunasetal., 2006; Chenetal., 2022),这种方法也需要额外添加碱性改性材料,且存在环境风险。
生物炭是在缺氧的条件下高温裂解农业废弃物获得的碳化产物(Guoetal., 2020),具有高比表面积和丰富的官能团,生产成本低(Sohietal., 2010),已广泛应用于水中各种污染物的处理(Mohanetal., 2014)。生物炭表面以负电荷为主,对磷酸根离子的吸附能力有限(Nardisetal., 2022),但经钙盐改性后,其吸附效率有显著提高(Wuetal., 2022)。
磷石膏中富含二水硫酸钙,Ca2+可在生物炭表面与磷生成难溶的磷酸钙,从而固化磷石膏的磷。相较传统除磷方法,生物炭除磷无需添加其他改性材料,可充分利用磷石膏成分,降低洗液的处理难度,且施用成本低廉。本实验利用生物炭固化磷石膏中磷,以改善磷石膏堆场附近水体环境,促进磷化工的可持续性发展。
1 实验原料与方法
1.1 试剂与原料
磷石膏取自四川德阳龙蟒工业园磷石膏堆场,呈灰白色,粉末状,主要化学组成为SO3(49.69%)、CaO(35.02%)、SiO2(6.61%)、P2O5(0.66%)、其他氧化物(A12O3、Fe2O3等)含量(0.86%)、灼失量(6.13%)、有机质(0.99%)以及Cu、Pb等重金属元素(0.02%),化学成分总量99.98%。
将采回的磷石膏样品充分混合,50℃烘干粉磨至过200 目筛后备用。稻草秸秆采集于四川某地农田。实验所用试剂均为分析纯,主要包括氢氧化钠、抗坏血酸、六水合钼酸铵、酒石酸锑钾、硫酸钙-二水,实验用水为去离子水。
分析测试均在成都理工大学地球科学学院完成,主要分析仪器有电子天平(JD300-3)、X射线衍射仪(XRD,D8 ADVANCE)、扫描电子显微镜(SEM,Noval Nano SEM 450)、紫外分光光度计(UV-2700i)、pH计(PHS-3Cb)。X射线衍射仪型号为D8 ADVANCE,CuKα辐照,扫描速度0.2°/s。
1.2 实验方法
1.2.1 生物炭的制备
将稻草秸秆用去离子水清洗后烘干,剪切成长5~8 cm小段,在管式炉中,以0.5 L/min通入氮气,在10℃/min速率下升温至700℃保温1 h,然后自然冷却至室温。通过研磨和筛分得到粒径为35~100 目的生物炭。制得的生物炭主要用于磷石膏的固化实验和XRD、SEM-EDS分析。
1.2.2 生物炭固化磷实验
磷石膏、生物炭、去离子水置于100 mL锥形瓶中,在恒温水浴振荡器中,以160 r/min转速振荡,反应结束后,在5 000 r/min下离心5 min,用0.45 μm有机尼龙滤膜过滤上清液,取2 mL滤液,用去离子水稀释至20 mL,使用紫外分光光度计在660 nm波长下用四水合钼酸铵分光光度法测定溶液中的磷浓度(Murphy and Riley, 1962)。所有实验重复3次,结果取平均值并保留3位有效数字。
加入5 mL左右的去离子水将剩余的固体反应产物倒出,在50℃下烘干6 h后进行XRD、SEM-EDS分析。
1.2.3 生物炭用量对磷的浸出影响
将100 mg磷石膏、50 mL去离子水置于100 mL锥形瓶中,温度为293 K,反应时间为72 h,在锥形瓶中分别加入0.01、0.02、0.025、0.050 和0.1 g的生物炭,测量在不同生物炭用量下浸出磷的平衡浓度Ce。所有实验重复3次,结果取平均值并保留3位有效数字。根据式(1)计算单位质量生物炭对磷的固化量,用于评价生物炭用量对磷的固化效率。
w=(Ci-Ce)V/m
(1)
式中,w是达到平衡时生物炭的单位固化量(mg/g),Ci和Ce分别为反应初始和平衡时溶液中的磷浓度(mg/L),V为溶液体积(L),m为生物炭用量(g)。根据实验结果选择固化效率最高的生物炭用量进行后续实验。
1.2.4 时间对磷的浸出影响
将100 mg磷石膏、50 mL去离子水、0.025 g生物炭,在温度为293 K,反应时间分别为0.2、0.5、1、2、4、8、12、24、48、56、72和96 h时,分析该溶液中浸出磷浓度Ct(mg/L)。所有实验重复3次,并进行不含生物炭的空白实验作为对照组,结果取平均值保留3位有效数字。
1.2.5 温度对磷的浸出影响
将100 mg磷石膏、50 mL去离子水、0.025 g生物炭,在反应时间为72 h的条件下,调整水浴温度,探究固化反应在温度分别为288、293、298、303和308 K条件下浸出磷平衡浓度Ce的变化。所有实验重复3次,并进行不含生物炭的空白实验作为对照组,结果取平均值保留3位有效数字。
1.2.6 初始pH值对磷的浸出影响
将100 mg磷石膏、50 mL去离子水、0.025 g生物炭,在温度为293 K、反应时间为72 h的条件下,分别用0.1 mol/L的HCl和NaOH溶液对反应初始pH值进行调整,探讨固化反应在初始pH值分别为3、5、7、9、11环境中浸出磷平衡浓度Ce的变化。所有实验重复3次,并进行不含生物炭的空白实验作为对照组,结果取平均值保留3位有效数字。
2 实验结果
2.1 生物炭用量对磷的浸出影响
随着生物炭用量的增加,浸出平衡浓度(Ce)逐渐降低,当生物炭用量大于0.025 g时,溶液中浸出磷的浓度趋于恒定(表1)。
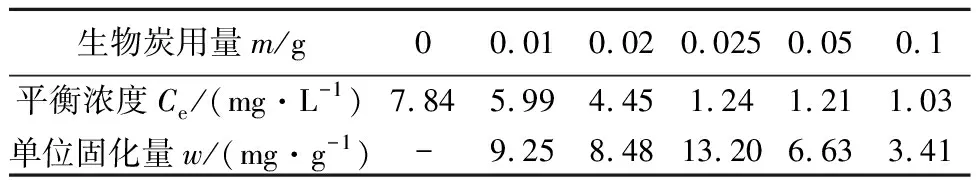
表 1 不同生物炭用量下磷固化量(w)的变化Table 1 Changes of w under different biochar addition
当不含生物炭时,0.1 g磷石膏在293 K水中反应72 h后,水体中磷平衡浓度Ce为7.84 mg/L。在生物炭加入量为0.025 g时,固化效率最高,单位固化量达到13.20 mg/g (表1)。故后续实验中生物炭加入量均采用0.025 g。
2.2 时间对磷的浸出影响
在293 K温度水中反应,含生物炭的磷石膏中浸出磷总量增加呈现先急后缓的趋势,72 h后浸出磷浓度达到平衡,此时Ct=1.40 mg/L;相同条件下不加生物炭的实验组Ct=7.84 mg/L,浸出量明显减少(图1a、1b)。因此后续实验反应平衡时间均设为72 h。
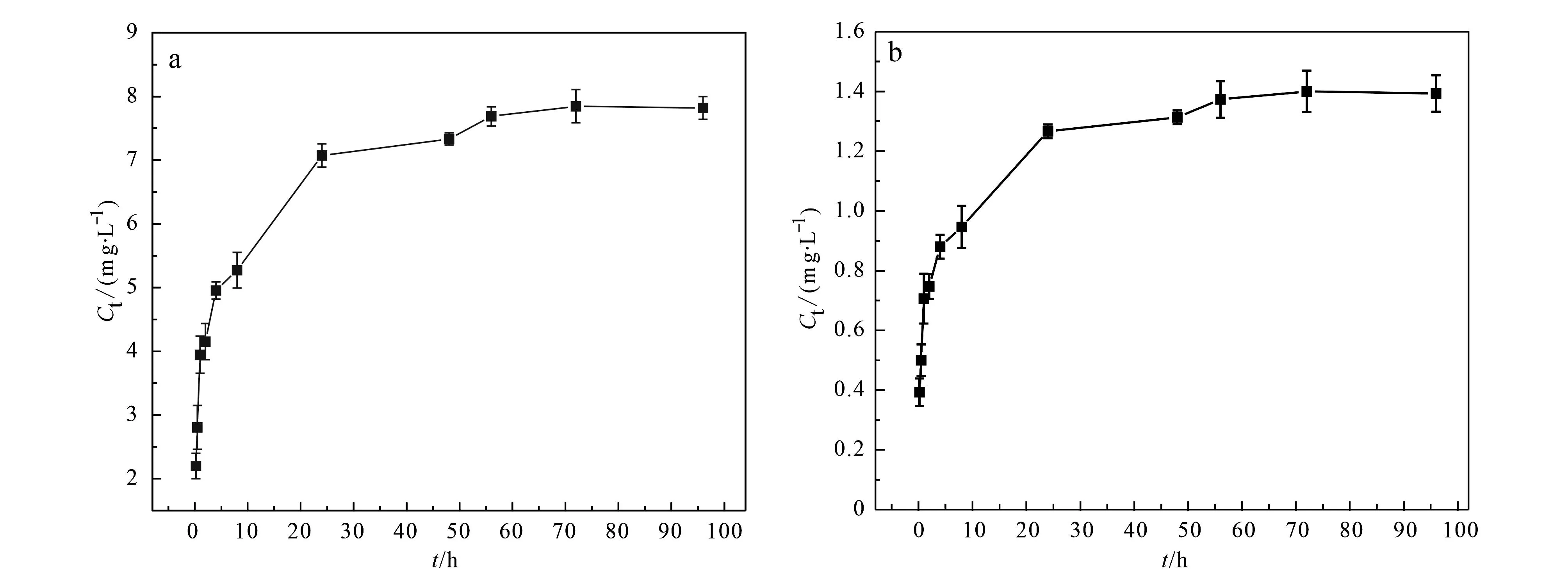
图 1 磷石膏(a)和加入生物炭后磷石膏(b)浸出磷浓度随时间变化图Fig.1 Changes of Ct leaching from phosphogypsum (a) and after addition of biochar (b) varing with time
2.3 温度对磷的浸出影响
含生物炭的磷石膏中浸出磷平衡浓度是随着温度升高逐渐下降的。当T=308 K时,浸出磷浓度Ce=0.167 mg/L,相同温度下不含生物炭的实验组Ce=9.81 mg/L(图2a、2b)。
2.4 初始pH值对磷的浸出影响
含生物炭的实验组在酸性条件下浸出磷平衡浓度Ce增加,在碱性条件下浸出磷平衡浓度Ce明显下降。在酸性条件下,反应的最终pH值有所上升;在碱性条件下最终pH值有所降低,除初始pH值为11的实验组略微降低外,其他实验组的最终pH值都向中性靠近。在初始pH值为11时,浸出磷浓度Ce=0.153 mg/L,相同条件下不加生物炭的实验组Ce=0.316 mg/L(图3a、3b)。

图 2 磷石膏(a)和加入生物炭后磷石膏(b)浸出磷浓度受温度影响变化图Fig. 2 Effect of temperature on Ce in phosphogypsum(a) and after the addition of biochar(b)

图 3 磷石膏(a)和加入生物炭后磷石膏(b)浸出磷浓度受初始pH影响变化图Fig. 3 Effect of initial pH on Ce and pH change in phosphogypsum(a) and after the addition of biochar(b)
3 讨论
3.1 磷的浸出机制

在反应的前24 h,被吸附在磷石膏表面的磷快速浸出到水体中,随时间变化的浸出磷浓度Ct迅速增加;在24~72 h间,由于水体的pH值受磷浸出影响而降低,导致难溶磷部分溶解,使浸出量缓慢增加,最终在72 h达到浸出平衡。
当水温上升到308 K时,浸出磷平衡浓度Ce有所上升,这可能是因为磷浸出后使水体呈弱酸性,同时高温加快了磷在水体中的溶解和扩散,提高了体系的离子活性,促进了离子交换反应(谢燕华等, 2020),使部分难溶磷溶解,Ce有所上升。而在低温下,体系的离子活性降低,磷的溶解减缓,Ce有所下降。
在酸性水体中,浸出磷平衡浓度Ce有所上升,这可能是因为HCl与氟磷灰石Ca5F(PO4)3反应,使其进一步溶解,反应式如下(王维, 2021):
Ca5F (PO4)3+10 HCl3 H3PO4+5 CaCl2+HF↑
(2)
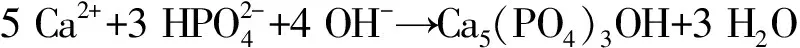
(3)
磷石膏中浸出到水体中的磷主要构成以可溶的弱吸附态磷和有机磷为主。高温和酸性水体条件会使难溶磷和共晶磷分解,使其中的磷浸出。
3.2 生物炭对磷的固化机理
采用XRD对生物炭和磷石膏原料进行的分析结果显示,生物炭中存在明显的漫散峰,该非晶态相的衍射峰是由石墨平面的堆叠基质组成的,表明形成了无定形的石墨微晶(Zhangetal., 2018),还存在KHCO3、KCl、CaCO3(图4a)。磷石膏中的主要矿物相为CaSO4·2 H2O和SiO2(图4b)。
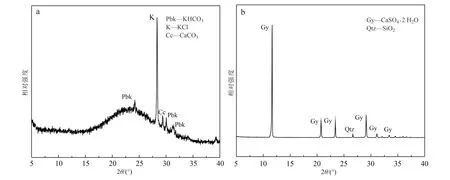
图 4 生物炭(a)和磷石膏(b)XRD图谱Fig. 4 XRD pattern of biochar (a) and phosphogypsum (b)
对1.2.3中反应时间为72 h实验组反应产物进行XRD、SEM-EDS分析,发现反应后生物炭和磷石膏反应产物中KHCO3、KCl的衍射峰因溶解而消失,主要矿物相为CaSO4·2 H2O和新生成的羟基磷灰石Ca5(PO4)3OH(HAP)。将磷石膏替换为石膏,其他实验条件相同的基础下,对比生物炭和石膏反应产物,主要矿物相为CaSO4·2 H2O和CaCO3(图5)。
通过SEM观察发现,生物炭保留了明显的生物结构(图6a、6b),在与磷石膏反应后,其表面显微结构的凹陷处出现明显的絮状、团簇状沉淀(图6c、6d)。通过EDS分析其主要成分为O、Si、Ca和P(图7b),其Ca∶P(原子比)为1.22。在该钙磷比下,生成的磷酸钙盐沉淀正从无定形磷酸钙(ACP)向羟基磷灰石(HAP)熟化转变(Wang and Nancollas, 2008),推测该絮状、团簇状沉淀为羟基磷灰石(HAP),反应如式(5)所示(刘雁, 2022):在考察时间对浸出磷浓度Ct的影响时,加入生物炭的实验组与磷石膏对照组的增长趋势相似。这可能是因为,生物炭对磷石膏中磷的固化效果受磷浸出速度和二水硫酸钙溶解速度的影响。磷石膏中的磷随着时间浸出到水体中,二水硫酸钙也逐渐溶解,游离在水体中的Ca2+更容易与带负电的生物炭相结合,在生物炭微观结构的凹陷处Ca与P的离子簇更容易局部过饱和,形成稳定的不定形磷酸钙(ACP) ,而后随着反应的进行逐渐生长熟化为HAP(李猛, 2019)。但是由于水体中的Ca2+含量较低,最后并未形成完整的HAP结晶,而是形成了絮状、团簇状沉淀(Dingetal., 2014)。

(5)

图 5 生物炭-磷石膏和生物炭-石膏反应产物XRD图谱Fig. 5 XRD patterns of reaction residue in biochar-phosphogypsum and biochar-gypsumGy—CaSO4·2 H2O; Qtz—SiO2; HAP—Ca5(PO4)3OH; Cc—CaCO3
温度升高会使Ce降低,这是因为高温环境有利于反应物的聚合(周珍旭等, 2014),促进分子间的交联,减小HAP的临界形核率,提高其生长速率(Markovicetal., 2004)。同时,温度升高会促使溶液中的有机磷酸盐和聚磷酸盐转化为正磷酸盐,正磷酸盐与Ca2+的结合性更好,有利于HAP的生长熟化(Huang and Tang, 2016)。

图 6 生物炭(a、b)和生物炭-磷石膏反应产物(c、d)的SEM图Fig. 6 SEM images of biochar(a, b) and biochar-phosphogypsum system reaction residue(c, d)

图 7 生物炭(a)和生物炭-磷石膏反应产物(b)的EDS分析结果Fig.7 EDS results of biochar (a) and biochar-phosphogypsum system reaction residue (b)
在酸性条件下,生物炭表面的羟基质子化(—OH+),虽然表面质子化后的官能团通过静电吸引吸附磷酸盐的能力增强,但是不利于钙离子与磷酸盐反应生成HAP,故此不利于生物炭对磷酸盐的固化(Jiaetal., 2020)。此时,生物炭对磷的固化作用主要以物理吸附为主(Eduahetal., 2020),固化的效果不佳。而在中性、碱性环境中,Ce随着初始pH值逐渐升高而降低。在碱性的环境下生物炭表面去质子化(—O-)表面带有更多的负电荷(Wangetal., 2018),增强了对二水硫酸钙电离出的游离态Ca2+的静电引力,Ca2+被生物炭表面的羟基吸引附着在其表面(孙华等, 2014),与水中的磷酸根发生反应,生成了HAP沉淀,即生物炭与溶解的Ca2+相结合对水中的磷产生了化学吸附作用(图8)。碱性环境能为反应提供充足的OH-,让HAP的结晶熟化过程能够持续进行(张迎盈, 2015),进一步固化浸出到水体中的磷。
4 结论
(1) 生物炭对磷石膏浸出到水体中的磷具有固化作用。生物炭用量为0.025 g时,达到最大固化效率,w=13.2 mg/g;含生物炭的实验组在t=72 h、T=293 K、pH=7条件下,达到浸出平衡,此时浸出磷平衡浓度Ce=1.40 mg/L;在相同实验条件下,不添加生物炭的对照组,浸出磷平衡浓度Ce=7.84 mg/L。

图 8 生物炭对磷的固化机理图Fig. 8 Mechanism of phosphorus solidifying by biochar
(2) 提高反应温度和初始pH值有利于生物炭固化磷石膏浸出到水体中的磷。在t=72 h、T=308 K、pH=7条件下,浸出磷平衡浓度Ce=0.167 mg/L,相同实验条件下,对照组Ce=9.81 mg/L;在t=72 h、T=293 K、pH=11条件下,浸出磷平衡浓度Ce=0.153 mg/L,相同实验条件下,对照组Ce=0.317 mg/L。
(3) 磷石膏中的二水硫酸钙溶解,游离在水中的Ca2+与表面带负电的生物炭结合,对水体中的磷酸根产生了化学吸附作用,在生物炭显微结构的凹陷处生成了絮状、团簇状的羟基磷灰石(HAP)沉淀。
