过表达lncRNA HEM2M改善非酒精性脂肪肝病小鼠的肝脏损伤
2024-01-29高灵犀汪梦燕王国栋
孔 祥,张 腾,张 妍,高灵犀,汪 文,汪梦燕,王国栋,吕 坤
皖南医学院1非编码RNA基础与临床转化安徽省重点实验室,安徽 芜湖 241001;皖南医学院弋矶山医院2中心实验室,3内分泌科,4消化内科,安徽 芜湖 241001;5皖南医学院药学院//安徽省多糖药物工程技术研究中心,安徽 芜湖241002
非酒精性脂肪性肝病(NAFLD)一种与肥胖、胰岛素抵抗等代谢紊乱相关的肝脏疾病,是肝硬化、肝癌的主要风险因素[1,2]。随着经济发展和生活方式改变,全球NAFLD病患数量不断攀升,已构成严重的公共卫生问题[3]。目前临床上尚无确定疗效的NAFLD治疗药物,因此探索NAFLD的发病机制尤为重要。
代谢性炎症是体内代谢失调所致产物(葡萄糖、游离脂肪酸、脂多糖等)触发的一种慢性、低程度的炎症反应。代谢性炎症是诱发胰岛素抵抗的重要原因,与2型糖尿病、NAFLD等疾病的发生和发展密切相关[4,5]。越来越多的证据表明,肝脏组织中的巨噬细胞是调控代谢性炎症和NAFLD之间的重要枢纽[6]。
长链非编码RNA(lncRNA)是指长度超过200 nt,不编码蛋白质的RNA分子[7]。在前期研究中,我们鉴定了M1和M2型小鼠骨髓源性巨噬细胞中差异表达的lncRNAs,其中NONMMUT058486.2 在M2 型巨噬细胞中显著上调,将其敲除可增加小鼠对病毒性心肌炎的敏感性[8,9]。为简便起见,在后续研究中将此lncRNA命名为HEM2M。
为进一步探讨lncRNA HEM2M的作用,我们构建了条件性髓系细胞lncRNA HEM2M 过表达(myeloid cell-specific knock-in,MYKI)小鼠,并发现过表达此lncRNA改善肥胖小鼠脂肪组织的代谢性炎症及胰岛素抵抗[10],但过表达lncRNA HEM2M对NAFLD小鼠肝脏损伤的作用仍未知。因此,本研究应用MYKI小鼠,喂饲HFD 构建NAFLD 模型,探索上调巨噬细胞中lncRNA HEM2M表达是否对NAFLD肝脏损伤具有保护作用,并初步探讨其可能的机制。
1 材料和方法
1.1 材料
MYKI 小鼠由赛业生物构建。HFD 饲料(60%kcal)(Research diets),谷丙转氨酶(ALT)和谷草转氨酶(AST)检测试剂盒(南京建成生物工程研究所)。TNF-α、IL-6 和IL-1β ELISA 试剂盒、诱导型一氧化氮合酶(iNOS)和精氨酸酶1(Arg-1)(ABclonal)。半胱氨酸蛋白酶-1(caspase-1)活性检测试剂盒和NOD-like receptor family CARD domain-containing protein 4(NLRC4)抗体(碧云天)。F4/80 抗体(Servicebio)。Caspase 1 和胞质蛋白gasdermin D(GSDMD)抗体(Santa)。总蛋白激酶B(T-AKT)和磷酸化AKT S473(PAKT)抗体(CST)。FAM-FLICA®Caspase-1(YVAD)检测试剂盒(Immunochemistry)。
1.2 方法
1.2.1 NAFLD小鼠模型建立 所有动物研究均经皖南医学院实验动物福利与伦理委员会审核和批准(批准号:WNMC-AWE-2020170)。6周龄MYKI小鼠与同窝C57BL/6野生型小鼠(WT)小鼠,随机分为高脂饮食组(HFD)和普通饮食(ND)组,每组10 只,即WT+ND、MYKI+ND,WT+HFD和MYKI+HFD组。小鼠持续喂饲12周,每周测量小鼠体质量和空腹血糖。
1.2.2 小鼠腹腔葡萄糖耐量(IGTT)和胰岛素耐量实验(ITT)部分小鼠禁食过夜后,腹腔注射葡萄糖(1.5 g/kg)后行IGTT实验;部分小鼠禁食6 h后,腹腔注射胰岛素(0.75 U/kg)后行ITT实验。应用罗氏血糖仪检测不同时间点小鼠末梢血糖水平并计算曲线下面积(AUC)。
1.2.3 生化指标检测 腹腔注射戊巴比妥钠麻醉小鼠,眼球摘除取血后离心分离血清,称取肝脏重量后留取肝脏标本。比色法检测血清和肝脏组织中ALT和AST水平以及caspase-1活性。ELISA法测定肝脏组织TNF-α、IL-6和IL-1β水平。
1.2.4 HE和免疫组化染色 取多聚甲醛固定的肝脏组织,按照梯度乙醇脱水后,石蜡包埋,4 μm 切片,HE染色后拍照。部分组织切片行F4/80染色,光镜下观察后拍照。
1.2.5 qRT-PCR Trizol提取肝脏组织中的总RNA,逆转录成cDNA,Rt-PCR 检测lncRNA HEM2M、M1 型(TNF-α、iNOS和IL-6)和M2型(Arg-1、YM-1和IL-10)巨噬细胞标志物mRNA水平,使用GAPDH作为内参。引物序列见前期报道[10,11]。
1.2.6 免疫印迹检测 取适量肝脏组织,加入含蛋白酶和磷酸酶抑制剂的RIPA裂解缓冲液,充分研磨后离心取上清,变性后30 μg上样。SDS-PAGE凝胶电泳后转移至NC膜上,5%脱脂奶粉封闭,iNOS(0.63µg/µL,1∶1000)、Arg-1(1.17µg/µL,1∶1500)、NLRC4(0.1µg/µL,1∶500)、caspase 1(0.2 µg/µL,1∶1000)、GSDMD(0.2 µg/µL,1∶1000)、T-AKT(0.1µg/µL,1∶1000)和P-AKT(0.1µg/µL,1∶1000)抗体孵育过夜,室温孵育二抗1 h,ECL发光拍照后进行蛋白定量。
1.2.7 肝脏组织活性caspase-1检测 OCT包埋,冷冻切片机制备5 μm 小鼠肝脏组织冰冻切片,利用FAMYVAD-FMK 探针标记活化caspase-1(绿色荧光,即为发生焦亡的肝脏细胞),共聚焦显微镜拍片。
1.2.8 统计学分析 应用SPSS 19.0软件进行统计学分析,所有数据作图应用Excel软件完成。数据以均数±标准差表示,组间比较采用单因素方差分析和LSD检验,Ρ<0.05为差异具有统计学意义。
2 结果
2.1 过表达lncRNA HEM2M对NAFLD小鼠肝功能的影响
HFD 喂饲12 周后,小鼠肝脏组织中lncRNA HEM2M表达较喂饲ND的小鼠显著降低(Ρ<0.05),但MYKI小鼠肝脏组织中lncRNA HEM2M表达显著增加(Ρ<0.01,图1A)。与喂饲ND相比,喂饲HFD的WT小鼠体质量显著增加。与WT+HFD小鼠相比,MYKI+HFD小鼠体质量无显著变化,但肝重和肝重体质量比显著降低(Ρ<0.01,图1B~D)。此外,MYKI+HFD小鼠血清和肝脏组织中ALT和AST水平均较WT+HFD小鼠显著降低(Ρ<0.01,图1E~H)。

图1 过表达lncRNAHEM2M对NAFLD小鼠肝功能的影响Fig.1 Effect of lncRNA HEM2M overexpression on liver function of wild-type (WT)C57BL/6 mice and myeloid cell-specific lncRNA HEM2M knock-in(MYKI)mice with normal(ND)or high-fat diet(HFD)feeding for 12 weeks.A:qRT-PCR analysis of HEM2M expression in liver tissues(n=4).B:Body weight of the mice measured weekly(n=10).C,D:Liver weight and liver weight/body weight ratio of the mice after 12-week feeding(n=10).E-H:Serum and liver ALT and AST levels of the mice(n=5).*P<0.05,**P<0.01 vs WT+ND group,#P<0.05,##P<0.01 vs WT+HFD group.
2.2 过表达lncRNA HEM2M对NAFLD小鼠肝脏组织病理的影响
肝脏组织HE染色所示,喂饲ND的WT和MYKI小鼠肝脏结构正常,WT+HFD小鼠肝脏组织排列紊乱,细胞肿胀,有大量脂肪积累,细胞核被脂滴移至边缘;MYKI+HFD小鼠肝脏细胞肿胀明显减轻,脂肪空泡显著减小(图2)。

图2 过表达lncRNAHEM2M对NAFLD小鼠肝脏组织病理的影响Fig.2 Effect of lncRNAHEM2M overexpression on hepatic histopathology of NAFLD mice(Scale bar=50 μm).
2.3 过表达lncRNA HEM2M对NAFLD小鼠肝脏组织炎症的影响
WT+HFD小鼠肝脏组织巨噬细胞数量(F4/80染色阳性细胞)显著增多,MYKI+HFD小鼠肝脏组织巨噬细胞浸润减少(图3A)。WT+HFD小鼠肝脏组织促炎因子IL-6、IL-1β和TNF-α水平较WT+ND小鼠显著增高,MYKI+HFD小鼠肝脏组织促炎因子水平降低(Ρ<0.01,图3B~D)。qRT-PCR结果表明MYKI+HFD小鼠肝脏组织中M1型巨噬细胞标志物(TNF-α、iNOS和IL-6)mRNA 水平较WT+HFD 小鼠显著降低(Ρ<0.01,图3E),而M2型标志物(Arg-1、YM-1和IL-10)mRNA水平显著升高(Ρ<0.01,图3F)。如图3G~I所示,免疫印迹结果表明WT+HFD小鼠肝脏组织中iNOS蛋白表达升高(Ρ<0.01),Arg-1蛋白表达降低(Ρ<0.01),而MYKI+HFD小鼠iNOS蛋白表达降低(Ρ<0.05),Arg-1蛋白表达升高(Ρ<0.05)。
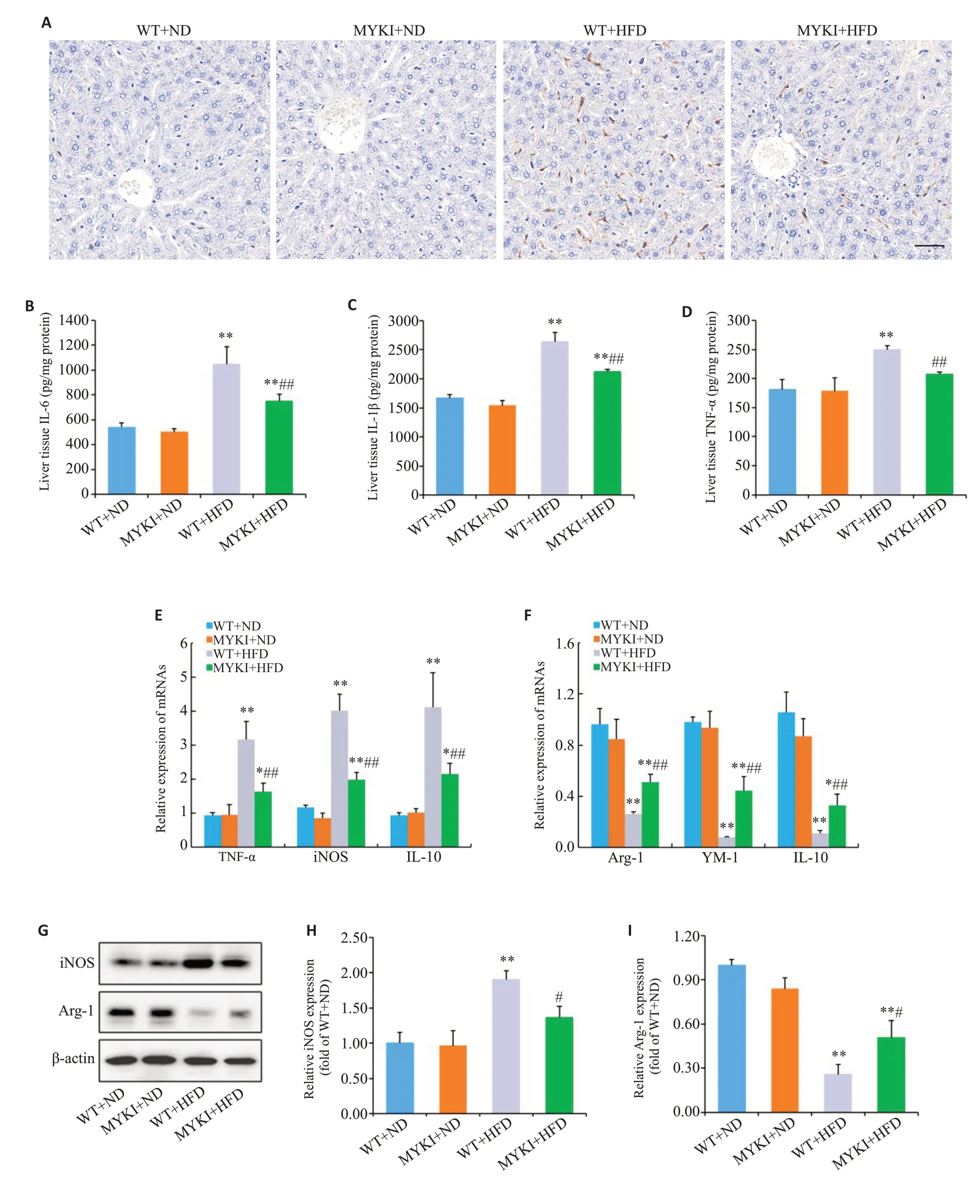
图3 过表达lncRNAHEM2M对NAFLD小鼠肝脏组织炎症的影响Fig.3 Effect of lncRNA HEM2M overexpression on liver inflammation of NAFLD mice.A:F4/80+staining of the liver tissues of the mice after the 12-week ND or HFD feeding(×200,Scale bar=50 μm).B,D:IL-6,IL-1β and TNF-α levels in the liver tissues detected using ELISA(n=5).E,F:mRNA expressions of M1 macrophage markers(TNF-α,IL-6,and iNOS)and M2 markers(Arg-1,YM-1 and IL-10)in the liver tissues analyzed using qRT-PCR(n=5).G-I:Expressions of iNOS and Arg-1 in the liver tissues of NAFLD mice detected by Western blotting(n=3).*P<0.05,**P<0.01 vs WT+ND group,#P<0.05,##P<0.01 vs WT+HFD group.
2.4 过表达lncRNA HEM2M对NAFLD小鼠肝脏胰岛素抵抗的影响
与WT+HFD小鼠相比,MYKI+HFD小鼠空腹血糖无显著变化(图4A)。但IGTT试验表明WT+HFD小鼠存在糖耐量损害,MYKI+HFD小鼠糖耐量异常显著改善(Ρ<0.01,图4B、C)。ITT试验表明WT+HFD小鼠存在胰岛素抵抗,MYKI+HFD小鼠对胰岛素敏感性增加(Ρ<0.01,图4D、E)。AKT是胰岛素信号通路中的重要调控分子,激活AKT能够增强细胞对胰岛素敏感性[12]。与喂饲ND的WT小鼠相比,WT+HFD小鼠肝脏组织PAKT和T-AKT比值显著降低,而MYKI+HFD小鼠肝脏组织P-AKT和T-AKT比值较WT+HFD小鼠显著升高(Ρ<0.05,图4F、G),

图4 过表达lncRNAHEM2M对NAFLD小鼠肝脏胰岛素抵抗的影响Fig.4 Effect of lncRNA HEM2M overexpression on liver insulin resistance of NAFLD mices.A:Fasting blood glucose levels measured weekly (n=10).B: Intraperitoneal glucose tolerance test (IGTT) results in different groups (n=5).C:Area under the curve (AUC) of IGTT results in different groups.D: Insulin tolerance test(ITT)results in different groups(n=5).E:AUC of ITT results.F,G:Expressions of P-AKT and T-AKT in the liver tissues of NAFLD mice(n=3).*P<0.05,**P<0.01 vs WT+ND group,#P<0.05,##P<0.01 vs WT+HFD group.
2.5 过表达lncRNA HEM2M 对NAFLD 小鼠肝脏NLRC4炎症小体和细胞焦亡的影响
与喂饲ND的WT小鼠相比,WT+HFD小鼠肝脏组织NLRC4、cleaved caspase-1、GSDMD-N末端片段的表达升高,而MYKI+HFD 小鼠上述蛋白的表达显著降低(Ρ<0.05,5A~D)。此外,MYKI+HFD 小鼠肝组织caspase-1活性较WT+HFD小鼠明显降低(Ρ<0.01,图5E)。与喂饲ND的WT小鼠相比,WT+HFD小鼠肝脏组织活化caspase-1阳性区域增多,而MYKI+HFD小鼠肝组织活化caspase-1阳性区域减少(图5F)。

图5 过表达lncRNAHEM2M对NAFLD小鼠肝脏NLRC4炎症小体和细胞焦亡的影响Fig.5 Effect of lncRNAHEM2M overexpression on NLRC4 inflammasomes and pyroptosis in liver tissues of NAFLD mice.AD:Expressions of NLRC4,caspase-1 p20 and GSDMD-N in the liver tissues of NAFLD mice with HFD feeding for 12 weeks(n=3).E: Caspase-1 activity in liver tissues measured using Ac-YVAD-pNA(n=5).F: Liver tissue sections stained with the YVAD-FMK probe (green,representing activated caspase-1 cells) and hoechst33342 (blue,representing cell nucleus) (×200;Scale bar=50 μm).*P<0.05,**P<0.01 vs WT+ND group,#P<0.05,##P<0.01 vs WT+HFD group.
3 讨论
NAFLD是指除酒精和其他明确的肝损因素所致的,以弥漫性肝细胞大泡性脂肪变为主要特征的临床病理综合征[13,14]。本研究应用HFD饲料(60%kcal)喂饲WT小鼠12周后,发现其肝脏质量、血清和肝脏组织中ALT和AST含量较喂饲ND的WT小鼠显著增加,同时HFD 喂饲的WT 小鼠存在显著肝脏脂肪变,说明NAFLD小鼠模型构建成功。
目前研究证实lncRNA在NAFLD的发生发展中起着重要作用[15]。LncRNA Platr4阻断NF-κB信号,抑制巨噬细胞NLRP3炎症小体激活,改善小鼠非酒精性脂肪肝炎[16]。LncRNA HCG18在NAFLD患者血清中水平升高,通过调控miR-197-3p/IL18轴促进肝脏脂肪沉积和糖代谢紊乱[17]。本研究首次发现与WT+HFD组小鼠相比,MYKI+HFD组小鼠肝脏质量、血清和肝脏组织中ALT和AST含量降低,肝脏脂肪变显著减轻,说明上调巨噬细胞中lncRNA HEM2M表达可以改善NAFLD小鼠肝脏损伤。
巨噬细胞是极具异质性和可塑性的细胞,髓系来源的巨噬细胞(经典活化M1表型)分泌炎症因子TNF-α、IL-1β和IL-6等,促进肝细胞脂肪变性和胰岛素抵抗,加剧NAFLD发展[18-20]。本研究结果显示,与WT+HFD组小鼠相比,MYKI+HFD组小鼠肝脏巨噬细胞浸润减少,炎症因子水平显著降低,且M1表型巨噬细胞减少,说明过表达lncRNA HEM2M调控肝脏组织巨噬细胞极化状态,减轻NAFLD小鼠肝脏组织炎症反应,其机制与lncRNA HEM2M 调节白介素增强子结合因子2 和3(ILF2-ILF3)复合物介导的miRNA-192生成而抑制巨噬细胞M1极化;结合细胞核中异质核核糖核蛋白U(hnRNP U),抑制hnRNP U 核质易位,阻断胞质中hnRNP U稳定TNF-α和IL-6 mRNA的作用有关[9,10]。
胰岛素抵抗是NAFLD的重要病理特征之一,而代谢性炎症是诱发胰岛素抵抗的重要原因[21-24]。在本研究中,尽管MYKI+HFD组小鼠空腹血糖较WT+HFD组小鼠无显著变化,但MYKI+HFD组小鼠糖耐量损伤减轻(葡萄糖摄入后30和60 min末梢血糖显著低于WT+HFD小鼠),胰岛素抵抗显著改善(胰岛素注射后末梢血糖下降程度显著高于WT+HFD小鼠),这可能与过表达lncRNA HEM2M 减少肝脏组织中炎症因子TNF-α、IL-1β和IL-6 对AKT 等胰岛素信号通路的抑制作用有关。
细胞焦亡是一种由炎症小体介导的新型细胞死亡方式[25,26]。与细胞凋亡相比,细胞焦亡发生速度更快,且随着胞膜破裂,细胞内容物外泄可引发严重的炎症反应[27]。研究发现TNF-α能够直接激活肝细胞NLRC4炎症小体并诱发细胞焦亡[28]。NLRC4炎症小体激活caspase-1切割GSDMD,形成GSDMD-N而导致细胞膜破裂的经典焦亡途径在NFALD的发生发展中发挥重要作用[29,30]。我们的研究发现,60%kcal HFD喂饲12周构建的NFALD模型小鼠肝脏组织中NLRC4炎症小体激活,cleaved caspase 1和GSDMD-N末端片段表达升高,活性caspase 1增多,提示存在明显肝脏细胞焦亡。过表达lncRNA HEM2M降低肝脏组织中炎症因子水平,抑制NLRC4 炎症小体激活,减少切割而GSDMD形成GSDMD-N末端片段,显著抑制肝脏细胞焦亡进而改善NFALD肝脏损伤。
综上所述,过表达lncRNA HEM2M减少肝脏中巨噬细胞浸润,抑制巨噬细胞炎症表型,改善胰岛素抵抗并抑制肝脏NLRC4炎症小体激活,减少肝细胞焦亡,显著改善NAFLD小鼠肝脏损伤。LncRNAHEM2M可能是治疗肥胖相关的代谢性炎症和胰岛素抵抗的重要治疗靶点。