甲基丙烯酸水溶液萃取分离液液相平衡数据测定与关联
2024-01-23蔡鑫磊曹靖淇孙玉玉汤吉海黄晶晶黄益平
蔡鑫磊,曹靖淇,孙玉玉,汤吉海,黄晶晶,黄益平,乔 旭
(1.中建安装集团有限公司,江苏 南京 210023;2.南京工业大学 化工学院,材料化学工程国家重点实验室,江苏 南京 211800)
purification
甲基丙烯酸(MAA)作为一种重要的化学品,主要用于合成有机玻璃聚甲基丙烯酸甲酯(PMMA),此外在水凝胶、涂料、树脂等生产过程中发挥关键作用[1-4]。MAA的制备主要采用甲基丙烯醛(MAL)氧化制得,由于氧化过程温度较高,反应得到的MAA以气态从反应器出口采出,需用水进行吸收、冷凝之后,通过解吸、精馏等方法进行分离[5]。水与MAA之间存在共沸,同时MAA易溶于水,传统的精馏方法无法分离获得较高纯度的MAA[6]。为了解决MAA水溶液共沸分离难度大的问题,研究人员利用MAA易溶于有机溶剂的特性,开发了萃取+精馏的分离MAA水溶液的技术路线[7-8]。上海华谊丙烯酸有限公司开发了一种优化的逆流萃取方法,利用酯类和烃类混合物萃取MAA水溶液,MAA萃取率可达98.7%,精制后MAA纯度可达99.7%以上[9]。Li等[10]设计了一种萃取+精馏的甲基丙烯酸提纯工艺,以甲苯为萃取剂,以年总成本(TAC)为优化目标函数,在MAA回收率大于99%、MAA产品纯度大于99.9%的基础上,确定了工艺参数,TAC为129 815美元/年。
萃取剂的选择对于从MAA水溶液中成功提取和分离MAA至关重要,萃取剂的筛选需要综合考虑以下因素:对目标产物的高选择性,能够有效地提高目标产物的提取效率;萃取剂与原溶剂之间的低互溶度;目标产物在萃取剂与原溶剂中的分配系数较大,以便利用差异性的分配行为进行快速、高效的分离纯化;溶剂与目标分子沸点的显著差异,容易回收再利用;毒性较小,萃取剂对人体或环境造成危害较小[11-14]。常用于该过程的萃取剂包括烷烃、芳香烃和酯类等[15-18]。Swarnkar等[19]考察了三辛基甲基氯化铵与异戊醇、乙酸正丁酯、甲基异丁基甲酮、甲苯、CCl4、米糠油及煤油等物质的混合萃取剂对MAA的萃取效果。结果表明,三辛基甲基氯化铵与甲苯混合的萃取剂萃取效率最高,经优化该萃取剂的萃取效率可达93.09%。近年来,离子液体在MAA水溶液的萃取过程中的应用也得到了广泛的研究。白银鸽[20]对10种离子液体在MAA质量分数为0.1%~11%范围内的萃取效果进行了研究,其中[N8,8,8,1]Cl离子液体萃取效率最高,可达96.49%。然而,由于离子液体价格较高以及在MAA实际生产浓度范围(质量分数为20%~35%)内萃取效率不佳等因素,该方法尚未在工业生产中得到广泛推广。
本研究选取甲苯、正己烷、环己烷和邻苯二甲酸二丁酯(DBP)4种物质作为MAA水溶液提纯过程的萃取剂,考察了其对近共沸组成下MAA水溶液的分离效果(MAA的质量分数为29.2%)。此外,为了提供MAA水溶液分离工业化放大与设计基础数据,本文测定了常压条件下,20、30、40 ℃时MAA-H2O-DBP三元体系的液液相平衡数据,采用Hand方程和Othmer-Tobias方程对相平衡数据进行一致性验证[21-22],运用UNIQUAC模型来拟合得到H2O-MAA-DBP的二元交互作用参数。
1 实验过程及方法
1.1 实验原料
MAA水溶液组成如下:水质量分数为61.5%,MAA质量分数为29.2%,乙酸质量分数为6.1%,丙烯酸质量分数为1.3%,其他杂质质量分数为1.9%。实验中所用化学试剂已列于表1。
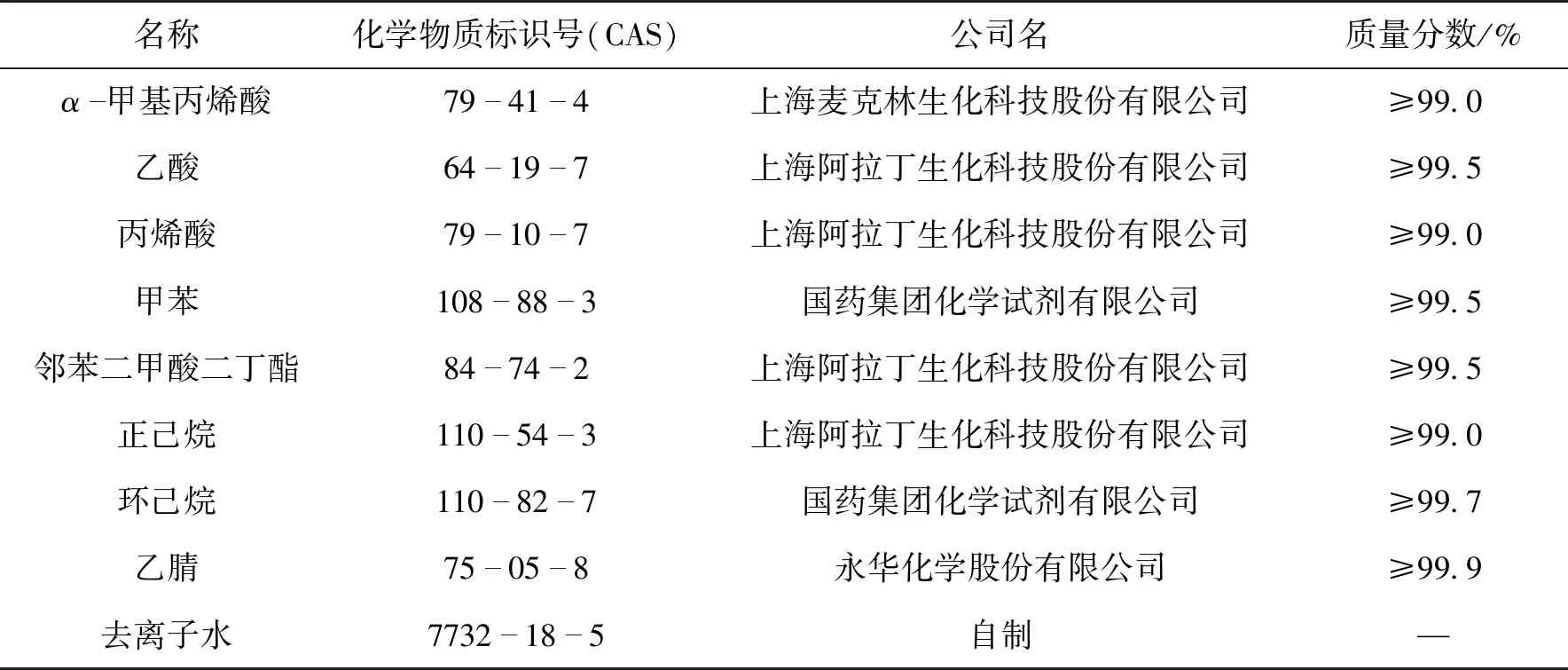
表1 化学试剂
1.2 实验仪器与分析方法
实验选用自制液液平衡釜(图1)进行萃取分离和液液平衡实验研究。此外,还使用到恒温反应浴槽(DFY-20,精度±0.1 ℃)、分析天平(美国普利赛斯公司,精度0.000 1 g)作为辅助实验研究。
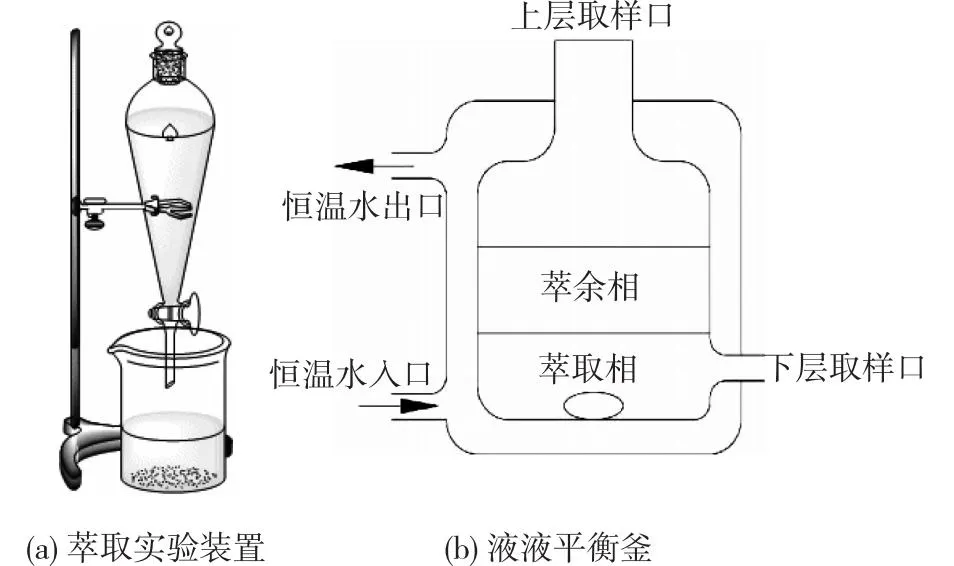
图1 实验装置Fig.1 Experimental device
分析检测仪器采用GC-2010pro型气相色谱仪(日本岛津制作所),TCD检测器(日本岛津制作所),INNOWAX型毛细管柱(安捷伦科技有限公司),其具体分析方法包括:进样口温度保持在240 ℃,TCD检测器温度保持在250 ℃。色谱柱采取程序升温方法,色谱柱初始以50 ℃保持2 min,以15 ℃/min升温速率将色谱柱温度升至140 ℃,随后以40 ℃/min升温速率将色谱柱温度升至250 ℃,保持2 min。采用内标法定量,内标物为乙腈。为确保色谱数据真实准确,每组试样测定3次以上,实验结果取其平均值。
1.3 萃取剂筛选实验、液液相平衡实验过程
萃取剂筛选实验步骤如下:将特定浓度的MAA水溶液与萃取剂倒入分液漏斗中,密封后手动摇晃均匀5 min,将其放置在恒温槽内静置2 h。之后,通过分液漏斗将水相与油相进行分离,并对它们分别进行称重。利用气相色谱对其组成进行分析。
液液平衡实验过程:将配备恒温夹套的液液平衡釜与恒温槽相连,使用分析天平准确称取MAA、H2O和DBP等物质分别加入液液平衡装置之中。将平衡釜密闭使其保持在恒温条件下,使用磁力搅拌器对其进行剧烈搅拌,持续2 h并使其静置4 h,达到三元系统相平衡。随后,从上下两个取样口分别采集上层萃取相(水相)试样及下层萃余相(油相)试样,使用气相色谱对试样分析。通过调整MAA、H2O和DBP 3种组分的添加量,并重复前述流程,得到多组浓度的液-液平衡数据。
2 实验结果讨论
2.1 萃取剂筛选
本研究选取了甲苯、正己烷、环己烷和DBP作为萃取剂,研究了4种萃取剂对MAA水溶液的萃取效率以及温度对萃取剂萃取效率的影响。
其中萃取率计算公式如式(1)所示。
(1)
式中:E为萃取率;上标Ⅰ代表萃余相、Ⅱ代表萃取相;β为MAA,下文符号均表示相同含义。
萃取剂用量和萃取温度对MAA的萃取率有着重要影响。图2考察了不同萃取剂在25 ℃条件下、萃取剂用量为1∶0.6~1∶1.4时,MAA萃取率的变化情况。从图2中可以看出,相同萃取剂用量时,甲苯和DBP对MAA的萃取率显著高于环己烷和正己烷的萃取率,且甲苯和DBP作萃取剂时,MAA萃取率接近。当萃取剂质量比从1∶0.6提高至1∶1.2,4种萃取剂对MAA萃取率均有所提升,其中DBP的萃取率从90.31%提升至92.16%;当萃取剂质量比超过1∶1.2以后,甲苯、DBP和环己烷对MAA萃取效率的提高不明显,甚至萃取剂质量比增加,正己烷对MAA萃取效率出现小幅下降。因此萃取剂适宜用量为MAA水溶液质量的1.2倍。
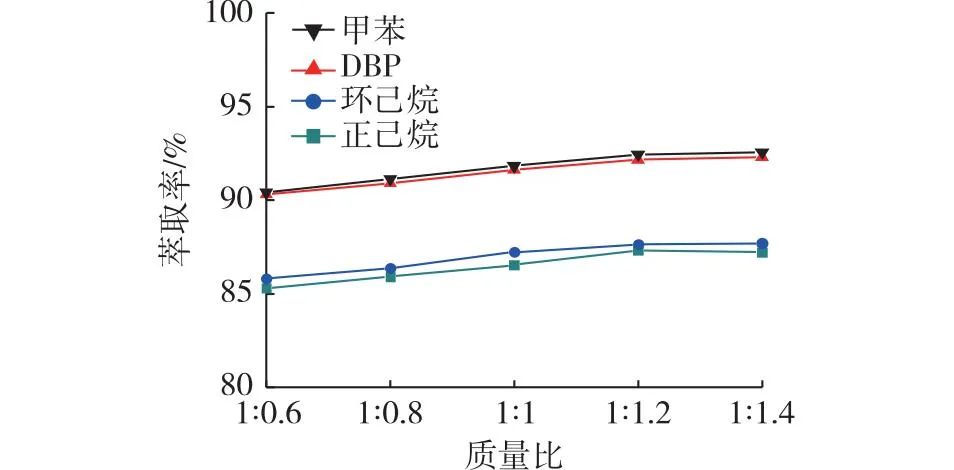
图2 萃取剂用量对MAA萃取率的影响Fig.2 Effect of mass ratio on MAA extraction rate
由于乙酸和丙烯酸与MAA有较好的相溶性,在萃取分离时易溶于萃取相,本研究考察了萃取剂用量为MAA水溶液的质量1.2倍时,不同萃取剂条件下,萃取分离后MAA水溶液中乙酸、丙烯酸在萃取相和萃余相中的分布情况,结果如表2所示。从表2中可以看出,乙酸和丙烯酸在萃余相中的含量与在萃取相中的含量相比较高,其中萃取相中乙酸和丙烯酸含量对MAA的后续提纯有较大影响。当选用甲苯和DBP为萃取剂时,萃取相中乙酸质量分数分别为1.74%和1.84%,略高于正己烷和环己烷为萃取剂时的质量分数,而甲苯和DBP为萃取剂时萃取相中乙酸质量分数相差较小,这与甲苯和DBP为萃取剂对MAA萃取率规律一致;而以DBP为萃取剂时,萃取相中丙烯酸质量分数最高,达到0.81%,与甲苯为萃取剂时,萃取相中丙烯酸质量分数为0.52%相差较小,因此萃取剂对丙烯酸的萃取率影响暂时不予考虑。
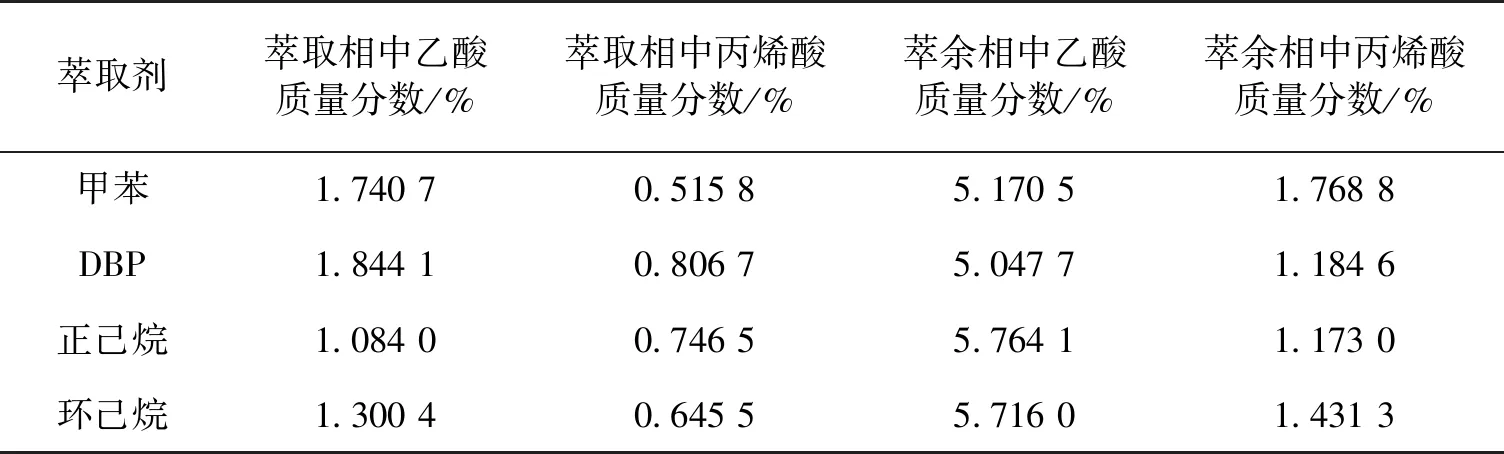
表2 萃取相及萃余相中乙酸及丙烯酸质量分数
综合MAA的萃取率和萃取相中乙酸的质量分数可知,当甲苯和DBP作为萃取剂时,萃取效果较佳。为了得到纯度较高的MAA产品,需要对萃取相进行分离提纯,考虑到DBP的沸点可达340 ℃,而水的沸点仅100 ℃,两者沸点差相差较大,采用减压闪蒸即可实现DBP与水的分离。此外DBP毒性较小,在实际应用时,对人体或环境造成危害较小,因此本文选取DBP为萃取剂进行后续研究。
2.2 三元液液相平衡数据
常压条件下,H2O-MAA-DBP体系在20、30、40 ℃时测得的液液平衡数据如表3所示,其中MAA分配系数及DBP分离因子计算公式如式(2)—(3)所示。
(2)
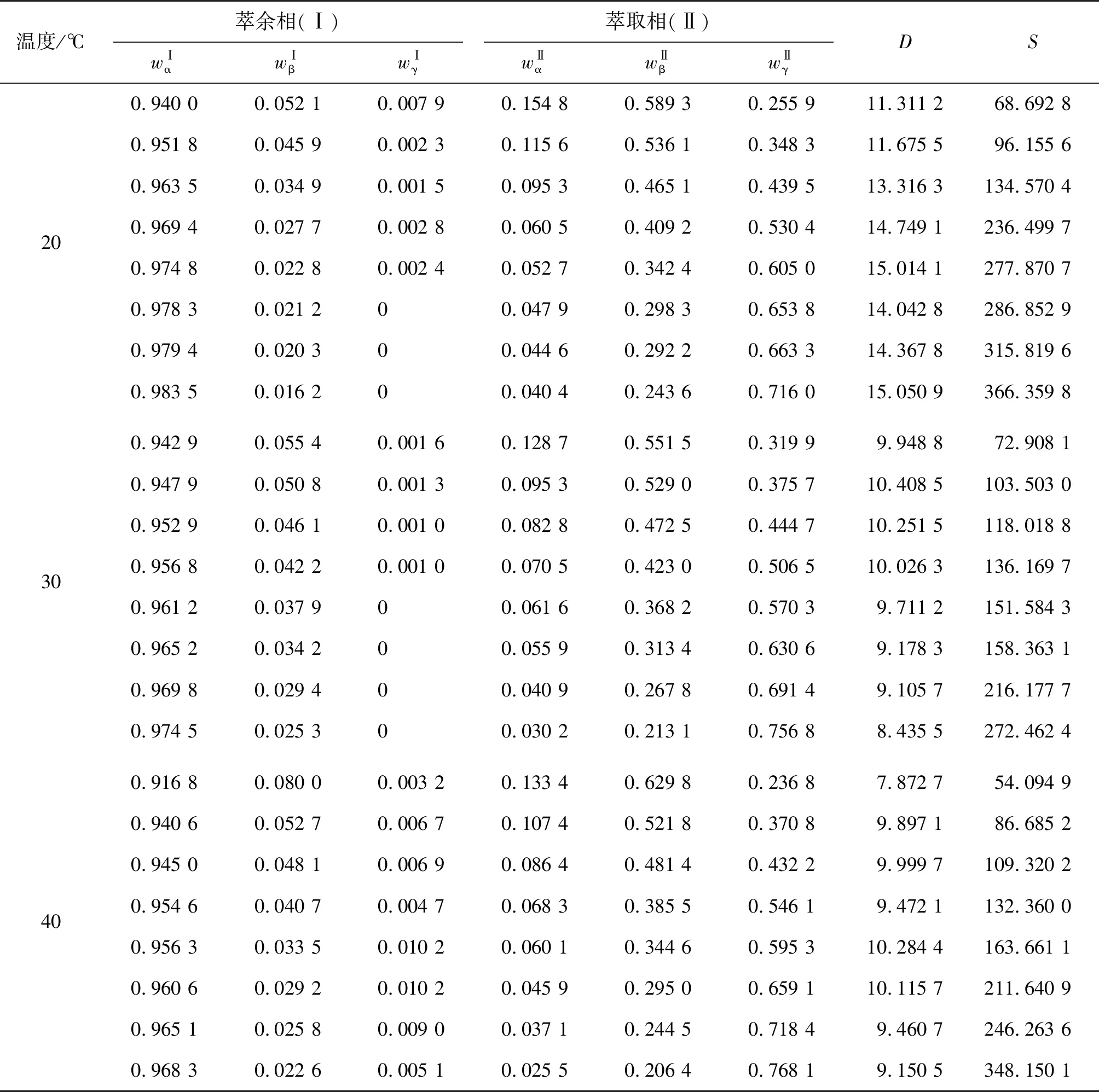
表3 H2O(α)+MAA(β)+DBP(γ)三元体系的液液相平衡数据
(3)
式中:D为MAA分配系数;S为DBP分离因子;α为水;计算结果列于表3之中。
从表3中可以看出,MAA分配系数D和DBP分离因子均远大于1,表明DBP对MAA具有较高的萃取能力和选择性,因此DBP可用于MAA与水的分离;20 ℃时,MAA分配系数及DBP分离因子普遍高于30 ℃及40 ℃数据,表明20 ℃时DBP对MAA萃取效果优于30 ℃和40 ℃,实际萃取过程中操作温度选择20 ℃较为适宜。
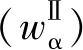
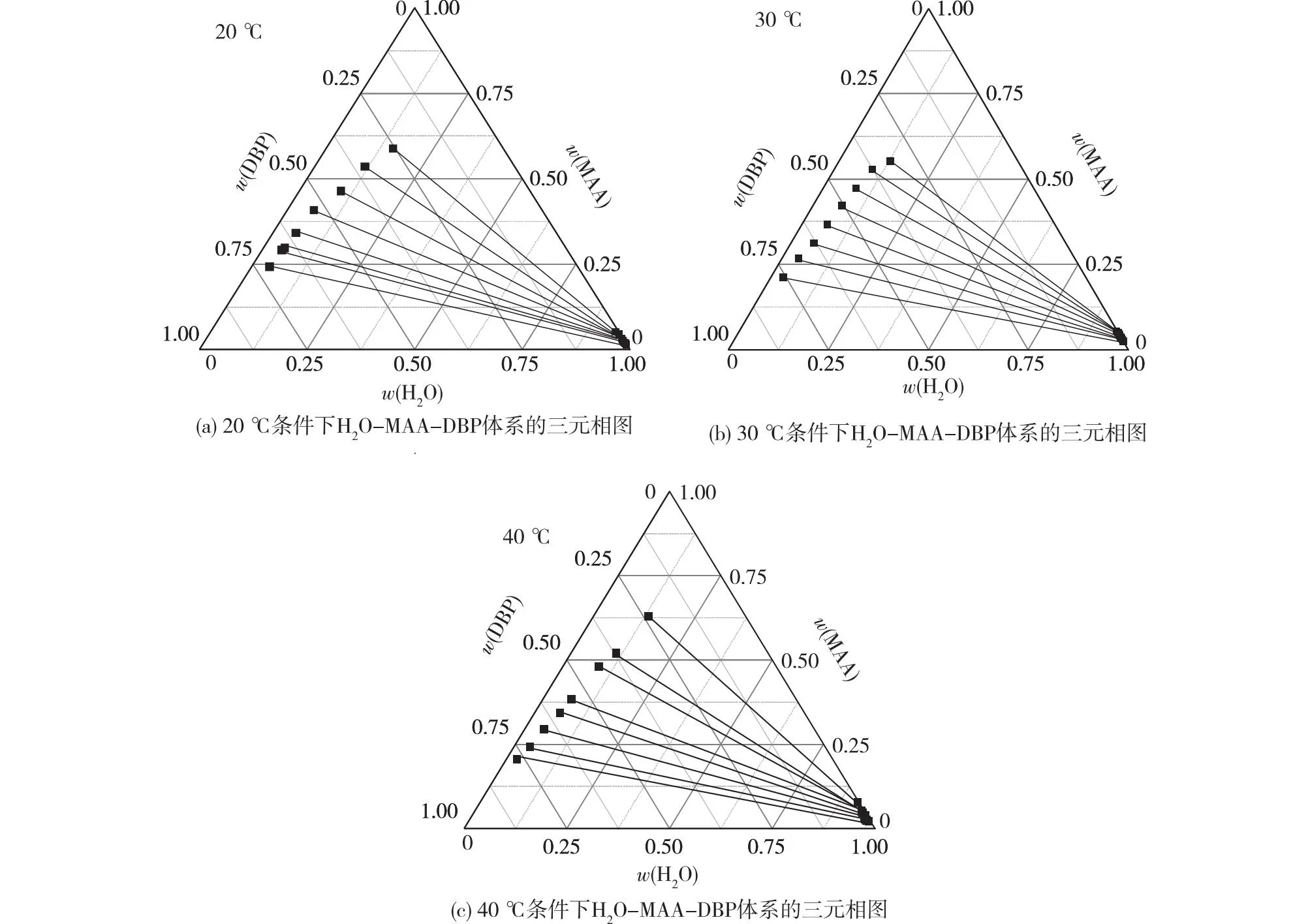
图3 20、30、40 ℃下H2O-MAA-DBP体系的三元相图Fig.3 Ternary phase diagram for H2O-MAA-DBP system at 20 ℃, 30 ℃ and 40 ℃
2.3 一致性检验
相平衡数据的一致性检验采用Hand方程以及Othmer-Tobias方程进行,具体公式表述参见式(4)与式(5)。
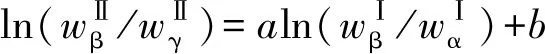
(4)
(5)
方程参数以及线性相关性系数R2的具体数值见表4,a、b、c与d代表了公式(4)和(5)中的各项参数。图4呈现了实验数据与Hand、Othmer-Tobias方程的线性关联,展示了较高的线性特性,线性相关性系数R2的值已经超0.99,证实了实验所测得的相平衡数据的准确性。
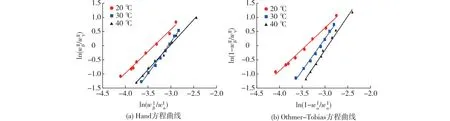
图4 H2O-MAA-DBP三元体系的Hand方程和Othmer-Tobias方程曲线Fig.4 Hand and Othmer-Tobias plots for H2O-MAA-DBP ternary systems
2.4 热力学模型关联
在本研究中,使用UNIQUAC模型关联H2O-MAA-DBP三元体系的液液相平衡实验数据。运用非线性最小二乘法,进行目标函数(OF)最小化计算,从而得到该模型的最优参数,具体结果参见表5。目标函数(OF)的计算公式参见式(6)[23-24]。
(6)
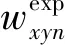
模型预测值与实验值的一致性评估采用均方根偏差(RMSD)[25-26],其计算方式如式(7)所示,所得均方根偏差数值列于表5。
RMSD=
(7)
拟合的UNIQUAC模型二元交互作用参数结果列于表5,从表5中可以看出,RMSD数值均小于0.07。这表明实验数据和模型预测数据有着较高的一致性,进一步证明了在MAA-H2O-DBP液液相平衡数据中,UNIQUAC模型具有有效的相关性。
3 结论
1)针对MAA水溶液提纯过程进行研究,探究了甲苯、正己烷、环己烷、DBP共4种萃取剂对MAA的萃取效果,经筛选得到DBP为综合性能最优的萃取剂,确定了萃取剂用量(质量比)1∶1.2、萃取温度20 ℃为适宜的萃取工艺条件。
2)测定了常压20、30 ℃和40 ℃的条件下,MAA-H2O-DBP三元体系的液液相平衡数据,绘制了MAA-H2O-DBP三组分不同温度下的三元相图。通过运用Hand方程和Othmer-Tobias方程进行了液液相平衡数据一致性检验,检验结果表明其线性相关系数R2均超过0.99,证明通过实验获取的相平衡数据具有较高的准确性。
3)实验测得的液液相平衡数据经UNIQUAC模型关联拟合获得MAA-H2O-DBP三组分间的二元交互作用参数,实验数据与模型预测结果的均方根差小于0.07,偏离较低,可为以DBP为萃取剂提纯工业生产中MAA水溶液中的MAA的过程开发提供依据。
