仪器分析课程中绿色度概念的引入
2024-01-23张红医何珺瑶石志红
张红医,何珺瑶,石志红,2
1 河北大学化学与环境科学学院,河北 保定 071002
2 河北大学化学教学研究所,河北 保定 071002
1 前言
在分析化学各版本教科书上[1-5],我们很容易找到从功能性角度对分析方法进行评价的指标,诸如精密度、准确度、灵敏度、检出限和定量限等。在分析化学相关学术期刊中,由这些基本概念延伸而来的评价指标更是随处可见,例如,以日内精密度[6]和日间精密度[6]等来表征分析方法的精密度;以加标回收率[7]来表征分析方法的准确度。这些功能性评价指标极大地推动了人们去探索和建立更稳定、更可靠、更灵敏的分析方法。
近年来随着绿色化学[8]、绿色分析化学[9]和绿色液相色谱[10]等理念逐渐兴起,对分析方法的评价在原有功能性评价指标的基础上,又增加了绿色度的评价指标[11]。然而现在的分析化学教材中还没有绿色度的概念。分析化学教材承载着培养未来化学工作者的重任,绿色化学思想理应在分析化学教材中有所体现。为此,我们尝试着在仪器分析课程的色谱分析部分,对绿色分析化学、绿色液相色谱等进行了简单介绍,并引入了两种可对液相色谱绿色度进行定量评价的方法。为了引起教学同行对绿色度概念的重视,让绿色度概念尽早进入教材、进入课堂,被更多的学生(未来的化学工作者)掌握和运用,特将我们的做法呈现给大家。
2 绿色度引入到仪器分析课程的步骤
通过以下几个主要步骤将绿色度计算的两种方法引入到仪器分析课堂中(共51学时),在色谱分析部分占用2个学时进行讲述。
第一步,阐述绿色度引入到仪器分析课程中的重要意义。通过文献调研的方法让学生认识到发展绿色分析化学的必要性和重要性,强调绿色分析化学研究与国家发展及分析化学学科发展间的一致性。
第二步,简要讲解绿色化学、绿色分析化学和绿色液相色谱的发展脉络,并提供原文献供学生课下进一步学习。
第三步,向学生提出问题:绿色化学和绿色分析化学还只是停留在理念上吗?难道它不可以进行定量量度吗?由于分析对象和分析方法的多样性,样品基质的复杂性,以及对分析方法的特殊要求(准确度、精密度和检出限等),因此在绿色化学视阈下对分析方法进行全面的评价并不是一件容易的事情。因此,适于各类分析手段绿色度评价的方法还不多。绿色度研究的初期,仅能提供定性的评价结果,其中较有代表性的是National Environmental Methods Index (NEMI)[12]。这种方法用象限图表征绿色度,四个象限分别代表分析方法所用溶剂和产生废物的四个性质:1) PBT (表示持久性、生物累积性和毒性);2) 危害性;3) 腐蚀性(pH > 12或pH < 2);4) 废物的体积或质量(是否大于50 mL或50 g)。NEMI价方法可以直接给出各种分析方法绿色度的图像,非常形象和直观。但这种方法只能提供绿色度的定性比较,不能给出绿色度的定量结果。针对分离氨氯地平、阿托伐他汀、瓜林多普利和吲达帕胺等药物的8种液相色谱分析方法,文献[11]用NEMI方法以象限图的方式直观显示了不同方法的绿色度。作为一个选作的作业,我们也鼓励学生模仿文献[11]的做法,通过文献调研查找水样中氨基甲酸酯的测定方法(我校自编教材的实验内容),并用NEMI方法以象限图方式比较我们实验方法和文献方法的绿色度。在初期的绿色度定性评价的基础上,近年来又出现了绿色度的定量评价方法。
第四步,讲述HPLC-EAT[13]和CHEMS-1[14]法的基本原理,以及HPLC-EAT软件的安装与使用。
第五步,为了练习使用HPLC-EAT和CHEMS-1法,首先指导学生结组合作查阅一些关于液相色谱实验的SCI文献;然后引导学生快速找到文献中有关液相色谱流动相组成和比例、流速等信息,并将这些信息制作成表格以便计算时引用;最后,用两种方法分别计算液相色谱方法的绿色度。
第六步,对两种方法绿色度计算结果进行比较和分析。
3 绿色度引入课程的意义
发展绿色分析化学是相关从业者的社会责任。与化学其他专业实验室相比,分析化学实验室给人的第一印象是干净,因此有些学生会错误地认为没有必要发展绿色化学。为此,我们通过文献数据来证明这种观点的错误性。众所周知,气相色谱的分析对象一般只限于低沸点化合物,约占有机物总量的20%,而占有机物总数近80%的高沸点及热不稳定性物质普遍要采用液相色谱进行分析[15]。由此可见液相色谱在色谱分析中的重要地位和作用。然而,液相色谱在运行中会产生很多有毒有害的有机物废液。根据Welch等人的测算[16],一台配备了传统尺寸色谱柱的传统液相色谱仪器每天至少产生1 L的废液。如果按照全世界拥有13万台液相色谱仪来估算,那么全世界每年将因液相色谱的运行至少要产生3.4 × 107L化学废液。
发展绿色分析化学工作符合我国的发展理念。将绿色度引入到仪器分析课程中,不仅可达成课程专业目标,还能在一定程度上达成德育目标,实现知识传播与育人培养有机结合。早在2002年Science[17]上就刊文“Green Chemistry: Science and Politics of Change”,对绿色化学研究给予了高度肯定。绿色化学[8]和绿色分析化学[9]的研究,已经成为世界化学研究的潮流和重要方向之一。在我国的五大发展理念(“创新、协调、绿色、开放、共享”)中,“绿色”发展的理念占有重要地位。实现绿色生态文明是我国“五位一体”总体布局的重要方面,是新时代中国特色社会主义思想的重要组成部分。
4 绿色度的两种评价方法
蔡卫权等[18]对绿色化学原则的发展进行了综述。从源头上减少或消除化学污染是绿色化学的理想,而绿色化学原则是对绿色化学内涵最好的诠释。自Anastas等在1998年提出12条绿色化学原则以来,Anastas本人和Winterton又从技术、经济和商业等角度出发,分别提出了另外12条绿色化学补充原则[17]。近年来,绿色化学[8]、绿色分析化学[9]和绿色液相色谱[10]的研究工作越来越多。那么一个化学过程的绿色度到底能不能量度呢?回答当然是肯定的。例如,美国绿色化学研究所运用Green Profile对环境分析方法进行绿色化学评价,但这种方法只能实现半定量评价[19]。Eissen等人提出了用于有机合成的环境评价工具(Environmental Assessment Tool for Organic Syntheses,EATOS)[20]。接下来我们介绍两个液相色谱绿色度表征的方法:HPLC-EAT[13]和改进的CHEMS-1[14]。
4.1 HPLC-EAT
HPLC-EAT[13]是一款由瑞典隆德大学Gaber团队开发的免费的软件,软件和使用手册可以从网页[21]的右侧区域免费下载。软件名称中的EAT是环境评价工具的英文缩写(Environmental Assessment Tool)。该软件通过统筹考虑液相色谱方法对环境E、健康H和安全S的影响来实现方法绿色度的评价。EAT的计算原理如下:
式中下角标的数字表示所使用溶剂的编号;m代表各溶剂的质量;S、H和E分别是安全因子、健康因子和环境因子,它们取自于Koller等人所建立的EHS法[22]。HPLC-EAT方法可对样品前处理、液相色谱等度洗脱、梯度洗脱等方面进行定量评价。图1为该软件的截图。软件提供了13种可作流动相的有机溶剂。对于前处理步骤需要选择溶剂、填写使用溶剂的量;对于液相色谱等度洗脱方式,需要输入流动相的组成、流速和运行时间等实验数据;对于液相色谱梯度洗脱方式,需要填写梯度程序和运行时间等数据。运行结果可通过柱状图和数据表的形式展现出来。HPLC-EAT值越低则表示方法的绿色度高;反之,其值越高则表示方法的绿色度越差。为了强调有机溶剂的影响,该软件将作为流动相组成部分的纯水、改性剂和缓冲溶液等的E、H和S当做0来处理。
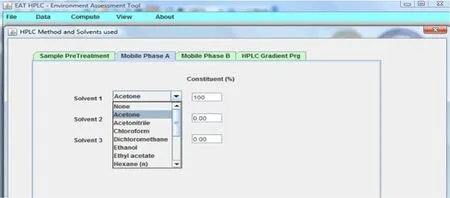
图1 HPLC-EAT软件的主界面
4.2 改进的CHEMS-1
CHEMS-1模型是由Swanson等人[23]于1997年提出的,主要用于工业中化学品的风险评价。总危害评价的算法是毒性相关的危害值之和与暴露相关参数值之和的乘积:
式中tHV为总危害值;HVORAL为口服毒性危害值;HVINH为吸入毒性危害值;HVCAR为致癌性危害值;HVHE为其他危害效应值;HVFA为水生动物急性毒性危害值;HVFC为水生动物慢性毒性危害值;HVBOD为生物降解能力参数;HVHYD为水解参数;HVBCF为生物浓缩参数。评价所需的毒理学和生态毒理学的数据取自于化学品安全技术说明书(MSDS),并经过转化和权重相似度的处理。
为了将CHEMS-1模型用于评价分析化学实验室的溶剂,2015年Tobiszewski等人[14]在原有模型计算方法的基础上进行了两点改进(一是引入了挥发性参数HVVOL,二是假设各危害是同等重要,因而忽略了权重的影响),提出了总分析危害值taHV,具体计算如下:
式中HVVOL为挥发性参数,且规定HVVOL按照三种方式赋值:
为了接下来使用改进的CHEMS-1模型做进一步的计算,将计算出的分析实验中常用的有机溶剂的tHV和taHV列于表1。
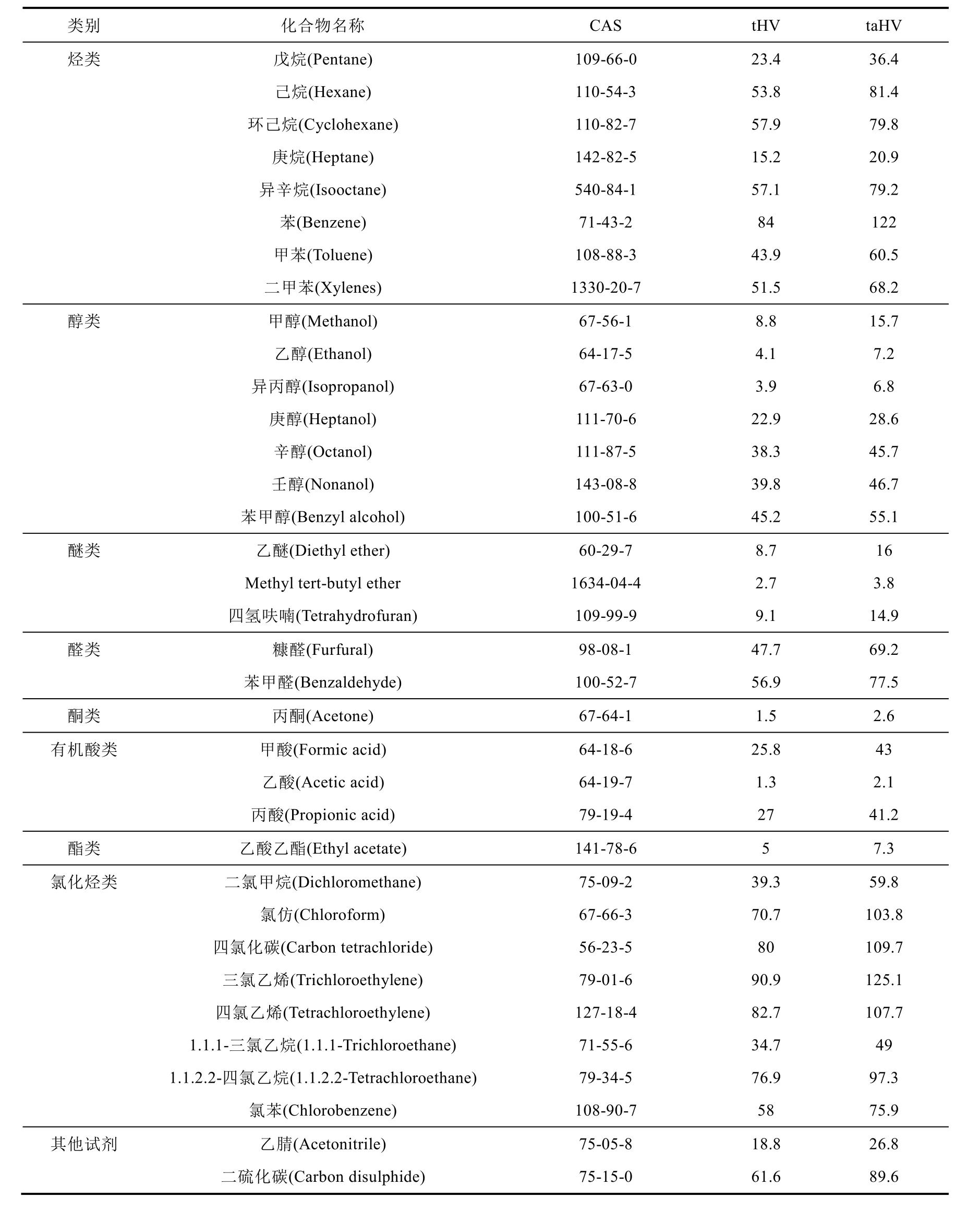
表1 常用试剂的总危害值(tHV)和总分析危害值(taHV) [14]
过程危害值pHV是评价总分析过程的危害得分,计算如下:
式中vtaHV1表示第1种溶剂的taHV (可从表1中获得)与其消耗体积(mL)的乘积;vtaHV2为第2种溶剂的taHV (可从表1中获得)与其消耗体积(mL)的乘积;vtaHVn为第n种溶剂的taHV (可从表1中获得)与其消耗体积(mL)的乘积。pHV值的大小代表着化学过程的绿色度。pHV值越大过程的绿色度越差,反之则越好。
5 两种绿色度表征方法的运用
5.1 高效液相色谱实验的几个实例
为了运用上述两种方法进行绿色度的计算,从文献中任意选择了六个液相色谱实验,将它们分别编号为I-VI,并将其流动相组成、流动相的消耗、梯度次数、流动相流速、运行时间以及参考文献序号等信息列于表2。为了达到以下三个目的,本文从SCI文献中任意选取了六个液相色谱实验方法,当然它们可以换成其他任何液相色谱实验方法,只不过为了达到下面第三条目标,选取的色谱实验方法数量最好大于6个。第一,可作为绿色度计算的例题,便于读者检查自己是否掌握了绿色度计算方法。第二,说明两种计算方法得出的绿色度数值存在较大的差异,因此在报告方法的绿色度时需要指明所采用的计算方法。第三,尽管两种计算方法绿色度数值存在较大差异,但它们所给出的对应液相色谱方法绿色度顺序却是完全相同的,更重要的是两者的绿色度数值间存在明显的线性相关性,所以说两种方法在揭示绿色度大小方面都具有同等的量度效果。
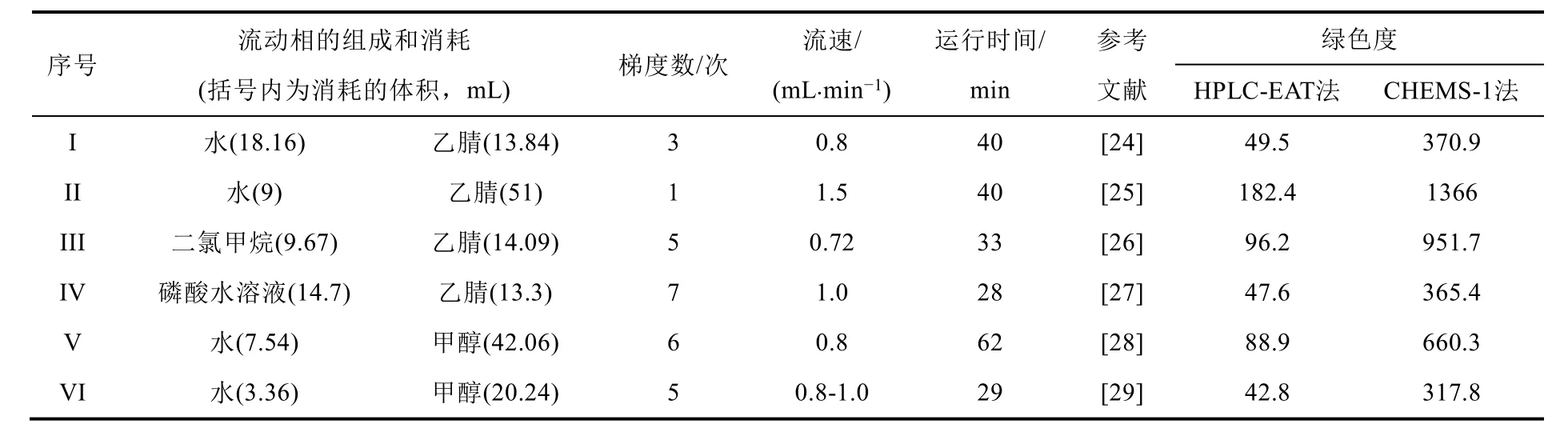
表2 几个液相色谱实例中的溶剂消耗、梯度数目、流速和运行时间
5.2 计算结果的比较
表2的最后两列为HPLC-EAT和CHEMS-1两种方法计算所得的绿色度。单纯从数值上进行比较,两种方法计算出来的绿色度数值存在较大的差异性,但如果观察它们计算结果的趋势就会看出:HPLC-EAT法得到的较大数值,对应着CHEMS-1法得到较大的数值;反之亦然。图2是两种方法相关性的重要证据,其中横坐标为CHEMS-1法计算的绿色度值,纵坐标为HPLC-EAT法计算的绿色度值。线性方程为y= (1.315 ± 10.83) + (0.1236 ± 0.01403)x,r2= 0.9508,表明两种方法计算出的绿色度有较好的相关性。
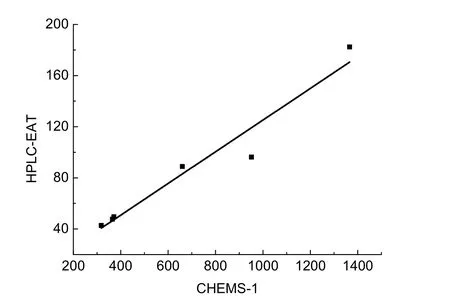
图2 两种方法(HPLC-EAT和CHEMS-1)绿色度计算结果的相关性
HPLC-EAT绿色度的计算是通过软件来完成。运行时只需要将流动相的组成、梯度程序和流速等信息输入到软件中就可算出对应的绿色度数值。这种方法具有计算快、计算过程简单的优点,但因为这种方法主要解决的是液相色谱方法绿色度评价的问题,可供选择的溶剂只有13种:丙酮、乙腈、氯仿、二氯甲烷、乙醇、乙酸乙酯、己烷、辛烷、异丙醇、甲醇、硫酸96%、叔丁基甲基醚、四氢呋喃。如果使用了它所提供的溶剂库之外的其他溶剂,这种方法就不能用于绿色度的计算了。
改进的CHEMS-1法[14]对分析方法绿色度的计算,实际上是通过式(7)计算过程危害值pHV来完成的。pHV由各溶剂的vtaHV加和而成,而vtaHV值是由查表1获得的taHV与所消耗的该溶剂体积之积而求得。taHV是在改进原始的CHEMS-1法tHV基础上而由Tobiszewski等人[14]提出的,具体计算详见式(3)。表1列出了一些常用溶剂的taHV和tHV数据,便于以后查阅和计算使用。对于表1中没有包含的溶剂,也可通过式(3)自行计算。因此,改进的CHEMS-1法计算绿色度(pHV)时,是需要查表手动计算的,但该方法不需要固定溶剂库的限制(只是为了计算方便,把一些常用试剂的tHV和taHV列于表1中),有较广泛的适用性和灵活性。它不仅可以对液相色谱过程绿色度进行计算,也可用于样品预处理过程的绿色度计算。
6 绿色度在建立绿色色谱分析中的指导作用
绿色度的数值对于人们选择、使用和建立更加绿色的色谱分析方法具有明确的指导意义。(1) 它有助于绿色洗脱溶剂的选择。在所介绍的两种绿色度计算方法中,实际上都是计算的绿色度的罚点,就是说计算数值越大,越远离绿色的要求。这种罚点的计算均是根据试剂的各单项危害罚点值(例如HPLC-EAT法是从安全、健康和环境三个角度去考虑)与各试剂用量的乘积然后再求和。因此,为了建立更加绿色的液相色谱方法,应该尽可能选择罚点值低的溶剂。例如,从表1中可以看到甲醇、乙醇和丙酮的taHV值分别为15.7、7.2和2.6,显然如果单纯从绿色度的角度出发,丙酮和乙醇做流动相成分会优于甲醇,这也恰恰是近年来绿色液相色谱发展的一个方向[10]。(2) 减少分析时间和降低洗脱剂的用量。绿色度的罚点总和等于试剂的单项罚点与试剂用量的乘积再求和。试剂用量在罚点总和计算中起到了重要作用。为了降低绿色度的罚点总和,需要尽可能地降低溶剂的消耗量。近年来,UHPLC (ultra high performance liquid chromatography)已开始被广泛使用,它不仅可以显著缩短色谱分析时间,而且流动相的流速也由传统HPLC的0.8-1.2 mL·min-1减少到0.3-0.6 mL·min-1,从而显著降低了有机溶剂的用量,UHPLC发展已成为绿色液相色谱方法发展的一个重要标志[13]。(3) 采用更加绿色的样品前处理方法。由前所述,选用绿色度罚点值低的溶剂和使用更少量有机溶剂,是绿色分析化学的要求。对于复杂样品的色谱分析往往需要一定的前处理步骤。在传统的样品前处理中,往往使用大量的有机溶剂,这种做法不符合绿色分析化学的要求。为此,近年来发展了多种符合绿色分析化学要求且与后续液相色谱分析相适应的新型样品前处理技术[30],诸如:单滴微萃取、分散液-液微萃取、悬浮固化分散液-液微萃取等,在这些处理过程中有机溶剂的消耗由传统方法的几十mL降低到几个μL。这些微萃取技术的发展和使用,有力地保证了绿色液相色谱分析的快速发展。
7 结语
我们尝试着将两个绿色度的定量计算方法(HPLC-EAT和改进的CHEM-1)引入到“仪器分析”课程的液相色谱分析部分中,绿色度的大小是选择、使用和建立液相色谱方法时需要考虑的一个新评价指标,它强化了分析方法开发和使用中所应考虑和承担的社会责任,绿色度的引入有助于学生从专业课程角度理解绿色发展的重要性。所介绍的两种计算方法均出自于近年来的重要学术期刊(GreenChemistry、EcotoxicologyandEnvironmentalSafety),计算方法易于掌握,为仪器分析课程增加了新的知识点。学生对增加的绿色度内容,抱有较高的学习热情,知识掌握情况较好,收到了良好的教学效果,达到了传授知识和技能以及育人的目的。
经过课上讲解和课下的作业练习,听课的43名学生都完全理解了发展绿色化学,特别是发展绿色液相色谱的重要性和必要性。全部同学都掌握了定量表征分析方法绿色度的原理,可以运用CHEMS-1法计算绿色度。对于NEMI和HPLC-EAT法表征和计算绿色度,只有约1/3的同学反馈了作业。尽管HPLC-EAT是一款免费的软件,课上我们已经把下载地址甚至软件直接提供给学生。但由于软件和网站均是英文的,普通大学的大学二年级学生对完全英文的内容还存在一些阅读障碍,不少同学存在畏难情绪,有大约1/3的同学直接放弃了尝试。约2/3的学生积极尝试并安装了HPLC-EAT软件,但由于该软件需要在Java环境下运行。该软件建议下载的Java版本与学生计算机win10系统之间存在一些冲突,导致软件不能正常运行,一些同学经过几次失败的试运行后,也选择了放弃。这样最终掌握HPLC-EAT法计算绿色度的学生约占全班人数的1/3。教学实践表明,相比于HPLC-EAT法和NEMI法,CHEMS-1法更易于学生掌握。
