有机化学实验的副产物分析引导实验创新与科研素养培育
——以4-苯基丁-2-酮合成实验为例
2024-01-23陈建军曹月洋陈万红黄国生高坤
陈建军,曹月洋,陈万红,黄国生,高坤
兰州大学化学化工学院,兰州 730000
有机化学实验是高等学校化学、化工、材料、生物、医学等专业本科生的一门重要基础实验课程。该课程旨在通过实验教学,使学生熟练掌握有机化学实验的基本操作技能;加深学生对有机化学基础知识和反应机理的理解;提高学生独立操作实验、准确观察实验现象、合理处理实验数据、规范撰写实验报告的能力;培养学生通过分析问题、查阅资料等方法进行创新实验设计并解决实际问题的能力[1-5]。在实际教学过程中,会经常出现实验产率低以及结果不符合预期的情况。我们以4-苯基丁-2-酮的合成实验为例,在教学中教师通过引导学生对该实验中的副产物进行分析,并找出产生副产物的原因,进而启发学生对实验方案进行改进,并以此探究过程为素材,树立学生的科研意识,培养学生的科研素养,提升学生的科研能力和综合素质。
1 4-苯基丁-2-酮的合成实验简介
1.1 实验教学目标
4-苯基丁-2-酮是烈香杜鹃(RhododendronanthopogonoidesMaxim)挥发油中的一种成分,具有止咳祛痰的功效。为了便于服用和存放,该化合物常被制成亚硫酸氢钠的加成物,并命名为“止咳酮”[6,7]。此外,4-苯基丁-2-酮也是重要的香料和医药中间体,具有广泛的应用[8]。由于4-苯基丁-2-酮在烈香杜鹃中的含量有限,因此其在实际应用中主要通过合成的方法制备。在实验教学中,4-苯基丁-2-酮是以乙酰乙酸乙酯与氯化苄作为原料,经过系列的亲核取代、水解、脱羧等反应合成的[9]。其教学目标在于让学生通过实践学习β-酮酸酯类化合物的烯醇盐作为负离子与卤代烷发生亲核取代反应形成碳碳键,进一步发生酮式分解合成取代甲基酮的策略,并掌握β-酮酸酯类化合物在有机合成中的初步应用。在基础有机化学的理论教学中,β-酮酸酯类化合物中亚甲基的酸性、酮式分解、酸式分解是该类化合物的重要特征反应,利用其性质在合成取代丙酮、取代羧酸、1,3-二酮等化合物的应用是整个基础有机化学教学中的一个重点和难点。乙酰乙酸乙酯是经典的β-酮酸酯类化合物,将其作为原料合成4-苯基丁-2-酮的反应同时包含酸碱反应、亲核取代反应、酯水解反应、脱羧反应,实验过程包括无水回流、常压蒸馏、萃取、干燥、减压蒸馏等系列操作,是一个设计巧妙的涉及多步骤合成的综合有机化学教学实验。该实验不仅可以很好地帮助学生理解β-酮酸酯类化合物的化学性质和反应原理,掌握合成实验的综合操作技能,其目标产物的药用价值更能激发学生的实验兴趣。因此用乙酰乙酸乙酯和氯化苄合成4-苯基丁-2-酮实验是基础有机化学实验教学中经常开设的实验,国内的很多《有机化学实验》教材中都选用了该实验[9-12]。
1.2 实验原理
该实验的原理在多部实验教材里有详细论述。首先,乙酰乙酸乙酯在乙醇钠的作用下,拔去亚甲基上的质子后形成乙酰乙酸乙酯负离子(简称:EAA-)中间体,该负离子与氯化苄发生亲核取代反应以后形成2-苄基-3-氧代丁酸乙酯,然后将2-苄基-3-氧代丁酸乙酯在碱性(10% NaOH溶液)条件下进行水解,得到2-苄基-3-氧代丁酸钠,最后通过加入20%的HCl溶液将2-苄基-3-氧代丁酸钠酸化,进而加热脱羧便可得到最终产物4-苯基丁-2-酮(图1)。
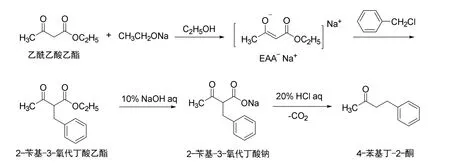
图1 4-苯基丁-2-酮合成的反应式
1.3 实验操作
100 mL干燥的三口瓶上装上温度计及带有氧化钙干燥管的回流冷凝管,用油浴加热,并配置电磁搅拌器。
往反应瓶中加入20 mL无水乙醇,并分次加入1.0 g (0.044 mol)切成小片的金属钠,加入速度以维持溶液微沸为宜。待钠完全作用后,在搅拌下加入5.7 g (5.5 mL,0.044 mol)乙酰乙酸乙酯,继续搅拌10 min。再缓慢加入5.8 g (5.3 mL,0.046 mol)重新蒸馏过的氯化苄(约20 min),这时有大量白色沉淀产生,然后加热使反应物微沸回流至反应物几乎呈中性。
使用常压蒸馏法蒸出大部分乙醇,向剩余液体中加入25 mL 10%的NaOH溶液,在搅拌条件下加热回流1 h,再滴加20%的盐酸溶液调节溶液pH为2-3,再加热搅拌至无二氧化碳气泡逸出为止。将液体冷却后用10%的氢氧化钠溶液调节至中性,用乙醚萃取(15 mL × 3),合并乙醚提取液,用水洗涤一次,经无水Na2SO4干燥后,使用水浴常压蒸出乙醚。将剩余物进行减压蒸馏,收集86-88 °C/665 Pa的馏分。
1.4 仪器与试剂
主要仪器:核磁共振仪(Bruker AVANCE III-400,瑞士)、高分辨质谱仪(Thermo Scientific LTQOrbitrap EliteETD,美国)、AE224型电子天平(上海舜宇恒平科学仪器有限公司)。
材料与试剂:乙酰乙酸乙酯、氯化苄、钠、无水乙醇、NaOH、Na2SO4、无水乙醚均为国药分析纯试剂。柱层析硅胶(200-300目)购自青岛海洋化工厂,GF254高效薄层层析硅胶板购自烟台银龙硅胶有限公司,使用UV254紫外灯检测并配以5%的硫酸-乙醇溶液显色。
2 4-苯基丁-2-酮合成实验中的低产率现象及副产物分析
2.1 实验结果中出现的低产率现象及思考
在实际教学中,该实验最后得到4-苯基丁-2-酮的产率较低,通常大约在20%-30%之间。尽管有文献报道通过延长脱羧时间或者运用微型化合成的方法可以提高4-苯基丁-2-酮的产率,但是按照文献提供的操作方法进行实验仍然收效甚微[13,14]。在实验过程中我们发现,虽然蒸馏前反应粗产物的量并不少,但经过减压蒸馏获得4-苯基丁-2-酮后,仍有大量的副产物未被蒸出(图2),从而使得目标产物的收率较低。因此,教师引导学生对实验教学过程中可能出现的副产物进行讨论,以期找出副产物生成的原因,并给出合理的对策提高反应产率。学生们对该讨论表现出极大的热情和兴趣,结合反应机理积极思考,给出多种可能的副产物。

图2 4-苯基丁-2-酮合成实验得到的产物、减压蒸馏残液(左)以及蒸馏残液的TLC分析(右)
2.2 实验结果中副产物的鉴定
在学生们讨论结果的基础上,教师建议学生通过查阅资料或者文献找出副产物是什么的答案。通过查阅不同版本的实验教材发现教材中没有对该反应的副产物进行描述。但有文献报道乙酰乙酸乙酯在乙醇钠的作用下与氯化苄反应除了可以得到2-苄基-3-氧代丁酸乙酯外,还有2,2-二苄基-3-氧代丁酸乙酯生成,由此推测反应的副产物可能为3-苄基-4-苯基丁-2-酮[15]。但是否为该化合物还需要进一步验证。因此,教师建议学生通过已经学过的薄层层析和柱层析的方法对减压蒸馏残液中的副产物进行分离纯化,并用核磁共振谱和质谱对主要副产物的结构进行鉴定。用V石油醚:V乙酸乙酯= 5 : 1的展开剂对减压蒸馏残液进行薄层色谱分析,发现其中主要含有一个未知副产物(Rf= 0.60)和少量的4-苯基丁-2-酮(Rf= 0.49) (图2)。利用硅胶柱层析对该未知副产物进行分离,用V石油醚:V乙酸乙酯= 10 : 1进行洗脱,得到纯的未知副产物(无色油状物)。通过核磁共振谱和质谱确定未知副产物为2,2-二苄基-3-氧代丁酸乙酯。
4-苯基丁-2-酮结构鉴定:该化合物为无色油状物,根据其HRESIMS谱(见补充材料图S1)在m/z171.0779处显示[M+Na]+的分子离子峰(计算值C10H12ONa,171.0780),可以推测该化合物的分子式为C10H12O。该化合物的1H NMR (400 MHz,CDCl3)谱(图S2)中显示存在1个一取代的苯环信号(δH7.28(t,J= 7.2 Hz, 2H),7.20 (d,J= 7.2 Hz, 1H),7.18 (d,J= 7.2 Hz, 2H)),1个苄位亚甲基质子信号(δH2.89(t,J= 8.0 Hz, 2H)),1个羰基α位亚甲基质子信号(δH2.74 (dd,J= 8.0, 7.2 Hz, 2H)),以及1个单峰甲基质子信号(δH2.12 (s, 3H))。该化合物的13C NMR (100 MHz,CDCl3)谱(图S3)中显示存在1个酮羰基碳信号(δC208.0),6个苯环碳信号(δC141.1,128.5 × 2,128.4 × 2,126.2),2个亚甲基碳信号(δC45.2,30.1),以及1个甲基碳信号(δC29.8)。综合上述谱图信息并与文献数据对比可以确定该化合物为4-苯基丁-2-酮[16]。
2,2-二苄基-3-氧代丁酸乙酯结构鉴定:该化合物为无色油状物,根据其HRESIMS谱(图S4)在m/z333.1457处显示[M+Na]+的分子离子峰(计算值C20H22O3Na,333.1461),可以推测该化合物的分子式为C20H22O3。该化合物的1H NMR (400 MHz,CDCl3)谱(图S5)中显示存在2个一取代的苯环信号(δH7.25 (m, 6H),7.12 (d,J= 6.8 Hz, 2H),7.18 (d,J= 8.0 Hz, 2H)),4个苄位亚基质子信号(δH3.21 (s,4H)),1个单峰甲基质子信号(δH1.96 (s, 3H)),以及1个连氧乙基信号(δH4.11 (q,J= 7.2 Hz, 2H),1.17(t,J= 7.2 Hz, 3H))。该化合物的13C NMR (100 MHz,CDCl3)谱(图S6)中显示存在1个酮羰基碳信号(δC205.8),1个酯羰基碳信号(δC171.8),12个苯环碳信号(δC136.3 × 2,130.1 × 4,128.3 × 4,126.9 × 2),1个季碳信号(δC66.1),1个连氧亚甲基碳信号(δC61.4),2个苄位亚甲基碳信号(δC39.8)以及2个甲基碳信号(δC29.3,13.9)。综合上述谱图信息并与文献数据对比可以确定该化合物为2,2-二苄基-3-氧代丁酸乙酯[15]。
2.3 副产物2,2-二苄基-3-氧代丁酸乙酯产生的原因分析及讨论
根据副产物2,2-二苄基-3-氧代丁酸乙酯的结构,学生们推测其可能是在亲核取代反应过程中,中间产物2-苄基-3-氧代丁酸乙酯与EAA-同时存在于反应体系中,前者分子中仍有一个活性较高的酮羰基和酯羰基的双重α-H,因此2-苄基-3-氧代丁酸乙酯可与EAA-作用生成一定量的2-苄基-3-氧代丁酸乙酯负离子(简称:2-Bn-EAA-),进而与氯化苄发生亲核取代反应生成最终副产物(图3)。至于为什么2-苄基-3-氧代丁酸乙酯容易被水解和脱羧,而2,2-二苄基-3-氧代丁酸乙酯不会被水解和脱羧,是由于2-苄基-3-氧代丁酸乙酯在碱性条件下更易于形成烯醇化的中间体,该中间体产生的分子内的氢键可以活化酯羰基,使得2-苄基-3-氧代丁酸乙酯容易被水解成相应的羧酸盐,进而发生后续的脱羧反应最终得到4-苯基丁-2-酮(图4)。而在2,2-二苄基-3-氧代丁酸乙酯中由于2位没有活泼质子存在,不能形成烯醇化中间体,再加上两个苄基的位阻作用,使得其中的酯在本实验条件下难以被水解,从而无法发生进一步的脱羧反应。
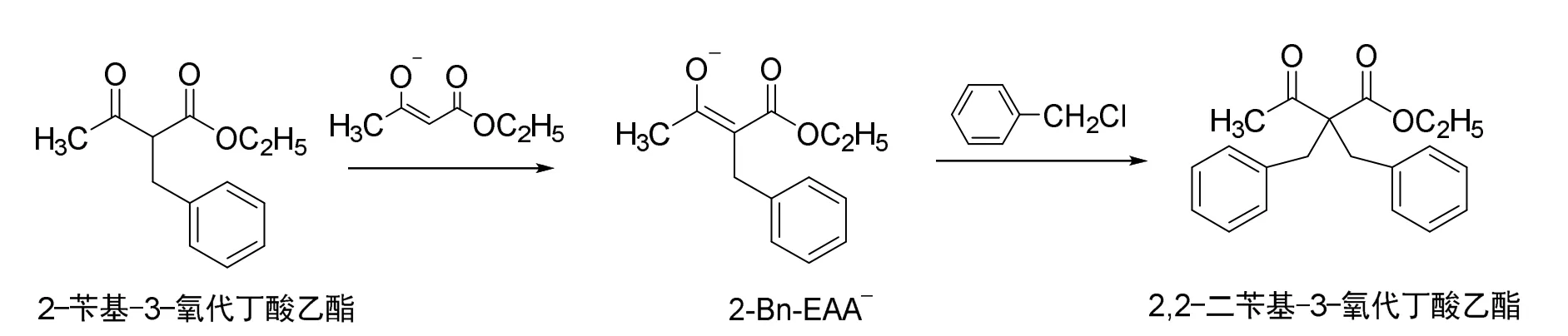
图3 2,2-二苄基-3-氧代丁酸乙酯的生成反应式
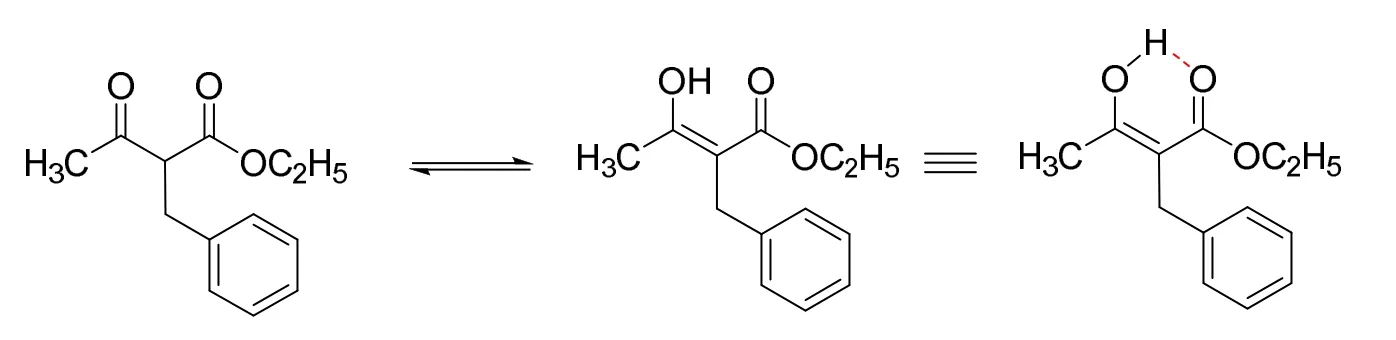
图4 2-二苄基-3-氧代丁酸乙酯的烯醇式互变及其分子内的氢键
2.4 提高4-苯基丁-2-酮的产率尝试
在明确副产物的结构和生成原因的基础上,教师引导学生思考如何能够提高4-苯基丁-2-酮产率。学生经过讨论给出两种方案:(1) 通过降低反应物浓度,以减少EAA-与2-苄基-3-氧代丁酸乙酯接触的几率;(2) 通过降低反应温度,使得2-Bn-EAA-更加难以生成。
学生通过将反应体系中无水乙醇的量提高至30 mL或者40 mL,从而使3-氧丁酸乙酯负离子的浓度降低约30%-50%,按照实验操作进行反应。通过检测发现4-苯基丁-2-酮的产率几乎没有变化。在降低反应温度的方案中,随着反应温度的降低,4-苯基丁-2-酮产率有一定的提高。但即便是温度降低至0 °C,4-苯基丁-2-酮产率也仅有32.1%,而且取代反应这一步需要2.5 h才能完成(表1)。从实验结果可以看出通过降低反应浓度和反应温度都不能有效地提高4-苯基丁-2-酮的产率,而且反应过程中2,2-二苄基-3-氧丁酸乙酯的比例要高于2-苄基-3-氧代丁酸乙酯的比例。这可能是因为烯醇化的2-Bn-EAA-中苄位的σ-π超共轭效应可以稳定该负离子,使得反应体系中的EAA-易于做为碱夺取新生成的2-苄基-3-氧代丁酸乙酯中的活波质子,形成更稳定的2-Bn-EAA-,最终二者达到一个平衡。
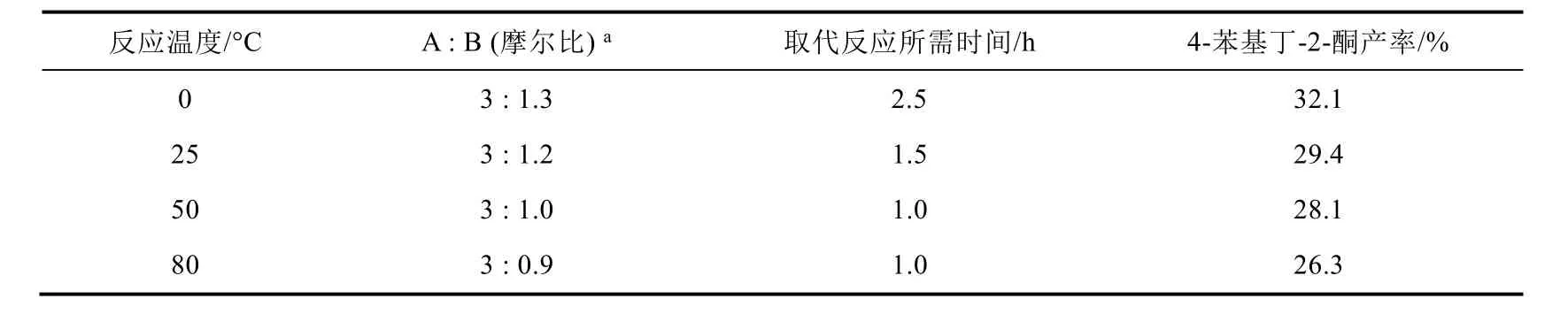
表1 按照教材中的方法,不同反应温度对两种中间产物的比例以及终产物产率的影响
基于上述分析,我们想如果使用反向滴加的方法将EAA-钠盐的乙醇溶液滴加进氯化苄中,由于滴加过程中反应体系中的氯化苄是过量的,EAA-会较大程度地与氯化苄反应,使反应体系中EAA-的浓度维持较低的水平,这样生成2-Bn-EAA-的机率就会降低,从而可以减少副产物的生成。按照该思路,学生设计了如下方案:首先,按照教材中的方法在100 mL干燥的三口瓶中制备EAA-钠盐,并将该钠盐的乙醇溶液转入到恒压滴液漏斗中待用;然后,向该三口瓶中加入5 mL的无水乙醇和5.8 g的氯化苄,将其混合均匀。并将装有EAA-钠盐乙醇溶液的恒压滴液漏斗装在一侧的侧口上。在磁力搅拌下用油浴加热使瓶内液体微沸后,打开恒压滴液漏斗活塞缓慢滴加其中的液体,控制滴加速度使滴加时间不少于20 min。待液体滴加完以后再反应10 min;最后,按照教材中的实验步骤进行后续的酯水解反应和脱羧反应。
学生按照设计的新方案进行实验,发现产物中副产物2,2-二苄基-3-氧代丁酸乙酯与4-苯基丁-2-酮的摩尔比为3 : 12.2,产物的产率达到了47.5%,与以前相比有了较大的提升。通过分析可以发现,在新实验方案中除了在微沸状态下向圆底烧瓶中滴加EAA-钠盐的乙醇溶液以保证EAA-快速与氯化苄反应外,EAA-的滴加速度和其中的溶剂体积也是影响其产率的主要因素。因此,学生又考察了在相同体积乙醇做溶剂条件下EAA-钠盐的乙醇溶液的滴加时间对4-苯基丁-2-酮产率的影响。从结果可以看出,EAA-钠盐的乙醇溶液的滴加时间越长,4-苯基丁-2-酮的产率越高。但考虑到实际实验学时以及滴加时间从40 min延长至60 min对产率影响较小的实验结果,将滴加时长控制在不小于40 min为宜(表2)。在时间限定的条件下,我们又进一步考察了EAA-中的溶剂体积对产率的影响。从实验结果来看,EAA-中的溶剂体积对产率略有影响(表3)。考虑到实验实际情况,选用25 mL无水乙醇制备EAA-为宜。
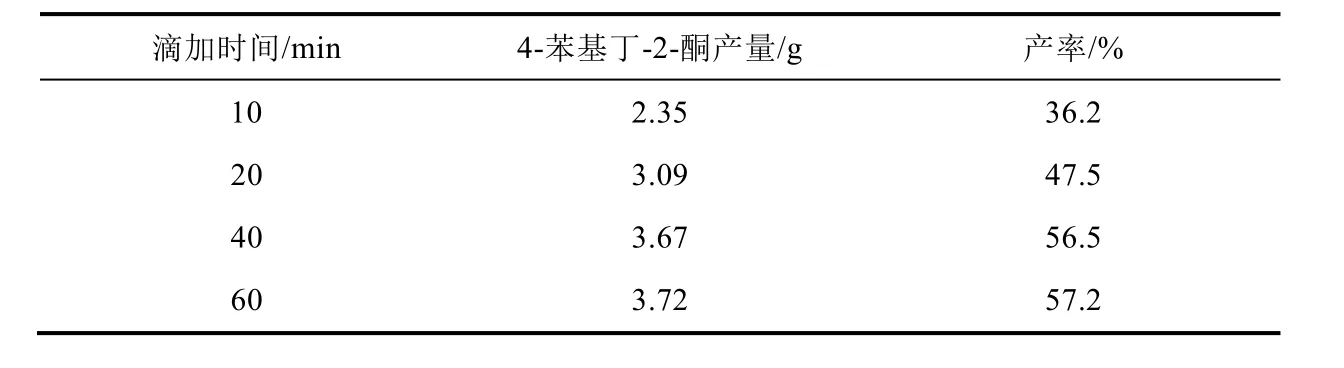
表2 新方案中反向滴加EAA-钠盐乙醇溶液的时间对终产物产率的影响
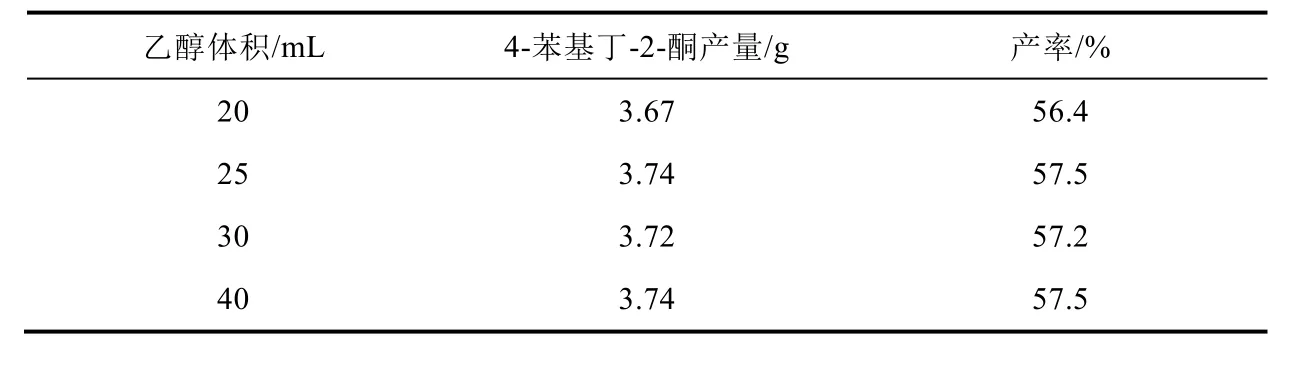
表3 新方案中EAA-中的乙醇体积对终产物产率的影响
综上所述,我们最终对4-苯基丁-2-酮的合成实验方案进行如下优化:首先,向100 mL干燥的三口瓶中加入25 mL无水乙醇,在中口装上带有氯化钙干燥管的回流冷凝管,并分次将1.0 g (0.044 mol)切成小片的金属钠由侧口加入。待钠完全作用后,在搅拌下加入5.7 g (5.5 mL,0.044 mol)乙酰乙酸乙酯,继续搅拌10 min。将瓶中的液体转入到恒压滴液漏斗中待用;然后,向该三口瓶中加入5 mL的无水乙醇和5.8 g (5.3 mL,0.046 mol)的氯化苄,将其混合均匀。并将上一步装有液体的恒压滴液漏斗装在一侧的侧口上。在磁力搅拌下用油浴加热使瓶内液体呈微沸状态后打开恒压滴液漏斗活塞缓慢滴加其中的液体,控制滴加速度使滴加时间不少于40 min,待液体滴加完以后再反应10 min;最后按照原来的实验步骤进行后续的水解反应和脱羧反应,并通过萃取、干燥、蒸馏以及减压蒸馏等操作得到4-苯基丁-2-酮(3.7 g,产率57.5%)。
3 科研素养的培育
高等教育的目标是培养高素质的创新型人才,作为人才培养摇篮的高校应着重培养学生的科研素养,提升科研能力[17]。科研素养的形成离不开基础实验课程的教学与引导。作为化学教学重要环节的实验教学,要求教师将科研素养与科学创新能力培养贯穿于教学中,积极引导学生主动探究,提高学生自主发现问题、分析问题并解决问题的能力,树立学生的科研意识,培养学生的创新思维,提升学生的科研能力和综合素质。
4-苯基丁-2-酮的合成教学实验中,教师引导学生通过副产物分析进行实验改进与创新,是一个培养学生科研素养、提升科研能力和综合素质的优秀案例。首先,学生在实验操作过程中,教师要求学生详细记录实验原始数据,包括试剂用量、操作时间、实验现象、实验结果等,培养了学生严谨的科研态度和实验习惯;其次,学生在教师的引导和帮助下利用所学知识积极思考和确定副产物是什么的问题,并以此为基础探索新的实验方案最终提高了反应产率,这一过程着重培养了学生发现问题、分析问题和解决问题的科研意识和创新思维;最后,学生在实验过程中既有成功后的喜悦,也有失败后的失落,更有不断摸索的艰辛。教师积极教导学生既要有吃苦耐劳、越挫越勇的精神,更要学会分析思考实验失败的原因,通过实验探究的过程,体会实验成功的快乐,最终助力培养内心强大、追求卓越的高素质创新型人才。
4 结语
4-苯基丁-2-酮的合成实验是有机化学合成实验中一个具有代表性的综合合成实验,但是实际教学中该实验产率较低,通常只有20%-30%。本文记录了在该教学实验中教师通过引导学生对该实验中的副产物进行分析,并找出产生副产物的原因,进而启发学生对实验方案进行创新改进。根据新的实验方案,4-苯基丁-2-酮的产率被提高至57.5%。此外,整个实验过程不仅提高了学生自主发现问题、分析问题并解决问题的能力,更是培养了学生的科研素养,提升了学生的科研能力和综合素质。在教学实践中,诸如4-苯基丁-2-酮的合成教学实验的案例还有许多,教师应该以此为契机,有目的地引导和鼓励学生进行自主探索和创新,激发学生的学习兴趣和自主能力,提高学生的科研素养,为培养新时代高素质创新型人才奠定基础。
补充材料:可通过链接https://www.dxhx.pku.edu.cn免费下载。
