Ph-C≡C-Cu基新型功能材料的结构-性质-效能关系探究
2024-01-23蒋海英穆玥如张媛媛孙雪王云侠郭慧林岳可芬
蒋海英,穆玥如,张媛媛,孙雪,王云侠,郭慧林,岳可芬
西北大学化学与材料科学学院,西安 710127
在现代社会新工科的背景下,培养一大批具有实践性、综合性、创新性的人才,为实现“中国制造2025”行动纲领提供重要的智力和人才支撑,是化学专业最重要的教育目标之一[1]。在化学和材料专业本科高年级开展化学综合实验,能够有效培养学生理论联系实际和实践操作的能力,指导他们综合运用化学基础知识解决实际生活生产问题的能力,提升学生的创新意识,增强学生学习的积极性[2]。目前国内高校的综合化学实验中,涉及物理化学方面的综合化学实验较少[3,4];且大多属于验证性实验,实验课程教学处于“自上而下”的被动教-授状态,探索性和思考性不足,无法提升实际科研中所需的逆向思维能力。
Ph-C≡C-Cu是苯乙炔偶联反应过程中产生的一种中间体,长期以来在有机合成领域并没有引起科研工作者广泛的研究兴趣[5-7]。随着科研的不断发展和深入,不同学科之间的交叉与融合逐渐成为当今科学研究的常态,这为Ph-C≡C-Cu基材料的发展和应用提供了新的机会和战场[8,9]。本文选取最新报道的Ph-C≡C-Cu基新型功能材料作为研究对象,通过官能团修饰来调控其化学结构,分析不同官能团的电子效应,探究其材料物理化学性质对效能的作用关系。本实验的学习和实践不仅能够帮助学生深入了解科技前沿,将不同学科的知识融会贯通,引导学生理解绿色化学和光催化反应的重要意义,更能启发学生以实际问题为导向,根据所学理论和知识,从源头上出发,对功能材料的结构进行设计,同时也培养了学生“自下而上”的逆向思维方式,提升了学生理论与实践相结合的能力。
1 实验部分
1.1 实验目的
(1) 掌握光热合成法制备Ph-C≡C-Cu基新型功能材料的基本原理和方法;
(2) 掌握红外光谱仪、紫外-可见吸收光谱仪、DSA25型接触角测试仪的仪器结构、测试原理和使用方法;
(3) 学习并掌握光催化降解反应的实验流程和反应进度监测方法;
(4) 深入理解Ph-C≡C-Cu基光催化剂的结构-性质-效能关系;
(5) 启发并引导学生以问题为导向,根据已有的理论出发,从源头上对功能材料的结构进行设计,培养本科生的逆向思维方式。
1.2 实验原理
作为一个优良的可见光催化剂,Ph-C≡C-Cu具有良好的可见光响应,对甲基橙(MO)等染料污染物的降解去除非常有效。根据文献报道,Ph-C≡C-Cu基光催化剂的最高占据轨道(HOMO)主要由Cu的3d轨道组成,最低空轨道(LUMO)主要由sp和sp2杂化的C的2p轨道组成[10]。如图1所示:将Ph-C≡C-Cu基光催化剂置于光照条件下,当入射光的能量大于或等于其HOMO和LUMO轨道之间的能量差时,电子会从一价铜的3d轨道跃迁到碳的2p轨道,形成具有一定氧化-还原能力的光生空穴-电子对。对于Ph-C≡C-Cu基光催化剂来说,光生电子具有很强的还原能力,可以活化分子氧,产生O2-•等一系列活性氧自由基,这些活性氧自由基能够有效地将MO等染料分子氧化成CO2和H2O等无毒小分子,从而实现工业废水中染料污染物的有效降解和去除。
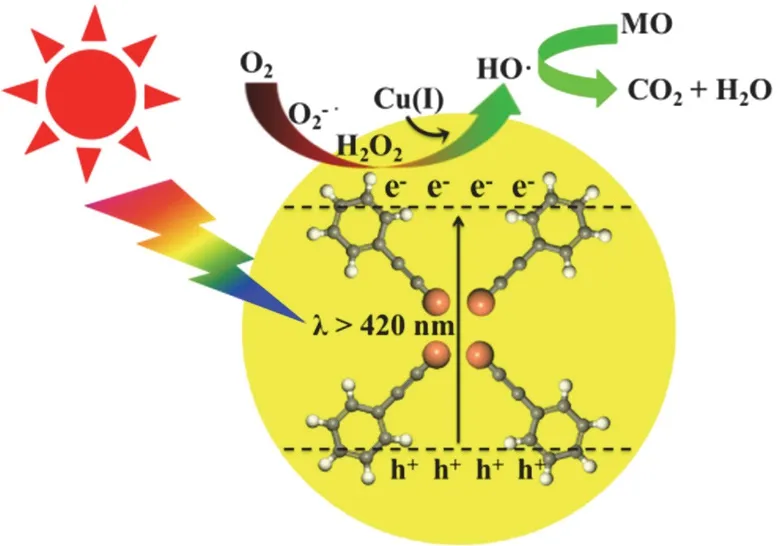
图1 Ph-C≡C-Cu光催化降解MO的示意图[10]
通过研究Ph-C≡C-Cu分子苯环上取代基的种类和电子效应对Ph-C≡C-Cu基光催化剂的物理化学性质(比如亲疏水性和颜色)的影响,探索苯乙炔铜系列化合物对于MO去除效率(吸附和光催化降解)的影响,进一步讨论基于官能团修饰的Ph-C≡C-Cu基新型功能材料在降解MO过程中的结构、性质和效能之间的关系(如图2所示)。
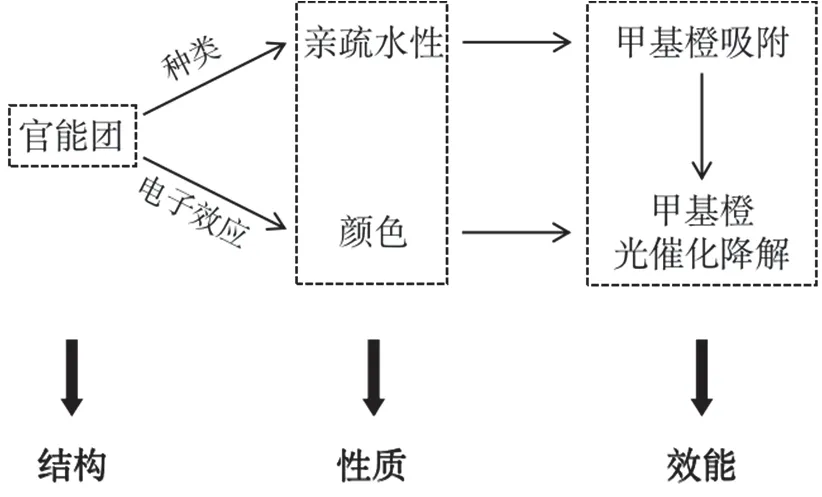
图2 Ph-C≡C-Cu基材料的结构-性质-效能关系总结
1.3 试剂和仪器设备
实验所需要的主要试剂和仪器如表1和表2所示,其余仪器包含:50 mL烧杯、分析天平、烘箱、钥匙、磁子、铁架台、恒压滴液漏斗、超声波清洗器、250 mL容量瓶、玻璃棒、注射器、0.22 μm微孔滤膜、4 mL离心管。

表1 主要实验试剂

表2 主要实验仪器
1.4 实验步骤
1.4.1 Ph-C≡C-Cu基新型功能材料的制备
本实验通过光热合成法制备Ph-C≡C-Cu基新型功能材料[11]:
(1) 称量211 mg CuCl和320 mg NaOH,分别转移至于两个小烧杯中,均溶于20 mL CH3OH。将NaOH的CH3OH溶液置于超声中振荡,直至完全溶解。
(2) 将NaOH的CH3OH溶液转移至恒压滴液漏斗,在持续搅拌下加入CuCl溶液中,控制滴速为:前10 mL每3-4秒1滴,后10 mL每秒1滴。
(3) 使用移液枪逐滴加入一定体积(如表3所示)含不同官能团的Ph-C≡C-H。需要注意的是,4-FPh-C≡C-H在保存时为固体,需待其融化方可取用。
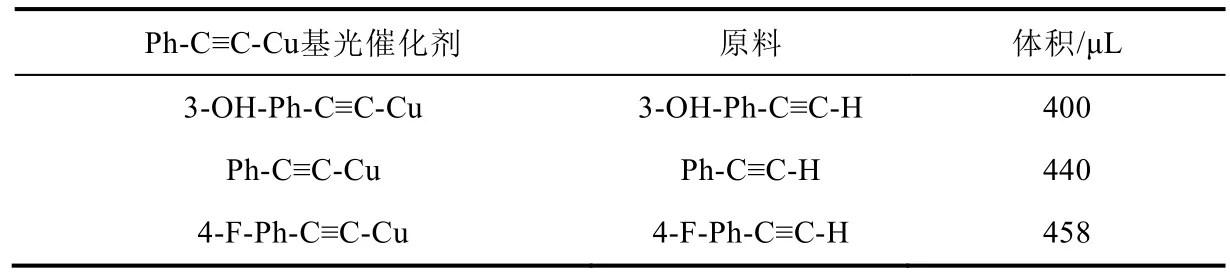
表3 不同的苯乙炔原料所需的体积
(4) 将配好的混合液置于氙灯下搅拌1 h后,即可得到的含有产物的悬浊液。
(5) 抽滤,分别用水和乙醇洗涤2-3次,并置于60 °C烘箱内进行干燥。
1.4.2 Ph-C≡C-Cu基光催化剂的结构表征
使用FT-IR表征含不同官能团的Ph-C≡C-Cu分子的特征振动峰,利用KBr压片法测定Ph-C≡C-Cu及其系列材料的红外光谱:
(1) 样品制备:取100-200 mg干燥KBr充分研磨后倒入压片模具中压制成透明薄片,并保存在干燥器中;另取1-2 mg干燥的Ph-C≡C-Cu基材料和100-200 mg干燥的KBr,一并倒入玛瑙研钵中研磨直至混合均匀,取少许上述混合物粉末导入压片模具中压制成透明薄片,并保存在干燥器内。
(2) 以空气为参比扫描背景后,进行样品测试。把样品放入样品室,点“Sample”进行测试,测试完成后可以获得样品的FT-IR谱图。
1.4.3 Ph-C≡C-Cu基光催化剂的性质表征
A、吸光性:
使用UV-Vis Abs测量Ph-C≡C-Cu基新型功能材料的吸收光谱。取3 mg Ph-C≡C-Cu基材料溶于4 mL二甲基亚砜(DMSO)中,测量其200-800 nm的紫外吸收光谱。
B、亲疏水性:
(1) 通过测量含不同Ph-C≡C-Cu光催化剂的静态水接触角来表征其亲疏水性:
(2) 在制样板上分别制备Ph-C≡C-Cu、3-OH-Ph-C≡C-Cu、4-F-Ph-C≡C-Cu的粉末状薄片。
(3) 打开接触角的软件和光源旋钮,进行亮度和对比度调节,使电脑画面清晰。
(4) 点击“制造液滴”,使液滴滴落在样品薄片上。
(5) 调整平台高度直至液滴完全显示在屏幕中并拍摄照片。
1.4.4 Ph-C≡C-Cu基光催化剂的性能表征
(1) MO标准曲线的绘制:将预先配制好的200 mg·L-1的MO储备溶液分别稀释至12 mg·L-1、10 mg·L-1、8 mg·L-1、6 mg·L-1、4 mg·L-1、2 mg·L-1。使用UV-Vis Abs计测定MO在463 nm处的吸光度,得到MO的浓度-吸光度曲线。
(2) MO悬浮液配制:将预先配制好的200 mg·L-1的MO储备溶液分别稀释至20和10 mg·L-1。取200 mg·L-1、20 mg·L-1、10 mg·L-1的MO溶液各40 mL,分别加入40 mg 3-OH-Ph-C≡C-Cu、Ph-C≡C-Cu和4-F-Ph-C≡C-Cu,进行后续的吸附和光催化降解实验。
(3) 吸附性能测试:将混合好的MO悬浮液用锡纸包裹后避光搅拌,每隔10 min用注射器各吸取2 mL MO悬浮液,透过滤膜注入5 mL离心管中,进行定量稀释后,通过UV-Vis Abs进行检测,监测吸附进程,直至最大吸收波长处的吸收值不再减小,即达到吸附平衡。需要注意:当吸光度超过1时,应将溶液稀释后进行测量,以确保吸收值和浓度之间准确的线性关系。
(4) MO的光催化降解性能:达到吸附平衡后,将烧杯中的MO悬浮液转移至带有冷凝装置的烧杯中,并将其置于氙灯下搅拌,每隔10 min用注射器各吸取2 mL烧杯中的MO悬浮液,透过滤膜过滤注入5 mL离心管中,通过UV-Vis Abs检测并监测反应进程,直至滤出液变成无色。
(5) 根据标准曲线计算吸附和光催化降解过程中所取各样的浓度,绘制浓度-时间曲线。
2 结果与讨论
2.1 结构表征
本实验通过红外光谱来表征Ph-C≡C-Cu基新型功能材料的结构。如图3所示:在Ph-C≡C-Cu的红外光谱中,3442 cm-1处为材料表面吸附水的O—H键的伸缩振动峰[12];1700-1300 cm-1范围内的峰为苯环骨架的伸缩振动峰[12];746 cm-1和683 cm-1处的峰说明其为单取代苯环[12];515 cm-1处的峰说明分子中有C≡C键[13]。在3-OH-Ph-C≡C-Cu的红外光谱中,3340 cm-1和1236 cm-1处分别为酚羟基的伸缩振动峰和面内变形振动峰[12];1271 cm-1处的峰为酚的C—O键的伸缩振动峰[12];779 cm-1和679 cm-1处的峰说明分子中含间位取代的苯环[12]。在4-F-Ph-C≡C-Cu的红外光谱中,1232 cm-1处的峰为C—F键的伸缩振动峰[12];827 cm-1处的峰说明分子中含对位取代的苯环[12]。通过对位、间位、单取代苯环的巧妙设计,提高了同学们的红外解谱能力。
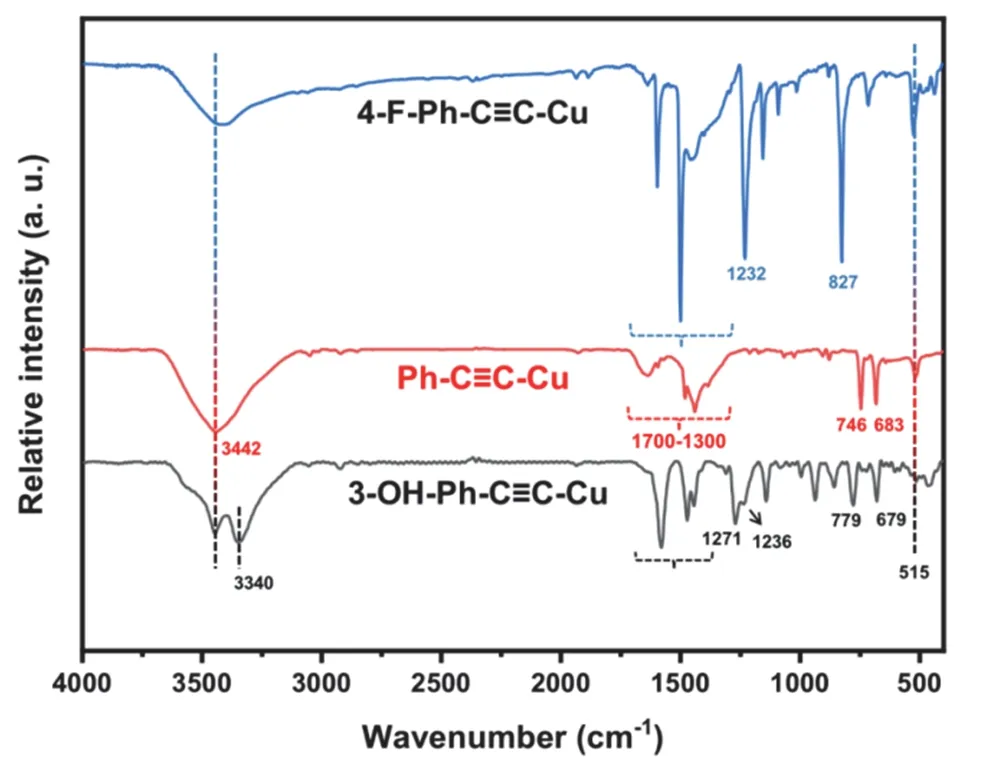
图3 Ph-C≡C-Cu基材料的红外光谱
2.2 性质表征
2.2.1 颜色及吸光范围
本实验通过UV-Vis Abs来表征所制备Ph-C≡C-Cu基新型功能材料对可见光的吸收。如图4所示:3-OH-Ph-C≡C-Cu的最大吸收波长λmax= 416 nm (图4A),Ph-C≡C-Cu的λmax= 444 nm (图4B),4-F-Ph-C≡C-Cu的λmax= 467 nm (图4C)。由此结果可知,当苯环上连接给电子基团(—OH)时,Ph-C≡C-Cu的λmax发生蓝移;当苯环上连接吸电子基团(—F)时,Ph-C≡C-Cu的λmax发生红移。
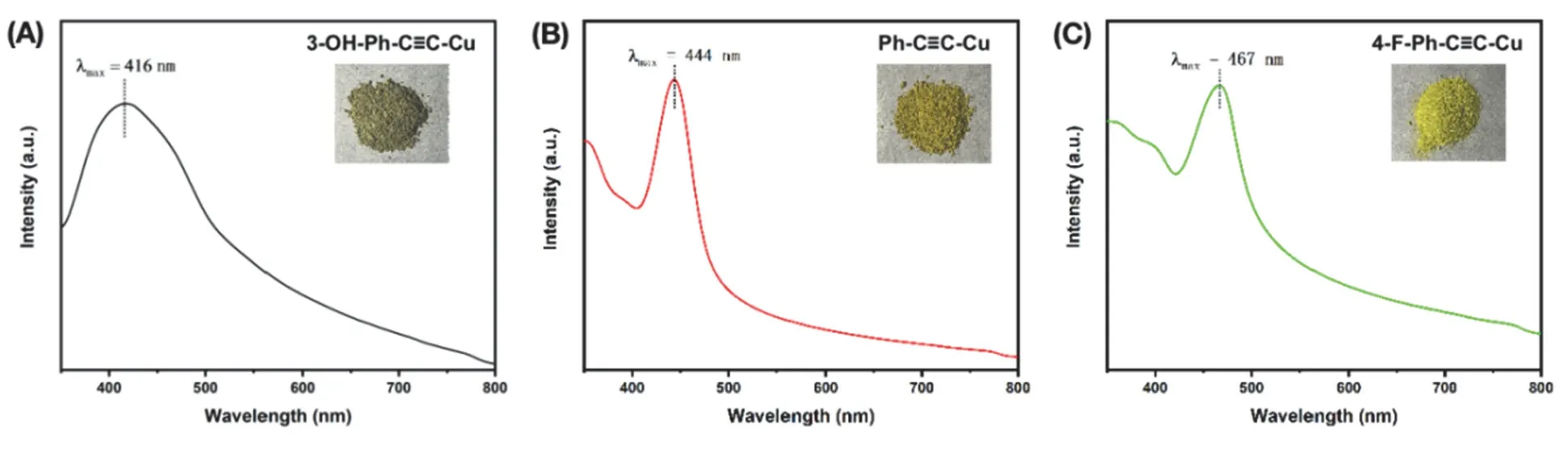
图4 Ph-C≡C-Cu基材料的紫外-可见吸收光谱和制备的粉末样品
根据互补色原理(图5)[14],3-OH-Ph-C≡C-Cu的最大吸收波长在紫色区,因此表现出其互补色——黄绿色,Ph-C≡C-Cu和4-F-Ph-C≡C-Cu的λmax在蓝色区,因此表现出其互补色——黄色,Ph-C≡C-Cu的λmax小于4-F-Ph-C≡C-Cu,因此Ph-C≡C-Cu表现出的颜色偏绿。该实验进一步加深了同学们对于光和物质颜色的认识。
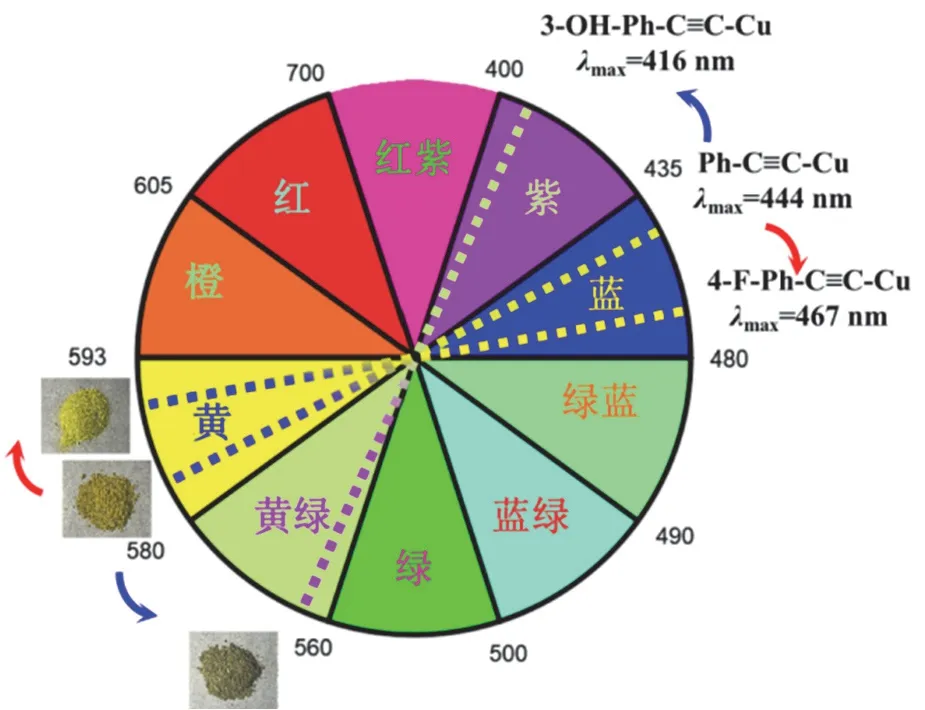
图5 Ph-C≡C-Cu基材料的本体颜色及互补可见颜色
2.2.2 亲疏水性
本实验通过测定所制备的Ph-C≡C-Cu基新型功能材料的稳定水接触角来表征其亲疏水性。如图6所示:3-OH-Ph-C≡C-Cu的稳定水接触角为70° (图6A),Ph-C≡C-Cu的稳定水接触角为137° (图6B),4-F-Ph-C≡C-Cu的稳定水接触角为160° (图6C)。其中,3-OH-Ph-C≡C-Cu为亲水性材料,Ph-C≡C-Cu和4-F-Ph-C≡C-Cu为疏水性材料。这是由于—OH为亲水性基团,—F为疏水性基团的缘故。该实验加强了同学们对界面现象的认识,了解并掌握了接触角的测试原理和测试方法。

图6 Ph-C≡C-Cu基材料的稳定水接触角
2.3 性能表征
2.3.1 标准曲线的建立
分别配制2 mg·L-1、4 mg·L-1、6 mg·L-1、8 mg·L-1、10 mg·L-1、12 mg·L-1的MO溶液,在λ= 463 nm(MO的λmax)处测其吸收值,可得MO在该波长处的吸收值和浓度之间的关系,如图7所示。
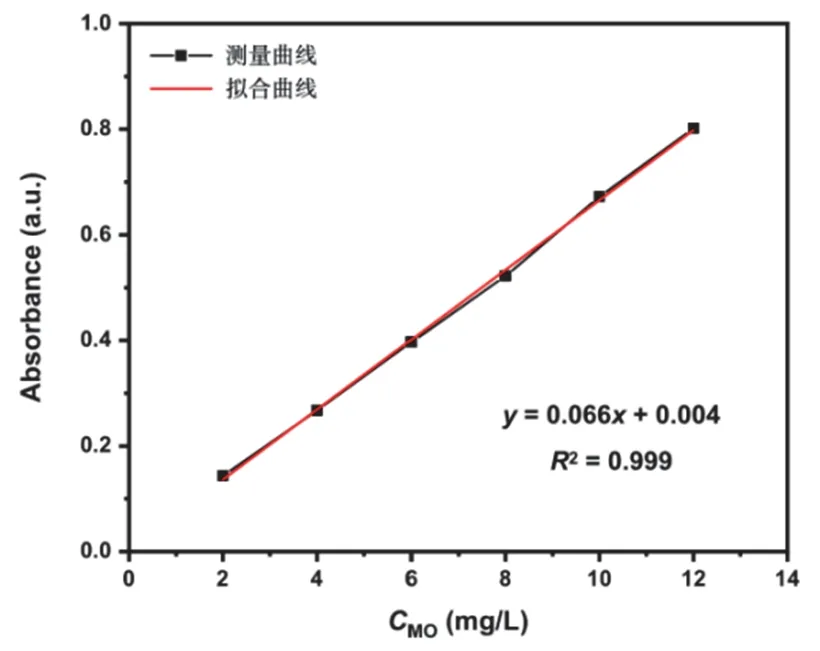
图7 MO在463 nm处的吸收值-浓度的标准曲线
2.3.2 吸附性能及其反应动力学
不同Ph-C≡C-Cu基材料对MO的吸附过程如图8所示。由图可知:3-OH-Ph-C≡C-Cu亲水性更好,更利于分散在水中与染料分子接触,因此对MO的吸附量最大,其饱和吸附量为171.7 mg·g-1。而Ph-C≡C-Cu和4-F-Ph-C≡C-Cu对MO的饱和吸附量分别为9.3 mg·g-1和3.2 mg·g-1。这与其亲水性顺序一致,说明材料的亲水性是影响MO吸附的主要因素。
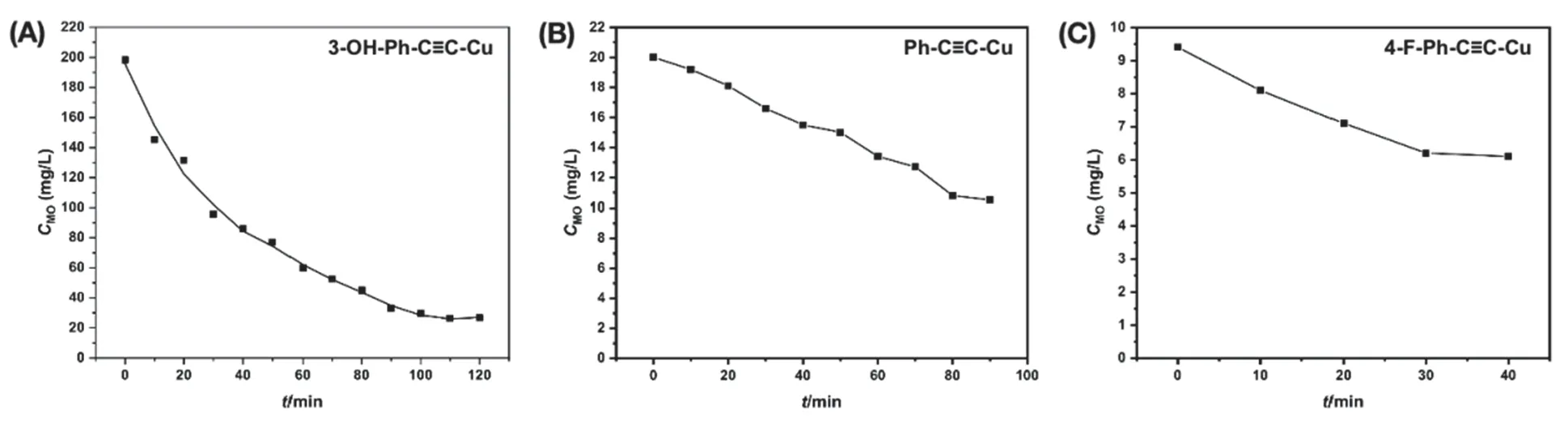
图8 不同Ph-C≡C-Cu基材料吸附MO实验:MO的浓度-时间曲线
我们对饱和吸附量最大的3-OH-Ph-C≡C-Cu吸附过程的动力学进行分析,通过不同反应级数的动力学方程对其吸附量-时间曲线进行拟合[15],根据拟合结果中所得k值的R2(拟合优度)来判断其反应级数。R2越接近1,说明拟合曲线越接近真实曲线。如图9所示,3-OH-Ph-C≡C-Cu对MO的吸附过程最接近一级反应。
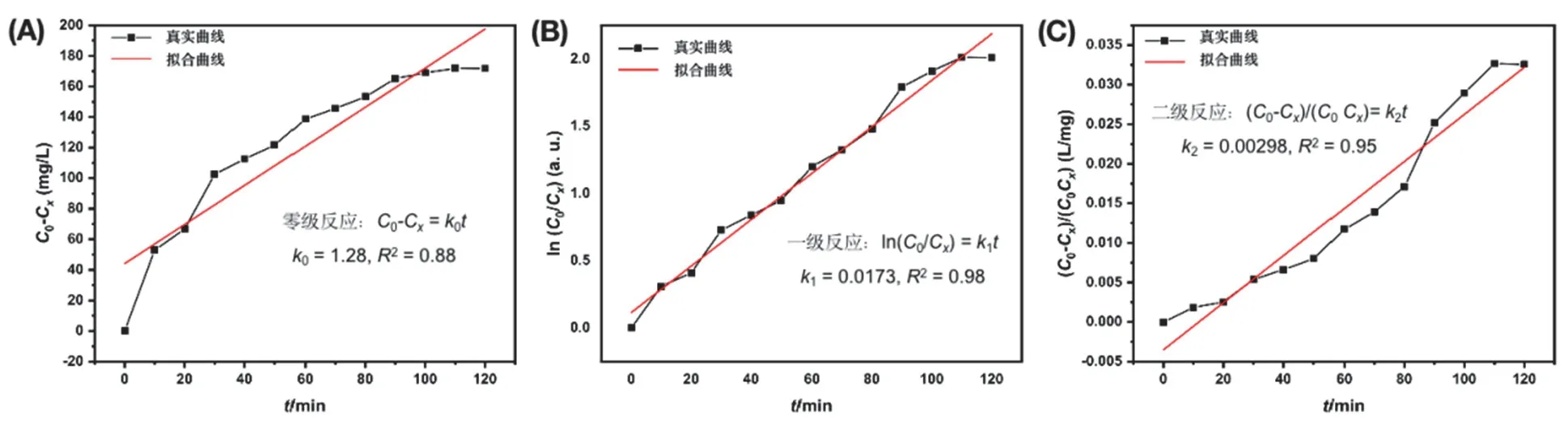
图9 3-OH-Ph-C≡C-Cu吸附MO的动力学过程:不同反应级数的拟合曲线
图中:C0为初始浓度,Cx为剩余浓度,单位为mg·L-1;t为反应时间,单位为min (分钟)。
2.3.3 光催化性能及其反应动力学
吸附平衡后,用全光谱氙灯对上述混合液进行光照,并检测不同时间、溶液中MO的浓度。不同Ph-C≡C-Cu基材料对MO的光催化降解过程如图10所示。由图10可知:MO降解速率最快、降解效率最高的是3-OH-Ph-C≡C-Cu,其次为Ph-C≡C-Cu,最后为4-F-Ph-C≡C-Cu。该顺序与其饱和吸附量和亲水性一致。说明材料的亲水性能够通过对水溶性染料分子MO的吸附的影响,来进一步影响其光催化降解效果。
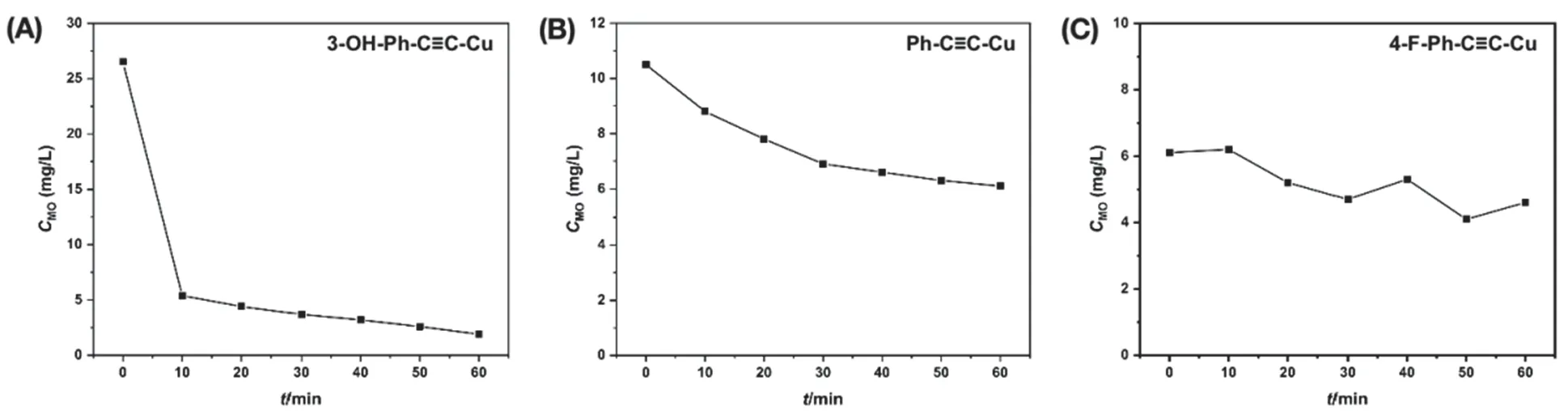
图10 不同Ph-C≡C-Cu基材料光催化降解MO实验:MO的浓度-时间曲线
实验结果表明:光催化降解效率最高的是3-OH-Ph-C≡C-Cu,其次为Ph-C≡C-Cu,最后为4-F-Ph-C≡C-Cu。该顺序与其亲水性和饱和吸附量一致。说明材料的亲水性能够通过对水溶性染料分子MO的吸附来影响其光催化降解效果。同样,我们对效果最好的3-OH-Ph-C≡C-Cu光催化降解MO过程的动力学进行拟合分析,结果如图11所示:3-OH-Ph-C≡C-Cu对MO的光催化降解过程也同样最接近一级反应。这进一步巩固了反应动力学中反应级数的相关概念,也能促进学生对光催化反应的了解和认识。
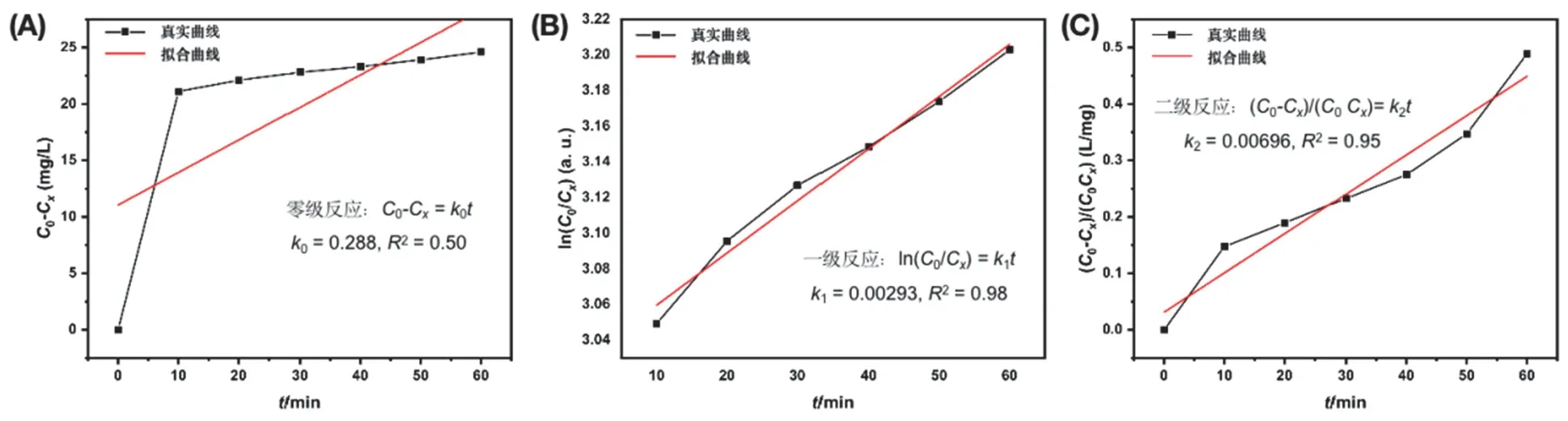
图11 3-OH-Ph-C≡C-Cu光催化降解MO的动力学过程:不同反应级数的拟合曲线
2.4 Ph-C≡C-Cu基新型功能材料的结构-性质-效能关系总结
(1) 当苯环上连接给电子基团(—OH)时,Ph-C≡C-Cu材料的λmax发生蓝移;当苯环上连接吸电子基团(—F)时,Ph-C≡C-Cu材料的λmax发生红移。
(2) 当苯环上连接亲水性基团(—OH)时,Ph-C≡C-Cu材料的稳定水接触角减小,亲水性增强;当苯环上连接疏水性基团(—F)时,Ph-C≡C-Cu材料的稳定水接触角增大,疏水性增强。
(3) Ph-C≡C-Cu基材料的亲水性越强,对水溶性染料MO的吸附越多。
(4) Ph-C≡C-Cu基材料对MO的吸附越强,光催化降解能力也越强;由于三种材料的λmax接近,因此对光催化降解能力影响不大。
3 思考与讨论
3.1 思考题
(1) 什么是亲水材料、疏水材料、超亲水材料、超疏水材料?各有什么应用前景?
(2) 如何设计Ph-C≡C-Cu的结构,能够增强其亲水性和疏水性?
(3) 针对光催化分解水和CO2还原反应,Ph-C≡C-Cu基光催化剂的结构应该如何设计?
3.2 拓展实验
(1) 3-OH-Ph-C≡C-Cu吸附和光催化降解MO的最优条件探索(光源、温度、酸碱性环境、共存离子等)。
(2) 光催化降解MO的工业化应用和设计。
4 课程安排
本实验制备了三种不同官能团的Ph-C≡C-Cu基新型功能材料,使用多种表征手段表征了其结构和相关物理化学性质,探究其对甲基橙(MO)的吸附和降解性能,涉及物理化学、有机化学、无机化学以及仪器分析等多个学科的实验操作技能,因此建议以综合化学实验的形式在本科的高年级阶段开展。在实验过程中,建议以小组为单位开展实验:每四人为一组共同合作完成,教学时间建议共计10小时,表4是我们给出的教学时间安排建议:

表4 教学时间建议
5 注意事项
在本实验的操作过程中,请注意全程佩戴手套和口罩;制备样品的过程中,由于苯乙炔具有一定挥发性和毒性,请注意全程在通风橱中进行;使用氙灯时,请佩戴好墨镜以防灼伤双眼。
6 实验效果
在传统的实验教学中,我们往往会拿到一个结构已知、性质确定的化合物,并对其性质和效能进行验证,即一种从结构到性质到效能的“自上而下”的教学模式;而在实际的生产生活中,我们往往需要跟据实际的需要,对材料的结构进行设计,即一种从效能反推性质、再到结构设计的“自下而上”的思维模式。这种思维方式无论在科研实践还是日常生产生活中都是非常必要的,同时,也是我们的学生最缺乏、最不擅长的。事实上,在实际生产生活中,我们往往需要根据实际需求对材料及其结构进行筛选和设计。比如:我们需要寻找一种能够高效去除水溶性污染物的材料,那我们首先推测它需要具有良好的亲水性,然后对其结构进行修饰,使其同时具备亲水性和高效去除水溶性污染物的性能。因此,我们通过设置思考题,启发学生进行“自下而上”的思考。该实验的设置能很好地启发学生“自下而上”的思维模式,在实验的过程,我们也看到了更多同学有了根据实际生活需要思考所需结构的意识。
该实验所需的实验仪器及实验药品都较为廉价和易于获得,教学成本较低;以一次实验32人计算,共计八组,每人每次的实验成本约为10元。本实验已被本校高年级学生反复实验验证,表现出较好的重复性和易于操作性。
7 结语
本论文以Ph-C≡C-Cu基新型功能材料为研究对象,通过研究和讨论苯环上官能团对其物理化学性质的影响,总结出基于官能团修饰的Ph-C≡C-Cu基新型功能材料的结构-性质-效能关系。该实验融合了有机化学中不同官能团的电子效应、物理化学中液-固界面相互作用、固体在溶液中的吸附、催化反应动力学以及反应级数的判定等化学基础知识,教会学生综合运用不同学科的基础知识。基于传统“自上而下”的教学模式,本文通过思考题和拓展实验的设计,启发学生立足于已掌握的基础知识,从实际需求出发,有针对性地对材料的结构进行设计,不仅锻炼了学生的实验操作技能,还培养了学生“自下而上”的逆向思维模式,提升了学生的思维品质,能够很好地实现综合化学实验的教学和育人目标。
