MoSe2/Co-MOF/NF复合材料的制备及电催化产氧性能
2024-01-20商文静王炳昊田翌钦娄永兵陈金喜
商文静 邓 鑫 王炳昊 田翌钦 李 香 娄永兵 陈金喜
(东南大学化学化工学院,南京 211189)
0 引 言
化石燃料在使用过程中会对环境造成较大的污染,产生许多严重的环境问题,因此,寻找一种高效清洁的可代替能源已经成为目前社会发展的重大任务之一[1-3]。由于其环境友好性和高能量密度等优点,氢能源正在逐渐走进人们的视野[4-6],如何通过绿色清洁的方法获取氢是开发利用过程中的一大难题。电解水制氢因为其高效无污染的优点目前被认为是生产高纯度氢的方法之一[7]。但是作为电解水的半反应之一的析氧反应(OER)涉及了4电子过程,其反应速率缓慢,需要较高的过电位来克服反应势垒,因此极大地限制了电解水的效率[8-9]。催化剂的使用则可以降低反应的势垒,从而促进OER 过程的发生。目前比较优异的催化剂主要是IrO2和RuO2等贵金属基催化剂,但是其生产成本较高,不适合广泛的使用。因此,迫切需要寻找廉价高效的OER电催化剂[10-11]。
金属有机骨架(MOFs)由于其结构可调、孔径大、比表面积大等特点受到了广泛的关注[12-13]。但是,部分MOFs 不能直接作为催化剂,这主要是因为它们存在着导电率低、稳定性差等缺点。目前常见的方法主要是将MOFs 作为前驱体进行热解、磷化等后处理,但是这些后处理经常会使MOFs 丧失自身原始的优点。构建MOFs 复合材料作为催化剂是一种非常有效的方法[14],复合材料不仅可以继承MOFs原始的结构特征,还可以通过与另一材料复合来改善MOFs 导电性差的缺点。例如,姜炜团队在Ni2S3表面成功生长了MIL-53,复合材料Ni3S2/MIL-53(Fe)在碱性溶液中展现出优异的OER活性[15]。
过渡金属化合物作为高效的OER 电催化剂在电解水方面表现出了优异的性能[16]。在各种过渡金属化合物中,金属硒化物(TMSe)不仅具有丰富的电子态,还在结构和功能上表现出优异的灵活性和可调节性,因此被认为是理想的催化剂之一[17-18]。更重要的是,硒(Se)是一种独特的候选元素,可以与复合材料中的许多元素结合,并以Se—P、Se—C、Se—O和Se—M 键(M 表示金属)的形式存在。由于其半金属性质,硒的引入通常可以使材料展现出令人满意的导电性[19]。但是在合成过程中,TMSe 往往会发生严重的堆积,导致部分活性位点被包裹在内部而无法发挥催化作用[20-21]。更糟糕的是,由于没有导电基体的支持,粉末状的TMSe 催化性能受到了很大影响[22]。若使用黏结剂将其涂覆在导电基底上,则会堵塞电荷转移的通道,对电荷的转移形成阻碍。目前常用的解决方法是通过将生长在导电基底上的前驱体进行硒化来获得TMSe。例如,王得丽团队通过硒化NiFe-PBA 前驱体得到了Ni-Fe-Se1∶1-180,该材料在碱性溶液中展现出较好的OER活性[17]。
将MOFs 与TMSe 结合,可以改善MOFs 导电性差的缺点,同时也可以解决TMSe 团聚严重的问题。基于以上的考虑,本研究提出了一种将Co基金属有机骨架(Co-MOF)与MoSe2复合的策略。在导电基底泡沫镍(NF)上自生长出Co-MOF,MoSe2分散在MOF的表面,将二者复合到一起。本工作不仅可以很好地保持MOFs和MoSe2自身的优势,还可以通过二者的复合改善它们各自的缺点。除此之外,将NF 直接作为材料的生长基底,可以避免黏结剂的使用而产生的“额外电阻”问题,并且催化材料与底物结合得更紧密,这有助于材料的均匀分布和电荷的快速转移。
1 实验部分
1.1 实验材料
六水合硝酸钴、硒粉、水合肼、氢氧化钠、二氧化钌、氢氧化钾均购于上海阿拉丁生化科技股份有限公司;二水合钼酸钠、盐酸、N,N-二甲基甲酰胺、配体4,4′-联苯二甲酸(H2BPDC)、无水乙醇均购于国药集团化学试剂有限公司;NF、去离子水购于南京晶格科技有限公司。以上药品均为分析纯,并且未经过进一步纯化,直接进行使用。
1.2 材料的合成
1.2.1 NF的清洗
由于NF 表面存在着污垢和氧化层,因此在使用之前要进行清洗。将购买的NF 裁剪为1 cm×1.5 cm 的规格,然后将其浸入到提前准备好的3 mol·L-1的盐酸溶液中,使用超声清洗器清洗20 min。紧接着再用去离子水和无水乙醇分别超声清洗10 min,将清洗后的NF放置在真空干燥箱中干燥。
1.2.2 MoSe2的制备
首先将160 mg 的硒粉加入到5 mL 的水合肼溶剂中,搅拌30 min后得到深红棕色的混合液A;接着再将240 mg二水合钼酸钠加入到25 mL的去离子水中,同样也搅拌30 min 得到透明混合液B。然后将混合液A 加入到混合液B 中搅拌1 h,二者混合均匀后转移至聚四氟乙烯内衬中,在200 ℃的条件下反应4 h。待反应釜冷却至室温之后,用去离子水和无水乙醇多次洗涤,得到黑色的产物MoSe2。
1.2.3 MoSe2/Co-MOF/NF的制备
将242.2 mg 的H2BPDC、32 mg 的氢氧化钠、290 mg 的六水合硝酸钴依次加入到20 mL 的N,N-二甲基甲酰胺中,搅拌10 min 之后形成了粉紫色混合液。将50 mg 的MoSe2加入到混合液中并搅拌45 min,紧接着再将提前清洗过的NF 浸入到混合液中。将混合液转移到聚四氟乙烯内衬中,在100 ℃温度下反应15 h。待降至室温时,取出负载着复合材料的NF,并用N,N-二甲基甲酰胺和无水乙醇清洗数次去除表面物质。
1.3 材料的结构表征
采用X 射线衍射仪(XRD,Ultima ⅣX,CuKα作为辐射源(λ=0.154 06 nm),2θ范围5°~80°,最小可控步长0.000 1°,工作电压40 kV,工作电流40 mA)分析材料的物相组成。使用扫描电子显微镜(SEM,Navo Nano SEM450,加速电压15 kV)和透射电子显微镜(TEM,Talos F200X G2,加速电压200 kV)观察材料的形貌结构及晶体学信息。通过X射线光电子能谱仪(XPS,Therno Scientific K-Alpha,AlKα作为射线源)详细分析了样品的元素组成与状态。
1.4 电化学性能测试
所有的电化学测试均在上海辰华仪器有限公司生产的电化学工作站(CHI660D)进行。测试过程中,铂片电极(1 cm×1 cm)作为对电极,银/氯化银电极(饱和氯化钾作为填充液)为参比电极,面积为1 cm2的负载着复合材料的NF 作为工作电极。所有测试的电压值均被转化为可逆氢电极电位,公式为ERHE=EAg/AgCl+0.059pH+0.197,其中ERHE代表可逆氢电极电位,EAg/AgCl代表标准银/氯化银电极的电极电势,pH 数值是指测试时配制的浓度为1 mol·L-1KOH 溶液的pH。在扫描速度为5 mV·s-1的条件下得到线性扫描伏安(LSV)曲线。为了得到更加稳定可靠的数据,在获得LSV 曲线前工作电极都经过了活化,并且所有的极化曲线均进行了90%的IR补偿。在非法拉第区域内(1.00~1.13 V)使用不同扫描速度(40、50、60、70、80、90、100、110和120 mV·s-1)收集循环伏安(CV)曲线。在开路电压的条件下测试了电化学阻抗谱(EIS),并利用软件ZView 对其进行分析拟合。
2 结果与讨论
2.1 结构与形貌表征
材料的合成过程如图1 所示,首先合成MoSe2,之后再通过水热法将其与Co-MOF 复合。使用XRD对材料的晶体结构进行了表征。从图2中可以观察到,复合材料的XRD 图中除了明显的Co-MOF 的衍射峰外[23],在2θ为33.1°和55.3°处也出现了宽展的衍射峰,这些衍射峰分别可以归属于1T-2H 相的MoSe2[24]。这说明了2 种物质的成功复合,并且MoSe2的引入并没有影响原始的Co-MOF 的晶体结构。为了进一步确定材料的结构与组成,使用SEM和TEM 表征了材料的形貌。从SEM 图中可以清楚的观察到材料的形貌,Co-MOF 主要是由薄片组成的花状物质,而MoSe2则是纳米片堆积形成的蓬松团簇状物质(图3a和3b)。这种薄片结构可以使得活性位点充分地暴露在外面,催化剂与底物之间更直接紧密地接触,从而提高催化剂的活性。经过复合之后,在复合材料MoSe2/Co-MOF/NF 的SEM 图上可以清楚地看到团簇分布在花状结构表面,这说明了MoSe2与Co-MOF 成功地复合在一起,并且2 种物质的形貌在复合前后没有发生明显的改变(图3c 和3d)。除此之外,通过图4a 的TEM 图也可以清楚地观察到MoSe2与Co-MOF 的复合界面。高倍透射电镜(HRTEM)可以观察到明显的晶格条纹,其中的间距为0.284 nm 的晶格条纹可以归属到MoSe2的(101)晶面(图4b)。并且根据相应的元素映射图可以观察到C、O、Co、Mo、Se 均匀分布在复合材料中(图4c~4h)。以上证据都证明了Co-MOF 与MoSe2的成功复合,总之,这些表征均说明了通过水热法将二者复合的策略是可行的。

图1 MoSe2/Co-MOF/NF的合成示意图Fig.1 Synthesis process of MoSe2/Co-MOF/NF
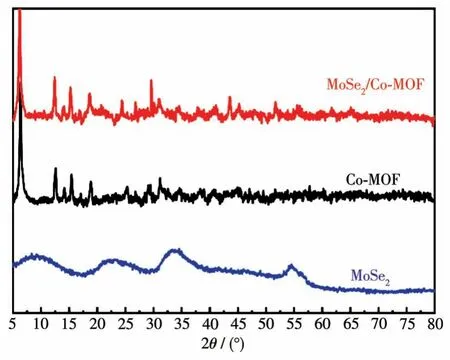
图2 Co-MOF、MoSe2和MoSe2/Co-MOF的XRD图Fig.2 XRD patterns of Co-MOF,MoSe2,and MoSe2/Co-MOF

图3 (a)Co-MOF、(b)MoSe2和(c,d)MoSe2/Co-MOF/NF的SEM图Fig.3 SEM images of(a)Co-MOF,(b)MoSe2,and(c,d)MoSe2/Co-MOF/NF
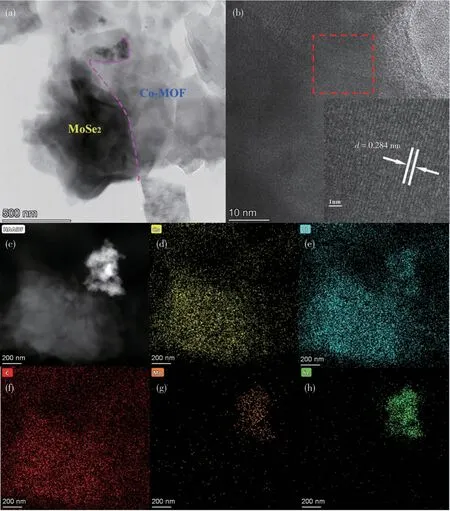
图4 MoSe2/Co-MOF/NF的(a)TEM图、(b)HRTEM图和(c~h)元素映射图Fig.4 (a)TEM image,(b)HRTEM image,and(c-h)element mapping images of MoSe2/Co-MOF/NF
2.2 XPS分析
为了研究材料表面化学价态和电子的相互作用,通过XPS 手段对材料复合前后元素的价态进行了分析(图5)。在Co-MOF/NF 样品中Co2p的XPS 图谱可以观察到6 个明显的峰,其中在803.21 和786.37 eV 处是卫星峰,799.58 和782.71 eV 处的峰对应Co3+,位于796.21和780.42 eV 的峰属于Co2+,这说明Co 主要是以+2 价和+3 价的形式存在于Co-MOF/NF 中[25-26]。MoSe2中Mo3d的光谱图可拟合为2个峰,229.69 和232.79 eV 处的峰分别对应于Mo3d5/2和Mo3d3/2,这说明MoSe2中的Mo 元素主要是由Mo4+的形式存在[27]。值得注意的是,在复合之后Co2p和Mo3d发生了趋势相反的移动,Mo3d谱图中的2个峰都移向了更低的结合能,Co2p峰则移向了更高的结合能。这说明在Co 与Mo 之间存在强烈的相互作用,部分电荷从Co 移向了Mo,调节了Co 的电子分布,Co 中心的电子云密度降低使其展现出更高的价态。据报道,高价态的Co通常被认为是催化的活性中心,该材料中相对高的氧化态更易转化为高价态的Co[28-29],因此该复合策略对于提高催化剂活性是十分有效的。
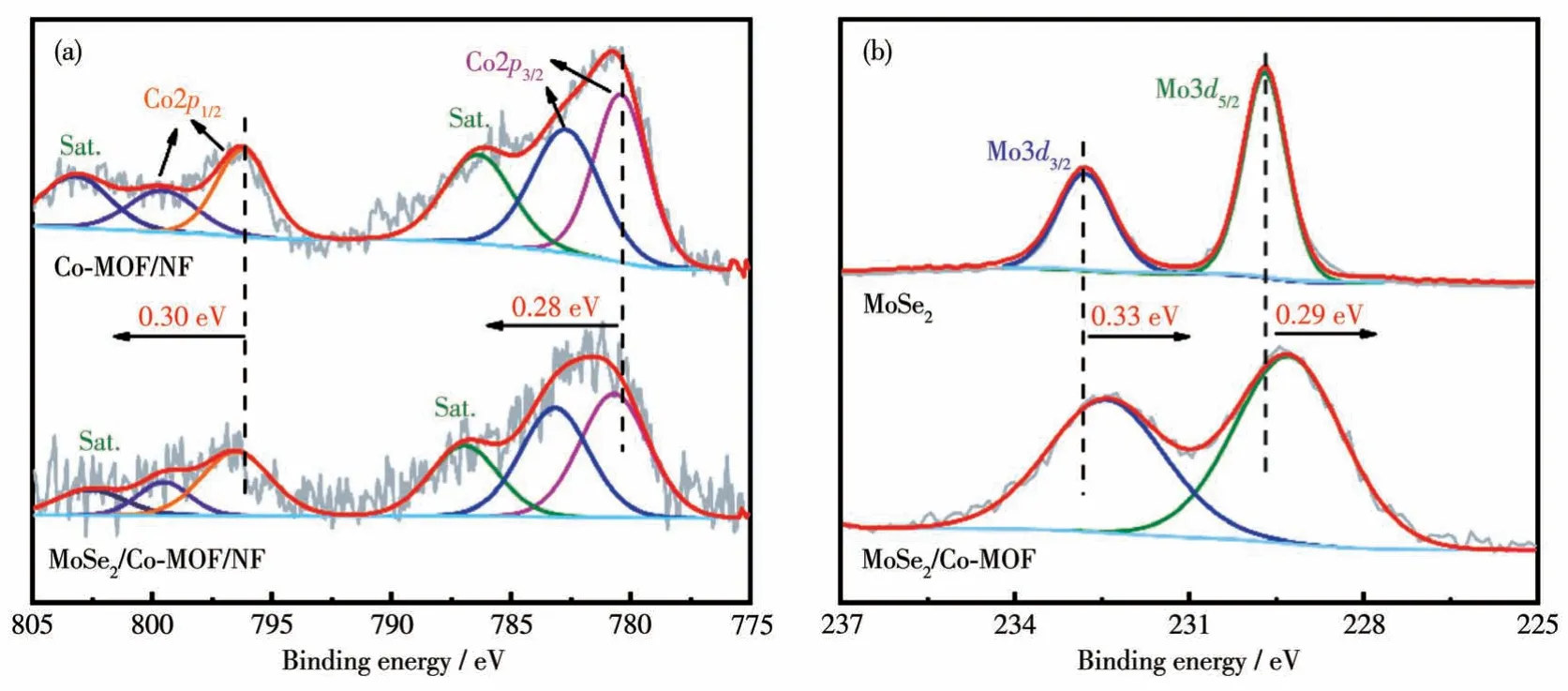
图5 Co-MOF和MoSe2/Co-MOF/NF的XPS谱图:(a)Co2p、(b)Mo3dFig.5 XPS spectra of Co-MOF and MoSe2/Co-MOF/NF:(a)Co2p,(b)Mo3d
2.3 电化学性能分析
在配制的浓度为1 mol·L-1(pH=13.6)的氢氧化钾溶液中采用三电极体系对材料的电化学性能进行评估。为了避免氧化峰对评估材料电催化性能的影响,本工作均使用反扫(从高电压到低电压)的方法在电压范围为1.8~1.0 V(vs RHE)内收集LSV 曲线[26]。在电流密度为10 mA·cm-2时,其过电位仅为242 mV,甚至还可以与贵金属RuO2相媲美(240 mV)。为了揭示复合作用对OER 动力学的影响,还得到了由LSV 曲线导出的塔菲尔斜率。它与反应动力学密切相关,其数值越小,则说明反应速率越快,因此在这里通过比较塔菲尔斜率数值的大小来评价反应的动力学。如图6b 所示,MoSe2/Co-MOF/NF 在合成的所有催化剂中有着最小的塔菲尔斜率(50.64 mV·dec-1),表明其在OER 过程中具有快的反应速率。除了反应动力学外,还利用EIS 对电荷转移能力进行了评价。半圆的大小与电子转移的快慢成反比,在图6c中可以观察到,MoSe2/Co-MOF/NF的半圆比其他催化剂小得多,这意味着复合物的电子转移速度更快,有助于提高材料的电催化活性。考虑到电化学活性表面积(ECSA)与双电层电容(Cdl)呈正相关,因此在这里通过比较Cdl的大小来评价ECSA[30]。催化剂的Cdl通过在非法拉第区收集CV曲线(图7)来进行计算,绘制1.06 V 时的ΔJ/v直线(其中ΔJ=Ja-Jc,Ja代表阳极电流数值,Jc代表阴极电流数值,ΔJ则代表了阳极电流和阴极电流之间的差值,v为扫描速率),直线斜率的1/2 即为Cdl的数值。通过图6d中可以看到,MoSe2/Co-MOF/NF(11.30 mF·cm-2)作为电催化剂具有比Co-MOF/NF(9.15 mF·cm-2)和MoSe2/NF(7.00 mF·cm-2)更大的ECSA。更大的ECSA 有助于更多的活性位点暴露,从而使催化剂展现出更优异的催化活性,这与前面讨论的LSV、塔菲尔斜率和EIS 的趋势是一致的。为了更好地证明本策略的有效性,将合成的催化剂与其他Co-MOFs 衍生物催化剂的性能做了对比,如图8 所示,该催化剂在这些材料中表现出了较高的活性[31-37]。这些结果均表明,将MoSe2与Co-MOF 复合可以显著提高OER 活性。这可能是因为当MoSe2加入之后,Se 元素的半金属性质使得复合材料的导电性大大提高,并且薄片花状的Co-MOF 可以很好地暴露活性位点和分散MoSe2。除此之外,MoSe2与Co-MOF 之间存在着强烈的相互作用,使Co 展现出较高的氧化态,有助于提高催化剂的OER活性。
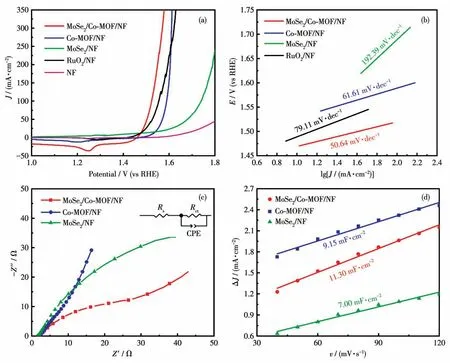
图6 催化剂的(a)LSV曲线、(b)塔菲尔斜率、(c)EIS曲线(插图为等效电路图)、(d)CdlFig.6 (a)LSV curves,(b)Tafel slopes,(c)EIS plots(Inset:the equivalent circuit diagram),(d)Cdl of the catalysts
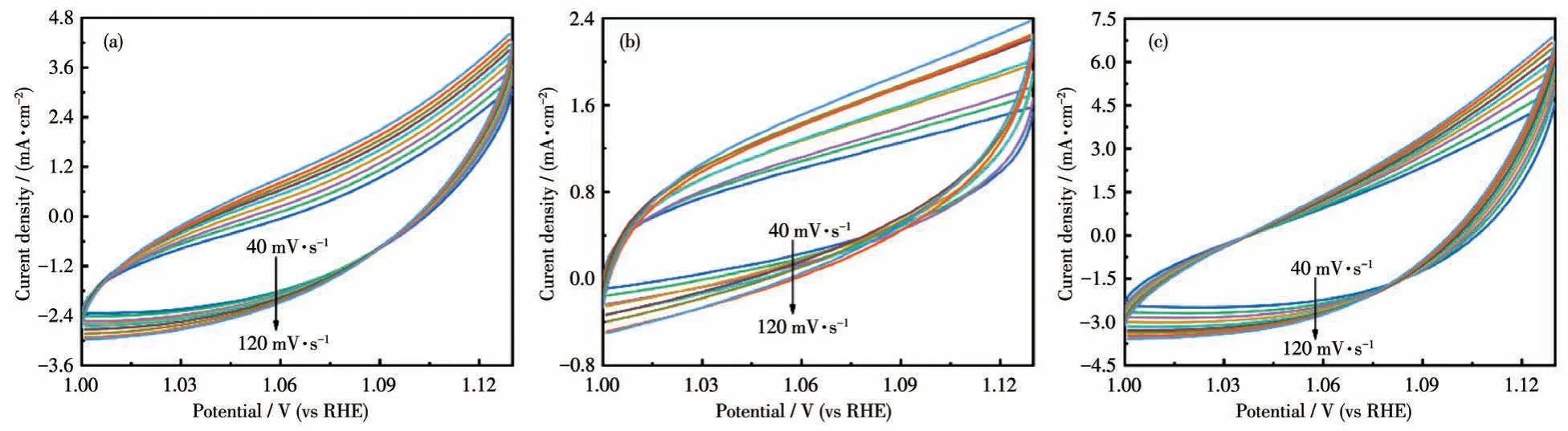
图7 (a)Co-MOF/NF、(b)MoSe2/NF和(c)MoSe2/Co-MOF/NF的CV曲线Fig.7 CV curves of(a)Co-MOF/NF,(b)MoSe2/NF,and(c)MoSe2/Co-MOF/NF
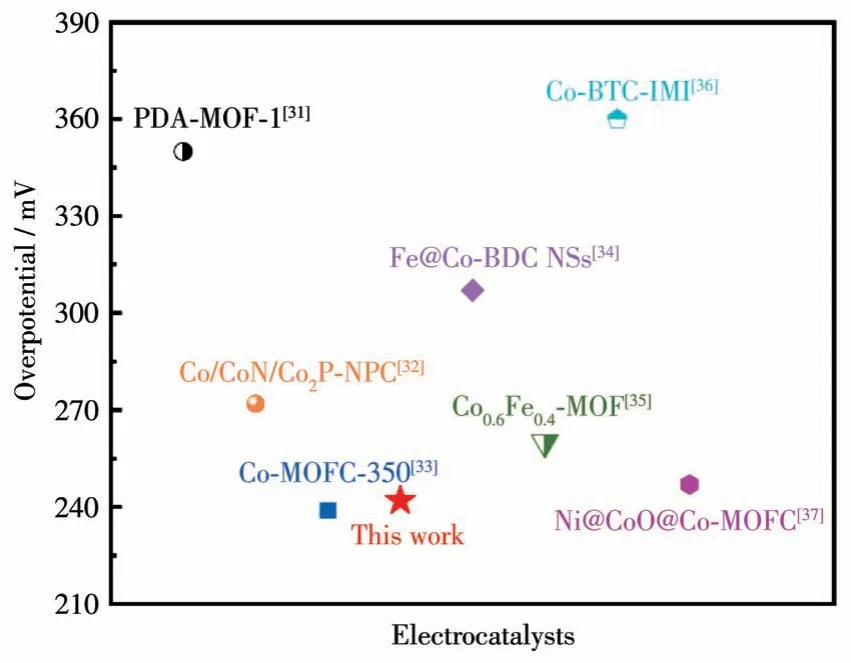
图8 不同电催化剂在电流密度为10 mA·cm-2时的过电位比较Fig.8 Comparison of overpotentials of different electrocatalysts at the current density of 10 mA·cm-2
除了优异的电化学活性外,稳定性也是评价催化剂性能至关重要的指标。为了评价该材料的稳定性,使用计时电位法进行了30 h 的稳定性测试,如图9a 所示,MoSe2/Co-MOF/NF 在施加恒定电压30 h 的测试中表现出较强的耐久性。除此之外,还收集1 000 圈CV 循环前后的LSV 曲线,2 条曲线之间的差别几乎可以忽略,甚至可以重合在一起,这些均证明了这种电催化剂具有良好的稳定性(图9b)。
为了进一步证明该材料的稳定性,将经过30 h测试之后的电极样品进行了XRD 测试。在XRD 图上可以明显观察到Co-MOF 的衍射峰,衍射峰的强度略有降低(图10a),这可能是测试过程中碱液腐蚀和O2快速释放对形貌的部分损坏导致的。但是并没有观察到明显MoSe2的存在,可能是由于NF 的衍射峰过强,而MoSe2的结晶度很弱,因此没有观察它的衍射峰。为了进一步确定其组成,使用SEM 观察了样品的形貌。可以观察到花状的Co-MOF 和团簇状的MoSe2,材料的结构大部分未发生明显改变,说明其稳定性良好(图10b)。但是与未反应的样品的SEM 图对比发现,花状结构变得不再整齐,花瓣的边缘也发生一定程度的破碎。

图10 测试了30 h后MoSe2/Co-MOF/NF的(a)XRD图和(b)SEM图Fig.10 (a)XRD spectra and(b)SEM image of MoSe2/Co-MOF/NF after 30 h of stability
3 结 论
本研究通过简便的溶剂热的方法合成了复合材料MoSe2/Co-MOF/NF。研究表明该催化剂具有较高的OER 活性,在10 mA·cm-2时过电位仅为242 mV,塔菲尔斜率为50.64 mV·dec-1。该催化剂展现的OER 活性不仅优于MoSe2和Co-MOF 单体,甚至超过了贵金属催化剂RuO2。这主要是因为本研究在不破坏Co-MOF 自身结构特点的前提下,将MoSe2与Co-MOF 成功复合在一起。MoSe2的引入弥补了Co-MOF 导电性差的缺点,同时Mo与Co之间的相互作用可以有效调节金属中心的电荷分布,使Co展示出较高的氧化态,这有助于提高催化剂的OER 活性。除此之外,MoSe2在Co-MOF 表面分散,避免了团聚现象的发生,增大了ECSA,暴露出了更多的活性位点。本研究结合了MOFs 与TMSe 各自优点,同时又弥补了它们的缺点,为开发高效的电催化剂提供了一条有用的策略。
