UPLC-MS/MS法同时测定蛋白饮料和液体调味品中36种防腐剂
2024-01-18魏宇涛温泉唐维英黄璐瑶余晓琴杜钢李澍才李航
魏宇涛,温泉,唐维英,黄璐瑶,余晓琴,杜钢,李澍才*,李航*
1(四川省食品检验研究院,四川 成都,611731)2(国家市场监管重点实验室(白酒监管技术),四川 成都,611731) 3(四川省药品检验研究院,四川 成都,611731)
随着人们生活水平的不断提高,消费者对食品品质有了更高的要求,越来越关注食品中防腐剂的使用,尤其是一些宣称“绿色”、“零添加”或者“纯天然”等食品更是深得广大消费者喜爱[1]。防腐剂作为食品生产加工过程中常用的添加剂,其广泛用于食品、药品、生物标本等方面[2-5],但是一些不法生产者为谋取利益非法滥用和虚假宣传,对人体健康构成潜在危害[6]。
蛋白饮料、液体调味品是人们日常生活中不可或缺的食品,其由于含有大量的蛋白质、水体基质,更容易滋生细菌引起腐败变质。在GB 2760—2014《食品安全国家标准 食品添加剂使用标准》中列入可使用的防腐剂大约有30多种,而日常监督抽检中的项目不到10种。目前针对防腐剂的高通量检测技术研究,主要集中在药品方面[7-10]。而食品中相关研究较少且研究都是针对单一化合物或者多类添加剂,其检测的化合物和涉及的食品基质有限[6,11-15]。目前现有国家标准和方法针对防腐剂检测都存在目标化合物单一,前处理方法复杂等问题[11],缺乏能够同时检测多种防腐剂的技术方法,也没有将不允许在食品中使用的多种防腐剂纳入检测范围,尤其在监管此类“零添加”产品时,检测能力明显不足。因此急需建立一套防腐剂的高通量筛查技术,以解决此类产品的检测痛点问题,本文应用超高效液相色谱-串联质谱建立了能够同时检测蛋白饮料和液体调味品中36种防腐剂的方法,该方法灵敏、快速、准确度高且是现有文献报道中能同时检测最多种类防腐剂的方法,对加强食品中防腐剂的监测监管力度具有十分重要的意义。
1 材料与方法
1.1 仪器、试剂与材料
Agilent 1290 Infinity Ⅱ超高效液相色谱仪、Agilent 6495三重四极杆质谱仪,美国Agilent公司;X3R高速离心机,美国Thermo Fisher Scientific公司;IRMsci超声仪,德国IRM Technology GmbH公司;IKA MS3涡旋混合器,德国IKA公司。
甲酸、乙腈、甲醇、乙酸铵(均为色谱纯),美国Thermo Fisher Scientific公司;氨水、磷酸、NaCl(均为色谱纯),成都科隆化学品有限公司;实验用水为Milli-Q超纯水。
实验样品:醋、酱油、蛋白饮料、其他液体调味品[酱汁、料酒、调味汁(料)],市售或网购。
1.2 标准溶液
1.2.1 标准品
混合标准品1:苯甲酸、山梨酸、纳他霉素、脱氢乙酸、邻苯基苯酚混合标准储备液,质量浓度均为1 000 μg/mL,北京曼哈格生物科技有限公司。
混合标准品2:肉桂酸、4-氯-3,5-二甲基苯酚(对氯间二甲酚)混合标准储备液,质量浓度均为1 000 μg/mL,天津阿尔塔科技有限公司。
混合标准品3:4-羟基苯甲酸、三氯卡班、4-氯-3-甲基苯酚(对氯间甲酚)、苄氯酚、溴氯芬、4-羟基苯甲酸甲酯、4-羟基苯甲酸乙酯、4-羟基苯甲酸丙酯、4-羟基苯甲酸丁酯、4-羟基苯甲酸异丙酯、4-羟基苯甲酸异丁酯、2,4-二氯苯氧乙酸、苯氧乙酸、三氯生、水杨酸、2-溴-2-硝基-1,3丙二醇(布罗波尔)、甲基异噻唑啉酮、甲基氯异噻唑啉酮、碘丙炔醇丁基氨甲酸酯、氯咪巴唑、苄索氯铵、十四烷基二甲基苄基氯化铵、十六烷基二甲基苄基氯化铵、4-羟基苯甲酸戊酯、十二烷基二甲基苄基氯化铵、4-羟基苯甲酸苯酯、4-羟基苯甲酸苄酯、噻苯咪唑、月桂酰精氨酸乙酯盐酸盐混合标准储备液,质量浓度均为100 μg/mL,北京曼哈格生物科技有限公司。
1.2.2 标准溶液配制
标准溶液的配制:根据各防腐剂的质谱响应不同,配制各分析物不同浓度的混合标准溶液。分别准确吸取混合标准品1溶液0.025 mL、混合标准品2溶液0.01 mL以及混合标准品3溶液0.05 mL,置于同一10 mL容量瓶中,用甲醇稀释至刻度,摇匀后,作为混合标准工作溶液中间液。
1.3 样品分析检测
1.3.1 样品前处理
称取1 g混合均匀的样品(精确至0.001 g),置于50 mL离心管中(醋类样品先用体积分数为10%氨水调节pH至中性,与其他基质pH保持一致,防止pH变化使化合物保留时间发生变化)加入5 mL饱和NaCl溶液(用磷酸调节pH=3),涡旋混匀1 min使样品在饱和NaCl水溶液中充分分散,再准确加入20 mL乙腈-甲醇(9∶1,体积比)(含体积分数为0.2%甲酸)涡旋混匀5 min,超声提取15 min,置于高速离心机中9 000 r/min离心5 min,取上层有机相过0.22 μm滤膜,滤液用于液相色谱-串联质谱仪分析。
1.3.2 色谱条件
Agilent Eclipse Plus C18柱(150 mm×3.0 mm,1.8 μm);柱温35 ℃:进样量5 μL;流动相A为5 mmol/L乙酸铵,B为甲醇。流速0.3 mL/min;流动相梯度洗脱程序见表1。
1.3.3 质谱条件
离子源:电喷雾离子源(electrospray ionization, ESI);扫描方式:正、负离子扫描;检测方式动态多反应监测(dynamic multiple reaction monitoring,DMRM);毛细管电压3.0 kV;干燥气温度250 ℃;干燥气流量11 L/min;雾化气压力45 psi;鞘气温度300 ℃;鞘气流量11 L/min。

表1 流动相梯度洗脱程序Table 1 The gradient elution procedure ofmobile phase
2 结果与分析
2.1 实验条件的考察
2.1.1 仪器方法的建立和优化
实验中考察了ACQUITY UPLC BEH C18柱(100 mm×3.0 mm,1.7 μm)、ACE EXCEL C18柱(75 mm×2.1 mm,1.7 μm)、Hypersil GOLDC18柱(100 mm×3.0 mm,1.9 μm)和Agilent Eclipse Plus C18柱(150 mm×3.0 mm,1.8 μm)4种不同品牌色谱柱对36种防腐剂的分离情况,结合化合物峰形、分离度以及系统压力,最终选择Agilent Eclipse Plus C18柱(150 mm×3.0 mm,1.8 μm)。同时比较了甲醇-乙酸铵、甲醇-甲酸铵和乙腈-乙酸铵3种流动相体系对36种防腐剂的影响,结果表明甲醇-乙酸铵作为流动相时,系统压力较乙腈更低,目标分析物分离度和峰形相对较好,同时进一步优化了乙酸铵的浓度,最终选择甲醇-5 mmol/L乙酸铵作为流动相。选择采用ESI+和ESI-模式对36种防腐剂进行了一级质谱全扫描和子离子扫描分析,筛选出36种目标分析物的碎片离子。由于碎片离子较多,传统的多反应扫描模式可能会使目标分析物碎片离子的色谱峰采集点不够,影响峰形和质谱响应。采用DMRM能利用保留时间和保留时间窗口2个参数,可以实现对目标分析物进行精确扫描,保证定性定量的准确性。36种防腐剂总离子流图见图1。
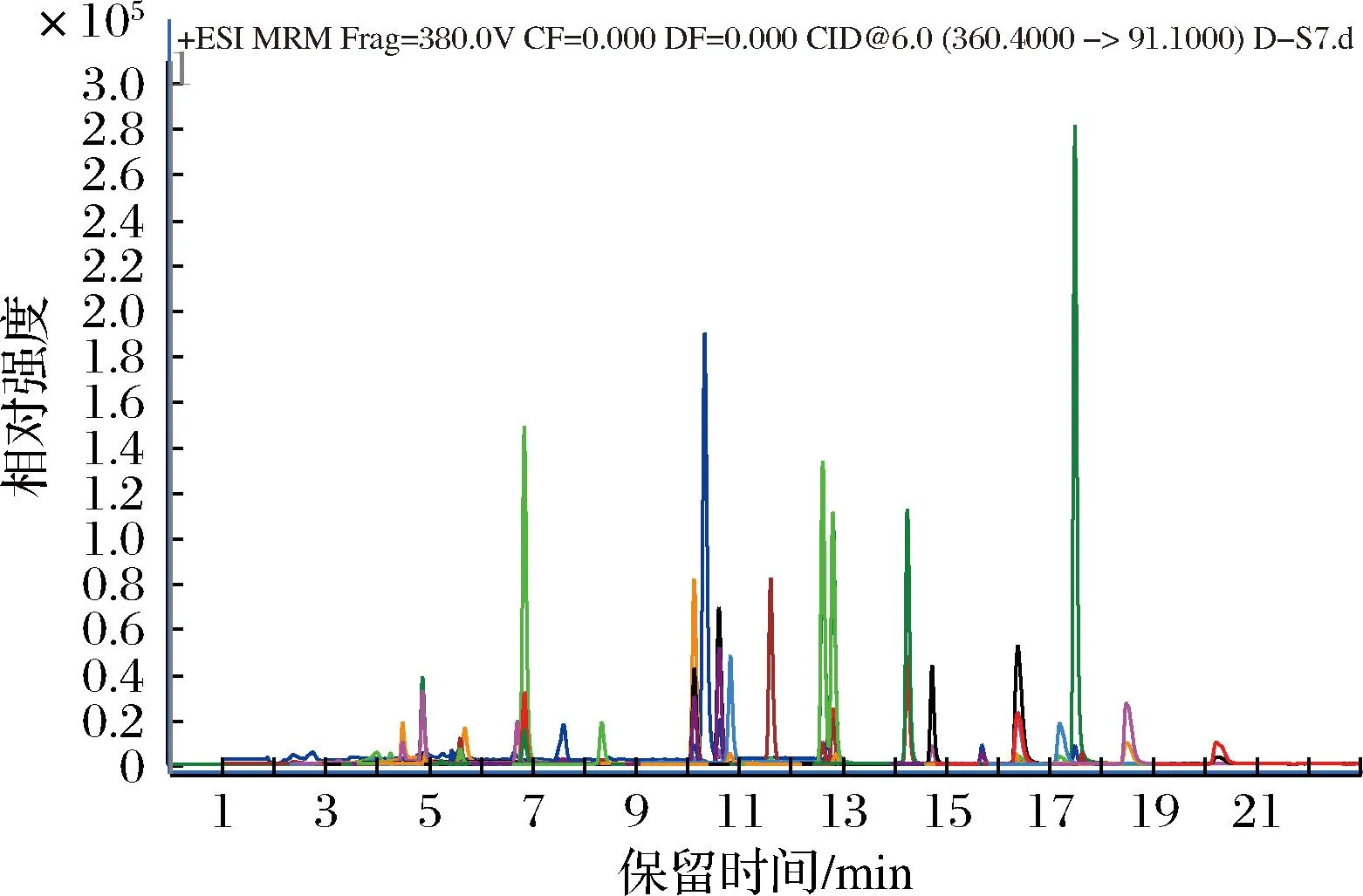
图1 36种防腐剂的总离子流图Fig.1 Total ion current diagram of 36 preservatives
2.1.2 基质效应(matrix effect, ME)考察
由于36种防腐剂化合物性质差异较大,大多为酸性化合物,还有两性化合物和弱碱性化合物,且基质之间性质也差异较大,本研究采用斜率法考察了化合物的ME,即ME=基质标准曲线斜率/溶剂标准曲线斜率。若ME=1,则表示不存在基质效应;ME>1,为增强效应;ME<1为抑制效应。由表2可知,不同样品基质中一些化合物的ME不一致,为了兼顾多种防腐剂同时检测,因此实验中采用基质标准曲线以抵消基质干扰、保证结果的准确性。
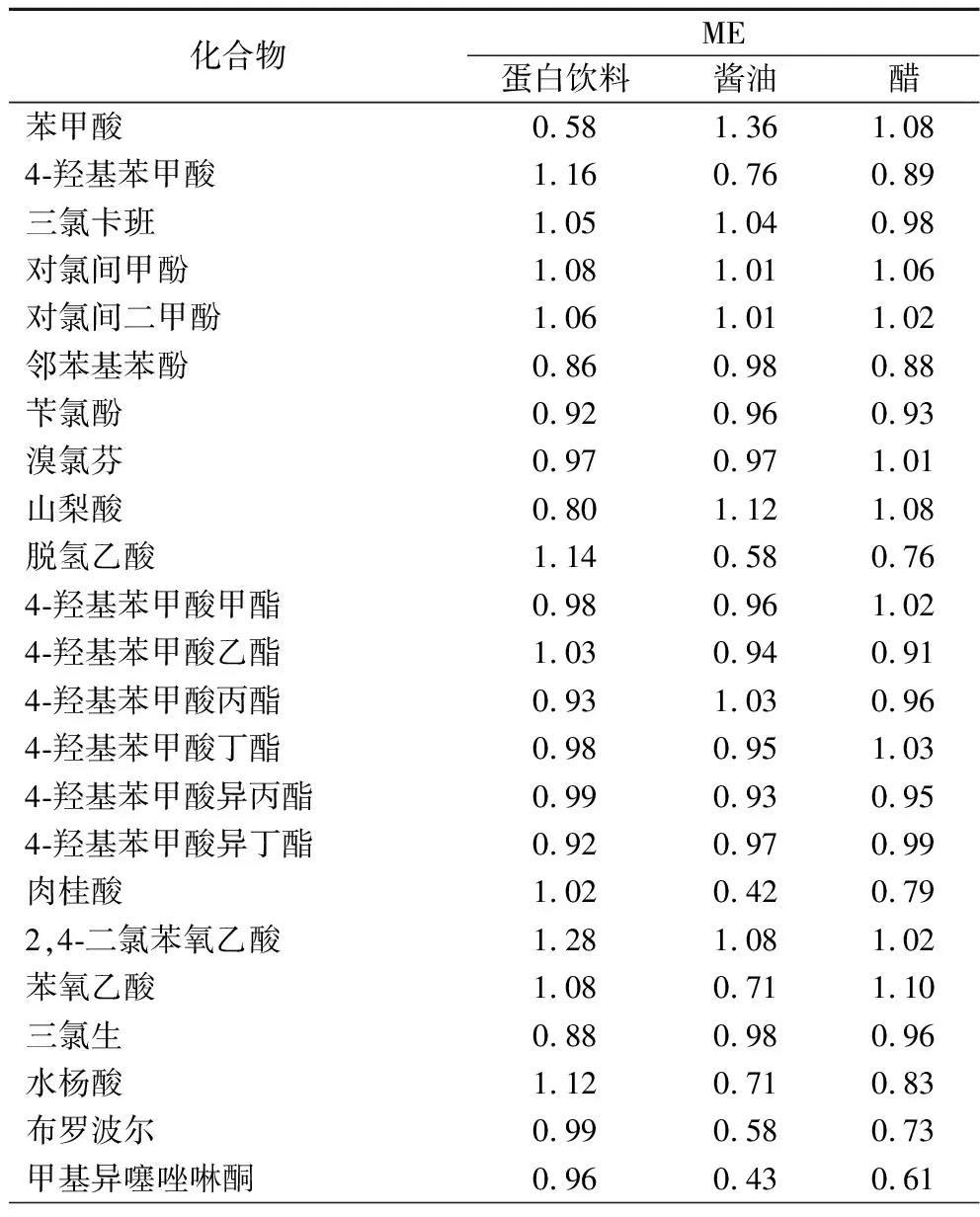
表2 不同样品基质中36种目标分析物的基质效应Table 2 The matrix effect of 36 compounds in different sample matrices
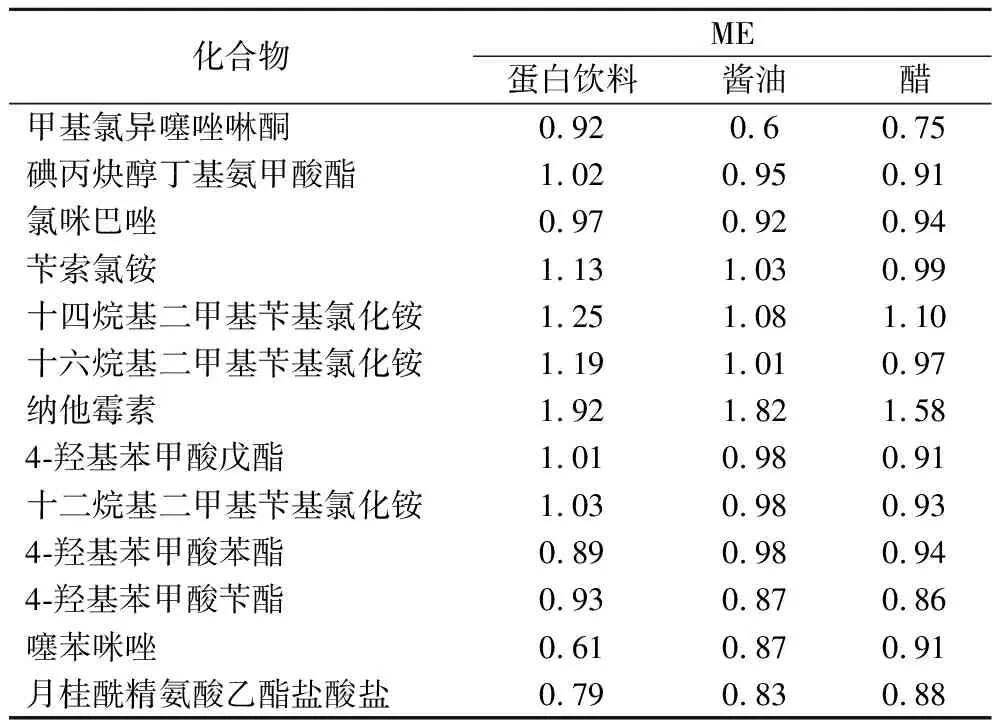
续表2
2.1.3 提取条件的优化
研究中考察了不同提取溶剂、混合比例、不同甲酸浓度对目标化合物提取效率的影响,采用甲醇或者乙腈作为提取溶剂时,甲基异噻唑啉酮、苯甲酸、噻苯咪唑峰形较差,由于乙腈具有沉淀蛋白的作用,而低比例乙腈会影响甲基异噻唑啉酮峰形,故综合考虑采用乙腈-甲醇(9∶1,体积比)作为提取溶剂,进一步考察了不同甲酸浓度对提取效果的影响,结果如图2所示,考虑到提取效果、色谱柱耐受性和化合物峰形,最终采用0.2%(体积分数)甲酸。
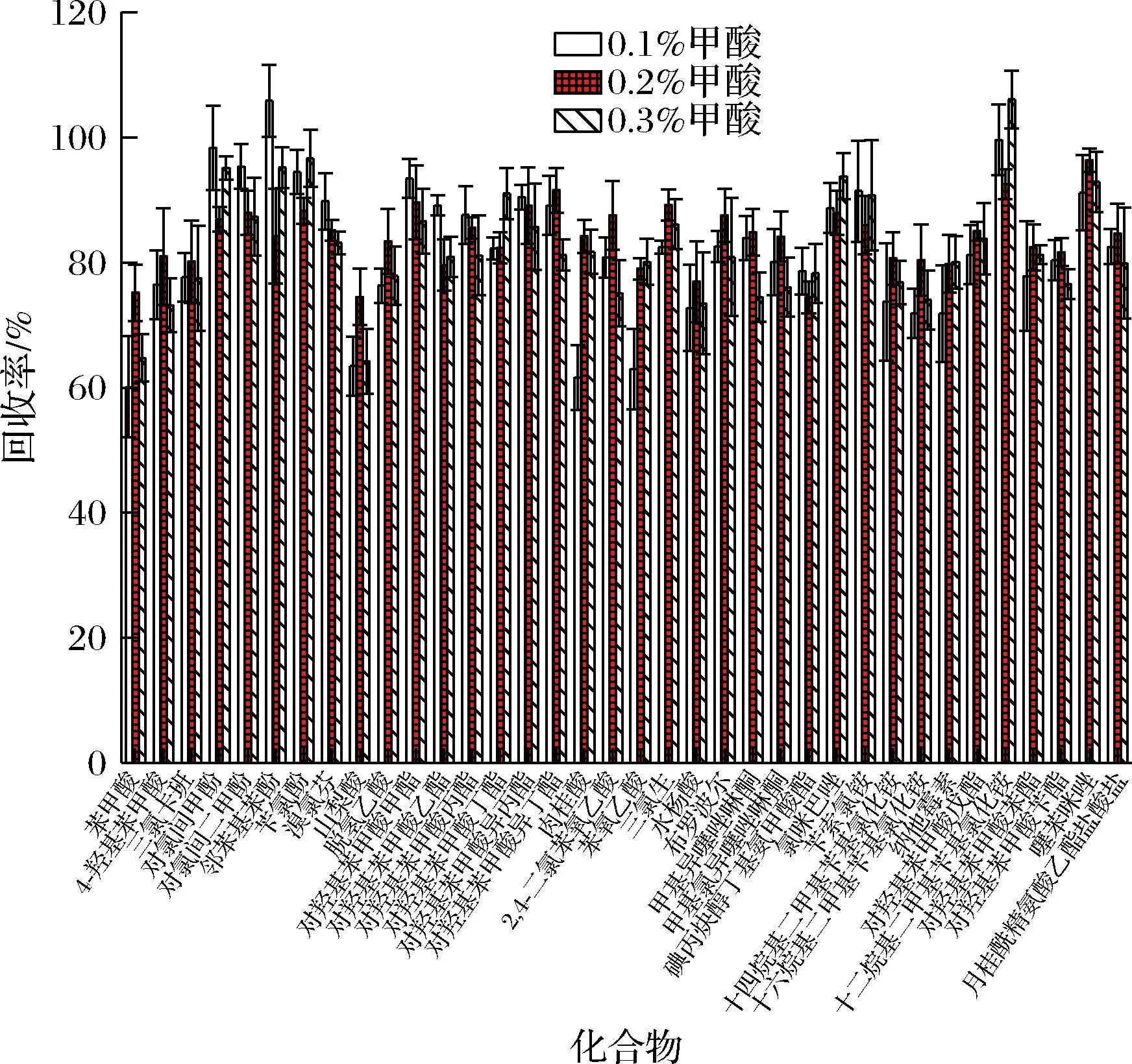
图2 甲酸浓度对目标分析物的影响Fig.2 Effect of the formic acid concentrations on compounds
2.1.4 净化方式的考察
由于液体调味品中基质较复杂且一些基质含盐量很高,会影响目标化合物的离子化效率以及质谱检测的灵敏度,实验中采用空白基质加标回收率方式考察EMR小柱(Agilent,Captiva EMR-Lipid,600 mg,6 mL)、PRiME HLB小柱(Waters Oasis PRiME HLB,200 mg,6 mL)、QuEChERS(乙二胺-N-丙基硅烷+C18+硫酸镁+碳黑,Agela和Sepax)、饱和NaCl溶液(pH=3)4种净化方式,结果如图3所示,实验表明饱和NaCl溶液整体效果最好,且前处理方便快速。饱和NaCl溶液在高有机相环境中具有盐析的作用,使基质中的盐和一些蛋白质等杂质留在水相中,起到分层净化的作用。
2.2 方法学考察
2.2.1 线性范围与定量限
分别称取3份不同基质的空白样品,按照前处理方法得到空白基质溶液。配制36种目标化合物质量浓度为1~250 ng/mL的系列混合基质标准溶液进行测定,以目标组分的峰面积y对相应的质量浓度x(ng/mL)绘制标准曲线,其相关系数R2均大于0.999。以信噪比(S/N)≥10作为方法的定量限,其线性方程和定量限见表3。
2.2.2 方法回收率与精密度
在蛋白饮料、酱油和醋的空白样品中分别添加低、中、高3个浓度的目标分析物,每个添加水平重复测定6次,计算平均加标回收率和精密度,结果见表4。目标分析物的回收率为75%~119%;相对标准偏差(relative standard deviation, RSD)为0.90%~9.8%。
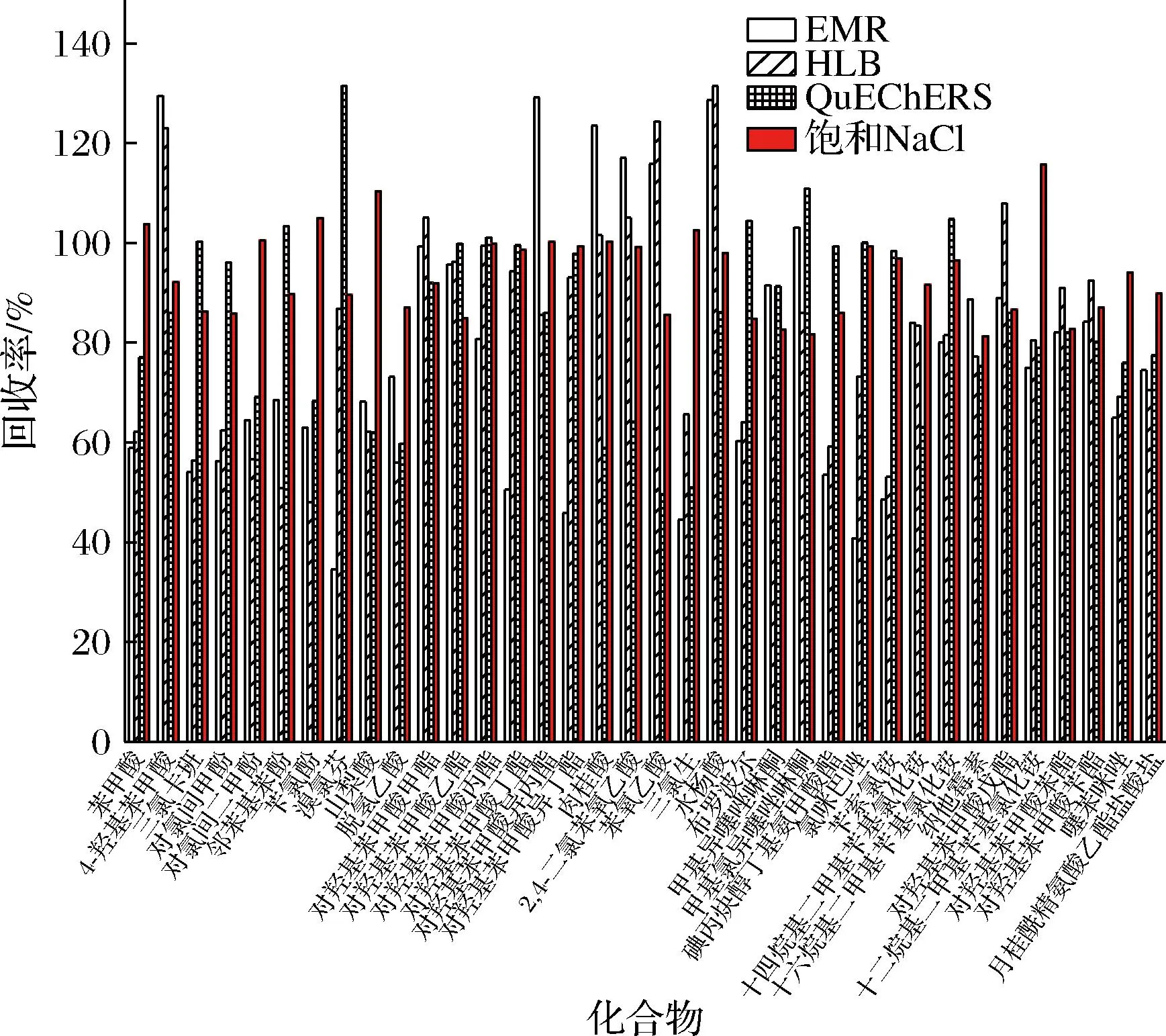
图3 净化方式对目标分析物的影响Fig.3 Effect of the purification methods on compounds
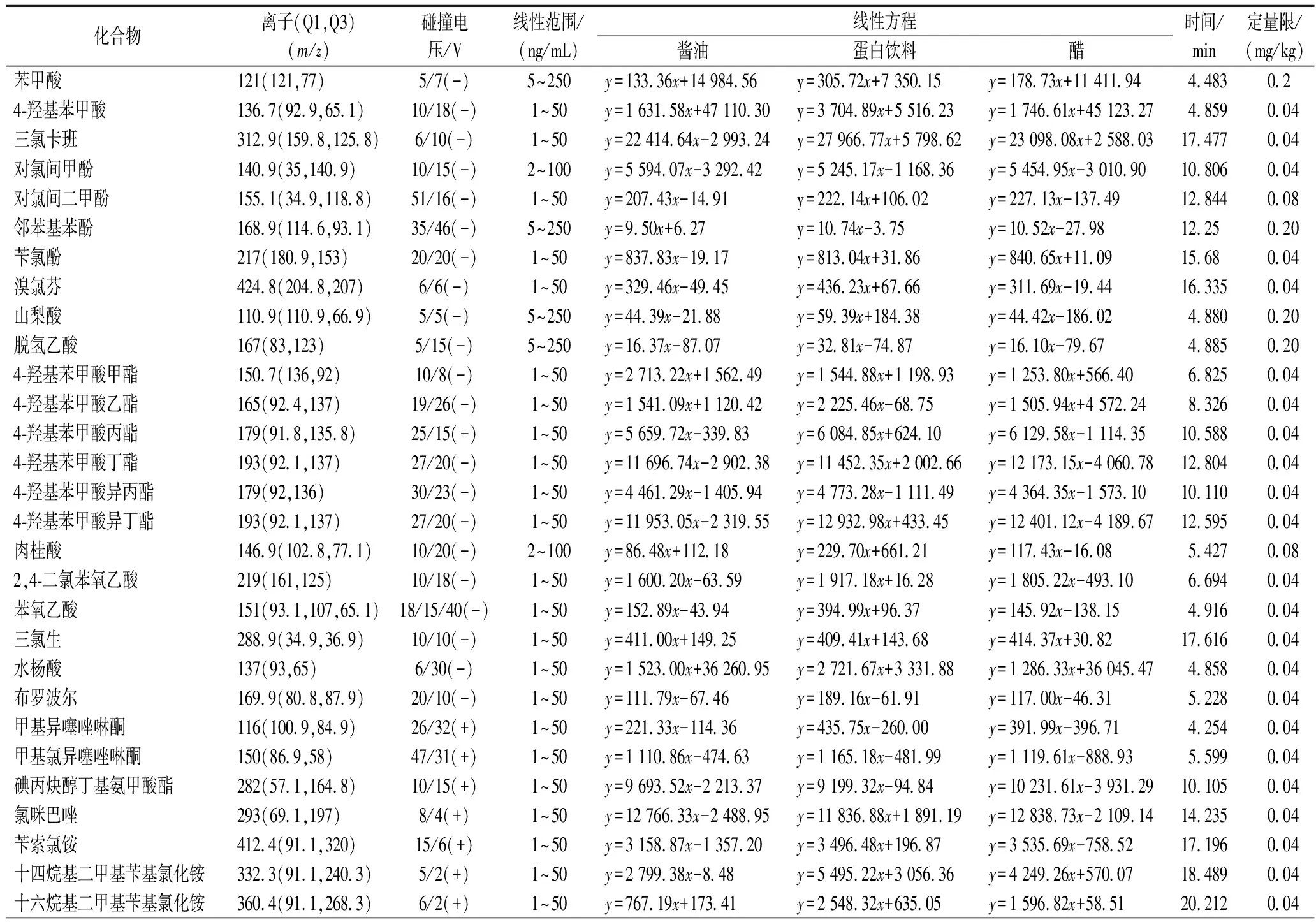
表3 36种目标分析物的质谱参数、线性关系和定量限Table 3 MS/MS parameters,linear relationships,and limits of quantification of 36 compounds
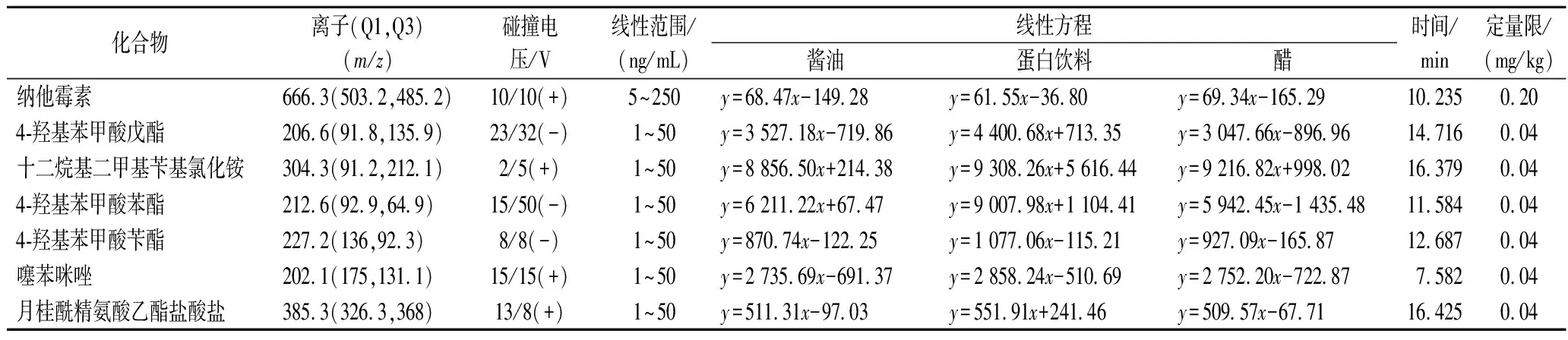
续表3
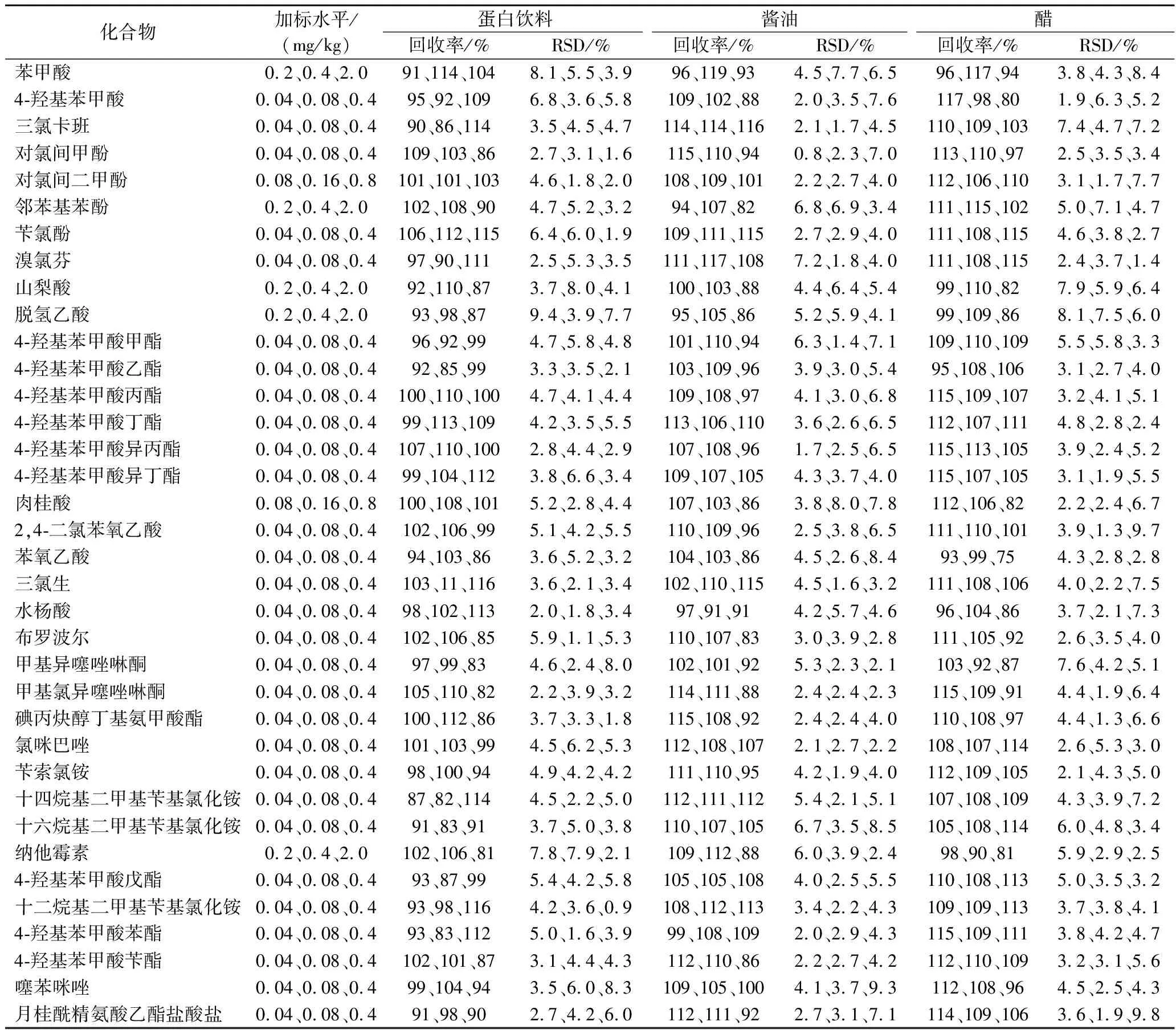
表4 36种目标分析物的加标回收率和精密度(n=6)Table 4 Recoveries and RSDs of 36 compounds(n=6)
2.3 实际样品测定
采用本文建立的方法,对从市场购买的50批样品(醋10批、酱油10批、蛋白饮料20批、其他液体调味品10批)进行检测,其中1批蛋白饮料和1批醋分别检出肉桂酸(0.000 17、0.001 3 g/kg),2批蛋白饮料、2批醋和2批酱油中分别检出4-羟基苯甲酸(0.000 009、0.000 18、0.005 2、0.002 3、0.003 0、0.002 7 g/kg);2批醋和1批液体调味品分别检出4-羟基苯甲酸乙酯,1批液体调味品中检出脱氢乙酸,8批酱油、6批醋和9批其他液体调味品分别检出苯甲酸和山梨酸;其余样品中未检出相关防腐剂化合物。
3 结论
本实验建立的蛋白饮料、液体调味品中36种防腐剂的超高效液相色谱-串联质谱检测方法,尤其覆盖一些新型和不常见防腐剂的高通量定性定量检测方法。前处理方法采用提取和净化相结合的方式,能有效减少基质干扰,建立的检测方法灵敏、快速,准确度高,操作简便、检测成本较低,可极大提高多种防腐剂的定性定量检测效率,对监测食品中防腐剂使用情况具有重要的意义。