Li(Ni0.8Co0.15Al0.05)O2锂电池正极材料的水热-高温固相法合成及参数控制
2024-01-12郭小毓吕光哲张文康徐有申仝斌斌
郭小毓,吕光哲,张文康,徐有申,仝斌斌
(辽宁科技学院 冶金与材料工程学院,辽宁 本溪 117004)
0 引言
近年来,化学储能和混合动力汽车的飞速发展对锂离子电池的能量密度和生产成本提出了更高的要求[1-4]。作为锂离子电池的限容因素和主要成本来源,理想的阴极材料应具有高的能量密度和良好的热稳定性,这对开发下一代新型锂电池尤为重要。阳离子代位的LiNiO2,特别是富镍Li[Ni1-xMx]O2受到越来越多的关注,其中Li(Ni0.8Co0.15Al0.05)O2(NCA)由于其具有突出的环境友好性、低成本、相对良好的热稳定性、高的容量和良好的循环稳定性等,是理想的体相掺杂正极材料[5-7]。目前适合工业化生产NCA阴极材料的方法主要是共沉淀-固相法,但共沉淀法合成(Ni0.8Co0.15Al0.05)(OH)2先驱体存在制备时间长、形貌复杂(由于Al3+的存在)的问题[4]。水热法广泛应用于合成氧化物尤其是具有高的晶体质量和纳米/微米尺度上的各种独特形态的多组分氧化物,通过先驱体制备参数的简单调节,即可得到具有不同表面结构、形貌和堆积密度的粉体材料[3]。
由此,文章尝试采用水热-固相法合成Li(Ni0.8Co0.15Al0.05)O2阴极材料。通过调节水热合成条件,对先驱体及NCA正极材料晶体结构、煅烧过程及形貌特征的影响进行了研究,为水热法条件下制备NCA阴极材料提供一些有益的参考。
1 实验方法
1.1 水热法合成(Ni0.8Co0.15Al0.05)(OH)2先驱体
将分析纯的碱式碳酸镍(NiCO3·2NiO2H2·4H2O)、碳酸钴(CoCO3·xH2O)溶解于适量稀硝酸,配制成含Ni/Co的2 M硝酸盐溶液(Ni/Co摩尔比为80∶15)并持续搅拌0.5 h,加入适量尿素[CO(NH2)2,(Ni+Co+Al) ∶CO(NH2)2=1∶2,质量比]并持续搅拌。随后,混合物转入25 mL反应釜中于160 ℃~220 ℃下保温10 h~28 h,待反应釜冷却到室温(先驱体1,记为NC-OH),加入适量Al(NO3)3·9H2O(Ni/Al摩尔比为80∶5)并继续在160 ℃~220 ℃下保温10 h~28 h(先驱体2,记为NCA-OH)。NCA-OH反应产物用去离子水和酒精多次清洗、过滤,在80 ℃中真空干燥10 h。
1.2 高温固相法制备NCA正极材料
将先驱体NCA-OH与LiOH·4H2O按照1∶1.05(摩尔比)的比例混合后,放入超声波清洗器中进行分散2 h,分散结束后放入真空干燥箱中烘干。最后将上述混合物置于马弗炉中,在空气条件下700 ℃煅烧6 h,得到Li(Ni0.8Co0.15Al0.05)O2(NCA)阴极粉体材料。
1.3 样品表征
采用X-ray衍射仪(XRD,布鲁克D8-ADVANCE型)对NC-OH/NCA-OH先驱体及NCA阴极粉体的晶体结构进行分析;采用扫描电镜(SEM,蔡司EVO18型扫描电镜,装有牛津X-Max能谱仪)观测上述样品的形貌及粒径的大小;采用DZ3320A型差热分析仪(DZ3320A型)测量先驱粉体的差热和失重曲线。
2 结果和讨论
2.1 先驱体及NCA阴极材料形貌分析
2.1.1 合成条件对先驱体NCA-OH形貌和粒径的影响
图1是不同水热温度制备NC-OH后得到的NCA-OH先驱体形貌,颗粒平均粒径为1 μm ~3 μm,且随反应温度的提高,颗粒尺寸逐渐增大。可以明显看出,160 ℃~180 ℃合成NC-OH得到的NCA-OH先驱体颗粒由细小的纳米片/纳米线组成,当反应温度提高到200 ℃~220 ℃,NCA-OH产物的精细结构转变为纳米针状。

图1 不同水热温度(a:160 °C,b:180 °C,c:200 °C,d:220 °C)合成NC-OH(×16 h)得到的NCA-OH(180 °C×16 h)形貌
在相同温度下制备NC-OH后,不同温度下合成的NCA-OH先驱体形貌见图2。从图2可看出,颗粒平均粒径为2 μm~4 μm,所有颗粒的精细结构皆为纳米针状一次颗粒聚合而成。随反应温度的提高,纳米针尺寸逐渐增大,在220 ℃时达到最大值。水热合成条件下,笼状物[Ni(CO(NH2)2)2]2+、[Ci(CO(NH2)2)2]2+和尿素在高温高压作用下逐渐发生水解或分解,因此,通过Ni2+和Co2+与OH-等构晶离子不断碰撞形核和长大,形成花瓣状的Ni(OH)2/ Co(OH)2先驱体水合物[8]。另外,随着合成温度的提高,尿素水解速度加快,高浓度的水解OH-可引起相邻粒子相互融合形成针状纳米晶并进一步长大。

图2 相同水热温度(180 °C×16 h)合成NC-OH,不同水热温度(a:160 °C,b:180 °C,c:200 °C,d:220 °C) JZ合成的NCA-OH(×16 h)形貌
2.1.2 合成条件对NCA形貌和粒径的影响
图3和图4分别是不同水热温度合成NC-OH/NCA-OH,700 ℃×6 h煅烧后的NCA形貌。由图可知,经煅烧后,NCA形貌与先驱体存在很大的差异。经过煅烧处理,NCA颗粒已由纳米针状一次颗粒聚合成的花瓣状先驱体形貌转变为纳米棒状为基本单元的块状粉体,平均颗粒尺寸约为3 μm~5 μm,且经200 °C水热合成的先驱体,煅烧后得到的NCA阴极粉体存在比较严重的团聚。这说明煅烧后的产物形貌可以继承先驱体的形貌特征,即具有形貌的遗传性。通过控制NC-OH/NCA-OH先驱体的合成条件,可以最终调节NCA阴极材料的形貌特点。

图4 相同条件(180 °C×16 h)合成NC-OH,不同水热温度(a:180 °C,b: 200 °C)得到的NCA-OH(×16 h)煅烧后NCA形貌(700 ℃×6 h)
2.2 NCA-OH先驱体的TG/DSC分析
图5是水热法合成的先驱体粉体TG/DSC曲线。由图5可看出,样品失重主要发生在3个阶段,100 ℃~320 ℃为第一阶段失重,在DSC曲线上对应195 ℃吸热峰和311.5 ℃放热峰,此阶段主要是先驱体失去结晶水和部分脱除碳酸根,失重率约为6.83%。320 ℃~420 ℃为第二阶段失重,对应DSC曲线上351.9 ℃、393.6 ℃两个吸热峰,此阶段主要是先驱体脱除剩余碳酸根,生成[Ni/Co/Al] (OH)2,失重率约为19.99%。420 ℃~540 ℃为第三阶段失重,失重率约为4.68%,此阶段可能是由于[Ni/Co/Al] (OH)2分解为金属氧化物,540 ℃后TG曲线趋于平缓。

图5 180 °C×16 h合成NC-OH,200 °C×16 h得到NCA-OH的TG/DSC曲线
结合图5的分析可知,无论何种制备方法得到的前驱体成分基本相同,整个分解过程可用以下方程式表示[9]:
[Ni/Co/Al]2(CO3)3·xH2O→[Ni/Co/Al]2
(CO3)3·H2O+ H2O
[Ni/Co/Al]2(CO3)3·H2O→2[Ni/Co/Al]
(OH)CO3+2CO2↑
2[Ni/Co/Al] (OH)CO3→[Ni/Co/Al]2O3+
H2O+2CO2↑
2.3 NCA先驱体及阴极材料的结晶过程分析
2.3.1 NCA-OH先驱体的XRD分析
图6是在不同保温时间下合成NC-OH后,180 °C×22 h得到的NCA-OH先驱体XRD检验结果。由图可知,随着NC-OH保温时间的延长,所有样品的NCA-OH先驱体表现出相似的XRD衍射图谱,说明随着保温时间的延长,NCA-OH结晶相没有发生明显的结构改变。
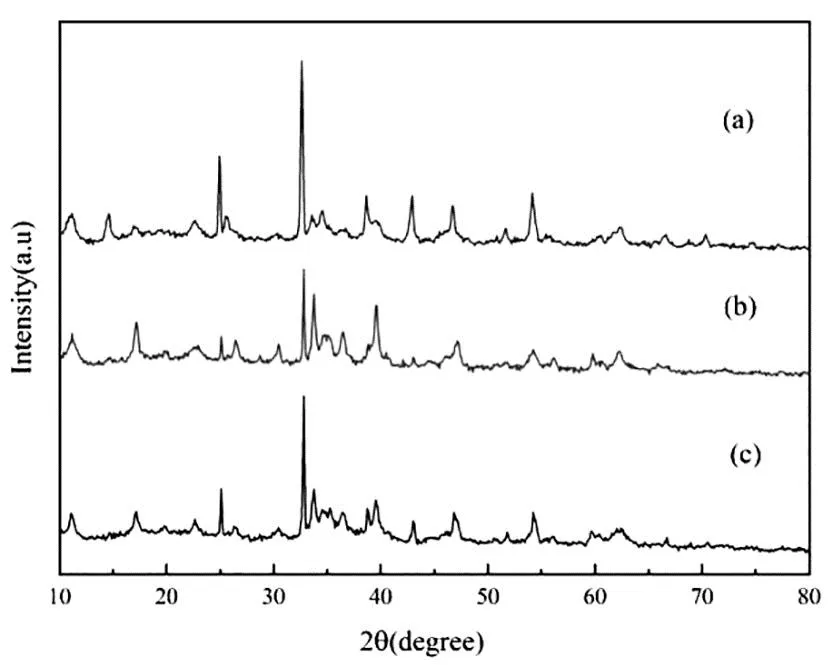
图6 不同保温时间(a: 16 h,b: 22 h,c: 28 h)合成(180 °C)NC-OH,得到的NCA-OH(180 °C×22 h)的先驱体XRD图谱
图7是在相同条件下合成NC-OH后,不同水热温度合成的NCA-OH先驱体XRD检验结果。由图可知,随着NCA-OH合成温度的提高,先驱体表现出与图6变化趋势相同的衍射图谱。当温度达到220 °C时,先驱体的衍射峰明显变得尖锐,说明温度的提高有利于NCA-OH的快速结晶。另外,图6和图7中的XRD衍射图谱与标准Ni(OH)2有着明显的不同,说明获得的先驱体极有可能是某种复杂的金属阳离子水合物。
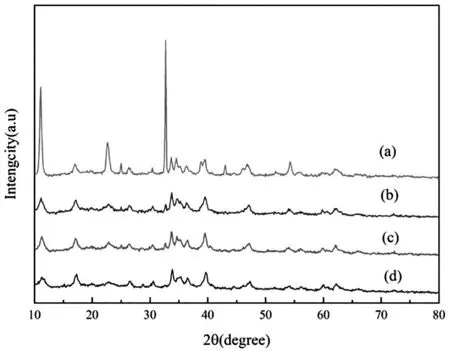
图7 相同条件下合成NC-OH(200 °C×16 h),不同水热温度的(a:160 °C,b:180 °C,c:200 °C,d:220 °C)NCA-OH先驱体(×28 h)的XRD图谱
2.3.2 NCA阴极材料的XRD分析
图8是在不同水热时间合成下NC-OH得到的先驱体NCA-OH(180 °C×22 h),煅烧后(700 ℃×6 h)NCA阴极材料XRD图谱。由图可知,每个样品的所有衍射峰都很好地指向LiNiO2(JCPD no-09-0063),说明Co和Al原子都成功地替代LiNiO2晶格中的Ni原子并形成NCA固溶体。另外,对在不同水热时间下合成NC-OH得到的所有先驱体,经煅烧后不同样品间的衍射峰差异比较明显。合成温度由160 °C提高到200 °C,I003/I104的峰强比逐渐增大,表明NCA正极材料层状结构中Li/Ni离子混排程度逐渐减轻,有利于正极材料的电化学性能得到改善[10]。
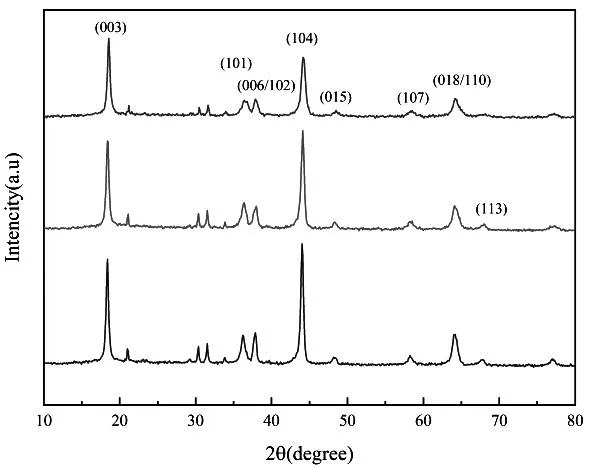
图8 不同水热时间(a:16 h, b: 22 h,c: 28 h)合成NC-OH(180 °C)得到的NCA-OH(180 °C×22 h),煅烧后NCA(700 ℃×6 h)的XRD图谱
图9是在相同水热条件下的NC-OH,经不同保温时间合成先驱体NCA-OH后,煅烧(700 ℃×6 h)得到的NCA XRD图谱。由图可知,每个样品的所有衍射峰都严格符合LiNiO2(JCPD no-09-0063),并且随合成NCA-OH的时间延长,I003/I104的峰强比逐渐增大,说明延长反应时间有利于Li/Ni离子混排程度的减轻。

图9 相同条件合成NC-OH(200 °C×16 h),不同水热时间(a:10 h,b: 16 h,c: 22 h,d: 28 h)的NCA-OH(180 °C),煅烧后(700 ℃×6 h)NCA的XRD图谱
图10 是在不同水热温度下合成的NC-OH,相同条件合成NCA-OH并煅烧后的NCA正极材料XRD图谱。由图可知,在不同温度下的样品衍射峰都严格对应 LiNiO2(JCPD no-09-0063), 但合成温度的不同导致图谱中(003)晶面的衍射峰强度存在差异,较低温度时合成的样品强度明显偏大。参照图3,由于较高温度合成的NCA-OH团聚现象比较严重,粉体的比表面积下降。在随后的煅烧过程中,反应物离子由于扩散路径的减少,导致结晶过程变得缓慢,因而结晶程度有所降低。
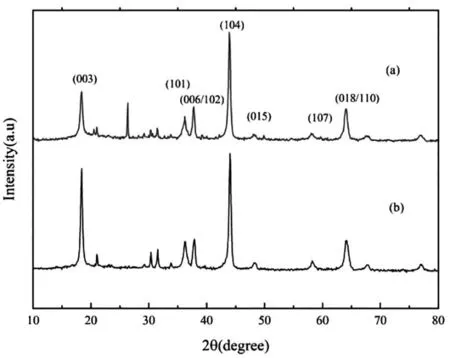
图10 不同水热温度(a: 180 °C ,b:200 °C)合成NC-OH(×16 h),相同条件的先驱体NCA-OH(180 °C×22 h),煅烧后(700 ℃×6 h)NCA的XRD图谱
3 结论
采用水热-高温固相法制备了Li(Ni0.8Co0.15Al0.05)O2阴极材料,结合相关检测手段,对先驱体NC-OH/NCA-OH及NCA阴极材料性能与水热条件的关系进行了有益的探索,得到以下结论:
(1)水热温度对先驱体NCA-OH/阴极材料NCA的形貌可产生很大的影响。随反应温度的提高,NCA-OH颗粒尺寸逐渐增大,先驱体一次颗粒由细小的纳米片∥纳米线精细结构转变为纳米针状,其尺寸随温度的提高而逐渐变大。经过在高温固相下的煅烧处理,NCA颗粒已由花瓣状先驱体形貌转变为纳米棒状为基本单元的块状粉体,随温度的提高,粉体团聚程度加剧。
(2)水热条件可影响先驱体NCA-OH/阴极材料NCA的结晶过程。随着反应温度和保温时间的延长,先驱体NCA-OH表现出相似的XRD衍射图谱,晶相结构没有发生明显的改变,温度的提高有利于NCA-OH的快速结晶。
不同水热温度合成的阴极材料NCA,经XRD检测皆为层状结构的LiNiO2(JCPD no-09-0063)相。不同的合成温度可引起(003)晶面峰强存在差异。由于较高水热温度可导致先驱体NCA-OH粉体发生团聚,减少了粉体可供反应的比表面积,使(003)晶面结晶度有所降低。
不同水热时间合成的NCA阴极材料,经高温固相煅烧后,不同样品间的衍射峰差异比较明显。随反应时间的延长,I003/I104的峰强比逐渐增大,表明NCA正极材料层状结构中Li/Ni离子混排程度逐渐减轻,延长反应时间有利于阴极材料电化学性能的改善。
