结直肠癌组织中GPR15和HMGA1表达情况及其临床预后价值研究
2024-01-10王鹏辉潘荣延
王鹏辉, 胡 杰, 潘荣延
结直肠癌(colorectal cancer,CRC)是常见的消化系统恶性肿瘤,2020年全球新发187万例,死亡92万例[1]。CRC起病较为隐匿,多数患者发现时已为中晚期,即使经过积极的综合治疗,仍可发生肿瘤复发和转移,导致患者死亡[2]。深入研究CRC疾病机制,寻找能够评估患者预后的肿瘤标志物,对该病的诊治具有重要意义。孤儿受体G蛋白偶联受体15(orphan receptor G protein coupled receptor 15,GPR15)是一种鸟嘌呤核苷酸结合蛋白偶联受体,参与趋化T淋巴细胞等免疫细胞,与炎症、免疫及肿瘤等疾病的发生密切相关[3-4]。研究表明,GPR15在肺腺癌、胃癌等恶性肿瘤中表达水平上调,其通过影响肿瘤免疫微环境,促进免疫逃逸,导致患者不良预后[5]。高迁移率族蛋白组A1(high mobility group proteome A1,HMGA1)属于高迁移率族蛋白家族成员,能够与DNA或蛋白质相互作用改变染色质结构,参与调节基因转录、逆转录病毒整合到染色体等过程[6]。近年来发现,HMGA1在肝癌[7]、乳腺癌[8]等恶性肿瘤中表达水平上调,能激活Wnt/β-连环蛋白通路,促进肿瘤侵袭和转移。目前,GPR15和HMGA1在CRC中的表达及临床意义尚不明确。鉴此,本研究通过检测CRC组织中的GPR15和HMGA1表达水平,探讨两者与CRC患者临床病理特征的关系及其临床预后价值。
1 对象与方法
1.1研究对象 选取2019年1月至2020年1月于扬州大学附属医院接受根治性手术治疗的89例CRC患者。其中男49例,女40例;年龄31~79(64.12±9.78)岁;病理类型:腺癌53例,黏液腺癌及其他36例;肿瘤位置:结肠55例,直肠34例;肿瘤分化程度:高中分化51例,低分化38例;合并淋巴结转移26例;肿瘤TNM分期:Ⅰ~Ⅱ期63例,Ⅲ期26例。纳入标准:(1)符合《中国结直肠癌诊疗规范(2017年版)》[9]中关于CRC的诊断标准;(2)首次发病;(3)术前未经任何化疗药物、放疗等抗肿瘤治疗。排除标准:(1)伴有肝、肾等重要脏器功能衰竭者;(2)伴有其他系统恶性肿瘤者;(3)临床资料不完整者;(4)妊娠期或哺乳期患者。本研究获扬州大学附属医院医学伦理委员会批准(批号:伦审S2018第014号),研究对象签署知情同意书。
1.2主要试剂及仪器 (1)主要试剂:GPR15、HMGA1兔单克隆抗体购自美国Abcam公司;免疫组化染色试剂盒购自北京中杉金桥公司。(2)主要仪器:ASP3005组织脱水机和RM2235切片机购自德国徕卡公司;XDS-1A倒置光学显微镜购自日本奥林巴斯公司;ABI7500实时荧光定量PCR仪购自美国ABI公司。
1.3实时荧光定量聚合酶链式反应(quantitative real-time polymerase chain reaction,qRT-PCR)检测组织中GPR15、HMGA1 mRNA表达水平 术中切取患者癌组织和癌旁组织(距离癌组织边缘2 cm以上),液氮中研磨制成匀浆后,以3 000 r/min离心10 min,取上清液,-80 ℃保存备检。采用Trizol法提取组织总RNA,应用反转录试剂盒(北京索莱宝科技有限公司)将其反转录为cDNA,并以cDNA为模板进行qRT-PCR。反应条件:94 ℃预变性5 min,94 ℃变性30 s,58 ℃退火30 s,72 ℃延伸30 s,变性退火延伸共35个循环。反应体系:2×SYBR Premix Master Mix 10 μl,正、反向引物各1 μl,cDNA 1 μl,双蒸水7 μl。引物由上海生工生物工程股份有限公司设计与合成。引物序列见表1。以GAPDH为内参,通过2-△△Ct法计算组织中GPR15和HMGA1的相对表达量。
1.4免疫组化染色检测组织中GPR15、HMGA1蛋白表达情况 术中切取患者癌组织和癌旁组织(距离癌组织边缘2 cm以上),用4%中性甲醛固定24 h,梯度乙醇脱水透明化,石蜡包埋后切片,层厚4 μm,60 ℃烤片2 h。二甲苯脱蜡2次,10 min/次,100%、95%、70%、50%梯度乙醇水化,每个梯度5 min。柠檬酸钠溶液中100 ℃抗原热修复10 min,3%过氧化氢封闭20 min。一抗4 ℃孵育16 h,二抗室温孵育30 min。采用二氨基联苯胺(diaminobenzidine,DAB)显色5 min后,苏木素复染,0.5%盐酸酒精分化,50%、70%、95%、100%梯度乙醇脱水,每个梯度5 min,二甲苯透明化5 min后,中性树脂封片,显微镜下观察染色结果。根据阳性细胞占比和染色强度情况进行免疫组化染色评分[10]:阳性细胞占比<5%计0分;5%~25%计1分;26%~50%计2分;51%~75%计3分;>75%计4分。染色强度为无染色计0分,淡黄色计1分,棕褐色计2分。阳性细胞占比评分与染色强度评分的乘积<2分为阴性,≥2分为阳性。
1.5随访方法 在术后通过电话或门诊复诊的方式进行随访,第1年每3个月随访1次,第2~3年每6个月随访1次,每位患者随访时间为36个月,记录患者的生存情况及生存时间。随访终点为随访时间结束或患者死亡。
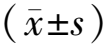
2 结果
2.1CRC癌组织和癌旁组织中GPR15、HMGA1 mRNA表达水平比较 qRT-PCR结果显示,CRC癌组织中GPR15、HMGA1 mRNA相对表达量高于癌旁组织,差异有统计学意义(P<0.05)。见表2。
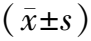
表2 89例患者CRC癌组织和癌旁组织中GPR15、HMGA1 mRNA表达水平比较
2.2CRC癌组织和癌旁组织中GPR15、HMGA1蛋白表达情况比较 免疫组化染色结果显示,CRC癌组织中GPR15蛋白主要表达于细胞浆和细胞膜,HMGA1蛋白主要表达于细胞核。CRC癌组织中GPR15、HMGA1蛋白的阳性表达率高于癌旁组织,差异有统计学意义(P<0.05)。见表3,图1。

表3 89例患者CRC癌组织和癌旁组织中GPR15、HMGA1蛋白表达情况比较[n(%)]
2.3CRC癌组织中GPR15、HMGA1表达情况与患者临床病理特征的关联性分析结果 TNM分期Ⅲ期、低分化程度及合并淋巴结转移的CRC癌组织中GPR15、HMGA1阳性表达率分别高于Ⅰ~Ⅱ期、高中分化程度及无淋巴结转移的CRC癌组织,差异有统计学意义(P<0.05)。见表4,5。

表4 CRC癌组织中GPR15表达情况与患者临床病理特征的关联性分析结果[n(%)]

表5 CRC癌组织中HMGA1表达情况与患者临床病理特征的关联性分析结果[n(%)]
2.4CRC癌组织中GPR15、HMGA1表达情况与患者生存预后的关联性分析结果 GPR15阴性组的生存预后优于GPR15阳性组,差异有统计学意义(log-rank检验:χ2=9.124,P=0.003);HMGA1阴性组的生存预后优于HMGA1阳性组,差异有统计学意义(log-rank检验:χ2=10.140,P=0.001)。见图2。
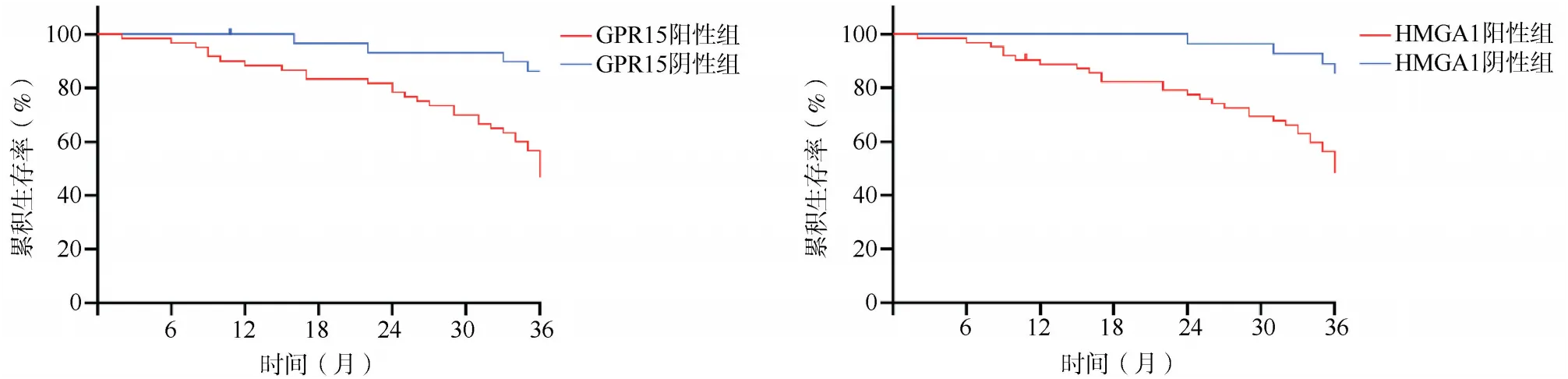
图2 CRC癌组织中GPR15、HMGA1表达情况与患者生存预后关联性的Kaplan-Meier曲线图
2.5影响CRC患者预后的Cox回归分析结果 以CRC患者术后生存情况为因变量(1=死亡,0=生存),以性别、年龄、病理类型、肿瘤位置、肿瘤分化程度、肿瘤TNM分期、淋巴结转移,以及GPR15、HMGA1表达情况为自变量进行Cox回归分析。结果显示,肿瘤TNM分期Ⅲ期、低分化程度、合并淋巴结转移、GPR15阳性、HMGA1阳性是促进CRC患者不良预后的独立危险因素(P<0.05)。见表6。

表6 CRC患者预后影响因素的单因素和多因素Cox回归分析结果
3 讨论
3.1CRC是我国常见的恶性肿瘤之一,近年来随着我国人民生活和饮食习惯的改变,其发病率呈现不断上升的趋势。目前CRC的临床治疗是以手术辅以放化疗为主的综合治疗,临床上主要根据CRC的TNM分期、肿瘤分化程度等临床病理特征对患者预后进行评估。但由于CRC患者具有异质性,不同患者发生复发及转移的风险差异较大,同一治疗模式并不能使所有患者获益[2]。深入研究CRC疾病机制,寻找能够评估CRC预后的肿瘤标志物,对于CRC的个体化治疗具有重要意义。
3.2GPR15是一种G蛋白偶联受体,能作为人类免疫缺陷病毒的共受体,发挥抗病毒的免疫调节作用。近年来发现,GPR15能够促进Foxp3阳性的调节性T淋巴细胞浸润至肿瘤组织,促进肿瘤免疫逃逸,是潜在的肿瘤标志物[11]。本研究中,CRC癌组织中GPR15 mRNA和蛋白表达均明显升高,提示GPR15参与CRC的肿瘤发生。CRC中GPR15表达升高与转录后调控异常有关。有学者通过生物信息学和荧光素酶实验证实,CRC肿瘤细胞中GPR15的表达受到miR-1225的转录后调节,miR-1225在CRC细胞中的表达下调导致GPR15 mRNA的稳定性增加,促进CRC肿瘤细胞过度增殖[12]。本研究中,CRC癌组织中GPR15的表达与不良临床病理特征有关,提示GPR15表达升高促进CRC肿瘤的恶性进展。分析其机制,可能是GPR15表达上调促进CRC肿瘤免疫逃逸,导致肿瘤进展。Adamczyk等[13]研究证实,CRC肿瘤发生时,GPR15能够促进肿瘤微环境中肿瘤相关调节性T淋巴细胞浸润到肿瘤组织,抑制肿瘤杀伤性CD8+T淋巴细胞的肿瘤杀伤作用,导致肿瘤过度增殖和侵袭。另外,GPR15表达升高还能促进树突状细胞中白细胞介素6、白细胞介素17等细胞因子分泌,诱导肿瘤细胞发生上皮间质转化,增强肿瘤的侵袭和转移能力[14-15]。本研究中,GPR15阳性表达的CRC患者预后较差,表明GPR15表达有助于评估CRC患者的临床预后。分析其原因,GPR15表达升高的CRC肿瘤细胞增殖及侵袭能力强,机体抗肿瘤免疫能力较差,肿瘤容易出现复发和转移,从而导致患者不良预后[16]。因此,GPR15可能是新的评估CRC患者预后的标志物。
3.3HMGA1又称为高迁移率组蛋白亚型I和Y(high mobility group protein isoform I and Y,HMGIY),编码基因位于6p21,能重塑染色质结构,参与胚胎发育分化、细胞周期调控及细胞衰老等生物学过程。近年来,在肺癌、前列腺癌等多种恶性肿瘤中均发现HMGA1表达升高,其能促进肿瘤增殖、转移及放疗耐药性形成,是潜在的预后相关肿瘤标志物[7,17]。本研究中,CRC癌组织中HMGA1的mRNA和蛋白表达水平均高于癌旁组织,提示HMGA1参与CRC的肿瘤发生。CRC中HMGA1的表达升高与非编码RNA调控有关。研究表明,CRC中长链非编码RNA 00460表达升高能够与胰岛素样生长因子结合蛋白2相互作用,促进HMGA1 mRNA的N6-甲基腺苷修饰,增强HMGA1 mRNA的稳定性,上调HMGA1蛋白表达,诱导CRC肿瘤细胞增殖、迁移和侵袭[18]。本研究中,HMGA1的表达与CRC患者不良临床病理特征有关,表明HMGA1能促进CRC的肿瘤进展。乳腺癌中HMGA1的表达上调能够结合叉头框蛋白M1,HMGA1和叉头框蛋白M1形成复合物进入细胞核中,促进血管内皮生长因子A的转录表达,导致肿瘤血管生成及肿瘤转移[19]。此外,HMGA1过表达能上调胃癌肿瘤细胞中Snail和Slug的表达,下调E-钙黏蛋白的表达,诱导肿瘤发生上皮间质转化,增强胃癌MGC803细胞系的侵袭和迁移能力[20]。本研究中,HMGA1阳性表达的CRC患者预后较差,是影响CRC患者不良预后的独立危险因素,表明HMGA1的表达有助于评估CRC患者的生存预后。分析其原因,CRC中HMGA1能够与CRC肿瘤干细胞表面的程序性死亡因子配体1相互作用,激活磷脂酰肌醇3激酶/AKT途径,促进干细胞的增殖及对化疗耐药性的形成,导致患者不良预后[21]。
综上所述,CRC中GPR15、HMGA1表达升高,两者与肿瘤TNM分期、肿瘤分化程度及淋巴结转移有关,均参与CRC肿瘤的发生发展过程。CRC中GPR15、HMGA1阳性表达是患者不良预后的独立危险因素,有利于辅助临床医师对CRC患者的预后进行评估,对预后不良的高危CRC患者予以积极诊治及随访,以改善其临床预后。
