Na2CO3改性粉煤灰制备吸附剂及其对橙黄IV的吸附性能
2024-01-08徐佳辉李新甜周维华
康 华, 徐佳辉, 李新甜, 周维华
(黑龙江科技大学 矿业工程学院, 哈尔滨 150022)
0 引 言
粉煤灰是煤炭在高温燃烧过程中产生的飞灰,在燃烧过程中,煤中的各种物质流失,骤冷时形成较为致密的熔融体,主要成分是石英、莫来石以及刚玉等,同时,也会含有微量的重金属和其他元素。粉煤灰一般情况下呈灰褐色,显酸性,透射显微镜下观察可以看到圆球状的玻璃微珠。由于粉煤灰尺寸小,且含重金属,简单的堆放处置,不仅会使其逸散进入空气,形成空气污染,而且也会通过溶渗作用进入水中,造成水资源污染,既污染土地又会间接危害人体健康。因此,如何合理利用粉煤灰,对其进行高值利用,使用低成本,易操作,绿色健康的方法实现对粉煤灰的综合利用是一个亟待解决的课题[1]。
粉煤灰具有良好的吸附性能,广泛应用于染印废水的处理,但直接投放效果并不理想,废水中的色度以及重金属离子的去除率都不是很高。因此,想要更大程度地利用开发粉煤灰的吸附性能,就要对其进行改性处理,激发其吸附潜能,国内外应用得较为普遍的改性方法主要分为物理方法和化学方法。物理方法包括:机械研磨法,高温煅烧法等;化学方法包括:酸、碱、盐、有机物的干法改性或者湿法的包覆。其中,盐类改性法是利用盐类改性剂电离出的阳离子附着在粉煤灰表面,与废水中的污染物絮凝、沉降,进而增强粉煤灰的吸附性能[2],从而达到废水处理的目的。
笔者使用碳酸钠(Na2CO3)对来自鹤岗矿务局的粉煤灰(FA)进行改性处理,制备碳酸钠改性粉煤灰(NFA)作为吸附剂,对橙黄IV染料模拟的废水进行脱色研究,探讨了橙黄IV溶液的初始质量浓度、pH值以及吸附剂用量等对吸附效果的影响,找出最佳吸附条件。
1 试 验
1.1 试剂及设备
本试验选取的粉煤灰原灰是来自鹤岗矿务局某电厂,在105 ℃下恒温干燥后过250目筛。碳酸钠、盐酸、氢氧化钠、橙黄IV均为化学分析纯,试验用水为去离子水。
废水模拟液使用橙黄IV配置,将0.25 g染料加入500 mL的去离子水配置浓度为500 mg/L的标准液,可根据后续试验设置,稀释至指定浓度。
试验过程中使用的主要设备仪器:集热式恒温加热磁力搅拌器(DF-101S);电热恒温鼓风干燥箱(DHG-9070A);离心机(KL05A);循环水式真空泵(SHZ-DIII);紫外可见分光光度计(760CRT);扫描电镜;傅里叶红外光谱仪。
1.2 试验方法及内容
改性试验:取40 mL浓度为1.0 mol/L的Na2CO3溶液,与10 g粉煤灰(FA)混合均匀后,在室温下恒温搅拌1.5 h,然后,经过过滤、洗涤、烘干等操作,制备出碳酸钠改性粉煤灰(NFA),对其进行SEM、FT-IR、氮气吸附脱附等表征分析,探究NFA的表面形貌、官能团等微观变化,然后,使用橙黄IV溶液对废水进行模拟,使用紫外可见分光光度计测定吸附前后橙黄IV的浓度,探究不同条件下NFA吸附容量Q和吸附率R的变化规律。
吸附试验:将橙黄IV的标准溶液稀释配置不同浓度的废水模拟液,添加一定质量的改性粉煤灰(NFA),混合搅拌至吸附平衡状态,用装有滤膜的针管吸取清液,用紫外可见分光光度计测定吸附前后橙黄IV质量浓度的变化[3]。探究橙黄IV溶液初始质量浓度100~300 mg/L、吸附剂用量1~5 g、吸附时间0~60 min、温度25~65 ℃、溶液pH值2~10等条件,对吸附性能的影响。NFA对橙黄IV溶液的吸附量Q与吸附率R的计算公式为
式中:ρ0——吸附前橙黄IV的质量浓度,mg/L;
ρ1——吸附后橙黄IV的质量浓度,mg/L。
2 结果与讨论
2.1 NFA的结构表征
2.1.1 扫描电镜
FA与NFA样品的SEM见图1。由图1a可知,未改性的原状粉煤灰是圆球状的光滑颗粒,尺寸不一,表面包覆一层致密的玻璃薄膜。由图1b可知,改性后的粉煤灰表面粗糙,出现孔隙,整体感觉像窝状的“松糕”[4]。说明Na2CO3改性,使得原本致密的球形玻璃体被破坏,增加了一些微孔,从而扩大本身的比表面积。同时,Na2CO3作为一种碱性激发剂,溶于水后呈碱性,一定程度上也能够腐蚀粉煤灰表面,提升粉煤灰的活性[5]。Na2CO3溶液会打开粉煤灰中的Si-O和Al-O化学键,提高四面体结构的活化能,释放活性因子,从而增强吸附剂的吸附能力。
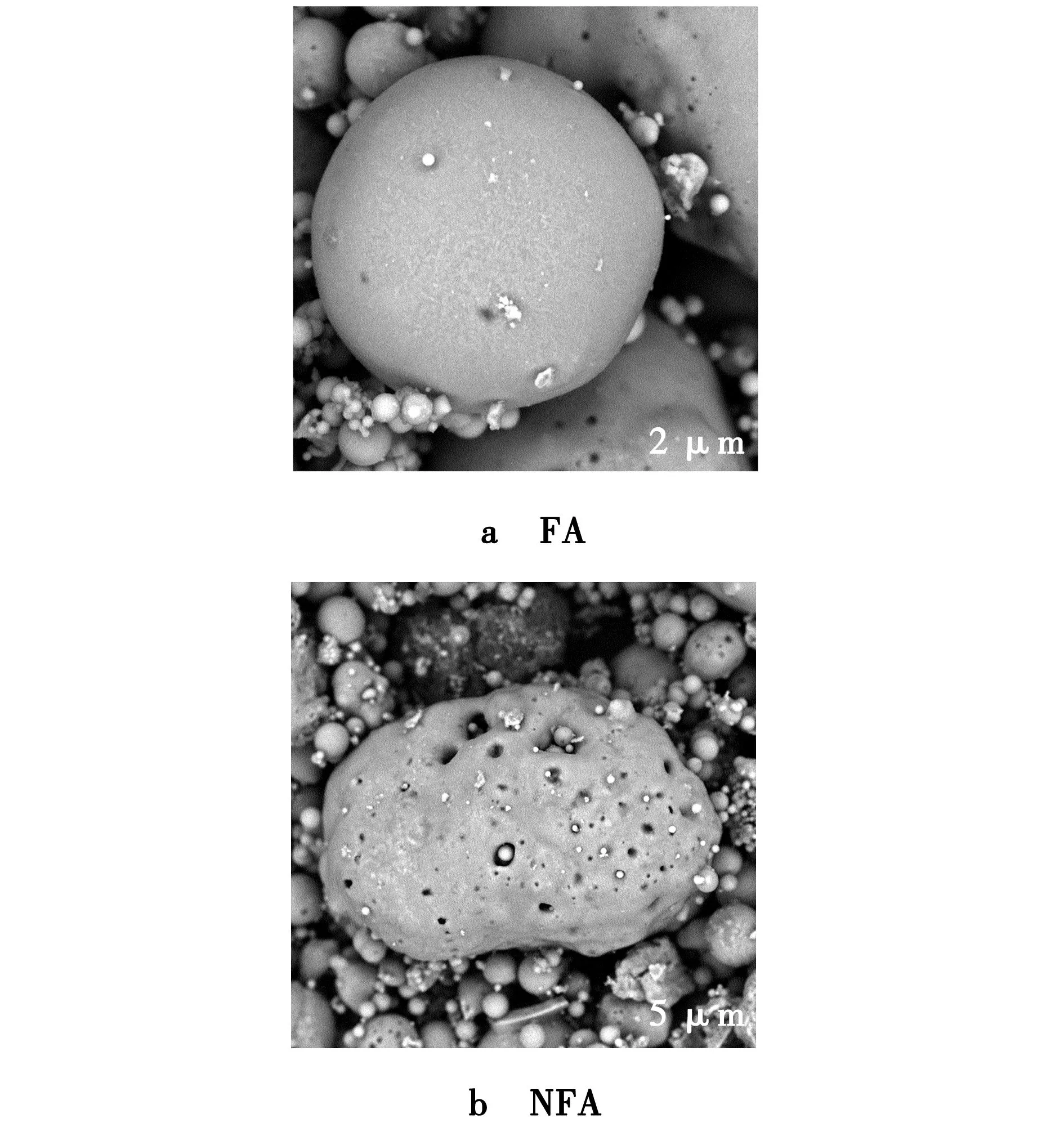
图1 自动化目标物检测算法总体框架
2.1.2 傅里叶红外光谱
FA与NFA样品的FT-IR见图2。由图2可以看出,改性前后的红外谱图基本一致,但改性后的NFA各个吸收峰强度略有减弱。3 473 cm-1与1 635 cm-1附近为H2O的特征峰,可能是样品在测试前后吸收空气中的水分而导致的。1 132 cm-1处的Si-O-Si特征峰,583 cm-1处的Si-O和Al-O的特征峰的减弱,说明在改性过程中,粉煤灰中的SiO2与Na2CO3发生反应形成硅酸盐,硅酸盐的溶出,使得Si-O与Al-O键破裂,SiO2和Al2O3的聚合度降低,吸收峰减弱[6]。

图2 FA和NFA的红外光谱
2.1.3 X射线衍射
FA与NFA的XRD谱图见图3。在5°~70°的范围内,扫描到FA的矿物组成主要有莫来石(Al4Si2O10)和石英(SiO2)以及少量的尖晶石(MgAl2O4)和赤铁矿(Fe2O3),其中,莫来石(Al4Si2O10)在17.12°、26.35°、31.01°、35°、41.35°、43.52°、61.34°和65.21°处都出现明显的衍射峰。NFA和FA的衍射峰位置大致相同,强度略有差异,且没有出现新的衍射峰,说明Na2CO3改性前后FA的矿物组成没有发生变化,与之前一致。之所以NFA的衍射峰强度出现减弱,是因为Na2CO3与FA的组成成分发生了反应,使得FA中的Si-O-Si键和Al-O-Al键断裂,活性点位增加,激发了硅铝酸盐这样的稳定活性基团的生成,使得FA表面光滑致密的玻璃薄膜被破坏,变得粗糙多孔,进而增大比表面积,有利于吸附质的附着,以及吸附反应的进行[7]。

图3 FA和NFA的XRD谱
2.1.4 氮气吸附/脱附
FA与NFA样品的氮气吸附/脱附等温线见图4,数据参数见表1。

表1 FA和NFA比表面积及孔结构参数

图4 FA和NFA的氮气吸附-脱附等温线
由表1可以看出,改性后的BET比表面积、孔径、孔容均有所提高,其中,比表面积增加了8.64 m2/g,孔径增加了0.22 nm,孔容增加了0.036 2 cm3/g,说明改性有助于提高FA的吸附性能。图4中出现了H3型回滞环,表明其在同等压力条件下,可以表现出更大的吸附能力。
2.2 单因素吸附试验
试验采取单一变量原则,对橙黄IV溶液初始质量浓度、吸附剂用量、吸附时间、吸附温度、溶液pH等因素逐个进行探究,确定最佳工艺参数。
2.2.1 橙黄IV溶液初始质量浓度
在吸附剂用量为1 g/L的条件下,常温振荡吸附90 min。吸附性能如图5所示。随着橙黄IV溶液初始质量浓度的升高,吸附量整体呈上升趋势,二者呈正比;吸附率呈下降趋势,二者呈反比。但吸附量的曲线中有一处转折点,在溶液质量浓度为100~250 mg/L时,吸附量不断上升,从79.40 mg/g上升到144.65 mg/g;溶液质量浓度大于250 mg/L时,吸附量逐渐下降至142.44 mg/g,下降了2.21 mg/g。这是因为在橙黄IV浓度较低时,吸附剂与吸附质间的分子驱动力愈强,吸附效果愈好[8],吸附量不断上升;当溶液浓度变高,NFA的用量不变,吸附达到饱和状态,吸附量便开始下降。同时随着橙黄IV溶液浓度的不断升高,NFA表面会形成一层阻碍吸附的保护膜,造成吸附率下降。综上所述,橙黄IV的最佳初始质量浓度为250 mg/L。
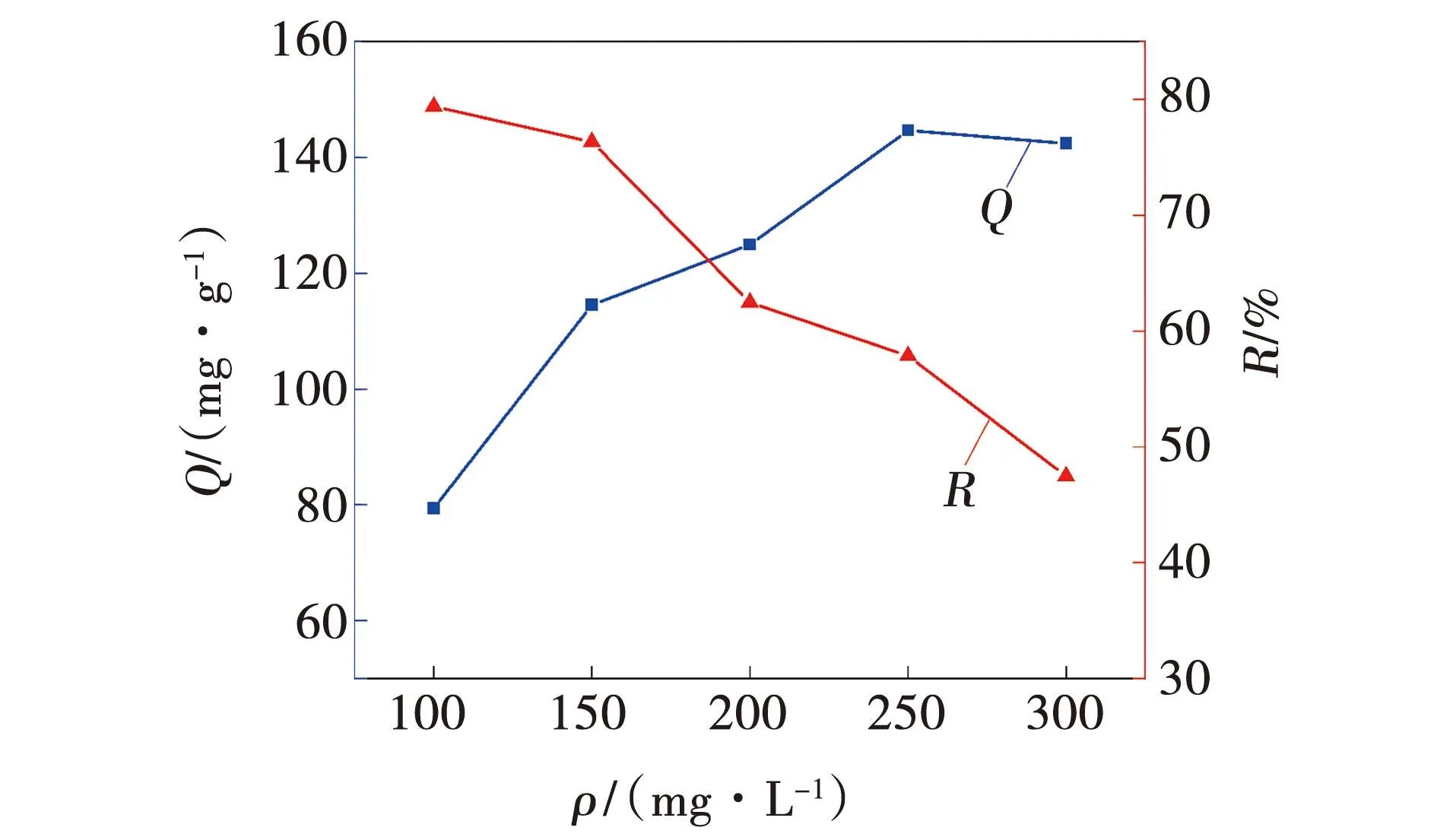
图5 初始质量浓度对NFA吸附性能的影响
2.2.2 吸附剂用量
在橙黄IV溶液初始质量浓度为250 mg/L的条件下,常温震荡吸附90 min。吸附性能如图6所示。
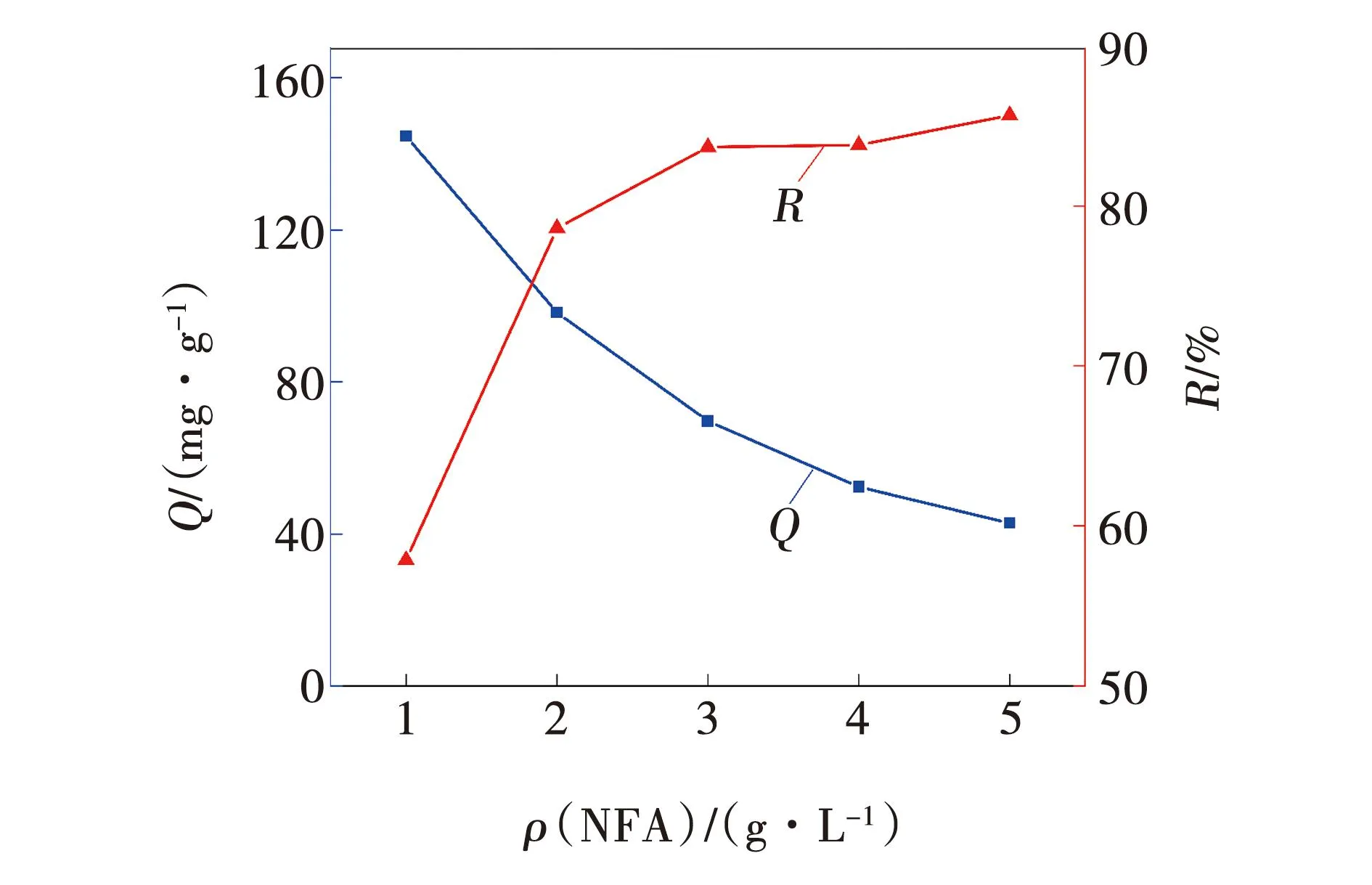
图6 NFA用量对吸附性能的影响
随着NFA的用量不断增加,橙黄IV的吸附量逐渐降低,在吸附剂添加量为1 g/L时出现最大值,为144.66 mg/g,然后逐步降低至42.83 mg/g;橙黄IV的吸附率不断增加,由57.86%增长到83.68%,然后趋于平缓。这是因为随着NFA用量的增加,吸附剂的比重不断增大,单位面积上吸附质的吸附量降低,且溶液中吸附质也被消耗殆尽,吸附率增加缓慢直至平缓[9]。综上所述,吸附橙黄IV的最佳吸附剂用量为3 g/L。
2.2.3 吸附温度与时间
在橙黄IV溶液初始质量浓度为250 mg/L的条件下,NFA用量为3 g/L,分别在25、35、45、55、65 ℃下振荡吸附90 min,在5、10、20、30、60 min时取样。吸附性能如图7所示。

图7 NFA吸附温度和吸附时间对吸附性能的影响
由图7可知,随着时间的增长,吸附量的增长呈先快后慢直至平缓的趋势;而温度升高,吸附量反而开始下降,在25 ℃时,吸附量最高可达67.95 mg/g。这是因为在0~30 min时,吸附剂表面的活性位点逐渐被占据,使得吸附剂表面变得致密,比表面积减小,在30 min时吸附量达到饱和状态;而NFA的吸附过程本身是一个放热反应,温度的升高让吸附质与吸附剂之间的作用力减弱,导致吸附量降低[10]。综上所述,吸附橙黄IV的最佳吸附时间为30 min,吸附温度为25 ℃。
2.2.4 溶液pH值
在橙黄IV溶液初始质量浓度为250 mg/L的条件下,NFA用量为3 g/L,常温振荡吸附30 min,试验过程中使用硫酸,氢氧化钠标准滴定液调节溶液pH值。吸附性能如图8所示,吸附量与吸附率都随着pH值的升高而逐渐降低,在酸性条件下,吸附性能更好,pH为2时,吸附量与吸附率的值最高,分别为74.58 mg/g、89.51%。这是因为橙黄IV是一种酸性染料,本身带有负电荷,在pH值较低时,与NFA表面的正电荷之间的静电吸引力更强,吸附效果更好[11]。随着pH值的升高,这种吸引力消失,吸附质与吸附剂之间相互排斥,吸附效果变差。
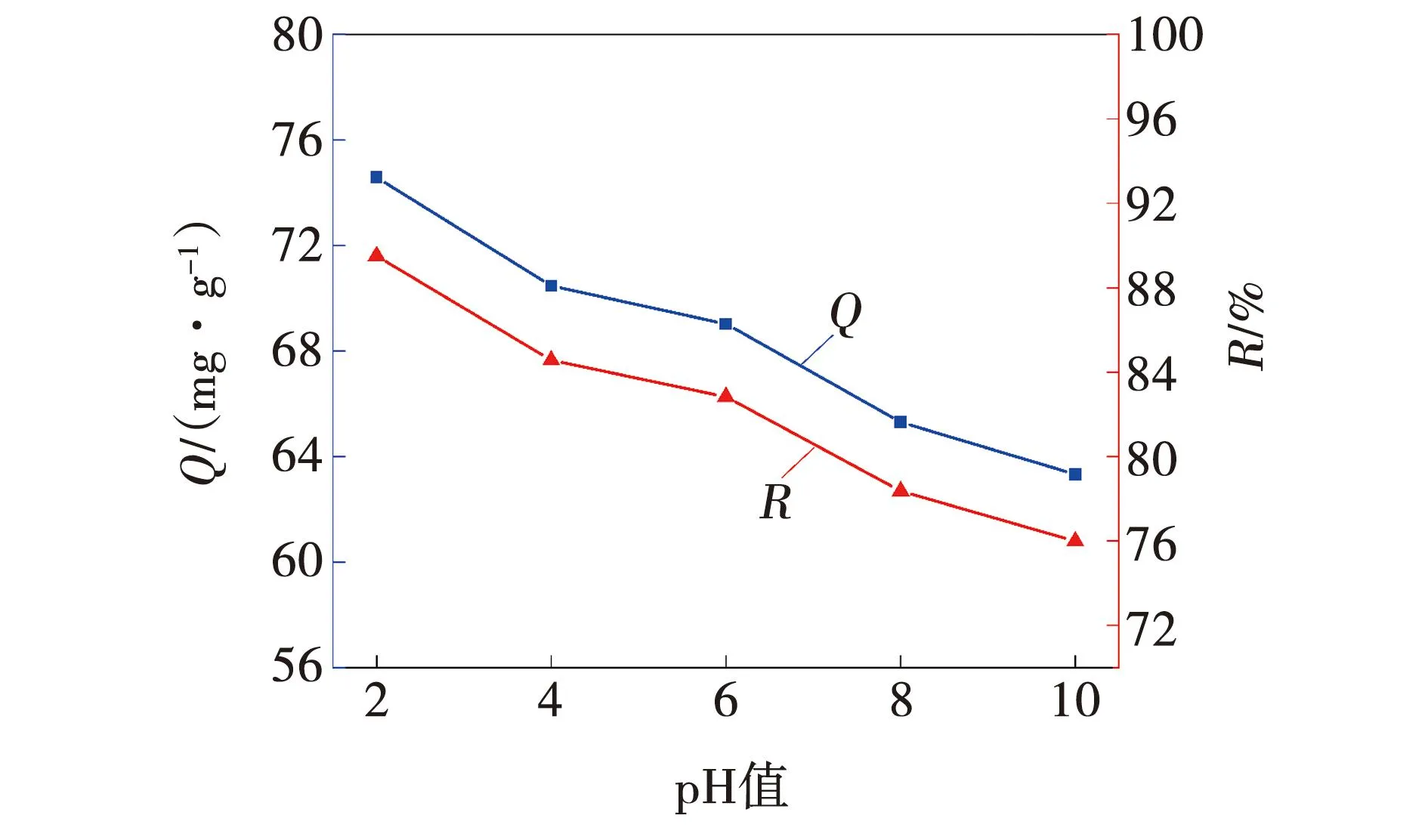
图8 溶液pH对吸附性能的影响
2.2.5 吸附性能比较
在室温下,分别使用FA与NFA作为吸附剂,吸附质量浓度为250 mg/L的橙黄IV溶液,吸附剂投加量为3 g/L,pH为溶液自身pH值,试验结果如表2所示。
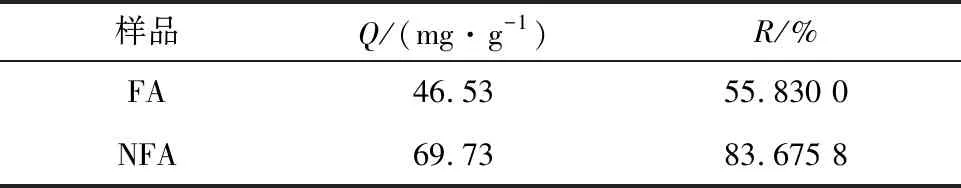
表2 FA与NFA吸附性能的比较
由表2可知,使用Na2CO3对FA进行改性处理,可以极大地提高其吸附性能,吸附率上升27.85%,说明其在吸附水体中染料的领域具有重要应用前景。
2.3 正交吸附试验
在单因素试验的基础上,为了确定各因素之间是否存在交叉影响,探究最佳吸附参数,对橙黄Ⅳ溶液的初始质量浓度(A)、溶液pH值(B)、吸附剂用量(C)三个因素,设置3因素3水平的正交试验。试验因素及水平设置取值如表3所示。该表设置NFA的正交试验因素、水平矩阵,橙黄IV溶液初始质量浓度的三个水平取值分别为200、250、300 mg/L,初始溶液pH分别为1、2、3,吸附剂用量分别为2、3、4 g/L,三水平的取值参考单因素试验的最佳吸附方案。以NFA对橙黄Ⅳ的吸附率R为评价指标对正交试验结果进行极差分析,NFA吸附剂的正交试验结果,如表4所示,其中,Ki表示任一列上水平号为i(i=1,2,3)时所对应的试验结果之和。RK表示极差,该列Ki中的最大值与最小值之差。

表3 正交试验因素编码与取值L9(33)
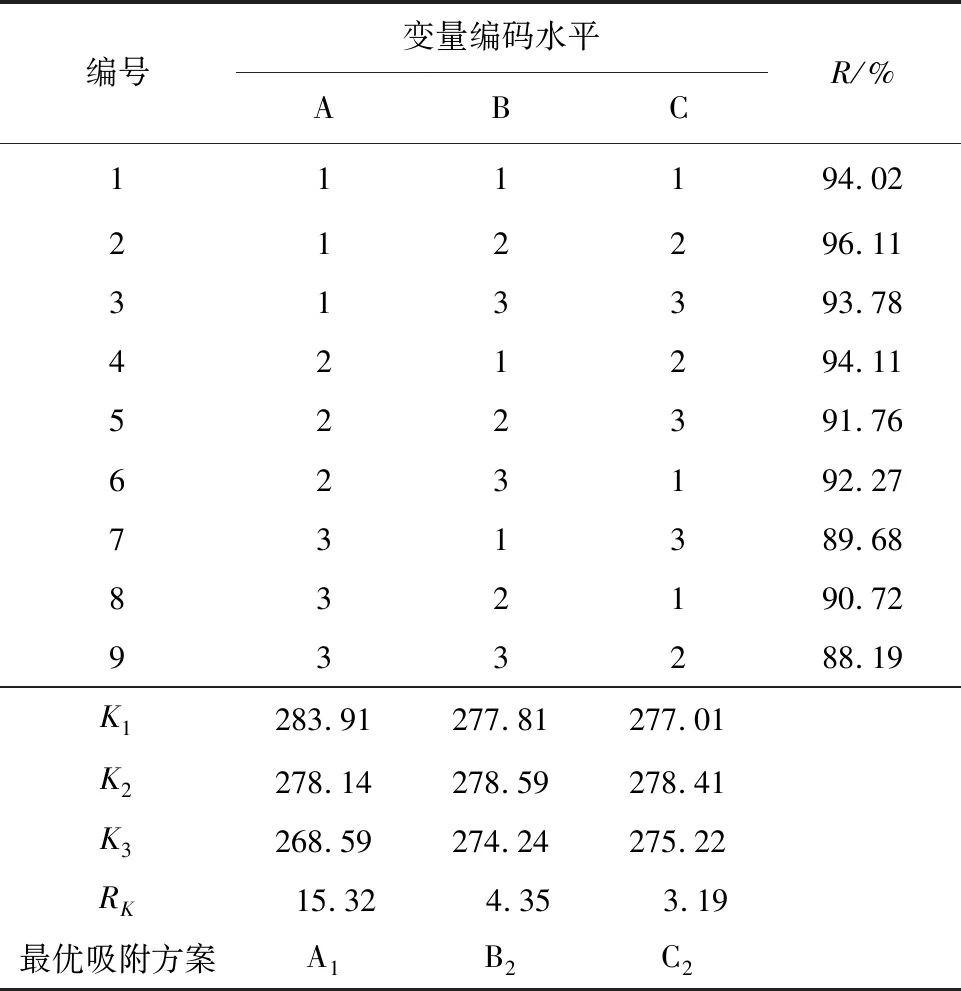
表4 NFA的正交试验结果L9(33)
由表4正交试验结果可知,对NFA吸附效果影响因素的主次顺序为橙黄IV溶液的初始质量浓度>溶液pH>吸附剂用量,RK值分别为15.32、4.35、3.19,橙黄IV溶液的初始质量浓度。最佳吸附方案为编号2,即橙黄IV溶液的初始质量浓度为200 mg/L,溶液pH为2,吸附剂投加量为3 g/L,吸附温度为25 ℃,吸附时间为30 min。在此条件下,吸附率可达96.11%。
2.4 等温吸附模型
等温吸附数学模型对揭示吸附剂与吸附质之间的吸附机理具有重要作用,是定量研究环境中胶体对各种元素迁移的影响的重要方法。为了研究NFA对橙黄IV的吸附机理,在室温条件下,进行吸附试验,使用Langmuir和Freundlich等温模型拟合分析试验数据。其中,Langmuir用于描述单分子层吸附,Freundlich模型用于描述多分子层吸附[12-13]。Langmuir等温模型的应用基于三个假设:(1)吸附分子间无作用力;(2)表面是均匀的,即吸附热不随吸附量而变化,每一个吸附点的能量不变;(3)吸附限制在单分子层。Freundlich模型则是经验式,适用于不均匀表面的吸附,吸附热随覆盖度指数下降,该模型假设吸附到物质表面的不同层之间是独立的。
Langmuir模型为
式中:Qe——平衡时吸附量,mg/g;
ρe——平衡时溶液质量浓度,mg/L;
Qm——吸附剂最大吸附量,mg/g;
Kl——吸附亲和力常数,mol/L。
Freundlich模型为
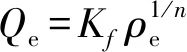
式中:Kf——吸附容量指标,mg/g;
n——吸附强度参数。
相关参数如表5所示,NFA的等温拟合曲线如图9所示。
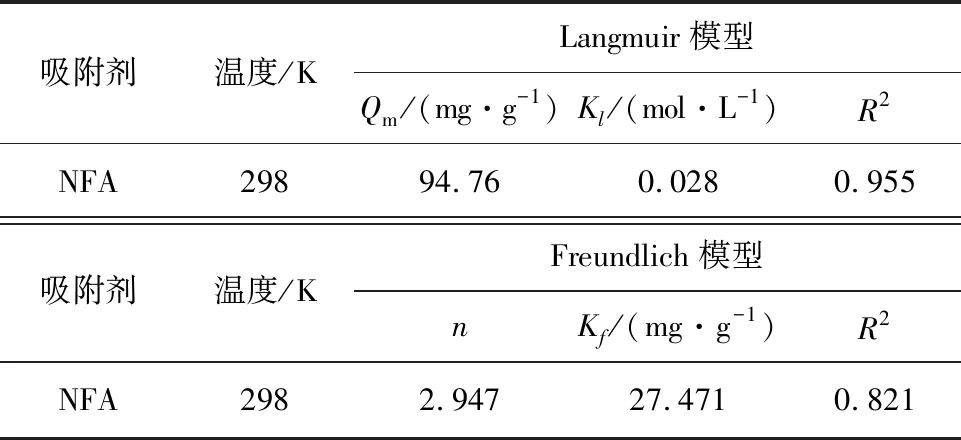
表5 NFA的等温吸附拟合参数

图9 等温吸附线
由图9可知,两种曲线均可以拟合NFA对橙黄IV的吸附过程,其中,Langmuir的R2为0.955大于Freundlich的R2为0.821,说明Langmuir的拟合效果更好,NFA对橙黄IV的吸附属于单分子层吸附。由Langmuir模型方程可以计算出,NFA对橙黄IV的理论吸附量最大可达94.76 mg/g。在Freundlich模型中n值为2.947,介于2~10之间,说明NFA对橙黄IV的吸附性能良好,有利于吸附的进行[14]。
2.5 反应动力学分析
Pseudo模型被广泛应用于化学反应动力学和吸附平衡的研究中,用来描述物质的吸附与反应情况,是分析吸附行为的有效工具。为了进一步了解NFA对橙黄IV的吸附过程,使用Pseudo反应动力学模型对各温度(25、35、45 ℃)下的试验数据进行拟合分析。
Pseudo准二级方程表达式为
式中:Qe——达到反应平衡时NFA对橙黄Ⅳ的吸附容量,mg/g;
Qt——t时刻NFA对橙黄Ⅳ溶液的吸附容量,mg/g;
k2——NFA对橙黄Ⅳ溶液的准二级动力学吸附平衡常数,min-1。
Pseudo准二级方程拟合直线如图10所示。

图10 Pseudo准二级方程拟合线
由图10可知,各温度下,t/Qt与吸附时间t呈线性关系。在温度为25、35、45 ℃下计算平衡常数k2的值分别为0.014、0.028 4、0.166 4 min-1,Qe的值分别为66.67、50.94和40.24 mg/g,与试验中所测的数据值接近。拟合相关系数R2的值分别为0.996、0.998和0.999,说明NFA对橙黄Ⅳ的吸附过程符合Pseudo准二级反应动力学模型,即其吸附类型为化学吸附。
3 结 论
(1)采用湿法改性制备了碳酸钠改性粉煤灰(NFA),通过SEM、FT-IR、XRD、氮气吸附脱附对其进行表征,分析结果表明,碳酸钠改性粉煤灰(NFA)的改性效果明显,吸附性能有所提升。
(2)使用碳酸钠改性粉煤灰(NFA)作为吸附剂,在常温下,吸附初始质量浓度为200 mg/L的橙黄IV溶液,最佳的吸附剂用量为3 g/L,最佳pH为2,在30 min时可以达到吸附平衡,最大吸附率为96.11%。
(3)NFA对橙黄IV的等温吸附符合Langmuir模型,属于单分子层吸附,理论吸附量最高可达94.76 mg/g,相关系数R2值为0.955。NFA对橙黄IV的吸附过程遵循Pseudo准二级反应动力学模型,在吸附温度为25 ℃条件下,吸附平衡常数k2值为
0.014 min-1,吸附容量Qe值为66.67 mg/g,相关系数R2值为0.996。
