右美托咪定不同时段给药对小儿开颅手术麻醉苏醒质量及炎症反应的影响分析
2024-01-08杨迎春吕红杰史晓燕刘晶晶
杨迎春,吕红杰,史晓燕,刘晶晶
1.北京丰台医院麻醉科,北京 100071;2.中国人民武装警察部队北京市总队医院麻醉科,北京 100027
小儿开颅手术围手术期尤其是麻醉恢复期常出现不配合、烦躁、血流动力学不稳定、恶心呕吐等不良反应[1];易导致颅内高压、再次出血等严重危害,甚至直接致残、致死[2]。主要原因:首先患儿身智发育不全,配合能力差,对气管内导管耐受差,对分离焦虑敏感;其次手术为颅内操作,易致颅内高压,表现出神经精神等方面症状。预防措施主要为镇静下入室、家属陪同入室及苏醒、深麻醉下拔管、麻醉恢复室慢拔管、右美托咪定围手术期应用等[3]。
右美托咪定在小儿开颅手术中因应用时机、应用目的不同而有较大区别:诱导前使用目的主要是术前镇静,方便患儿入室;术中使用目的主要是术中唤醒;术后使用目的主要是桥接术后麻醉恢复室镇静[4-8]。因此在保障麻醉效果的同时,如何维持小儿开颅手术患者麻醉恢复期血流动力学稳定及降低机体炎症应激反应是值得深入研究的问题。鉴于此,本研究选取200例在北京丰台医院接受小儿开颅手术患儿,分别于术前、术中、术后静脉泵注右美托咪定,并以生理盐水作为对照,比较各组患儿的麻醉苏醒质量、炎症反应、血流动力学及不良反应等指标,以期对右美托咪定在小儿开颅手术中应用的具体时机进行研究。
1 资料与方法
1.1 一般资料
选取2017年8月至2022年8月在北京丰台医院接受小儿开颅手术的200例患儿进行研究,采用随机双盲法分为4组。每组各50例。术前组男29例,女21例;年龄1~6岁,平均(4.73±1.07)岁;体质量指数(body mass index,BMI)18~25kg/m2,平均(22.42±1.57)kg/m2;美国麻醉医师协会(American Society of Anesthesiologists,ASA)分级:Ⅰ级18例,Ⅱ级32例。术中组男27例,女23例;年龄1~6岁,平均(4.95±0.85)岁;BMI 17~25kg/m2,平均(22.37±1.62)kg/m2;ASA分级:Ⅰ级17例,Ⅱ级33例。术后组男29例,女21例;年龄1~6岁,平均(4.82±1.08)岁;BMI 18~25kg/m2,平均(22.52±1.38)kg/m2;ASA分级:Ⅰ级16例,Ⅱ级34例。对照组男27例,女23例;年龄1~6岁,平均(4.88±0.82)岁;BMI 17~25kg/m2,平均(21.67±1.36)kg/m2;ASA分级:Ⅰ级15例,Ⅱ级35例。4组患儿的一般资料均符合正态分布且均衡性良好(P>0.05),具有可比性。本研究经北京丰台医院医学伦理委员会审批通过(伦理审批号:2017-03-02),患儿家属均签署知情同意书。
1.2 纳排标准
纳入标准:①年龄1~6岁;②ASA分级为Ⅰ级、Ⅱ级;③于北京丰台医院接受脑室引流术、颅内血肿清除术、脑内肿瘤摘除术、癫痫等手术者。
排除标准:①脑死亡、脑疝晚期、双瞳孔散大者;②术中心跳骤停、心肺复苏者;③上呼吸道感染者;④脑干肿瘤和颅咽管瘤等计划长期保留气管导管者;⑤长期接受催眠药物、麻醉性镇痛药物及抗焦虑药物治疗者;⑥伴有心动过缓、房室传导阻滞者;⑦伴有严重肝、肾等重要脏器功能受损者;⑧伴有精神性疾病者;⑨对右美托咪定过敏者。
1.3 方法
术前组于麻醉诱导前30min静脉泵注0.5μg/(kg·h)右美托咪定(批准文号:国药准字H20090248,生产单位:江苏恒瑞医药股份有限公司,规格:200μg/2ml),手术开始前停药;术中组于手术开始后静脉泵注0.5μg/(kg·h)右美托咪定,手术结束前30min停药;术后组于手术主要步骤结束后静脉泵注0.5μg/(kg·h)右美托咪定,术毕停药;对照组于麻醉诱导前30min泵入同等容量的生理盐水,所有麻醉操作均由同一组麻醉医师执行。具体措施:入室后将中心静脉通路及有创动脉监测开放,密切监测患儿各项生命体征及脑电双频谱指数(bispectral index,BIS)。麻醉诱导:静脉注射0.5μg/kg舒芬太尼(批准文号:国药准字H20054171,生产单位:宜昌人福药业有限责任公司,规格:50μg/ml)、0.04mg/kg咪达唑仑(批准文号:国药准字H19990027,生产单位:江苏恩华药业有限公司,规格:5mg/ml)、2mg/kg丙泊酚(批准文号:国药准字H20010368,生产单位:西安力邦制药有限公司,规格:500mg/50ml)、0.2mg/kg顺苯磺阿曲库铵(批准文号:国药准字H20060869,生产单位:上海恒瑞医药有限公司,规格:10mg/5ml),2min后接受气管插管麻醉机机械通气,将呼吸比设置为1∶2,呼吸频率设为15~22次/min,潮气量设为8ml/kg,呼气末二氧化碳分压(endtidal carbon dioxide tension,PETCO2)维持在30~40mmHg(1mmHg=0.133kPa),吸入氧浓度50%。麻醉维持:靶控输注丙泊酚,血浆靶浓度控制在3~4μg/ml,瑞芬太尼(批准文号:国药准字H20030198,生产单位:宜昌人福药业有限责任公司,规格:1mg/支)的血浆浓度为4~8μg/ml,BIS控制在40~50;术中按1∶1输注羟乙基淀粉(批准文号:国药准字H20103690,生产单位:山东齐都药业有限公司,规格:500ml/袋)、乳酸林格液(批准文号:国药准字H13023036,生产单位:石家庄四药有限公司,规格:500ml/袋),维持中心静脉压(central venous pressure,CVP)在8~10cmH2O(1cmH2O=0.098kPa);心率(heat rate,HR)超过基础值30%给予艾司洛尔(批准文号:国药准字H19991059,生产单位:齐鲁制药有限公司,规格:0.1g/10ml)0.5mg/kg;HR低于基础值30%或低于50次/min给予阿托品(批准文号:国药准字H12020382,生产单位:天津金耀药业有限公司,规格:0.5mg/ml)0.02mg/kg;平均动脉压(mean arterial pressure,MAP)低于基础值30%或60mmHg时,给予去氧肾上腺素(批准文号:国药准字H31021175,生产单位:上海禾丰制药有限公司,规格:10mg/ml)0.05mg/次;MAP高于基础值30%给予盐酸乌拉地尔(批准文号:国药准字H20123353,生产单位:河北一品制药股份有限公司,规格:25mg/5ml)2mg/次;根据术中变化每隔1.0~1.5h对动脉血气进行复查,根据复查结果对潮气量、呼吸频率、电解质进行调节,必要时输注红细胞悬液。完成头皮缝合后停止丙泊酚及瑞芬太尼。术后入麻醉恢复室拔管。
1.4 观察指标
1.4.1 记录4组患儿的Ramsay镇静评分及拔管时间 其中Ramsay镇静评分判定标准:烦躁、不安静计1分;安静合作计2分;嗜睡但可听从指令计3分;睡眠状态但可唤醒计4分;睡眠状态,较强刺激才可反应且反应迟钝计5分;深睡状态,呼唤不醒计6分[4]。拔管标准:①潮气量≥6ml/kg;②呼吸节律正常,呼吸频率≥13次/min;③咳嗽、吞咽反射恢复;④吸空气10min以上血氧饱和度(pulse oxygen saturation,SpO2)>90%;⑤呼之可睁眼。
1.4.2 血流动力学 记录4组患儿麻醉诱导前安静状态下(T0)、拔管即刻(T1)、拔管后5min(T2)的MAP、HR。
1.4 3 炎症反应 于不同时间点取患儿静脉血4ml,离心5min(3000转/min,半径6cm),取上清液用于检测,C反应蛋白(C-reactive protein,CRP)、肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)均采用酶联免疫吸附法测定,仪器选用雅培C8000型全自动生化分析仪;白细胞介素(interleukin)-6利用化学发光免疫分析法测定,仪器选用贝克曼DXI800化学发光分析仪。
1.4.4 不良反应 观察并记录4组患儿是否出现呼吸抑制、心动过缓、恶心呕吐等不适症状。
1.5 统计学方法
采用GraphPad Prism 8.0统计学软件对数据进行处理,计量资料以均数±标准差(±s)表示,总体间比较采用单因素方差分析,组间比较采用Tukey检验;计数资料以例数(百分率)[n(%)]表示,比较采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 Ramsay镇静评分及拔管时间比较
术前组、术中组、术后组患儿T0时点Ramsay镇静评分比较,差异无统计学意义(P>0.05);术前组、术中组患儿不同时点的Ramsay镇静评分及拔管时间比较,差异无统计学意义(P>0.05);术后组患儿T1、T2时点Ramsay镇静评分均比T0时点高,且比同期术前组、术中组、对照组高,拔管时间长于术前组、术中组、对照组,差异有统计学意义(P<0.05),见图1。

图1 4组患儿不同时点的Ramsay镇静评分及拔管时间比较
2.2 血流动力学比较
4组患儿T0时点的MAP、HR比较,差异无统计学意义(P>0.05);术前组、术中组、对照组患儿不同时点的MAP、HR相比,差异无统计学意义(P>0.05);术后组患儿T1、T2时点的MAP、HR均比T0时点低,且比同期术前组、术中组、对照组低,差异有统计学意义(P<0.05),见图2。
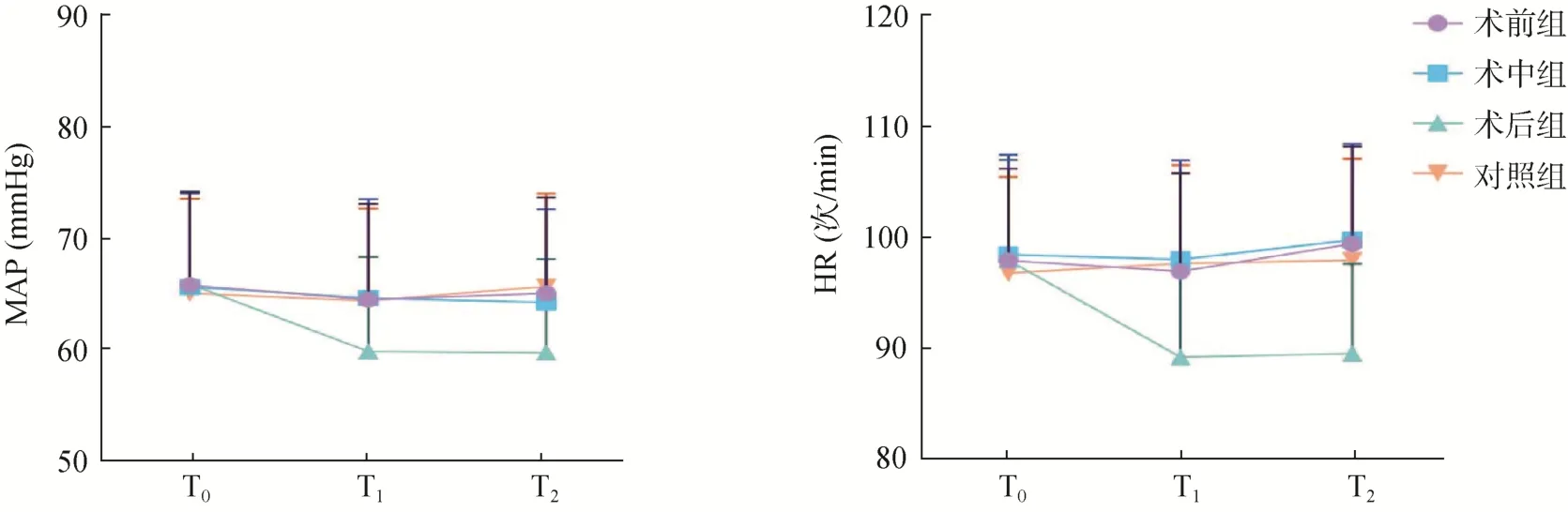
图2 4组患儿不同时点血流动力学比较
2.3 炎症反应比较
4组患儿T0时点的CRP、TNF-α、IL-6比较,差异无统计学意义(P>0.05);术前组、术中组、对照组患儿不同时点的CRP、TNF-α、IL-6比较,差异无统计学意义(P>0.05);术后组患儿T1、T2时点的CRP、TNF-α、IL-6水平均比T0时点高,且比同期术前组、术中组、对照组高,差异有统计学意义(P<0.05)。见图3。

图3 4组患儿不同时点炎症反应比较
2.4 不良反应
4组患儿不良反应总体发生率比较,差异无统计学意义(P>0.05),且及时给予对症处理后症状均缓解或消失,见表1。
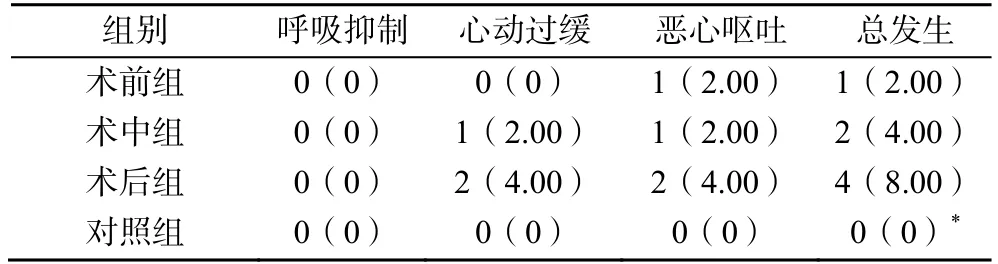
表1 4组患儿不良反应情况比较[n(%),n=50]
3 讨论
正常情况下,脑血管可通过自行调节、改变血管阻力维持脑灌注压在一定范围内,从而维持稳定的脑血流量,但在手术、麻醉、创伤、药物等因素影响下,脑血管自动调节功能逐渐降低或丧失,脑灌注压发生改变,一定程度上破坏血-脑脊液屏障,增高颅内压,损伤脑组织[9]。
右美托咪定具有高效的镇静催眠作用,且患者可被言语刺激唤醒,在镇静催眠过程中无明显呼吸抑制;同时具有降低炎症反应、多器官保护功能,在神经外科、麻醉科、ICU都得到非常广泛的应用[10-11]。右美托咪啶属于高选择性α2肾上腺素能受体激动剂之一,可通过作用于蓝斑核α2受体及激动内源性促睡眠通路发挥镇静催眠作用,使患者维持非快动眼Ⅲ期自然睡眠状态,具有强大的镇静、抗焦虑、降低应激反应等作用[12];其分布半衰期为5~10min,清除半衰期为2~3h。本研究中,术前组、术中组、术后组患儿T0、T1、T2时点的Ramsay镇静评分均比对照组高,可见相比生理盐水,围手术期使用右美托咪定有助于抑制因气管拔管诱发的躁动。术前组、术中组患儿不同时点的Ramsay镇静评分及MAP、HR比较未见明显差异,但术后组患儿T1、T2时点Ramsay镇静评分较高,拔管时间较长,MAP、HR较低,表明在患儿开颅手术的术前、术中右美托咪定对麻醉恢复期血流动力学影响较小,苏醒质量及镇静质量较佳,但术后会延长拔管时间,影响苏醒质量。右美托咪定可抑制气管拔管造成的应激反应机制在于其可选择性地兴奋中枢孤束核突触后α2受体,降低交感神经张力,提高压力感受性反射及迷走神经心脏反射,减少及抑制去甲肾上腺素的释放,进而降低血浆中儿茶酚胺水平,调节血流动力学,降低神经元损伤[13-15]。右美托咪定发挥镇静效果的可能机制[16-20]:①通过G蛋白介导产生3种效应:a.阻碍神经末梢钙离子内流,降低及避免递质的释放,进而促进突触前抑制的产生;b.激活钾离子通道,加快钙离子的外流,导致细胞膜超极化,进而诱发突触后抑制;c.阻碍腺苷酸环化酶及细胞内cAMP聚集。②降低交感神经活性程度,抑制交感神经张力,抑制去甲肾上腺素的分泌及释放,减弱突触后膜的兴奋性,减少中枢交感神经冲动传出。
近年来,随着神经外科手术的不断发展及加速康复外科的普及,对开颅手术麻醉管理也提出越来越高的要求。小儿开颅手术麻醉管理包含术前镇静、术中神经检测、术中唤醒、无呛咳拔管、术后镇静等要点。即使采取优质的麻醉管理、微创的手术操作,小儿开颅手术仍无可避免地造成中枢神经系统损伤,促使大量炎性因子产生,同时破坏血-脑脊液屏障,部分炎症因子可募集外周血中的炎症细胞向中枢神经系统聚集,且血-脑脊液屏障的破坏进一步加重这一进程,最终导致中枢神经细胞受损、死亡,加重脑水肿及颅内炎症反应。CRP是一种炎症反应蛋白,可清除机体坏死组织并清除机体异物,炎症反应早期呈高表达,可作为反映炎症严重程度的指标;TNF-α是中枢神经系统参与机体炎症反应、免疫反应的重要介质,多由活化的巨噬细胞分泌,可诱导细胞因子的生成、聚集及释放;IL-6可破坏血-脑脊液屏障,诱发脑水肿,增加脑损伤程度,参与炎症性损害过程。CRP、TNF-α及IL-6等炎性因子的急性时相反应程度变化与脑组织受损程度呈正相关,可反映继发性脑损伤程度。本研究中,术前组、术中组、对照组患儿不同时点的CRP、TNF-α及IL-6水平比较未见明显差异;术后组患儿T1、T2时点的CRP、TNF-α及IL-6水平均比T0时点高,且比同期术前组、术中组、对照组高,可见术前、术后使用右美托咪定有利于抑制开颅手术患儿的炎性应激反应,改善脑代谢紊乱状态,这归因于右美托咪定可避免因有害刺激而造成的机体交感兴奋,利于激活胆碱能抗炎通路,对神经内分泌反应进行调节,避免过度分泌炎性介质,减低海马组织中凋亡蛋白酶caspase-3含量,进而发挥降低颅内炎症反应的作用。从安全角度而言,术前组、术中组、术后组不良反应总体发生率差异无统计学意义,以恶心、呕吐为主,均未见呼吸抑制,且及时给予对症处理后症状均缓解或消失,可见右美托咪定的用药安全性较高,患者可耐受。
综上所述,于小儿开颅手术不同时段给予右美托咪定均未见明显不良反应,术前、术中给予右美托咪定对麻醉恢复期血流动力学、炎症反应影响较小,苏醒质量及镇静质量较佳,但术后泵注可延长拔管时间。
