水中PFAS吸附去除技术研究进展
2024-01-06包一翔钟金魁李井峰曹志国
王 菟,包一翔,钟金魁,李井峰,曹志国,吴 敏
水中PFAS吸附去除技术研究进展
王 菟1,2,包一翔2*,钟金魁1,李井峰2,曹志国2,吴 敏2
(1.兰州交通大学环境与市政工程学院,甘肃 兰州 730070;2.北京低碳清洁能源研究院,煤炭开采水资源保护与利用全国重点实验室,北京 102209)
总结了不同吸附剂(活性炭,树脂,矿物材料,分子印迹聚合物,生物基材料等)对PFAS吸附性能,机理,影响因素,优势及潜在问题.孔径与PFAS分子尺寸相近,表面带相反电荷的吸附剂对PFAS具有更高的吸附性能.低pH值和高温度的水质条件对PFAS吸附更有利,共存有机物会与PFAS发生竞争吸附.吸附剂对PFAS的吸附性能与其链长呈正相关,在相同链长的情况下,吸附剂对磺酸类PFAS的吸附容量普遍高于羧酸类PFAS.主要的吸附机理包括静电吸引,疏水相互作用,离子交换,配体交换等.吸附剂的合理再生和处置是实际工程应用中重要挑战,如化学再生法和生物再生法再生效果差,热再生法能耗高,溶剂再生,填埋处置易造成二次污染等.通过对水中PFAS吸附去除材料及技术的研究进展进行综述,系统阐述了不同技术的优劣势,并展望了吸附去除技术的发展方向,可为水中PFAS污染控制提供参考.
PFAS;吸附;机理;工程应用;再生;新污染物
全氟或多氟烷基化合物(PFAS)是指有机化合物分子中与碳连接的氢原子全部或部分被氟原子取代而生成的化合物[1-2].PFAS结构中含有亲水性官能团(如磺酸基团和羧基)和疏水疏油性C-F链[2-4],PFAS具有良好的化学稳定性,因此被广泛应用于消防,镀铬,农药,医药,服装,食品等领域[2-3,5-8].目前所发现的PFAS种类有9000多种[9],一些典型PFAS的相关物理和化学性质见表1.全氟辛酸(PFOA)和全氟辛烷磺酸(PFOS)是使用历史最长,检出频率最高的两类PFAS,在人体内的半衰期长达2.3~5.4a[2,10].PFAS对生物体的毒性包括生殖毒性,肝脏毒性,心脏毒性,免疫毒性和神经毒性等[11-14].考虑到PFAS对生态环境和人体健康的危害,PFAS的全球监管力度正在逐年加强.PFOS及其盐类和全氟辛基磺酰氟(PFOSF),PFOA及其盐类和相关化合物,全氟己基磺酸(PFHxS)及其盐类和相关化合物分别于2009,2019和2022年被纳入《关于持久性有机污染物斯德哥尔摩公约》进行管控[2,6].2022年,美国环境保护署发布了饮用水中PFOA,PFOS,全氟(2-甲基-3-氧杂己酸)铵(GenX),全氟丁烷磺酸(PFBS)4种PFAS的健康建议值,分别为0.004,0.02,10和2000ng/L.我国也将PFOA和PFOS加入《生活饮用水卫生标准》(GB 5749-2022)[15],PFOS和PFOA的限值分别为40和80ng/L.但由于短期内缺乏合适的替代品,部分PFAS仍被允许使用.在我国公布的《重点管控新污染物清单》(2023年版)中, PFOS和PFOSF被允许用于生产灭火泡沫药剂,PFOA被允许用于半导体光刻和蚀刻,胶卷涂料,高压电线电缆等领域.水环境是PFAS的主要环境归宿,如何控制和去除水体中PFAS已经成为全球研究热点,亟需经济可行的PFAS处理技术.
现有的PFAS处理技术有微生物法,吸附法,电化学法,热化学,光化学法,膜技术等[16-17].其中生物氧化或生物降解对PFAS几乎没有降解效果[18],电化学降解PFAS可用的电极材料较少且制备成本较高[17].由于PFAS氟代结构,其更易接受电子,且碳氟键键能较高,臭氧和羟基自由基很难彻底氧化PFAS而形成短链PFAS产物[19].超声,微波(热化学),光化学等降解技术获得了一定的研究进展,但这些技术存在能耗高,操作复杂,反应条件苛刻,易产生二次污染等弊端,不利于大规模去除水体中PFAS[17,20-21].
吸附是一种成熟的污染物去除技术[22-24],由于其操作简单,成本低,效率高,被广泛应用于水中PFAS的去除[17,25].常见的PFAS吸附剂有活性炭,树脂,沸石,碳纳米管,针铁矿,壳聚糖和生物炭等[26-27].本文系统归纳了不同吸附剂对PFAS的吸附性能,吸附机理和优缺点等.讨论了影响PFAS吸附去除的关键因素以及吸附剂的再生,处置方法,展望了PFAS吸附去除所面临的挑战和未来重要的研究方向,可为水中PFAS污染控制提供理论参考.
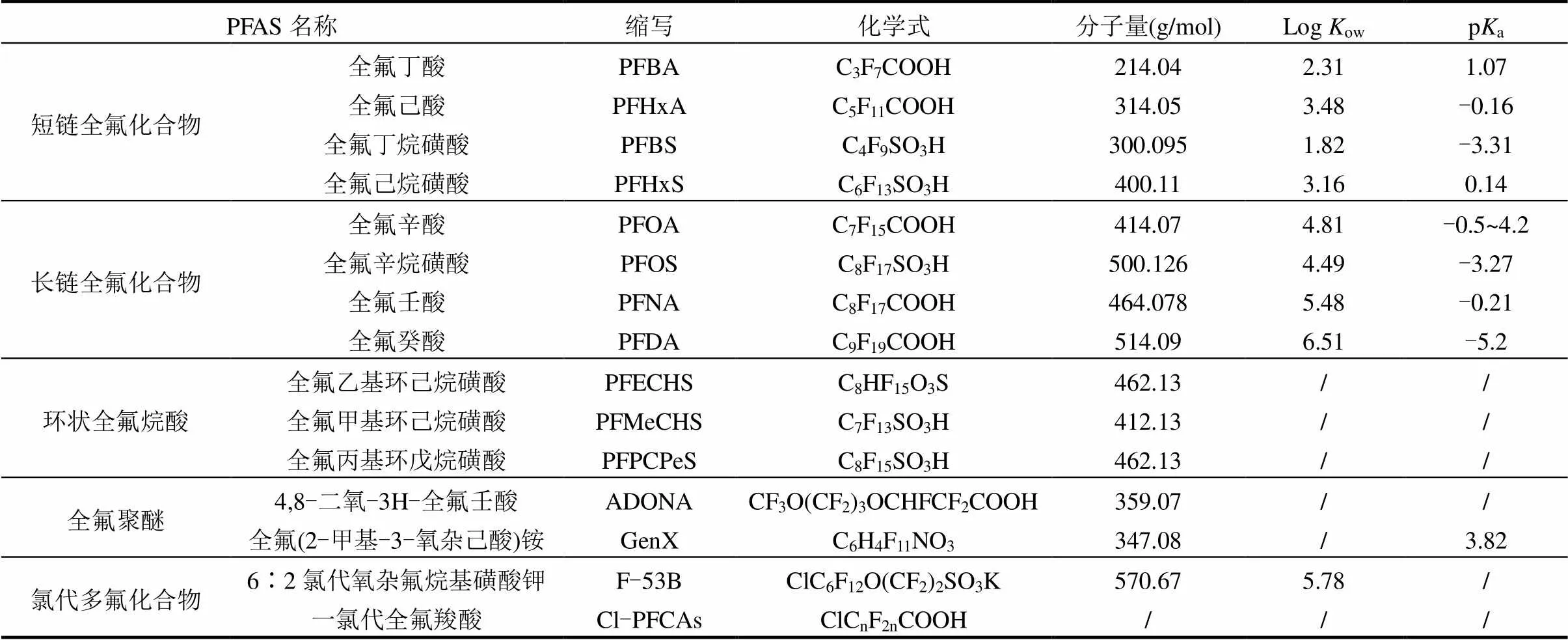
表1 典型PFAS的物化性质[10]
注: Logow为正辛醇/水分配系数对数值,pa为解离常数.
1 吸附技术及优缺点
1.1 活性炭吸附
活性炭是水处理中最常用的吸附剂之一,因其比表面积大,孔隙结构发达,成本低,吸附效果好,制备简单,材料来源广泛而被应用于多种污染物的去除[28],通过适当的改性可以进一步提高对PFAS的吸附性能,但活性炭也存在再生性能较差的缺点[29].
1.1.1 未改性活性炭 活性炭对PFAS具有较高的吸附容量,不同粒度,制备原料的活性炭对PFAS的吸附性能有差异.Du等[30]研究了竹源活性炭(BAC)对实际废水中PFAS(0.10mmol/L全氟己酸(PFHxA), 0.11mmol/L全氟庚酸(PFHpA),0.29mmol/LPFOA)的去除,BAC投加量为1.9g/L,pH=4,吸附平衡时间为48h,PFHxA,PFHpA,PFOA的饱和吸附量分别为15.2, 20.23,61.04mg/g.Ochoa-Herrera等[31]研究了煤质颗粒活性炭(GAC)吸附去除水中PFAS(PFOS, PFOA, PFBS)的效果,PFOS,PFOA和PFBS的饱和吸附量分别为182,57和48mg/g.显然不同原料制备的活性炭对PFAS的吸附性能具有差异性,可能是由于活性炭性质和结构的不同所导致.Yu等[32]对比了粉末活性炭(PAC)和GAC对PFOA与PFOS的吸附性能,发现PAC对PFOA和PFOS的饱和吸附量分别为277.3,518.96mg/g,吸附平衡时间在4h左右,GAC对PFOA和PFOS的饱和吸附量分别为161.46, 184.63mg/g,吸附平衡时间为168h,由于小粒径的PAC比GAC具有更大的比表面积,可以提供更多的吸附点位[33],因此对PFAS的吸附性能更高.
PFAS结构对吸附去除效果影响较大.Rostvall等[34]评估了GAC对不同PFAS的吸附性能,去除率随PFAS碳氟链长度的增加而增加且全氟磺酸的去除效率要高于相同链长的全氟羧酸.Westreich等[35]研究了GAC去除地下水中一系列长链和短链PFAS(全氟丁酸(PFBA),PFHxA,PFBS,PFOA,PFHxS, PFOS)的效果,长链和短链PFAS都能被GAC吸附,吸附能力顺序为PFBA 1.1.2 改性活性炭 传统活性炭对部分PFAS不能有效去除[37],因此通过改性活性炭以提高对PFAS的去除效果和选择性具有重要意义[38].目前已广泛应用化学和物理改性工艺来改变活性炭的表面特征[39],如热处理,微波,超声化学改性氧化还原改性,酸碱改性,负载改性,等离子体改性和电化学改性等[40]. 负载金属改性是较为常用的活性炭改性方法,具有操作简单,成本较低等优点[40].童锡臻等[38]分别用FeCl3及中功率微波对椰壳活性炭进行改性.改性椰壳活性炭与原炭吸附PFOS达到吸附平衡的时间基本相同,均为6h左右.椰壳活性炭经FeCl3及中功率微波改性后对PFOS的吸附量明显提高,原因是椰壳活性炭经微波及FeCl3改性后,BET,中孔比表面积及总孔容,平均孔径显著增大,且酸性含氧官能团减少,碱性含氧官能团增加,有利于PFAS的吸附. 惰性气体,氢气或氨气中高温处理活性炭是一类有效的改性方法[41-43].Saeidi等[44]在900℃的H2中进行热处理以及用乙二胺改性活性炭,得到氨基官能化活性炭和脱官能化活性炭两种改性活性炭,对PFOA,PFOS和PFBA进行吸附实验.三种吸附剂的吸附能力顺序为脱官能化活性炭>氨基官能化活性炭>未改性活性炭,未改性活性炭的等电点为5.9,氨基官能化活性炭为7.3,脱官能化活性炭为9.3.脱官能化活性炭具有足够密度的正电荷来吸附PFAS,其吸附容量提高了40倍.而氨基官能化活性炭表面正电荷的增加并未等效转化为PFAS吸附量的增加,只提升了2倍.这是因为氨基官能化活性炭表面的负电荷密度依旧较高,对PFAS具有一定的静电排斥作用. 浸渍法改性是使一些化合物或金属颗粒分布在活性炭的孔结构中的改性方法[40],苑晨等[45]以椰壳活性炭和木质活性炭两种炭材料作为改性活性炭的母体,3-氯-2-羟基丙基三甲氯化铵(QUAB188)和3-氯-2-羟基丙基烷基二甲基氯化铵(QUAB360)两种季铵盐化合物(QAE)为改性剂制备季铵盐改性活性炭(QAE-AC),通过快速小型柱实验考察QAE- AC对PFOA的吸附性能.1.5g木质活性炭经过4mol/L HNO3浸泡后,投加15.8g QUAB188,在温度50℃,溶液pH值为12.5的条件下,反应48h,得到的QAE-AC对PFOA的吸附效果可达到未改性活性炭的4倍.PFOA主要通过静电和疏水作用吸附在活性炭较小的介孔中,当QAE的分子数量增加,分子间会形成一个网状结构,该结构与活性炭形成一个带正电荷的特殊空间,增强对PFOA的吸附能力. 1.1.3 吸附机理 活性炭吸附PFAS的作用机理包括静电作用,疏水作用,配体交换,氢键,范德华力等[28],其中静电作用和疏水作用占主导地位.疏水作用是PFAS向非极性疏水表面运动而排斥水分子的现象[10].活性炭的疏水性越强,对PFAS的吸附效果越好. 静电作用包括静电引力和静电斥力,PFAS在水溶液中通常以阴离子形式存在,活性炭表面带正电可通过静电引力吸附水中PFAS.因此,活性炭表面所带正电荷的数量是决定PFAS吸附容量的关键因素之一.pH值是影响活性炭表面电荷的主要因素,当水体pH值低于活性炭等电点,活性炭表面发生质子化作用带正电,有利于PFAS吸附,pH值高于等电点则由于去质子化作用而带负电,发生静电排斥作用,不利于PFAS去除.此外,PFAS的离子端基团可通过交换反应吸附到活性炭上,如金属改性活性炭和季铵盐改性活性炭[38,45]. 活性炭的孔径,比表面积和粒度等物理性质会影响其吸附性能.当活性炭孔径与PFAS的尺寸相似时,吸附是有利的[46].Cantoni等[46]研究了8种PFAS(PFOA, PFOS, PFBA, PFBS,全氟戊酸(PFPeA), PFHxA, PFHpA)在4种活性炭(原始椰子基活性炭,再活化椰子基活性炭,原始沥青活性炭,再活化沥青活性炭)上的吸附行为,静电作用是主要吸附机制,在带正电荷活性炭中,孔径分布和微孔表面积对PFAS吸附的影响大于PFAS的疏水性,活性炭中存在大量的中孔(2~50nm)对强疏水性PFAS吸附更有利[46],因为中孔中溶解性有机物(DOM)的孔堵塞较少. Park等[47]研究了4种烟煤基活性炭对9种PFAS (PFOA, PFOS,PFBA,PFBS,全氟癸酸(PFDA), PFPeA, PFHxA,全氟十二酸(PFDoDA),PFHpA)的吸附效果,介孔碳(2~50nm)对长链PFAS的吸附效果比微孔碳(<2nm)好,因为微孔会被长链PFAS形成的胶束或半胶束堵塞,微孔占比较高的活性炭对短链PFAS具有更高的吸附容量[47-48]. 增加活性炭的比表面积以及表面所带正电荷的数量和改变孔隙结构分布是提高PFAS吸附容量的有效方式.活性炭孔隙结构的改变方法有活化过程控制法,热处理法,化学气相沉积法和添加剂法等[49-50],通过调节活性炭孔隙结构,与PFAS分子尺寸相匹配,从而提高活性炭吸附性能.改变表面电荷种类及数量的方式有金属负载和碱处理等[40],如季铵盐改性活性炭,季铵盐通过与活性炭表面的羟基反应负载在活性炭的边缘位点,增加了活性炭表面的正电荷,PFAS与形成含氧官能团的季铵盐结合而被吸附[45].一些通过金属改性的活性炭,金属首先被吸附在活性炭表面的负电荷位点,然后通过金属与PFAS之间的络合力吸附PFAS[51],从而提高PFAS吸附量. 活性炭的经济可行性和较高的吸附性能使其成为去除PFAS的首选吸附剂之一,但吸附PFAS后的活性炭可再生性差.一些研究对吸附PFOS,PFOA后的PAC和GAC使用甲醇,乙醇进行再生,PAC和GAC的再生率分别为75.4%和40%[52-53].而醇溶液对活性炭进行再生可能会产生二次污染等问题[29],不能应用于饮用水处理中吸附剂的再生.此外,活性炭的可重复使用性较差,经过几次再生后,吸附剂的吸附能力会下降[7],对于活性炭的后续处理是值得研究和关注的问题. 树脂包括离子交换树脂和非离子交换树脂,具有吸附效果好,化学稳定性好,交换能力强,可再生能力强,操作简便等优点[28],就吸附性能和原位再生能力而言,阴离子交换树脂被认为是去除PFAS最有效的吸附剂[54]. 1.2.1 未改性树脂 离子交换树脂由树脂基体骨架和骨架上的活性离子基团构成[28],阴离子交换树脂表面具有永久正电荷交换位点,因此对PFAS吸附性能较高[33].非离子交换树脂主要通过疏水相互作用和范德华力吸附PFAS,相较于阴离子交换树脂,它们更容易再生[55],但吸附性能远低于阴离子交换树脂,因此阴离子交换树脂在实际应用中更广泛[2].与其他吸附剂相比,阴离子交换树脂对PFAS有更高的吸附性能[56](表2),Carter等[56]发现树脂对PFOS的吸附平衡时间(10h)远小于传统GAC(50h),且4h后PFOS饱和吸附量达到17.46mg/g,而GAC需要15h才能达到17.46mg/g. 离子交换树脂上交换位点的可用性是影响PFAS吸附的关键因素[7].用于去除水中PFAS的阴离子交换树脂分为两类,分别是强碱和弱碱型阴离子交换树脂[3].具有季铵官能团的被称为强碱型阴离子交换树脂,根据化学结构分为I型(三甲基铵基)和II型(二甲基乙醇铵基)[3],强碱型阴离子交换树脂具有优异的物理和化学稳定性,能够在较宽的pH值范围内交换不同的阴离子.弱碱型阴离子交换树脂以伯胺,仲胺,叔胺或混合胺作为官能团,具有优异的再生能力[3].不同树脂去除PFAS的能力具有差异[57]. Zaggia等[36]考察了A532E(三甲基季胺聚合物,高疏水性),A520E(三乙基季胺聚合物,一般疏水性)和A600E(双功能季胺聚合物,非疏水性)三种阴离子交换树脂对饮用水中PFOS与PFOA的吸附性能, A532E对PFOS和PFOA的饱和吸附量分别为142.1和260.5mg/g, A520E为134.7和210.4mg/g, A600E为125.2和186.2mg/g.树脂的官能团及基体的疏水性在PFAS去除方面起主导作用[33],A532E的疏水性最强,因此对PFAS的吸附性能越高. 树脂对不同PFAS的吸附性能也有差异,Gao等[6]研究了F-53B和PFOS在弱碱型阴离子交换树脂IRA67上的吸附,F-53B和PFOS在IRA67上的吸附容量分别为2396.81和2744.5mg/g.Du等[30]也对阴离子交换树脂IRA67去除PFAS(PFOA,PFHxA, PFHpA)做了研究,去除效果为PFOA>PFHpA> PFHxA.这是由于PFAS结构的不同(官能团,链长等)所导致,全氟化碳链越短,疏水性越弱,吸附容量越低. 注:0为污染物初始浓度,平衡为吸附平衡时间,m为吸附剂饱和吸附量. 1.2.2 改性树脂 传统树脂存在机械强度低,选择性差等缺点[58],一些共存有机物和不同PFAS在树脂上会产生竞争吸附,为改善其吸附性能和吸附选择性,需要对其进行改性.常用的改性方法有氢键改性,接枝改性,磁改性,氟化改性等[58-59]. 氢键改性是先将树脂氯甲基化,然后引入极性基团从而制得氢键型树脂,通过极性基团与吸附质之间形成氢键实现树脂吸附量增加的方法[58].常用的极性基团有酚羟基,胺基,羧基,酰胺基等[60].接枝改性是使一定的单体聚合,在主干聚合物上将分支聚合物通过化学键结合上一种分枝的反应[61],常采用的接枝方法有链转移接枝,化学接枝和辐射接枝等[58].磁性树脂是指将磁性粒子嵌入到树脂中,使其能够沉淀分离,具有吸附效率快,易分离,操作简单等优点[62].Park等[63]研究了磁性离子交换树脂(MIEX)对地下水中的6种羧基和3种磺酸基PFAS(PFBA, PFPeA,PFHxA,PFHpA,PFOA,PFDA,PFOS,PFBS,PFOS支链异构体)的吸附性能.MIEX投加量为15g/L,9种PFAS的饱和吸附量均高于16ng/g,静电作用是主要吸附机制,MIEX易于与水分离,通过10%NaCl溶液再生30min后,几乎完全恢复了MIEX的PFAS吸附量.含氟聚合物具有高耐化学性,耐氧化性和耐热性等优点[64],Dinesh等[65]开发了两种含氟杯芳烃基多孔聚合物(FCX 4-P和FCX 4-BP),研究了对水中PFOA的吸附性能.FCX 4-P具有较快的吸附速率(3.80g/mg•h)和较高的饱和吸附量(188.7mg/g).含氟结构的引入增强了吸附剂与PFOA之间的疏水相互作用,提高了PFOA的吸附速率和吸附容量.此外,该材料再生效果较好,PFOA可以通过甲醇洗涤而解吸且吸附剂没有显著性能损失. 为了提高树脂对PFAS的选择性,一些PFAS专用树脂开始生产,如A592E(大孔树脂)和PFA694E(凝胶树脂)[66]可有效地靶向阴离子PFAS,包括一些短链PFAS[67-68].但这些PFAS专用树脂制备成本较高且再生效果较差,如何降低经济成本,以及安全有效再生树脂和处理再生液是值得关注的问题. 1.2.3 吸附机理 离子交换是树脂吸附PFAS的主要机理[2],此外还包括静电作用,疏水作用,团聚和胶束等[33](图1). 在阴离子PFAS和带正电的树脂之间可以形成静电吸引作用[61].PFAS的离子端可通过离子交换吸附在阴离子交换树脂上.离子交换点位由树脂上的正电基团提供,如强碱性基团季胺基(-NR3OH,R为碳氢基团)和弱碱性基团伯胺基(-NH2),均可在水中解离出OH-,正电基团与PFAS吸附结合,从而发生离子交换作用. 图1 离子交换树脂吸附PFAS机理[69] Senevirathna等[53]研究了低浓度PFOS(100~ 1000ng/L)在离子及非离子交换聚合物,GAC上的吸附效果,GAC可在4h达到吸附平衡,远远快于非离子交换聚合物,但GAC对于PFOS的吸附量却远低于聚合物吸附剂,原因是离子交换聚合物与PFOS之间通过离子交换形成的化学键要强于GAC与PFOS之间的静电吸引作用. 在离子浓度较高的情况下,疏水作用在PFAS吸附中占主导地位[70], PFAS可以克服静电斥力通过疏水作用吸附到带负电的吸附剂表面[71-73].胶束和半胶束的形成也会影响PFAS的吸附,PFAS浓度达到一定程度时可在溶液中形成半胶束,当PFAS聚集到吸附剂表面时,较拥挤的空间使得表面比溶液中PFAS的浓度更高从而形成胶束[2,32,74].Du等[2]提到胶束和半胶束的形成可增强PFAS在带正电表面上的吸附,但是可能会阻碍PFAS扩散到吸附剂的微孔中,导致吸附容量降低.此外,树脂表面的官能团可以与PFAS的离子端基团形成内球络合物,进而去除PFAS[69].PFAS也可通过官能团中所含的氧原子与树脂官能团中的氢原子键合形成氢键被去除[69]. 矿物材料如活性氧化铝,二氧化硅,沸石和蒙脱石等[2]也被用于去除PFAS,它们具有高表面积,可调的中孔,可变的层状结构,高吸附能力和较好的可重复使用性[75].但也存在稳定性和选择性较差等缺点[76]. 1.3.1 未改性矿物材料 用于去除PFAS的矿物材料分为层状黏土矿物(高岭石,蒙脱石等)和非结晶黏土矿物(针铁矿,磁铁矿,赤铁矿等)[76].不同矿物材料对PFAS的吸附性能具有差异.Ochoa-Herrera等[31]研究并比较了三种具有不同Si/Al比的八面沸石,即13X沸石(Si/Al=2.8),NaY(Si/Al=5.5)和NaY80(Si/ Al=80)对于PFOS的吸附性能.Si/Al比较高的NaY80型沸石对PFOS具有更强的吸附作用,原因是疏水作用在沸石吸附PFOS过程中占主导地位,而二氧化硅含量是决定沸石疏水性的关键参数[31],因此高硅沸石NaY80对PFOS的吸附能力最高.Johnson等[77]研究了高岭石,渥太华砂,合成的针铁矿,高铁沙对PFOS的吸附性能.材料中的硅,铝和氧化铁对PFAS吸附的贡献较少.各材料对PFOS的吸附能力如下:针铁矿<高岭石<高铁沙<渥太华砂.当pH值升高,PFAS饱和吸附量随着高铁沙表面负电荷的增加而增加,而随着针铁矿和高岭石表面负电荷的增加而下降.静电作用的主导地位在不同材料上PFAS的吸附中是相反的.此现象的解释需要研究其他机制.一项研究[78]中公布了PFOS在污水处理厂污泥中的固液分配系数(Kd),该值(120)比Johnson等[77]研究材料的固液分配系数值(2.81~35.3)大一个数量级.PFOS更倾向于吸附在有机碳含量较高(53%)的污泥上.Jeon等[79]也发现了此现象,PFAS的饱和吸附量随黏土矿物表面有机碳含量的增加而增加,原因是当有机碳浓度较高时,疏水作用是PFAS吸附的主要驱动力.而当有机碳不存在时,静电吸引可能占主导地位. 氧化黏土矿物如金属氧化物(Al,Fe,Si氧化物)和勃姆石也被用于去除水中PFAS.Tang等[27]研究了不同溶液组分下PFOS在针铁矿和SiO2上的吸附行为,PFOS在针铁矿上的吸附量随H+和Ca2+增加而增加,原因是PFAS与带正电针铁矿表面之间的静电引力增强,且与针铁矿表面离子形成配体络合物.而PFOS在SiO2上的吸附几乎不受溶液pH值和Ca2+离子强度的影响,原因是该吸附过程中一些非静电作用力占主导地位.Gao等[80]研究了纳米级赤铁矿(Fe2O3)对PFOS和PFOA的吸附,在低pH值下(pH=3),Fe2O3对PFOS和PFOA具有较好的去除效果,除静电相互作用外,PFOA通过配体交换形成了内层羧酸铁络合物,而PFOS与矿物表面形成氢键,最后形成了外层络合物.勃姆石以水合氧化铝的形式存在于土壤中,由于其比表面积高,具有可变的表面电荷,也被用于PFAS去除.静电作用是其去除PFAS的主要机制,因此去除效果较为依赖pH值[81]. 1.3.2 改性矿物材料 天然矿物材料稳定性和选择性较差,为了提高其选择性,稳定性,吸附效果和表面功能性[76,81-83],需通过物理化学手段对矿物吸附剂进行改性,矿物材料常用的改性方法有酸碱活化,热处理,多羟基阳离子柱化,聚合物和表面活性剂改性等[76]. 通过物理吸附,化学接枝,离子交换等方式向矿物材料的层间空间添加聚合物可以改善矿物材料的吸附性能[76].常用的聚合物有聚氯乙烯,聚酯,环氧树脂,聚氨酯,聚丙烯,壳聚糖和聚苯乙烯[84].Bhattarai等[85]使用二氧化硅与β-环糊精聚合物交联,通过氢键的形成增强对PFAS的吸附能力,PFOA去除随着β-环糊精聚合物负载量的增加而增加,饱和吸附量为33.3μg/g.此外,一些表面活性剂也被用来改性矿物材料,周琴等[21]研究发现,负载在蒙脱石上的阳离子表面活性剂(蒙脱石负载阳离子表面活性剂会进入结构内层,增加层间空间,从而增强对PFOS的吸附能力.Du等[82]采用阳离子型含氟表面活性剂交换法制备了新型含氟蒙脱石(F-MT),研究了对水中PFOS和PFOA的吸附性能,由于氟的电负性大以及原子半径小,其极性很低,主链中氟原子由于相邻氟原子的相互排斥沿碳链作螺旋分布包裹住了碳链,使其他原子难以嵌入[86].此外,原子间共用电子对偏向于氟原子,形成一层负电荷保护,因此C-F链不仅疏水疏油而且对其他化合物具有一定排斥性[87].基于相似相溶原理, F-MT对低浓度(<10μg/L)的PFOS和PFOA具有较高的吸附性能和选择性(在苯酚,菲,十二烷基苯磺酸钠的存在下,PFOS和PFOA的吸附基本不受影响). 纳米金属氧化物是较为典型的矿物吸附材料,其表面官能团会在PFAS与金属阳离子之间发生桥接效应[76].金属氧化物的稳定性较差,Gong等[88]发现磁铁矿(Fe3O4)纳米粒子可以被淀粉稳定以防止团聚并保持高表面积,淀粉稳定的磁铁矿纳米颗粒的BET表面积(8.21m2/g)远高于未稳定的磁铁矿(3.98m2/g),使PFOA吸附量提高了2.4倍. Mancinelli[89]采用间歇吸附和同步辐射X射线粉末衍射(XRPD)相结合的方法研究了不同硅铝比的Y型分子筛(FAU型)对PFOA和PFOS的吸附性能.Y390对PFOA和PFOS的饱和吸附量分别为43和17mg/g,AgY390为62和32mg/g,吸附性能高于单一沸石材料,原因是Y390和AgY390与沸石骨架中的氧原子强烈相互作用形成氢键,增强了对PFAS的吸附.此外,在沸石上引入Ag+可以将防污和吸附相结合,协同去除PFAS. 复合材料是PFAS吸附去除技术的重要研究方向.碳质吸附剂被广泛应用于水中PFAS去除,但是其解吸率较高[90],Supriya等[91]考察了氧化石墨烯(GO),氧化铁改性还原GO复合材料(FeG)和活性炭/粘土/氧化铝基吸附剂(RemB)对PFOA的吸附性能.RemB对PFOA的吸附性能比GO高1.5倍(pH= 7.9),原因是RemB去除PFOA的主要作用机制为疏水相互作用和配体交换作用,受到pH值影响较小,而GO去除PFOA的机理主要是静电作用,在研究的pH值范围(3~9)内,GO表面带大量负电荷,不利于PFOA吸附. 1.3.3 吸附机理 静电相互作用,疏水相互作用和配体交换是矿物材料吸附PFAS的主要吸附机制[81].PFAS的吸附机理由天然或改性矿物材料的物化特性决定,且受水质条件影响,如pH值和离子强度,此外,天然有机物和温度等因素也会影响PFAS的去除[81]. pH值是从水中去除PFAS的关键影响因素,溶液pH值可以通过改变PFAS的形态和矿物材料的表面电荷而影响PFAS的吸附.如天然高岭石和蒙脱石的等电点分别为3.2和2.0[92],pH值高于其零电点时,矿物表面所带负电荷增加,而PFAS在水溶液中的阴离子形态,导致天然高岭石和蒙脱石对PFAS的吸附性能较低[81]. PFAS与疏水性表面活性剂改性的矿物材料之间会产生疏水作用[82].此外,一些疏水性有机物会与PFAS竞争吸附位点,造成PFAS的吸附量降低[93]. 以生物质为原料通过一系列的物化改性制备的生物基吸附材料具有来源广泛,易得,成本低廉等优势[102].常用的生物基材料有生物炭,壳聚糖以及一些基于生物提取,合成的材料. 1.4.1 未改性生物基材料 生物炭和壳聚糖是去除PFAS应用较多的生物基材料.生物炭与活性炭对PFAS具有相近的吸附性能,由于生物炭更具有环保性,近年来生物炭逐渐成为活性炭的可持续替代品[30].Wei等[103]将底泥和玉米秸秆生物炭(0%,2%和5%)混合,考察了生物炭含量对底泥吸附PFOS和17α-乙炔雌二醇(EE2)的影响,有机碳浓度是影响吸附过程的主要因素,EE2和PFOS在底泥上的吸附速率和吸附容量在添加生物炭后提高了1.7~3.5倍.原因可能是生物炭的添加降低了PFOS和EE2的迁移率,底泥中的腐殖酸通过电荷转移与PFOS中的供电荷基团形成了络合物.Palau等[104]研究了6种生物炭(树皮,桉树,甘蔗渣,蓖麻粗粉,椰壳和水葫芦)对7种PFAS(PFHxA,PFOA,全氟壬酸(PFNA),全氟十二烷酸(PFDoA),PFHxS,PFBS,PFOS)的吸附,12~24h内达到吸附平衡,由于初始溶液固液比较高(40g/L)且PFAS浓度较低(400 μg/L),因此等温吸附过程呈线性,PFAS的吸附机制主要为疏水相互作用,受水质条件(pH值,二价阳离子等)影响较小. 壳聚糖含有大量的氨基,乙酰氨基,伯羟基和仲羟基,使其成为PFAS的优良螯合位点,在PFAS污染水修复领域具有巨大的潜力[98].壳聚糖小球的成本介于活性炭和树脂之间,吸附PFAS的过程受pH值影响较大,交联的壳聚糖小球在pH=3下对PFOS具有很大的吸附量,甚至高于阴离子交换树脂[105],当pH=9.5时,壳聚糖小球对PFOS的饱和吸附量仅有359.28mg/g[106].Zhang等[107]以交联壳聚糖微球为吸附剂,研究了其对水溶液中PFOS的吸附性能,PFOS的饱和吸附量达到2744.5mg/g,吸附对pH值环境具有高度依懒性,在pH=3时吸附效果最佳,静电作用,疏水作用,胶束和半胶束的形成是壳聚糖吸附PFAS的主要吸附机制.其他生物基材料也被广泛用于去除水中PFAS,Militao等[108]研究了集成辣木(MO)种子粉的海藻酸钙珠对PFAS的吸附.在30min内达到平衡,其对PFOS具有较高的饱和吸附量(941.7 µg/g).吸附机制主要是疏水作用和氢键作用.Katinka等[109]利用污泥生物炭从水中去除PFAS,并比较了两种污泥生物炭(脱水污泥和厌氧消化污泥)和木质生物炭对PFAS的吸附性能,脱水污泥对PFAS的去除率与木质生物炭相近,厌氧消化污泥对PFAS的吸附性能低于木质生物炭.原因是脱水污泥的C/H比(0.04)和C/N比(26)较低. 新型生物基材料被开发用于PFAS吸附去除,Xin等[110]合成了一种新的吲哚衍生物—双吲哚十六烷基铵(DIHA),它能形成稳定的纳米球,优先选择性吸附水中的PFAS.还表现出极快的吸附速率和高饱和吸附量(764~857mg/g).这归因于纳米球超细粒度(亚纳米级),提供了大量比表面积,缩短了PFAS的扩散距离.植物蛋白可以提供疏水位点和氢键位(在氨基酸和谷氨酸的侧链)去除PFAS,Turner等[111]研究了6种不同的蛋白质(蛋白粉,大豆分离蛋白,羽扇豆和豌豆分离蛋白,鸡蛋,乳清)从污染的地下水中去除PFAS的能力,在不到1h内,PFOS和PFHxS的饱和吸附量为91.69和30.25 μg/g.PFAS与蛋白质疏水位点的结合以及与氨基酸之间形成氢键是主要的吸附机制. 1.4.2 改性生物基材料 传统生物基材料稳定性差,难以从水中回收,因此需要通过改性提升其吸附性能,常用的改性方法有金属掺杂,材料包覆和表面基团改性等[98].Elanchezhiya等[98]使用还原氧化石墨烯改性铁酸锌固定化壳聚糖珠(rGO-ZF@CB)从水中吸附PFOA和PFOS.PFOA和PFOS的饱和吸附量分别为16.07和21.64mg/g.静电吸引和疏水作用是主要吸附机制,rGO-ZF@CB可以通过外加磁源进行回收.Rodrigo等[112]研究了9种PFAS(PFOS, PFOA, PFBA,全氟辛烷磺酰胺(PFOSA), GenX, PFHxS, PFPeA, PFHxA和PFHpA)在商业花旗松生物炭(BC)及Fe3O4改性BC(Fe3O4-BC)上的吸附, Fe3O4-BC对PFOA和PFOS的吸附速率和吸附容量最高,在天然水的pH值范围(6~8)下,20~45min达到吸附平衡,PFOS和PFOA的饱和吸附量分别为14.6和652mg/g,疏水和静电作用以及与Fe3+或Fe2+形成络合物是主要的PFAS去除机制.Hassan等[113]制备了赤泥改性木屑生物炭和未改性木屑生物炭,考察了对水中PFOS的吸附性能,在赤泥改性木屑中发现了不同的金属氧化物,如磁铁矿,铁水化物和脱硅产物.在pH=3下,改性生物炭和未改性生物炭对PFOS的饱和吸附量分别为194.6和178.6mg/g.改性木屑生物炭表面具有丰富的质子化金属官能团,通过静电作用和离子交换作用增强了对PFOS的吸附. 使用新型包覆材料改性生物基材料成为研究热点,Verma等[114]通过戊二醛交联壳聚糖和β-环糊精制备了一种聚合物吸附剂(Chi-Glu-β-CD),并考察了对水中PFBS的吸附性能.饱和吸附量为135.7mg/g,主要吸附机制为质子化的胺与阴离子PFBS间的静电吸引作用,此外,PFBS通过与β-CD空腔形成包合物被去除.Chi-Glu-β-CD可用甲醇进行再生,经4次循环再生后,吸附性能无显著变化.基于β-CD吸附剂,Wang等[115]研究了一种新的β-CD聚合物平台,将苯乙烯基团共价连接到β-CD上,形成易于自由基聚合的独立单体,得到具有高比表面积和高分离产率(>93%)的β-CD聚合物.对水中初始浓度为1 μg/L的8种PFAS的去除率接近100%. 1.4.3 吸附机理 静电作用和疏水作用是生物基材料吸附PFAS的主要机制,由于PFAS的低pKa,在水溶液中一般为阴离子形态,吸附剂表面的一些官能团在一定pH值下质子化会吸引阴离子PFAS.此外,一些极性官能团如-NH和-OH会对PFAS产生离子-偶极作用[94].当疏水作用力为主导吸附机制时,PFAS可以克服静电排斥力,通过疏水作用力吸附到带负电荷的吸附剂表面[71-73,116]. 经过改性的生物基材料,例如金属氧化物改性材料,作用机制还包括配体交换,氢键等.PFAS具有疏水性,因此难以与吸附剂官能团中的氢原子结合形成氢键[117],但是PFAS的官能团中所含的氧原子可以成为吸附剂官能团形成氢键的受体[80,118-119]. PFAS可以通过电荷辅助氢键与吸附剂表面的含氧官能团相互作用[120],若吸附剂中含氧或含氮基团的pa值与PFAS的pa相近,则电荷辅助氢键会比正常氢键强得多[120-122]. 分子印迹技术是一种制造分子锁以匹配分子钥匙,创建分子印迹聚合物(MIP)的技术(图2),其具有与模板分子形状互补的定制结合位点,大小和功能组.MIP由于其独特的结构,可预测性,识别特异性和应用普适性等特点,在各个领域得到了广泛的应用.废水中含有大量的化合物和胶体,且这些共存物质浓度普遍比PFAS高,易与PFAS发生竞争吸附,导致去除率下降.因此,吸附的选择性对于去除水中PFAS很重要[123]. 图2 分子印迹技术原理图[125] 为了提高对PFAS的选择性吸附,一些研究通过分子印迹技术制备了对 PFAS 具有高选择性的MIP.Deng等[97]使用环氧氯丙烷交联的壳聚糖和乙二醇二甲基丙烯酸酯交联的 4-乙烯基吡啶制备了两种新型 MIP吸附剂,考察了MIP吸附剂对PFOS的吸附选择性,以2,4-D为竞争阴离子对PFOS进行吸附.2,4-D浓度为2.26mmol/L,MIP吸附剂对PFOS的吸附量下降不大.与非印迹聚合物(NIP)相比,MIP吸附剂对PFOS的吸附量在平衡浓度低于0.25mmol/L时增加了1倍以上.原因是MIP吸附剂对PFOS的选择性较强,而NIP吸附剂由于竞争吸附导致吸附量下降.林森等[124]以Fe3O4为内核,水作溶剂,利用多巴胺作为交联剂.多巴胺中的氨基和羟基作为双功能单体,通过一步聚合制备超顺磁性核壳型的Fe3O4@MIPDA微球.考察Fe3O4@MIPDA对PFOS的吸附性能,饱和吸附量为71.421mg/g.在PFHSK和F-53B共存下,PFOS吸附量显著下降,原因是PFHSK和F-53B与PFOS结构相似,对Fe3O4@MIPDA选择性影响较大. Yu等[12]以油茶籽壳为碳源,PFOS为模板,间苯三酚为助剂,采用一锅水热法合成了印迹碳微球(MIC).研究了PFOS在PFOS-MIC和相应的非印迹碳微球(NIC)上的吸附特性,NIC和PFOS-MIC在20°C时的饱和吸附量分别为2.93和5.38mg/g. PFOS-MIC对PFOS具有良好的吸附选择性(PFOS-MIC对PFOS的相对选择性系数大于1).MIP吸附剂用于PFAS去除的研究仍然较少,且具有PFAS相似分子大小,结构和官能团的竞争性化合物仍然会降低MIP的选择性[2,126]. MIP的合理设计需要将PFAS分子的结构和特性与相应的材料相匹配,基于PFAS分子特性的更精细设计将会是未来的研究方向. 其他常见吸附剂主要有金属有机框架(MOF),共价有机框架(COF),人工合成物等.COF是一种新兴的结晶多孔材料,通过坚固的共价键将有机分子结构单元连接在周期性网络中[127], MOF是一类通过金属离子或团簇单元与有机配体的配位组装而成的具有三维周期无限网状结构的配位聚合物[128].与传统吸附剂相比,它们具有显著增加的表面积,结构可调性和更多的的改进选择性[7]. MOF和COF作为新一代吸附剂,近年来被用于去除水中的PFAS[39].Yang等[103]研究了PFOA在铁基MOF(MIL-100-Fe和MIL-101-Fe)上的吸附,吸附机理包括π-CF相互作用,Lewis酸/碱(LAB)络合,氢键和阴离子-π相互作用.当PFOA浓度>1000mg/L时,MIL-101-Fe的饱和吸附量(370mg/g)高于MIL-100-Fe(349mg/g),原因可能是MIL- 101-Fe(三角形孔结构)较于MIL-100-Fe(六边形孔结构)有更多的吸附位点,因此对PFOA的吸附容量更高.Chang等[129]制备了一种新型金属有机骨架材料MOF-808,并研究了MOF-808对水中PFOS的吸附性能. MOF-808具有高比表面积(1610m2/g),在不同pH值水介质中,其结构可以稳定7d.MOF-808对PFOS的吸附在30min内达到平衡,在pH值为4.1~5.4时,饱和吸附量为939mg/g,吸附机制主要为静电相互作用,当pH>7时,吸附量逐渐降低.Hu等[130]制备了DUT-5-2等6种金属有机骨架材料,测定了它们对PFOS和PFOA的吸附性能.DUT- 5-2对PFOS的饱和吸附量为145.4mg/g,原因可能是采用微波辅助法提高了DUT-5-2的比表面积(1840m2/g).Ji等[131]将不同密度的胺官能团结合到亚胺连接的COF的孔隙中,同时保持高表面积(³1000m2/g),研究其对GenX的吸附性能.胺功能化的COF对GenX具有较高的吸附速率和亲和力.在胺功能化亚胺COF中,20%[NH2]-COF在高浓度GenX下具有最大吸附量,28%[NH2]-COF对GenX吸附表现出最快吸附速率.吸附机制主要是极性基团和疏水表面的协同作用.MOF和COF的应用仍然存在局限性,例如在极端条件下稳定性低,工艺复杂以及合成成本较高等[7]. 2.1.1 粒径的影响 吸附剂粒径会影响PFAS的扩散速率,一般来说,粒径越小,PFAS的扩散速率就越快[29],对于大颗粒吸附剂而言,堵塞和位阻作用更为明显[2],因此去除速率要低于粒径小的吸附剂.Yu等[32]通过伪二级吸附动力学模型拟合发现,PAC吸附水中PFOS和PFOA的性能高于GAC,吸附平衡时间短,饱和吸附量更高.比表面积相同条件下,PAC (<0.1mm)对PFOS和PFOA的吸附能力几乎是GAC(0.9~1mm)的两倍[2,29].孙博等[132]发现,研磨前后PAC(11μm)与超微粉末活性炭(S-PAC)的比表面积变化不大,但在相同的投加量(15mg/L)下,粒径更小的S-PAC(1.2μm)对0.5μg/L的PFHxA的吸附速度比PAC更快,饱和吸附量没有明显差异.Wu等[133]采用3种不同的活性炭材料和2种不同的β-环糊精聚合物对20种PFAS进行了吸附实验,粒径与PFAS去除速率之间为负相关,同种吸附材料,粒径小的吸附速率更快.而速率与粒径之间的关系建立在同种类型的吸附剂上,不同类型吸附剂的粒径与PFAS扩散速率相关性并不强[33]. 2.1.2 孔径的影响 吸附剂的孔径会影响PFAS的扩散速率,对不同分子大小PFAS的吸附具有差异性.树脂按孔径可分为普通树脂(4~6nm),凝胶型脂(<3nm)和大孔型树脂(10nm左右).活性炭的孔隙结构可以大致分为小于2nm的微孔,2~50nm的中孔和大于50nm的大孔[29].Chen等[48]制备了具有微介孔结构的聚丙烯腈纤维衍生活性炭,通过不同PFAS的吸附实验表明,分子量较大的PFAS更难扩散到吸附剂的微孔和中孔中.在Park等[47]的研究中得出了相似的结论,在带正电荷的活性炭中,微孔(<2nm)占比较高(80%)的活性炭对分子量较小的PFAS(PFBA, PFBS,PFPeA)吸附能力较高,而介孔(2~50nm)占比较高(58%)的活性炭对分子量较大的PFAS(PFOA, PFOS,PFDA)吸附能力比微孔炭强.在Cantoni等[46]的研究中解释了此现象,分子量较大,链长较长的PFAS堵塞微孔的程度较高,当活性炭孔径和PFAS大小相似时,吸附是较为有利的.Deng等[26]研究了6种阴离子交换树脂对PFOS吸附的影响,大孔树脂(聚丙烯酸树脂>10nm)比凝胶型树脂(聚苯乙烯树脂 <3nm)具有较高的吸附速率,原因是凝胶型树脂形成的微孔(<2nm)较多,不利于PFOS的吸附.Deng等[134]采用KOH活化法制备具有更大孔径的竹基GAC,KOH/C质量比为2时制得的GAC主要孔径分布小于2nm,KOH/C比值为6时制备的活性炭孔径增大到约4nm.对PFOS和PFOA的饱和吸附量也有所增加,这说明孔径的增加有利于PFOS和PFOA的吸附.Pauletto[135]研究了商用活性炭(BAX),炭黑(BP2000)和以锌为基础的金属有机骨架(UiO-66)对PFOS的吸附性能.它们的孔径分布不同,UiO-66主要为微孔(<2nm),BAX主要为微孔(<2nm)和介孔(>2nm),BP2000中以介孔(>2nm)为主.BP2000,BAX和UiO-66的PFOS饱和吸附量分别为0.81,0.55和0.38mg/g.比表面积增加的顺序为UiOe66 2.1.3 表面官能团的影响 PFAS的吸附受到吸附剂表面化学性质影响,如表面电荷,表面官能团种类,杂原子等[29].静电作用是去除水中PFAS的主要作用之一,吸附剂表面所带电荷是影响静电作用的关键因素之一.PFAS的pKa较低(表1),在水中通常以阴离子形态存在,表面带正电的吸附剂对PFAS的吸附性能更高. 含有不同官能团的同种吸附剂,对PFAS的吸附能力存在明显的差异[2].Punyapalakul等[95]发现具有不同表面官能团的同种二氧化硅之间存在明显的区别.一般情况下,吸附剂所含有的碱性基团越多,对PFAS的吸附能力就越强[26],这是由于碱性基团更容易被质子化带正电,从而有利于对阴离子PFAS的吸附[99],可以通过调节吸附剂表面碱性基团的含量来提高吸附性能.PFAS在交联壳聚糖珠,季铵化棉,胺化稻壳和坡缕石等胺改性材料上的高吸附量也与吸附剂的表面化学性质密切相关,羟基,羰基和含金属基团有助于PFAS的吸附[32,100,136-137].此外,亲水性或极性官能团有利于PFAS扩散到多孔材料中,从而提高PFAS吸附量[26,138]. 吸附剂表面的某些有机官能团或有机物通过疏水作用在一定程度上增强了PFAS的吸附[29,139],这一原理已被用于改性吸附剂提高对PFAS的吸附性能.Jeon等[139]用河水中的天然有机物单宁酸(TA)以及腐殖酸(HA)涂覆矿物材料,研究了矿物和沉积物在PFAS吸附方面的差异以及有机物的作用,矿物材料对PFAS的吸附与其有机碳含量密切相关,由于污泥不仅含有原始的有机和矿物质成分,而且含有生成的生物质和蛋白质,其有机成分对吸附过程也有显著影响[73,140].此外,吸附剂表面存在的杂原子和化合物也可以与PFAS形成较强的结合力,从而提高吸附剂的吸附性能[141]. 2.2.1 pH值 溶液pH值会对吸附剂带电种类, PFAS存在形态等溶液环境造成影响.溶液pH值低于吸附剂的等电点时,吸附剂的表面带正电荷,吸附剂和PFAS之间的静电吸引作用会增强[142].Yu[125]的研究表明,相对于中性环境,活性炭在pH值为3的酸性条件下对PFOS和PFOA的吸附量更大.原因是活性炭的等电点在7以下,酸性条件下活性炭表面基团质子化,正电荷数量增加.Du等[30]利用自制的竹基活性炭在pH值为2.0~9.0的条件下对PFOSF洗涤废水中的PFHpA和PFOA进行去除,当pH值从2.0增加到4.0时,竹基活性炭对PFHpA和PFOA的去除率迅速下降,但在pH值高于5.0后趋于稳定,原因是PFHpA和PFOA与活性炭之间的静电引力减弱,疏水相互作用在吸附过程中逐渐起主导作用. 当溶液中存在一定量的阳离子例如Ca2+或Mg2+时,当pH值增加时,吸附剂表面形成更多的碱性位点以结合阳离子,这时阳离子可以通过桥接效应增加对PFAS的吸附(图3)[116,140,143].Buckley等[144]在0~100mmol/L的钠离子浓度范围内进行了PFAS吸附实验,与不含任何阳离子的测试相比,在NaCl存在下,特别是在10mmol/L和更高浓度下,PFAS的去除速率更快且PFAS的去除率随着盐浓度增加而增加.原因是Na离子的加入降低了稳定气泡形成的最小表面张力,且抑制了表面活性剂头基之间的静电双层排斥作用. 图3 二价阳离子和有机物影响PFAS吸附的机制[69] pH值会显著影响吸附剂的吸附性能[145],可在宽pH值范围内工作的吸附剂是研究热点.一些相对不依赖于pH值(例如pH值为4~9)的吸附剂已被报道[2].Chang等[146]在pH值为9~11下共沉淀制备煅烧水滑石(CHT)并研究了对PFOA的去除.CHT对PFOA的饱和吸附量高达1587mg/g,由于CHT具有稳定的带正电的表面,使得PFOA吸附具有较高的去除速率且不依赖于pH值(pH值为4~12的影响较小).尽管目前pH值对吸附PFAS的影响研究较为丰富,但实验室中主要模拟的低pH值环境与实际水体差异较大,对实际水处理应用还待研究. 2.2.2 温度 温度对PFAS吸附具有显著的影响,包括PFAS吸附反应的吸放热和溶液中分子的扩散速率.PFAS的吸附自由能∆G在多数情况下为负,表明PFAS吸附过程多数是自发进行的.孙建强[147]等利用微波改性膨润土吸附PFOS,发现吸附过程是吸热反应,升温有利于吸附,∆S为正值也表明PFOS的吸附过程是由熵驱动而不是焓驱动[146,148].许晨敏[149]研究了温度对盐态聚苯胺纳米管(PASNTs)和基态聚苯胺纳米管(PABNTs)吸附PFOA和PFOS的影响,PFOS和PFOA的吸附量随温度的升高而上升. 温度也会影响PFAS在吸附剂中的扩散速率.温度越高,PFAS的扩散速率越快,导致吸附速率加快.温度对PFAS的影响也存在一定界限,Qu等[150]研究发现,活性炭对PFOA的吸附量存在最适温度,当温度从303K升高到313K时,PFOA的吸附量随着温度的升高而逐渐增加,当继续升温至323K时, PFOA的吸附量下降.可能是由于温度升高,PFAS在水中的溶解度升高,导致疏水相互作用变弱.此外,也可能是PFAS在较高的温度下发生解吸,导致吸附量下降. 2.2.3 共存有机物 不同浓度,分子量大小和电荷类型的有机物对PFAS吸附有不同影响[147]. 与PFAS具有相似特征的有机物(表面带负电荷和200~1000Da的分子量)会发生竞争吸附(通过静电和疏水相互作用,配体交换和氢键)和孔阻塞效应[67].Deng等[152]研究了腐殖酸,1-萘酚,苯酚和苯甲酸存在下,PFOS,PFOA,PFBS和PFHxS在未修饰多壁碳纳米管(MWCNTs-Pri),羧基修饰多壁碳纳米管(MWCTNs-COOH)和羟基修饰多壁碳纳米管(MWCNTs-OH)上的吸附行为,这些有机物的存在降低了PFAS的初始吸附速率和吸附量,PFAS的饱和吸附量随着共存有机物浓度的增加而降低,当共存有机物浓度为2.5mg/L时,PFOS的饱和吸附量降低了0.828~1.691mg/g.原因是不同的共存有机物与PFAS发生竞争吸附.当体系中存在多种PFAS时,单一PFAS的吸附也会受到影响,Kimura等[153]研究了PAC对混合体系中8种PFAS的吸附效果,发现各种PFAS的去除率都低于单溶质溶液.不同大小的有机物对PFAS吸附的影响程度也不同,Yu等[154]研究了在不同分子尺寸有机物存在下,活性炭从废水中去除PFAS的效果.结果表明分子量<1kDa的小分子有机物的竞争作用远大于分子量>30kDa的大分子物质,特别是与PFAS分子量相当的有机物质会产生更强的竞争吸附,显著减少PFAS吸附量.原因是分子量或结构与PFAS相似的有机物竞争吸附能力更强. 可溶性有机物如腐殖酸具有配体交换位点,会与溶液中的PFAS发生络合,从而降低PFAS在吸附剂上的饱和吸附容量[88].Gong等[88]用水溶性淀粉制备Fe3O4纳米颗粒,并测试了腐殖酸对PFOA去除的影响,12mg/L的腐殖酸使PFOA的饱和吸附量减少了24mg/g.同样在Wang等[145]的研究中,由于腐殖酸的竞争吸附,PFOS和PFBS勃姆石上几乎没有被勃姆石吸附.实际废水中存在的有机物更为复杂,要提高PFAS的吸附性能,必须避免或减少有机物的影响,目前已经对一些可以减少有机物影响的吸附剂进行了研究.Wang等[155]开发了一种基于荧光石墨烯(MNP@FG)的磁性纳米颗粒吸附剂,该吸附剂对PFOA和PFOS具有高亲和力,在天然有机物存在下, PFOA和PFOS的饱和吸附量依旧很高(12.82和13.095mg/g).Wang等[156]开发了共价三嗪基骨架(CTF)吸附剂,CTF均匀的纳米级孔(1.2nm)阻碍了大尺寸腐殖酸的吸附,最小化了对PFAS吸附的影响.Xiao等[157]开发了一种基于β-环糊精的聚合物,与PAC相比,它对PFOA 具有更高的亲和力,同时具有较高的吸附容量和速率.β-环糊精聚合物可将PFOA浓度从1μg/L降至10ng/L,且不受腐殖酸的影响. 除了吸附剂性质以及外界环境,PFAS本身的结构(如链长,官能团,杂原子等)对吸附性能影响也较为显著. 随着PFAS碳链长度的增加,疏水性增强[22],疏水性强的吸附剂对其吸附效果更好.Qiu等[158]研究了不同链长PFAS在活性炭上的吸附行为,长链PFAS在活性炭上的吸附速度更快,活性炭对碳链较长的PFAS具有较高的吸附容量[139,149,155].Cantoni等[46]研究了4种颗粒活性炭对8种PFAS的吸附效果,PFAS的碳链越长,疏水性越强,去除效果越好.Inyang等[96]研究了硬木(HWC)和松木(PWC)生物炭对PFAS的去除,也得到了同样的结论,其中长链PFAS(PFOA, PFOS)的吸附量是短链PFAS(PFBA, PFHxA)的3~4倍. 当PFAS碳链长度相同官能团不同时,同时去除可能会发生竞争吸附,吸附效果也有差异[160].根据软硬酸碱理论,磺酸基是硬碱,羧酸基是软碱,比如常见的一些黏土矿物吸附剂都是硬酸,硬酸硬碱更易反应,因而PFOS比PFOA更易吸附在黏土吸附剂的表面[92,161-162].Ochoa-Herrera等[31]测定了活性炭对PFOA,PFOS和PFBS的吸附性能,PFOS更容易被吸附,原因是磺酸基团产生的静电作用要强于羧酸基团.此外,PFAS同分异构体的吸附能力也不同,比如直链的PFOS比其同分异构体吸附容量更高,可能是由于带支链的PFOS直径较大在反应时影响了扩散[163-164]. 在实际工程应用中,PFAS的处理要考虑到技术可行和经济合理.与其他技术相比,吸附由于其操作,维护简单,处理效果好,在PFAS处理中应用更为广泛[28,160].Rahman等[165]对多个水处理厂使用不同技术(吸附,膜过滤,氧化,生物降解,混凝和浮选)进行PFAS去除,其中混凝,浮选,生物降解,氧化,紫外线照射和低压膜,都不能有效去除PFAS,只有活性炭吸附,离子交换树脂吸附和高压膜过滤可以有效去除PFAS.PFAS吸附剂的选择需要考虑到许多因素,包括易获取,高效率,低成本,可再生性以及环保性等.由于活性炭和离子交换树脂的经济性和吸附性能较高,它们仍然是当前去除PFAS更好的选择[166]. 水中PFAS的大规模去除是当前研究的热点,由于PFAS污染较为复杂,分析技术难度大,且不同研究水体差异大,导致研究结果有时差别较大[167].目前关于水中PFAS大规模去除的研究有限,可能是由于成本较高且分析较为困难而造成[167]. Shivakoti等[168]研究了两个水厂中活性炭滤池进出水中PFAS的含量,两个水厂的活性炭池运行参数相似,炭池厚度为2.1m,接触时间为8.5min,滤池对部分长链PFAS有一定程度的去除作用,而短链PFAS能够轻易穿过GAC滤池.目前短链PFAS和PFAS支链异构体的可用信息非常有限,而这些PFAS被越来越多地使用,对当前的PFAS处理技术提出了巨大的挑战. 目前对于受PFAS污染场地(特别是受水成膜泡沫灭火剂(AFFF)高度污染的地点)和实验室中PFAS的去除具有差异[169].有研究表明,在AFFF周围的环境介质中检测到大量PFAS,其浓度达到了几个mg/L水平[169].PFAS在此环境下的吸附行为较为复杂,PFAS可能会优先吸附到热解碳质材料(PCM)上,如生物炭和煤烟等,而不是土壤有机质(SOM),导致PFAS生物转化更加困难[170].此外,PCM的吸附位点可能被SOM和其他有机化合物占据,导致PFAS解吸到环境中,使其迁移和转化变得更加复杂,修复工作极具挑战性[69].意大利韦内托的氟化物生产导致附近地下水源受到严重的PFAS污染,Conte等[36]开展了一项研究,使用4种不同的树脂(A600E, PAD500,PAD428和MN102)从水源中去除PFBA, PFBS,PFOA和PFOS.4种树脂对PFOA和PFOS的去除效率都很高,但PAD500,PAD428和MN102对PFBA和PFBS的吸附容量较低.原因是PFBA和PFBS的链长较短,疏水性较弱,需要通过高度疏水的官能团改性加强吸附. 吸附剂上PFAS的逐渐累积会导致材料的吸附能力逐渐降低[171].吸附剂再生是在不破坏原有结构的前提下,用物理或化学方法,使PFAS脱离或分解,恢复吸附剂吸附性能[172].通过再生可以实现吸附剂的循环使用,降低PFAS处理成本.目前较常用的再生方法有热再生法,化学再生法以及溶剂再生法等[172-173]. 热再生法是当前应用最广泛,技术最成熟的再生方法[173-174].它是指通过外部加热,升高温度来提高PFAS分子振动,使吸附平衡关系发生改变,将PFAS从吸附剂中脱附的方法,具有再生率高,再生时间短等优点[172-173].但热再生法也存在处理后吸附剂表面积减小,吸附剂损失大等缺点[175],Castilla等[176]利用热再生法对吸附酚类饱和的活性炭进行再生研究,热再生温度为1100K,He作为保护气,经过4次循环吸附再生后,吸附剂的吸附容量下降了50%.这是由于热再生后的活性炭比表面积减少.微波辐照再生法是用微波产生高温使吸附剂上的PFAS炭化,恢复吸附剂吸附能力的方法[172].微波可产生介质损耗热,传导损耗热和磁性损耗热3种形式的热,具有再生时间短,再生效率高,耗能低等优点[173].微波辐射法是目前研究较多的新型再生方法,具有较大的发展潜力. 溶剂再生法是指利用化学药剂与PFAS之间的化学反应使吸附质解析至溶剂相中的再生方法,溶剂分为无机溶剂和有机溶剂[172].无机溶剂一般以HCl,NaOH等为主,使吸附剂上的污染物转化成易溶于水的物质,释放吸附位点而达到再生的效果.有机溶剂再生法是指用苯,丙酮,甲醇,二氯甲烷及乙酸乙酯等有机溶剂萃取吸附剂上的污染物[172].而钠盐溶液无法有效再生PFAS吸附饱和的吸附剂[10],钠盐和有机溶剂(如CH3OH,C2H5OH和C3H6O)的混合物已被广泛应用于PFAS吸附剂的再生,钠盐对PFAS头基进行解吸,而醇溶液主要解吸PFAS的尾部[10,134]. Deng等[134]研究了不同温度的去离子水作为再生溶液对PFOS解吸的影响.较高温度的去离子水(约80 ℃)可增强PFOS的解吸,再生率为53%. 化学再生法在实际应用中较为广泛的有湿式氧化再生法,电化学氧化再生法,Fenton氧化再生法,臭氧氧化再生法等[172,174].湿式氧化再生法是利用空气中的氧在高温和高压条件下使吸附质氧化的过程,适用于粉状吸附剂的再生[172].这种工艺操作条件比较严格(在完全封闭的系统中进行),吸附剂的再生率和损失率与再生温度和再生压力有关[172].电化学氧化法是指将吸附饱和的吸附剂作为阳极,使吸附质氧化分解,以达到恢复吸附剂吸附容量的方法[174].但可用于电化学降解PFAS的电极材料稀少且昂贵[17],且PFAS本身难以被氧化,因此通过氧化降解PFAS达到再生效果较为困难[17]. 生物再生法是指利用经过驯化培养的微生物降解吸附剂表面的污染物,从而恢复吸附剂的吸附容量,达到重复使用目的的方法[173-174].而微生物再生法仅适用于易被生物分解,具有吸附可逆性,容易脱附的污染物[172].由微生物解析下来的有机物必须可以一步分解成CO2和H2O.而PFAS基本不能被生物氧化或还原[18],其矿化是非常困难的,因此利用生物再生法再生PFAS吸附饱和的吸附剂难以实现. 再生后脱附的PFAS易造成二次污染,需要结合降解技术,才能达到PFAS无害化处理目的.PFAS降解技术包括化学氧化法和化学还原法等.化学氧化技术主要利用•OH和SO4•-等具有强氧化的活性物质降解PFAS,主要的降解体系包括Fenton体系,类Fenton体系,SO4•-降解体系,超声降解体系,光催化降解体系和电化学降解体系等[28, 177].但PFAS中所含的碳氟键键能较高,且分子表面的电子云密度较高,因此化学氧化技术很难彻底降解PFAS[178].氟原子具有很高的电负性,可以吸收电子发生还原降解,故化学还原技术可实现对PFAS的高效降解[176].目前应用于PFAS降解的还原体系主要包括水合电子体系,纳米零价铁体系和超氧阴离子体系等[28]. 焚烧技术因其在减量化和能量回收方面的优势逐渐成为处理PFAS吸附剂的主流技术[179].焚烧可以有效减少吸附剂的体积和质量,此外,一些碳质吸附剂中含有大量的聚合物,例如纤维素,半纤维素和木质素等[179],还可以从其燃烧中回收能量. 碳氟键的化学稳定性是焚烧处理PFAS的一大挑战,PFOA,PFOS已被证明可以通过焚烧有效分解[180].但是焚烧需要相当高的温度(>700℃)和较长的时间将PFAS转化为HF和非氟化产品,全氟化程度较高的PFAS则需要更长的时间和更高的温度[102,180].部分PFAS可以在较低温度(例如400℃)下催化氧化,然而由于效率较低尚未大规模应用[181]. PFAS在焚烧过程中的迁移和转化是亟需解决的问题[182].目前对于PFAS焚烧期间可能形成的全部潜在副产物目前并没有探究清楚,一些报告提出PFAS焚烧可能会释放氯氟烃,氟化温室气体(如四氟甲烷,六氟乙烷和氟代二噁英),氟化芳香族化合物等[183-184],还会释放出大量未识别和报道的分解产物[185].Watanabe等[186]研究了吸附有PFOS,PFOA和PFHxA的GAC在焚烧过程中PFAS的去向,在700℃下,很大一部分PFAS转化为无法进行最终分析的挥发性物质.因此,在焚烧产生的废气中捕获或销毁PFAS是研究的热点. 吸附剂的焚烧或热再生均是通过高温处理污染物,但它们的目的和应用场景不同[174].热再生是一种恢复吸附剂性能的方法,它通过升高温度,使吸附物脱附,从而恢复吸附剂的吸附能力,达到循环利用目的,适用范围广[173].而焚烧是一种以减量化和资源化为目标,处理危险废物的方法[179].焚烧旨在减少废物量并将其转化为更安全的形式,而热再生则旨在恢复吸附剂性能并保持吸附剂原有结构. 尽管焚烧可破坏部分PFAS,但仍需要从焚烧设施中获取详细数据,评估PFAS焚烧对人类和环境健康的影响[182-183].此外,一些PFAS不完全燃烧而产生的分解物质,需要结合其他方法(如填埋)进一步处理. 填埋处置具有操作简便,设备简单,成本效益良好等优点[187].但会占用大量土地资源,且会造成二次污染,并不利于废物资源化利用[187]. 填埋过程中,吸附剂中的PFAS会通过物理,化学和生物作用逐渐释放到渗滤液中[188].Lang等[189]测定了美国18个垃圾填埋场渗滤液中的PFAS,70种 PFAS的浓度达到66µg/L.Wang等[190]的调查结果显示,城市固体废物填埋场和转运站渗滤液中也含有多种PFAS,浓度为22~46µg/L.如果对这些PFAS未能有效捕获和处理,它们甚至可能穿透防渗层,使填埋场成为PFAS进入水环境的二次源头[188]. 目前对渗滤液中PFAS的研究较少,主要集中在一些发达国家[191-193].我国针对垃圾渗滤液中PFAS的调查研究尚处于起步阶段,仅有的少量研究主要集中在北京,上海等经济发达地区,而其他地区有关渗滤液中PFAS的调查鲜有报道[194-195].Yan等[195]收集了中国5个城市原始和处理过的垃圾填埋场样本,原始样本中多种PFAS的浓度从7280~292000ng/L不等,处理后渗滤液中的PFAS浓度为98.4~282000ng/L,其中PFOS和PFBS占比最高(分别为28.8%和26.1%). 不同类型的填埋场,渗滤液中所含PFAS的浓度也有差异.在Gallen等[192]的调查中,含有建筑和拆除碎片的填埋场,渗滤液中的PFAS平均浓度较高.在Gabriele等[188]的研究也发现了同样的结果,建筑垃圾填埋场和拆除垃圾填埋场渗滤液中PFAS含量较高.建筑材料中的密封剂和防水剂等含有PFAS,这可能是造成垃圾填埋场渗滤液中PFAS含量较高的原因之一.相比之下,灰烬填埋场渗滤液中的PFAS含量较低.这可能是由于PFAS在焚烧过程中被分解或挥发到大气中. 垃圾渗滤液收集系统的设计初衷是为了防止地下水和土壤受到污染.然而,目前在垃圾填埋场中,PFAS的径流和渗漏仍然是一个重要问题[188].据明尼苏达州污染控制机构报道[196],该州垃圾填埋场附近的地下水已受到PFAS污染.虽然通过填埋处理PFAS吸附剂可以临时封存这些物质,但由于大多数PFAS不会自然降解成非氟物质,填埋场最终可能成为新的PFAS污染源[187]. 吸附技术是水处理厂应对PFAS污染的最佳可行技术之一,相比复杂的降解技术体系,活性炭和树脂等吸附技术建造和运行成本更低,相比膜分离技术,操作的简便性是显著优势.依据水质和PFAS污染类型的不同,吸附剂的科学选型或者复合吸附填料的应用将决定技术的实际工程应用效果.针对水中PFAS的污染控制,吸附技术未来在以下几个方向可加强研究: (1)针对PFAS污染的复杂特征,制定具有普遍适用性的吸附策略,比如对多类型水体中不同碳链长度,离子端基团,电荷类型的PFAS都有高去除效率的吸附材料,技术,工艺及装备. (2)开发高效的吸附剂再生/处置技术,解决目前方法能耗高,效率低,易产生二次污染物等问题,使PFAS吸附技术形成闭环. (3)开发具有吸附协同降解功能的先进材料,实现PFAS的同步富集和矿化,延长吸附剂使用寿命,降低技术能耗,提高PFAS去除效率. [1] 袁雅静.全氟或多氟烷基物质水处理技术研究进展 [J]. 化工进展, 2021,40(S1):397-403. Yuan J Y. Progress in water treatment technology for perfluorinated or polyfluorinated alkyl substances [J]. Chemical Industry and Engineering Progress, 2021,40(S1):397-403. [2] Du Z W, Deng S B, Bei Y, et al. Adsorption behavior and mechanism of perfluorinated compounds on various adsorbents—A review [J]. Journal of Hazardous Materials, 2014,274:443-454. [3] Dixit F, Dutta R, Barbeau B, et al. PFAS removal by ion exchange resins: A review [J]. Chemosphere, 2021,272:129777. [4] Zenobio J E, Salawu O A, Han Z W, et al. Adsorption of per- and polyfluoroalkyl substances (PFAS) to containers [J]. Journal of Hazardous Materials Advances, 2022,7:100130. [5] Boyer T H, Fang Y D, Ellis A, et al. Anion exchange resin removal of per- and polyfluoroalkyl substances (PFAS) from impacted water: A critical review [J]. Water Research, 2021,200:117244. [6] Gao Y X, Deng S B, Du Z W, et al. Adsorptive removal of emerging polyfluoroalky substances F-53B and PFOS by anion-exchange resin: A comparative study [J]. Journal of Hazardous Materials, 2017,323 (Pt.A):550-557. [7] Elika K, Medha K, Sweta M, et al. A juxtaposed review on adsorptive removal of PFAS by metal-organic frameworks (MOFs) with carbon-based materials, ion exchange resins, and polymer adsorbents [J]. Chemosphere, 2023,311(Part 1):136933. [8] Pelch K E, Reade A, Wolffe T A M, et al. PFAS health effects database: protocol for a systematic evidence map [J]. Environment International, 2019,130:104851. [9] Baker E S, Knappe D R U. Per- and polyfluoroalkyl substances (PFAS)—contaminants of emerging concern [J]. Analytical and Bioanalytical Chemistry, 2022,414(3):1187-1188. [10] Gagliano E, Sgroi M, Falciglia P P, et al. Removal of poly- and perfluoroalkyl substances (PFAS) from water by adsorption: role of PFAS chain length, effect of organic matter and challenges in adsorbent regeneration [J]. Water Research, 2020,171:115381. [11] 温 馨,吕 佳,王园媛,等.常规处理工艺对饮用水中全氟化合物的去除效果研究 [J]. 环境卫生学杂志, 2022,12(7):526-532. Wen X, Lyu Jia, Wang Y Y, et al. Removal efficiency of perfluorinated compounds in drinking water by conventional treatment process [J]. Journal of Environmental Hygiene, 2022,12(7):526-532. [12] Yu H, Chen Y F, Guo H Q, et al. Preparation of molecularly imprinted carbon microspheres by one-pot hydrothermal method and their adsorption properties to perfluorooctane sulfonate [J]. Chinese Journal of Analytical Chemistry, 2019,47(11):1776-1784. [13] Dickman R A, Aga D S. A review of recent studies on toxicity, sequestration, and degradation of per- and polyfluoroalkyl substances (PFAS) [J]. Journal of Hazardous Materials, 2022,436:129120. [14] 杜玲玲.全氟辛烷磺酸分子印迹纳米材料的制备与性能研究 [D]. 重庆:西南大学, 2018. Du L L. Study on the preparation and properties of perfluorooctane sulfonate molecularly imprinted nanomaterials [D]. Chongqing: Southwest University, 2018. [15] GB 5749-2022 生活饮用水卫生标准[S].GB 5749-2022 Standards for drinking water quality [S]. [16] Leung S C E, Shukla P, Chen D C, et al. Emerging technologies for PFOS/PFOA degradation and removal: a review [J]. Science of the Total Environment, 2022,827:153669. [17] Kazwini T, Yadav S, Ibrar I, et al. Updated review on emerging technologies for PFAS contaminated water treatment [J]. Chemical Engineering Research and Design, 2022,182:667-700. [18] Zhang Z M, Sarkar D, Biswas J K, et al. Biodegradation of per- and polyfluoroalkyl substances (PFAS): a review [J]. Bioresource Technology, 2022,344(Part B):126223. [19] Nzeribe B N, Crimi M, Mededovic Thagard S, et al. Physico-chemical processes for the treatment of per- and polyfluoroalkyl substances (PFAS): a review [J]. Critical Reviews in Environmental Science and Technology, 2019,49(10):866-915. [20] 张春晖,刘 育,唐佳伟,等.典型工业废水中全氟化合物处理技术研究进展 [J]. 中国环境科学, 2021,41(3):1109-1118. Zhang C H, Liu Y, Tang J W, et al. Progress of research on treatment technology of perfluorinated compounds in typical industrial wastewater [J]. Chinese Environmental Sciences, 2021,41(3):1109- 1118. [21] 周 琴,栾 萱,潘 纲.水中典型全氟化合物的吸附行为 [J]. 科学通报, 2012,57(17):1526-1532. Zhou Q, Luan X, Pan G. Sorption of perfluorooctanoic acid (PFOA) and perfluorooctane sulfonate (PFOS) from water [J]. Chinese Science Bulletin, 2012,57(17):1526-1532. [22] Arvaniti O S, Stasinakis A S. Review on the occurrence, fate and removal of perfluorinated compounds during wastewater treatment [J]. Science of the Total Environment, 2015,524-525:81-92. [23] Eschauzier C, Beerendonk E, Scholte-Veenendaal P, et al. Impact of treatment processes on the removal of perfluoroalkyl acids from the drinking water production chain [J]. Environmental Science, 2012,46 (3):1708-1715. [24] Quiñones O, Snyder S A. Occurrence of perfluoroalkyl carboxylates and sulfonates in drinking water utilities and related waters from the united states [J]. Environmental Science, 2009,43(24):9089-9095. [25] 郭 睿,张超杰,周 琪.水环境中全氟化合物的去除技术研究综述 [J]. 净水技术, 2016,35(6):18-24. Guo R, Zhang C J, Zhou Q. Research overview of technology of perfluorinated compounds removal in water environment [J]. Water Purification Technology, 2016,35(6):18-24. [26] Deng S B, Yu Q, Huang J, et al. Removal of perfluorooctane sulfonate from wastewater by anion exchange resins: Effects of resin properties and solution chemistry [J]. Water Research, 2010,44(18):5188-5195. [27] Tang C Y, Fu Q S, Gao D, et al. Effect of solution chemistry on the adsorption of perfluorooctane sulfonate onto mineral surfaces [J]. Water Research, 2010,44(8):2654-2662. [28] 滕 影,王雯冉,黄柳青,等.全氟烷基化合物的去除技术研究进展 [J]. 环境化学, 2023,42(7):2210-2227. Teng Y, Wang W R, Huang L Q, et al. Research progress on the removal of perfluorinated allkyl substances: A review [J]. Environmental Chemistry, 2023,42(7):2210-2227. [29] 朱鹏宇,刘建广,辛晓东.活性炭吸附水中全氟化合物的研究进展 [J]. 净水技术, 2022,41(10):17-22,147. Zhu P Y, Liu J G, Xin X D. Research progress of activated carbon for adsorption of perfluorinated compounds in water [J]. Water Purification Technology, 2022,41(10):17-22,147. [30] Du Z W, Deng S B, Chen Y G, et al. Removal of perfluorinated carboxylates from washing wastewater of perfluorooctanesulfonyl fluoride using activated carbons and resins [J]. Journal of Hazardous Materials, 2015,286:136-143. [31] Ochoa-Herrera V, Sierra-Alvarez R. Removal of perfluorinated surfactants by sorption onto granular activated carbon, zeolite and sludge [J]. Chemosphere, 2008,72(10):1588-1593. [32] Yu Q, Zhang R Q, Deng S B, et al. Sorption of perfluorooctane sulfonate and perfluorooctanoate on activated carbons and resin: Kinetic and isotherm study [J]. Water Research, 2009,43(4):1150- 1158. [33] Yu H, Chen H, Fang B, et al. Sorptive removal of per- and polyfluoroalkyl substances from aqueous solution: Enhanced sorption, challenges and perspectives [J]. Science of The Total Environment, 2023,861:160647. [34] Rostvall A, Zhang W, Dürig W, et al. Removal of pharmaceuticals, perfluoroalkyl substances and other micropollutants from wastewater using lignite, xylit, sand, granular activated carbon (GAC) and GAC+polonite® in column tests – role of physicochemical properties [J]. Water Research, 2018,137:97-106. [35] Westreich P, Mimna R, Brewer J, et al. The removal of short‐chain and long‐chain perfluoroalkyl acids and sulfonates via granular activated carbons: A comparative column study [J]. Remediation Journal, 2018,29(1):19-26. [36] Zaggia A, Conte L, Falletti L, et al. Use of strong anion exchange resins for the removal of perfluoroalkylated substances from contaminated drinking water in batch and continuous pilot plants [J]. Water Research, 2016,91:137-146. [37] Westerhoff P, Yoon Y, Snyder S, et al. Fate of endocrine-disruptor, pharmaceutical, and personal care product chemicals during simulated drinking water treatment processes [J]. Environmental Science, 2005,39(17):6649-6663. [38] 童锡臻,石宝友,解 岳,等.改性活性炭对水中PFOS的吸附去除研究 [J]. 环境科学, 2012,33(9):3132-3138. Tong X Z, Shi B Y, Xie Y, et al. Adsorption of perfluorooctanesulfonate (PFOS) onto modified activated carbons [J]. Environmental Science, 2012,33(9):3132-3138. [39] Pauletto P S, Bandosz T J. Activated carbon versus metal-organic frameworks: A review of their PFAS adsorption performance [J]. Journal of Hazardous Materials, 2022,425:127810. [40] Bhatnagar A, Hogland W, Marques M, et al. An overview of the modification methods of activated carbon for its water treatment applications [J]. Chemical Engineering Journal, 2013,219(3):499–511. [41] Menéndez J A, phillips J, Xia B, et al. On the modification and characterization of chemical surface properties of activated carbon: In the search of carbons with stable basic properties [J]. Langmuir, 1996, 12(18):4404-4410. [42] Faria P C C, Orfao J J M, Pereira M F R. Adsorption of anionic and cationic dyes on activated carbons with different surface chemistries [J]. Water Research, 2004,38(8):2043-2052. [43] Shaarani F W, Hameed B H. Ammonia-modified activated carbon for the adsorption of 2,4-dichlorophenol [J]. Chemical Engineering Journal, 2011,169(1-3):180-185. [44] Saeidi N, Kopinke F D, Georgi A. What is specific in adsorption of perfluoroalkyl acids on carbon materials? [J]. Chemosphere, 2020,273: 128520. [45] 苑 晨.季铵盐改性活性炭吸附地下水中PFOA的效能及其机理研究 [D]. 重庆:重庆大学, 2019. Yuan C. Adsorption of PFOA in groundwater by quaternary ammonium epoxide compounds modified activated carbon and its mechanism analysis [D]. Chongqing: Chongqing University, 2019. [46] Cantoni B, Turolla A, Wellmitz J, et al. Perfluoroalkyl substances (PFAS) adsorption in drinking water by granular activated carbon: Influence of activated carbon and PFAS characteristics [J]. Science of The Total Environment, 2021,795:148821. [47] Park M, Wu S M, Lopez I J, et al. Adsorption of perfluoroalkyl substances (PFAS) in groundwater by granular activated carbons: Roles of hydrophobicity of PFAS and carbon characteristics [J]. Water Research, 2019,170:115364. [48] Chen W, Zhang X P, Mamadiev M, et al. Sorption of perfluorooctane sulfonate and perfluorooctanoate on polyacrylonitrile fiber-derived activated carbon fibers: in comparison with activated carbon [J]. RSC advances, 2017,7(2):927-938. [49] 赵丽媛,吕剑明,李庆利,等.活性炭制备及应用研究进展 [J]. 科学技术与工程, 2008,8(11):6. Zhao L Y, LÜ J M, Li Q L, et al. Present situation and progress in preparation of activated carbon [J]. Science Technology and Engineering, 2008,8(11):6. [50] Dastgheib S A, Karanfil T. Adsorption of oxygen by heat-treated granular and fibrous activated carbons [J]. Journal of Colloid and Interface Science, 2004,274(1):1-8. [51] 周 平,黄汝常,李永辉,等.去除废水中重金属离子的新工艺研究 [J]. 中国给水排水, 1998,14(4):17-20. Zhou P, Huang R C, Li Y H, et al. Study of a novel process for removal of heavy metals from industrial wastewater [J]. China Water & Wastewater, 1998,14(4):17-20. [52] Punyapalakul P, Soonglerdsongpha S, Kanlayaprasit C, et al. Effects of crystalline structures and surface functional groups on the adsorption of haloacetic acids by inorganic materials [J]. Journal of Hazardous Materials, 2009,171(1-3):491-499. [53] Senevirathna S, Tanaka S, Fujii S, et al. A comparative study of adsorption of perfluorooctane sulfonate (PFOS) onto granular activated carbon, ion-exchange polymers and non-ion-exchange polymers [J]. Chemosphere, 2010,80(6):647-651. [54] Zhang D Q, Zhang W L, Liang Y N. Adsorption of perfluoroalkyl and polyfluoroalkyl substances (PFASs) from aqueous solution - A review [J]. Science of the Total Environment, 2019,694:133606. [55] Ross I, McDonough J, Miles J, et al. A review of emerging technologies for remediation of PFASs [J]. Remediation Journal, 2018,28(2):101-126. [56] 许 罗,林秋风,李 聪,等.典型全氟化合物污染现状及其处理技术研究进展 [J]. 中国给水排水, 2022,38(10):56-62. Xu L, Lin Q F, Li C, et al. Current situation of typical perfluorinated compounds pollution and its treatment technology progress [J]. China Water & Wastewater, 2022,38(10):56-62. [57] Maimaiti A, Deng S B, Meng P P, et al. Competitive adsorption of perfluoroalkyl substances on anion exchange resins in simulated AFFF-impacted groundwater [J]. Chemical Engineering Journal, 2018, 348:494-502. [58] 马蕴杰,陈 程,张 伟.吸附树脂改性的研究进展 [J]. 辽宁化工, 2019,48(8):796-799. Ma Y J, Chen C, Zhang W. Research progress in the modification of adsorbent resin [J]. Liaoning Chemical Industry, 2019,48(8):796-799. [59] Xie R C, Zhou L, Smith A E, et al. A dual grafted fluorinated hydrocarbon amine weak anion exchange resin polymer for adsorption of perfluorooctanoic acid from water [J]. Journal of Hazardous Materials, 2022,431:128521. [60] 苏 球.含酚羟基超高交联分子印迹吸附树脂的制备及吸附性能研究 [D]. 镇江:江苏大学, 2016. Su Q. Preparation and adsorptive property of phenol hydroxyl hypercrosslinked and molecularly imprinted adsorption resin [D]. Zhenjiang: Jiangsu University, 2016. [61] Ateia M, Alsbaiee A, Karanfil T, et al. Efficient PFAS removal by amine-functionalized sorbents: critical review of the current literature [J]. Environmental Science & Technology, 2019,6(12):688-695. [62] 王梦乔.新型磁性胺基修饰超高交联树脂的合成及其应用研究 [D]. 南京:南京大学, 2014. Wang M Q. Synthesis and application of novel magnetic hypercrosslinked resin modified with amino group [D]. Nanjiang: Nanjing University, 2014. [63] Park M, Daniels K D, Wu S M, et al. Magnetic ion-exchange (MIEX) resin for perfluorinated alkylsubstance (PFAS) removal in groundwater: Roles of atomic charges for adsorption [J]. Water Research, 2020,181:115897. [64] Améduri Bruno. The promising future of fluoropolymers [J]. Macromolecular Chemistry and physics, 2019,221(8):1900573. [65] Shetty D, Jahović I, Skorjanc T, et al. Rapid and efficient removal of perfluorooctanoic acid from water with fluorine-rich calixarene-based porous polymers [J]. ACS applied materials & interfaces, 2020, 12(38):43160-43166. [66] Dixit F, Barbeau B, Mostafavi S G, et al. PFAS and DOM removal using an organic scavenger and PFAS-specific resin: Trade-off between regeneration and faster kinetics [J]. Science of The Total Environment, 2020,754:142107. [67] Kothawala D N, Köhler S J, Östlund A, et al. Influence of dissolved organic matter concentration and composition on the removal efficiency of perfluoroalkyl substances (PFASs) during drinking water treatment [J]. Water Research, 2017,121:320-328. [68] McCleaf P, Englund S, Östlund A, et al. Removal efficiency of multiple poly- and perfluoroalkyl substances (PFASs) in drinking water using granular activated carbon (GAC) and anion exchange (AE) column tests [J]. Water Research, 2017,120:77-87. [69] Vu C T, Wu T T. Recent progress in adsorptive removal of per- and poly-fluoroalkyl substances (PFAS) from water/wastewater [J]. Critical Reviews in Environmental Science and Technology, 2022, 52(1):90-129. [70] Levchuk I, Màrquez J J R, Sillanpää M. Removal of natural organic matter (NOM) from water by ion exchange - A review [J]. Chemosphere, 2018,192:90-104. [71] Deng S B, Zhang Q Y, Nie Y, et al. Sorption mechanisms of perfluorinated compounds on carbon nanotubes [J]. Environmental Pollution, 2012,168:138-144. [72] Wang F, Shih K. Adsorption of perfluorooctanesulfonate (PFOS) and perfluorooctanoate (PFOA) on alumina: Influence of solution pH and cations [J]. Water Research, 2011,45(9):2925-2930. [73] Zhou Q, Deng S B, Zhang Q Y, et al. Sorption of perfluorooctane sulfonate and perfluorooctanoate on activated sludge [J]. Chemosphere, 2010,81(4):453-458. [74] He G Z, Zhang M Y, Zhou Q, et al. Molecular dynamics simulations of structural transformation of perfluorooctane sulfonate (PFOS) at water/rutile interfaces [J]. Chemosphere, 2015,134:272-278. [75] Feng Y, Zhou Y, Lee P H, et al. Mineralization of perfluorooctanesulfonate (PFOS) and perfluorodecanoate (PFDA) from aqueous solution by porous hexagonal boron nitride: adsorption followed by simultaneous thermal decomposition and regeneration [J]. RSC advances, 2016,6(114):113773-113780. [76] Barakan S, Aghazadeh V. The advantages of clay mineral modification methods for enhancing adsorption efficiency in wastewater treatment: a review [J]. Environmental Science and Pollution Research, 2021, 28(3):2572-2599. [77] Johnson R L, Anschutz A J, Smolen J M, et al. The adsorption of perfluorooctane sulfonate onto sand, clay, and iron oxide surfaces [J]. Journal of Chemical & Engineering Data, 2007,52(4):1165-1170. [78] Ellefson M. Soil adsorption/desorption study of potassium perfluorooctane sulfonate(PFOS). EPA Docket AR226-1030a030, 3M Company, Maplewood, MN, 2001. [79] Junho Jeon, Kurunthachalam Kannan, Byung J Lim, et al. Effects of salinity and organic matter on the partitioning of perfluoroalkyl acid (PFAs) to clay particles [J]. Journal of Environmental Monitoring, 2011,13(6):1803-1810. [80] Gao X, Chorover J. Adsorption of perfluorooctanoic acid and perfluorooctanesulfonic acid to iron oxide surfaces as studied by flow-through ATR-FTIR spectroscopy [J]. Environmental Chemistry, 2012,9(2):148-157. [81] Mukhopadhyay R, Sarkar B, Palansooriya K N, et al. Natural and engineered clays and clay minerals for the removal of poly- and perfluoroalkyl substances from water: State-of-the-art and future perspectives [J]. Advances in Colloid and Interface Science, 2021, 297:102537. [82] Du Z W, Deng S B, Zhang S Y, et al. Selective and high Sorption of perfluorooctane sulfonate and perfluorooctanoate by fluorinated alkyl chain modified montmorillonite [J]. The Journal of Physical Chemistry C, 2016,120(30):16782-16790. [83] El Mouzdahir Y, Elmchaouri A, Mahboub R, et al. Equilibrium modeling for the adsorption of methylene blue from aqueous solutions on activated clay minerals [J]. Desalination, 2010,250(1):335-338. [84] Mukhopadhyay R, Bhaduri D, Sarkar B, et al. Clay-polymer nanocomposites: Progress and challenges for use in sustainable water treatment [J]. Journal of Hazardous Materials, 2020,383:121125. [85] Bhattarai B, Muruganandham M, Suri R P S. Development of high efficiency silica coated β-cyclodextrin polymeric adsorbent for the removal of emerging contaminants of concern from water [J]. Journal of Hazardous Materials, 2014,273:146-154. [86] Smart B E. Characteristics of C-F Systems [M]. Organofluorine Chemistry: Principles and Commercial Applications. Boston, MA: Springer US, 1994,57-88. [87] Riess J G. Understanding the fundamentals of perfluorocarbons and perfluorocarbon emulsions relevant to in vivo oxygen delivery [J]. Artificial Cells, Blood Substitutes, and Biotechnology, 2005,33(1):47- 63. [88] Gong Y Y, Wang L, Liu J C, et al. Removal of aqueous perfluorooctanoic acid (PFOA) using starch-stabilized magnetite nanoparticles [J]. Science of the Total Environment, 2016,562:191- 200. [89] Mancinelli M, Stevanin C, Ardit M, et al. PFAS as emerging pollutants in the environment: A challenge with FAU type and silver-FAU exchanged zeolites for their removal from water [J]. Journal of Environmental Chemical Engineering, 2022,10(4):108026. [90] Wei Z S, Xu T Y, Zhao D Y. Treatment of per- and polyfluoroalkyl substances in landfill leachate: status, chemistry and prospects [J]. Environmental Science: Water Research & Technology, 2019,5(11): 1814-1835. [91] Lath S, Navarro D A, Losic D, et al. Sorptive remediation of perfluorooctanoic acid (PFOA) using mixed mineral and graphene/ carbon-based materials [J]. Environmental Chemistry, 2018,15(8): 472-480. [92] Zhang R M, Yan W, Jing C Y. Mechanistic study of PFOS adsorption on kaolinite and montmorillonite [J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2014,462:252-258. [93] Pereira H C, Ullberg M, Kleja D B, et al. Sorption of perfluoroalkyl substances (PFASs) to an organic soil horizon – Effect of cation composition and pH [J]. Chemosphere, 2018,207:183-191. [94] Karoyo A H, Wilson L D. Tunable macromolecular-based materials for the adsorption of perfluorooctanoic and octanoic acid anions [J]. Journal of Colloid and Interface Science, 2013,402:196-203. [95] Meng P P, Fang X L, Maimaiti A, et al. Efficient removal of perfluorinated compounds from water using a regenerable magnetic activated carbon [J]. Chemosphere, 2019,224:187-194. [96] Inyang M, Dickenson E R V. The use of carbon adsorbents for the removal of perfluoroalkyl acids from potable reuse systems [J]. Chemosphere, 2017,184:168-175. [97] Yu Q, Deng S B, Yu G. Selective removal of perfluorooctane sulfonate from aqueous solution using chitosan-based molecularly imprinted polymer adsorbents [J]. Water Research, 2008,42(12):3089-3097. [98] Elanchezhiyan S S D, Preethi J, Rathinam K, et al. Synthesis of magnetic chitosan biopolymeric spheres and their adsorption performances for PFOA and PFOS from aqueous environment [J]. Carbohydrate Polymers, 2021,267:118165. [99] Punyapalakul P, Suksomboon K, Prarat P, et al. Effects of surface functional groups and porous structures on adsorption and recovery of perfluorinated compounds by inorganic porous silicas [J]. Separation Science and Technology, 2013,48(5):775-788. [100]Guo W, Huo S L, Feng J L, et al. Adsorption of perfluorooctane sulfonate (PFOS) on corn straw-derived biochar prepared at different pyrolytic temperatures [J]. Journal of the Taiwan Institute of Chemical Engineers, 2017,78:265-271. [101]Zhou Q, Deng S B, Yu Q, et al. Sorption of perfluorooctane sulfonate on organo-montmorillonites [J]. Chemosphere, 2010,78(6):688-694. [102]Rayne S, Forest K. Perfluoroalkyl sulfonic and carboxylic acids: a critical review of physicochemical properties, levels and patterns in waters and wastewaters, and treatment methods [J]. Journal of Environmental Science and Health Part A, 2009,44(12):1145-1199. [103]Guo W, Lu S Y, Shi J H, et al. Effect of corn straw biochar application to sediments on the adsorption of 17α-ethinyl estradiol and perfluorooctane sulfonate at sediment-water interface [J]. Ecotoxicology and Environmental Safety, 2019,174:363-369. [104]Fabregat-Palau J, Vidal M, Rigol A. Examining sorption of perfluoroalkyl substances (PFAS) in biochars and other carbon-rich materials [J]. Chemosphere, 2022,302:134733. [105]杜子文.吸附去除废水中全氟化合物及高选择性氟化吸附剂的研究 [D]. 北京:清华大学, 2017. Du Z W. Adsorptive removal of perfluorinated compounds from industrial wastewater and preparation of highly selective fluorinated adsorbents [D]. Beijing: Tsinghua University, 2017. [106]靳晓雨.污水中全氟化合物的去除方法 [J]. 化工管理, 2022,(20): 144-146. Jin X Y. Removal methods of perfluorinated compounds from sewage [J]. Chemical Enterprise Management, 2022,(20):144-146. [107]Zhang Q Y, Deng S B, Yu G, et al. Removal of perfluorooctane sulfonate from aqueous solution by crosslinked chitosan beads: Sorption kinetics and uptake mechanism [J]. Bioresource Technology, 2011,102(3):2265-2271. [108]Militao I M, Roddick F, Bergamasco R, et al. Rapid adsorption of PFAS: application of moringa oleifera seed powder encapsulated in alginate beads [J]. Environmental Technology & Innovation, 2022,28: 102761. [109]Krahn K M, Cornelissen G, Castro G, et al. Sewage sludge biochars as effective PFAS-sorbents [J]. Journal of Hazardous Materials, 2022, 445:130449. [110]Jin X, Wang Z, Hong R, et al. Supramolecular assemblies of a newly developed indole derivative for selective adsorption and photo- destruction of perfluoroalkyl substances [J]. Water Research, 2022, 225:119147. [111]Turner B D, Sloan S W, Currell G R. Novel remediation of per- and polyfluoroalkyl substances (PFASs) from contaminated groundwater using Cannabis Sativa L. (hemp) protein powder [J]. Chemosphere, 2019,229:22-31. [112]Rodrigo P M, Navarathna C, pham M T H, et al. Batch and fixed bed sorption of low to moderate concentrations of aqueous per- and poly-fluoroalkyl substances (PFAS) on Douglas fir biochar and its Fe3O4hybrids [J]. Chemosphere, 2022,308:136155. [113]Hassan M, Liu Y J, Naidu R, et al. Adsorption of perfluorooctane sulfonate (PFOS) onto metal oxides modified biochar [J]. Environmental Technology & Innovation, 2020,19:100816. [114]Verma M, Lee I, Kumar V, et al. Chitosan cross-linked β–cyclodextrin polymeric adsorbent for the removal of perfluorobutanesulfonate from aqueous solution: adsorption kinetics, isotherm, and mechanism [J]. Environmental Science and Pollution Research, 2022,30:19259– 19268. [115]Wang R, Lin Z W, Klemes M J, et al. A tunable porous β-cyclodextrin polymer platform to understand and improve anionic PFAS removal [J]. ACS Central Science, 2022,8(5):663-669. [116]Zhang C J, Yan H, Li F, et al. Sorption of short- and long-chain perfluoroalkyl surfactants on sewage sludges [J]. Journal of Hazardous Materials, 2013,260(18):689-699. [117]He G Z, Pan G, Zhang M Y. Assembling structures and dynamics properties of perfluorooctane sulfonate (PFOS) at water–titanium oxide interfaces [J]. Journal of Colloid and Interface Science, 2013, 405:189-194. [118]Takayose M, Nishimoto K, Matsui J. A fluorous synthetic receptor that recognizes perfluorooctanoic acid (PFOA) via fluorous interaction obtained by molecular imprinting [J]. Analyst, 2012,137(12):2762- 2765. [119]Xiao F, Davidsavor K J, Park S, et al. Batch and column study: Sorption of perfluorinated surfactants from water and cosolvent systems by Amberlite XAD resins [J]. Journal of Colloid and Interface Science, 2012,368(1):505-511. [120]Li X, Pignatello J J, Wang Y, et al. New insight into adsorption mechanism of ionizable compounds on carbon nanotubes [J]. Environmental science & technology, 2013,47(15):8334-8341. [121]Gilli P, Bertolasi V, Ferretti V, et al. Covalent nature of the strong homonuclear hydrogen bond. Study of the O-H-O system by crystal [J]. Journal of the American Chemical Society, 1994,116(3):909-915. [122]Ward M D. Design of crystalline molecular networks with charge- assisted hydrogen bonds [J]. Chemical communications, 2005,(47): 5838-5842. [123]Deng S B, Shuai D M, Yu Q, et al. Selective sorption of perfluorooctane sulfonate on molecularly imprinted polymer adsorbents [J]. Frontiers of Environmental Science & Engineering in China, 2009,3(2):171-177. [124]林 森.聚多巴胺表面功能化及其对水中PFOS分离富集性能研究 [D]. 南昌:南昌航空大学, 2019. Lin S. Surface functionalization of polydopamine and their separation and enrichment performance of PFOS in water [D]. Nanchang: Nanchang Hangkong University, 2019. [125]余 强.水中典型全氟化合物的吸附去除研究 [D]. 北京:清华大学, 2009. Yu Q. Removal of Representative Perfluorinated Compounds from Water by Sorption Process [D]. Beijing: Tsinghua University, 2009. [126]郭会琴,刘 宇,马文天,等.基于生物质碳微球的表面全氟辛磺酸盐(PFOS)分子印迹聚合物的制备及吸附特性[C]. 第21届全国色谱学术报告会及仪器展览会会议论文集, 2017. Guo H Q, Liu Y, Ma W T, et al. Preparation and adsorption properties of biomass carbon microsphere-based molecularly imprinted polymers with perfluorooctane sulfonate (PFOS) on the surface [C]. Proceedings of the 21 st National Chromatography Symposium and Instrument Exhibition, 2017. [127]Li H Y, Brédas J L. Large Out-of-Plane Deformations of two- dimensional covalent organic framework (COF) sheets [J]. The Journal of physical Chemistry Letters, 2018,9(15):4215-4220. [128]Fenlon E E. Double, double trefoil and trouble [J]. Nature Synthesis, 2022,1(8):586-587. [129]Chang P H, Chen C Y, Mukhopadhyay R, et al. Novel MOF- 808metal–organic framework as highly efficient adsorbent of perfluorooctane sulfonate in water [J]. Journal of Colloid and Interface Science, 2022,623:627-636. [130]Hu Y, Guo M M, Zhang S L, et al. Microwave synthesis of metal- organic frameworks absorbents (DUT-5-2) for the removal of PFOS and PFOA from aqueous solutions [J]. Microporous and Mesoporous Materials, 2022,333:111740. [131]Ji W J, Xiao L L, Ling Y H, et al. Removal of GenX and perfluorinated alkyl substances from water by amine-functionalized covalent organic frameworks [J]. Journal of the American Chemical Society, 2018,140(40):12677-12681. [132]孙 博,马 军.水中全氟化合物的活性炭吸附特性研究 [J]. 给水排水, 2017,53(2):14-18. Sun B, Ma J. Study on adsorption characteristic of perfluorinated compounds on activated carbon [J]. Water & Wastewater Engineering, 2017,53(2):14-18. [133]Wu C Y, Klemes M J, Trang B, et al. Exploring the factors that influence the adsorption of anionic PFAS on conventional and emerging adsorbents in aquatic matrices [J]. Water Research, 2020,182:115950. [134]Deng S B, Nie Y, Du Z W, et al. Enhanced adsorption of perfluorooctane sulfonate and perfluorooctanoate by bamboo-derived granular activated carbon [J]. Journal of Hazardous Materials, 2015, 282:150-157. [135]Pauletto P S, Florent M, Bandosz T J. Insight into the mechanism of perfluorooctanesulfonic acid adsorption on highly porous media: Sizes of hydrophobic pores and the extent of multilayer formation [J]. Carbon, 2022,191:535-545. [136]Sörengård M, Östblom E, Köhler S, et al. Adsorption behavior of per- and polyfluoralkyl substances (PFASs) to 44inorganic and organic sorbents and use of dyes as proxies for PFAS sorption [J]. Journal of Environmental Chemical Engineering, 2020,8(3):103744. [137]Furtado R X S, Sabatini C A, Zaiat M, et al. Perfluorooctane sulfonic acid (PFOS) degradation by optimized heterogeneous photocatalysis (TiO2/UV) using the response surface methodology (RSM) [J]. Journal of Water Process Engineering, 2021,41:101986. [138]Park S, Zenobio J E, Lee L S. Perfluorooctane sulfonate (PFOS) removal with Pd0/nFe0nanoparticles: Adsorption or aqueous Fe- complexation, not transformation? [J]. Journal of Hazardous Materials, 2018,342:20-28. [139]Jeon J, Kannan K, Lim B J, et al. Effects of salinity and organic matter on the partitioning of perfluoroalkyl acid (PFAs) to clay particles [J]. Journal of Environmental Monitoring, 2011,13(6):1803-1810. [140]Fagbayigbo B O, Opeolu B O, Fatoki O S, et al. Sorption and partitioning of perfluorooctanoic acid (PFOA) and perfluorooctane sulfonate (PFOS) onto sediments of Diep and Plankenburg river systems Western Cape, South Africa [J]. Environmental Technology & Innovation, 2022,25:102110. [141]王 鹏,张海禄.表面化学改性吸附用活性炭的研究进展 [J]. 炭素技术, 2003,(3):23-28. Wang P, Zhang H L. Progress in surface chemical modification of activated carbon for absorption [J]. Carbon Techniques, 2003,(3):23- 28. [142]Ahmadi A, Yang W W, Jones S, et al. Separation-free Al-Mg/ graphene oxide composites for enhancement of urban stormwater runoff quality [J]. Advanced Composites and Hybrid Materials, 2018, 1:591-601. [143]Hansen M C, Børresen M H, Schlabach M, et al. Sorption of perfluorinated compounds from contaminated water to activated carbon [J]. Journal of Soils and Sediments, 2010,10:179-185. [144]Buckley T, Karanam K, Xu X Y, et al. Effect of mono- and di-valent cations on PFAS removal from water using foam fractionation-A modelling and experimental study [J]. Separation and Purification Technology, 2022,286:120508. [145]Wang F, Shih K, Leckie J O. Effect of humic acid on the sorption of perfluorooctane sulfonate (PFOS) and perfluorobutane sulfonate (PFBS) on boehmite [J]. Chemosphere, 2015,118:213-218. [146]Chang P H, Jiang W T, Li Z. Removal of perfluorooctanoic acid from water using calcined hydrotalcite – A mechanistic study [J]. Journal of Hazardous Materials, 2019,368:487-495. [147]孙建强,洪 雷,贾旭日.微波改性膨润土对水中PFOS的吸附热力学和动力学研究 [J]. 离子交换与吸附, 2017,33(2):10. Sun J Q, Hong L, Jia X R. adsorption thermodynamics and kinetics of PFOS on microwave modified bentonite form aqueous solution [J]. Ion Exchange and Adsorption, 2017,33(2):10. [148]Qian J, Shen M M, Wang P F, et al. Perfluorooctane sulfonate adsorption on powder activated carbon: Effect of phosphate (P) competition, pH, and temperature [J]. Chemosphere, 2017,182:215- 222. [149]许晨敏.水中典型全氟化合物(PFCs)的吸附及光催化降解研究 [D]. 南京:南京理工大学, 2018. Xu C M. Removal of typical perfluorinated compounds(PFCs) by adsorption and photocatalysis [D]. Nanjing:Nanjing University of Science and Technology, 2018. [150]Qu Y, Zhang C J, Li F, et al. Equilibrium and kinetics study on the adsorption of perfluorooctanoic acid from aqueous solution onto powdered activated carbon [J]. Journal of Hazardous Materials, 2009, 169(1-3):146-152. [151]Siriwardena D P, Crimi M, Holsen T M, et al. Influence of groundwater conditions and co‐contaminants on sorption of perfluoroalkyl compounds on granular activated carbon [J]. Remediation Journal, 2019,29(3):5-15. [152]Deng S B, Bei Y, Lu X Y, et al. Effect of co-existing organic compounds on adsorption of perfluorinated compounds onto carbon nanotubes [J]. Frontiers of Environmental Science & Engineering, 2015,9:784–792. [153]Kimura K, Fujii S, Tanaka S, et al. A study on removal characteristics and effect factors of removal of persistent perfluorinated compounds by powdered activated carbon [J]. Eenvironmental Eengineering Rresearch, 2011,45:301-308. [154]Yu J, Lv L, Lan P, et al. Effect of effluent organic matter on the adsorption of perfluorinated compounds onto activated carbon [J]. Journal of Hazardous Materials, 2012,225-226:99-106. [155]Wang W J, Xu Z L, Zhang X X, et al. Rapid and efficient removal of organic micropollutants from environmental water using a magnetic nanoparticles-attached fluorographene-based sorbent [J]. Chemical Engineering Journal, 2018,343:61-68. [156]Wang B Y, Lee L S, Wei C H, et al. Covalent triazine-based framework: A promising adsorbent for removal of perfluoroalkyl acids from aqueous solution [J]. Environmental Pollution, 2016,216:884- 892. [157]Xiao L L, Ling Y H, Alsbaiee A, et al. β-Cyclodextrin polymer network sequesters perfluorooctanoic acid at environmentally relevant concentrations [J]. Journal of the American Chemical Society, 2017,139(23):7689-7692. [158]Qiu Y, Fujii S, Tanaka S. Removal of perfluorochemicals from wastewater by granular activated carbon adsorption [J]. Environmental Engineering Research, 2007,44:185-193. [159]Bao Y P, Niu J F, Xu Z S, et al. Removal of perfluorooctane sulfonate (PFOS) and perfluorooctanoate (PFOA) from water by coagulation: Mechanisms and influencing factors [J]. Journal of colloid and interface science, 2014,434:59-64. [160]洪 雷,丁倩云,亓祥坤,等.吸附法去除水中全氟化合物的研究进展 [J]. 环境化学, 2021,40(7):2193-2203. Hong L, Ding Q Y, Qi X K, et al. The research progress of removing perfluoroalkyl substances by adsorption in water [J]. Environmental Chemistry, 2021,40(7):2193-2203. [161]Chrysikopoulos C V, Syngouna V I. Attachment of bacteriophages MS2 and ΦX174 onto kaolinite and montmorillonite: Extended- DLVO interactions [J]. Colloids and Surfaces B: Biointerfaces, 2012,92(none):74-83. [162]Steenland K, Tinker S, Shankar A. Association of perfluorooctanoic acid (PFOA) and perfluorooctane sulfonate (PFOS) with uric acid among adults with elevated community exposure to PFOA [J]. Environmental Health Perspectives, 2010,118(2):229-233. [163]Uwayezu J N, Yeung L W Y, Bäckström M. Sorption of PFOS isomers on goethite as a function of pH, dissolved organic matter (humic and fulvic acid) and sulfate [J]. Chemosphere, 2019,233:896-904. [164]Schuricht F, Borovinskaya E S, Reschetilowski W. Removal of perfluorinated surfactants from wastewater by adsorption and ion exchange--Influence of material properties,sorption mechanism and modeling [J]. Journal of Environmental Sciences, 2017,54:160-170. [165]Rahman M F, Peldszus S, Anderson W B. Behaviour and fate of perfluoroalkyl and polyfluoroalkyl substances (PFASs) in drinking water treatment: A review [J]. Water Research, 2014,50:318-340. [166]Franke V, McCleaf P, Lindegren K, et al. Efficient removal of per- and polyfluoroalkyl substances (PFASs) in drinking water treatment: nanofiltration combined with active carbon or anion exchange [J]. Environmental Science: Water Research & Technology, 2019,5(11): 1836-1843. [167]Kucharzyk K H, Darlington R, Benotti M, et al. Novel treatment technologies for PFAS compounds: A critical review [J]. Journal of Environmental Management, 2017,204(Part 2):757-764. [168]Shivakoti B R, Fujii S, Nozoe M, et al. Perfluorinated chemicals (PFCs) in water purification plants (WPPs) with advanced treatment processes [J]. Water Science and Technology: Water Supply, 2010, 10(1):87-95. [169]DeWitt J C. Toxicological effects of perfluoroalkyl and polyfluoroalkyl substances [R]. Springer, 2015. [170]Zhi Y, Liu J X. Sorption and desorption of anionic, cationic and zwitterionic polyfluoroalkyl substances by soil organic matter and pyrogenic carbonaceous materials [J]. Chemical Engineering Journal, 2018,346:682-691. [171]Salvador F, Martin-Sanchez N, Sanchez-Hernandez R, et al. Regeneration of carbonaceous adsorbents. Part I: Thermal Regeneration [J]. Microporous and Mesoporous Materials, 2015,202: 259-276. [172]白玉洁,张爱丽,周集体.吸附剂再生技术的研究进展 [J]. 辽宁化工, 2012,41(1):21-24. Bai Y J, Zhang A L, Zhou J T. Research process in regeneration technologies of sorbents [J]. Liaoning Chemical Industry, 2012,41(1):21-24. [173]孙政钊.关于吸附剂再生技术的研究 [J]. 化工管理, 2014,(32):103. Sun Z Z. Research on adsorbent regeneration technology [J]. Chemical Enterprise Management, 2014,(32):103. [174]邓 勤,马少健,周显文.水处理吸附剂的再生技术研究进展 [C]. 第十三届全国粉体工程及矿产资源高效开发利用研讨会论文专辑, 2007. Deng L, Ma S J, Zhou X W. Progress in water treatment adsorbents regeneration [C]. The Thirteenth National Symposium on Powder Engineering and Efficient Development and Utilization of Mineral Resources Paper Series, 2007. [175]Zhu R L, Zhu J X, Ge F, et al. Regeneration of spent organoclays after the sorption of organic pollutants: A review [J]. Journal of Environmental Management, 2009,90(11):3212-3216. [176]Moreno-Castilla C, Rivera-Utrilla J, Joly J P, et al. Thermal regeneration of an activated carbon exhausted with different substituted phenols [J]. Carbon, 1995,33(10):1417-1423. [177]Alalm M G, Boffito D C. Mechanisms and pathways of PFAS degradation by advanced oxidation and reduction processes: A critical review [J]. Chemical Engineering Journal, 2022,450:138352. [178]Bao Y X, Deng S S, Jiang X S, et al. Degradation of PFOA substitute: GenX (HFPO-DA ammonium Salt): oxidation with UV/persulfate or reduction with UV/sulfite? [J]. Environmental Science & Technology, 2018,52(20):11728-11734. [179]Kumar M, Xiong X N, Sun Y Q, et al. Critical review on biochar- supported catalysts for pollutant degradation and sustainable biorefinery [J]. Advanced Sustainable Systems, 2020,4(10):1900149. [180]Khan M Y, Sui S, Gabriel da Silva. Decomposition kinetics of perfluorinated sulfonic acids [J]. Chemosphere, 2020,238:124615. [181]Riedel T P, Wallace M A G, Shields E P, et al. Low temperature thermal treatment of gas-phase fluorotelomer alcohols by calcium oxide [J]. Chemosphere, 2021,272:129859. [182]Margallo M, Taddei M B M, Hernández-Pellón A, et al. Environmental sustainability assessment of the management of municipal solid waste incineration residues: a review of the current situation [J]. Clean Technologies and Environmental Policy, 2015,17 (5):1333-1353. [183]Merino N, Qu Y, Deeb R A, et al. Degradation and removal methods for perfluoroalkyl and polyfluoroalkyl substances in water [J]. Environmental Engineering Science, 2016,33(9):615-649. [184]Feng M B, Qu R J, Zhong B W, et al. Characterization of the thermolysis products of Nafion membrane: A potential source of perfluorinated compounds in the environment [J]. Scientific Reports, 2015,5(1):9859. [185]Ellis D A, Martin J W, Muir D C G, et al. The use of 19F NMR and mass spectrometry for the elucidation of novel fluorinated acids and atmospheric fluoroacid precursors evolved in the thermolysis of fluoropolymers [J]. Analyst, 2003,128(6):756-764. [186]Watanabe N, Takata M, Takemine S, et al. Thermal mineralization behavior of PFOA, PFHxA, and PFOS during reactivation of granular activated carbon (GAC) in nitrogen atmosphere [J]. Environmental Science and Pollution Research, 2018,25(8):7200-7205. [187]Dhillon G S, Rosine G M L, Kaur S, et al. Novel biomaterials from citric acid fermentation as biosorbents for removal of metals from waste chromated copper arsenate wood leachates [J]. International Biodeterioration & Biodegradation, 2017,119:147-154. [188]Solo-Gabriele H M, Jones A S, Lindstrom A B, et al. Waste type, incineration, and aeration are associated with per- and polyfluoroalkyl levels in landfill leachates [J]. Waste Management, 2020,107:191-200. [189]Lang J R, Allred B M K, Field J A, et al. National estimate of per- and polyfluoroalkyl substance (PFAS) release to U.S. municipal landfill leachate [J]. Environmental Science & Technology, 2017,51(4):2197-2205. [190]Wang B, Yao Y M, Chen H, et al. Per- and polyfluoroalkyl substances and the contribution of unknown precursors and short-chain (C2-C3) perfluoroalkyl carboxylic acids at solid waste disposal facilities [J]. The Science of the Total Environment, 2020,705:135832. [191]Kallenborn R, Berger U, Jarnberg U, et al. Perfluorinated alkylated substances (PFAS) in the nordic environment [M]. Copenhagen: Nordic Council of Ministers, 2004. [192]Gallen C, Drage D, Eaglesham G, et al. Australia-wide assessment of perfluoroalkyl substances (PFASs) in landfill leachates [J]. Journal of Hazardous Materials, 2017,331:132-141. [193]Huset C A, Barlaz M A, Barofsky D F, et al. Quantitative determination of fluorochemicals in municipal landfill leachates [J]. Chemosphere, 2011,82(10):1380-1386. [194]Zhang C H, Peng Y, Ning K, et al. Remediation of perfluoroalkyl substances in landfill leachates by electrocoagulation [J]. CLEAN– Soil, Air, Water, 2014,42(12):1740-1743. [195]Yan H, Cousins I T, Zhang C J, et al. Perfluoroalkyl acids in municipal landfill leachates from China: occurrence, fate during leachate treatment and potential impact on groundwater [J]. Science of the Total Environment, 2015,524-525:23-31. [196]Stoiber T, Evans S, Naidenko O V. Disposal of products and materials containing per- and polyfluoroalkyl substances (PFAS): A cyclical problem [J]. Chemosphere, 2020,260:127659. Research progress on adsorption technologies for PFAS removal from water. WANG Tu1,2, BAO Yi-xiang2*, ZHONG Jin-kui1, LI Jing-feng2, CAO Zhi-guo2, WU Min2 (1.School of Environmental and Municipal Engineering, Lanzhou Jiaotong University, Lanzhou 730070, China;2.State Key Laboratory of Water Resource Protection and Utilization in Coal Mining, National Institute of Clean and Low Carbon Energy, Beijing 102209, China)., 2023,43(12):6413~6434 In this paper, the adsorption properties, mechanisms, influencing factors, advantages and potential problems of different adsorbents (activated carbon, resin, mineral materials, molecularly imprinted polymers, bio-based materials, etc.) for PFAS removal were summarized. Adsorbents with similar pore size to PFAS molecules, and with opposite surface charge had higher adsorption capacity to PFAS. Lower pH and higher temperature are more favorable for PFAS adsorption, and coexisting organic matter will compete with PFAS on adsorption. The adsorption performance of the adsorbent to PFAS was positively correlated with its chain length, and the adsorption capacity of the adsorbent to PFAS containing sulfonic group was higher than that of PFAS with carboxylic group at the same chain length. The main adsorption mechanisms include electrostatic attraction, hydrophobic interaction, ion exchange, ligand exchange, etc. The reasonable regeneration and disposal of adsorbents was a common problem in practical engineering applications, such as poor regeneration effect of chemical regeneration and biological regeneration, high energy consumption of thermal regeneration, easy to cause secondary pollution by solvent regeneration or landfill treatment. By reviewing the research progress of adsorption removal materials and technologies for PFAS from water, the advantages and disadvantages of different technologies are systematically expounded, and the research direction of adsorption removal technology is prospected, which could provide reference for PFAS pollution control in water. PFAS;adsorption;mechanism;engineering applications;regeneration;emerging pollutants X703.1 A 1000-6923(2023)12-6413-22 王 菟,包一翔,钟金魁,等.水中PFAS吸附去除技术研究进展 [J]. 中国环境科学, 2023,43(12):6413-6434. Wang T, Bao Y X, Zhong J K, et al. Research progress on adsorption technologies for PFAS removal from water [J]. China Environmental Science, 2023,43(12):6413-6434. 2023-04-21 国家自然科学基金青年基金资助项目(52100070);国家能源集团科技创新项目(SZY93002219N) * 责任作者, 高级工程师, baoja2008@163.com 王 菟(1999-),男,甘肃张掖人,兰州交通大学硕士研究生,主要研究方向为水污染控制.17718654733@163.com.1.2 树脂吸附

1.3 矿物材料吸附
1.4 生物基材料吸附
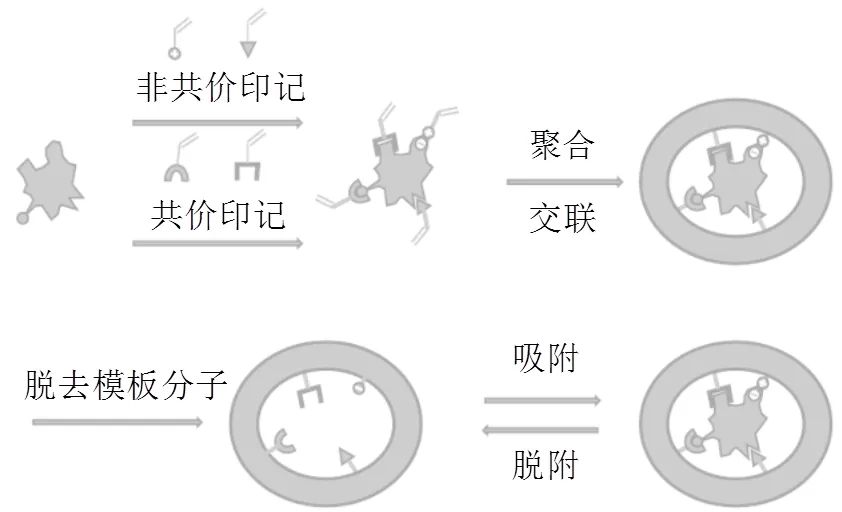
1.5 分子印迹聚合物吸附
1.6 其他吸附材料
2 影响PFAS吸附效果的关键因素
2.1 吸附剂结构的影响
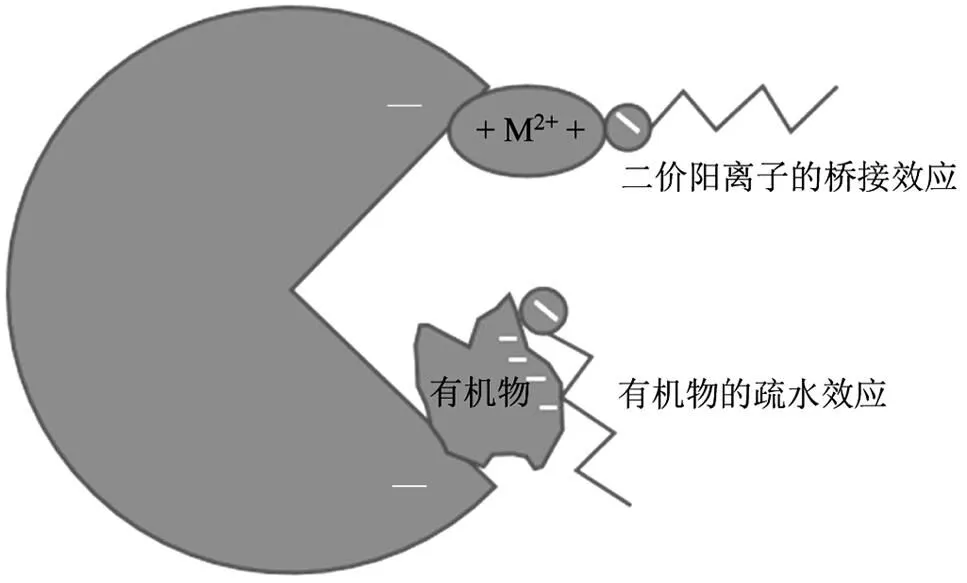
2.2 水质条件的影响
2.3 PFAS分子结构的影响
3 工程应用
4 吸附剂的处置
4.1 吸附剂再生处置
4.2 吸附剂焚烧处置
4.3 吸附剂填埋处置
5 结论与展望
