Al-淀粉配合物对白钨矿浮选中微细粒方解石的选择性抑制行为及机理
2023-12-16王若林韩海生孙文娟孙伟张洪亮程永彪
王若林,韩海生,孙文娟,孙伟,张洪亮,程永彪
1. 山东理工大学 资源与环境工程学院,山东 淄博 255000;
2. 中南大学 资源加工与生物工程学院,湖南 长沙 410083;
3. 中南大学 战略含钙矿物资源清洁高效利用湖南省重点实验室,湖南 长沙 410083;
4. 湖南省伴生萤石综合利用氟化学工程技术研究中心,湖南 郴州 423000;
5. 中化蓝天集团有限公司,浙江 杭州 310023
1 引言
钨资源是我国重要的战略资源,在航空航天、军事、医学、化工、电子电气、加工制造、高端材料制备等国民经济和国防领域有着非常广泛的应用[1-3]。随着我国钨资源的不断开发与利用,黑钨矿逐渐匮乏,而白钨矿逐渐贫细杂化[4]。由于白钨矿普遍原矿品位较低、组成成分复杂、与脉石嵌布关系紧密,直接导致了磨矿及分选过程中脉石矿物的细化[5]。同时,钨浮选精矿产品粒度细化成为典型钨多金属矿资源的选矿现状[6],因而微细粒方解石等脉石矿物成为阻碍白钨矿浮选指标提升的关键因素。
方解石在风化、开采、破碎、磨矿过程中容易发生过碎和泥化[7]。常规粒级的方解石(38~75 μm),通过表面转化使其表面生成难被苯甲羟肟酸铅(Pb-BHA)捕收的氟化物[8],或通过无机抑制剂的选择性吸附[9],可以实现有效抑制。但是微细粒级方解石的大比表面积使其与Pb-BHA 捕收剂反应的活性位点增多,增大了与伴生白钨矿的竞争吸附[10],从而降低了白钨矿与捕收剂的反应[11]以及与气泡的附着概率[12]。除此之外,由于细粒方解石等脉石矿物的比表面积较大、表面能较高[13-14],容易与白钨矿发生非选择性团聚,从而影响浮选分离的指标。
为了解决白钨矿与微细粒方解石的分离问题,国内外的学者常采用无机抑制剂和有机抑制剂。无机抑制剂主要有硅酸盐类抑制剂、磷酸盐类抑制剂[15],但其存在消耗量大、适应性差、抑制能力有限、精尾矿产品沉降过滤及选矿水处理困难等问题[16]。有机抑制剂主要包括单宁类、纤维素类、聚糖类、聚羧酸类、淀粉类等。但这些抑制剂通过特定的羟基或羧基等官能团[17],与白钨矿、方解石等含钙矿物的Ca 活性位点作用[18],因而未经过改性时选择性较差,难以实现有用矿物与脉石矿物的浮选分离。相比于其他有机抑制剂,淀粉只有羟基官能团,这既是其选择性、可溶性差的原因,又是利于改性处理的优势所在。在淀粉的诸多羟基中,伯醇基羟基为支链羟基,其他位置的羟基则均与主体环结构相连,因而伯醇基羟基具有更高的活性,在改性过程中更容易发生反应[19]。近年来的金属离子配合物理论,如Pb-BHA 捕收剂[20]和Ca-油酸捕收剂[21]等,为提高浮选药剂的选择性提供了一种新方法。在金属离子配位化合物中,配位金属离子起着重要作用[22]。而有关金属离子对淀粉的改性,仅仅局限在赤铁矿和石英的分离[23],在白钨矿与微细粒方解石浮选分离中的作用机理及相关的应用还未见报道。本研究在此基础上,设计开发了Al-淀粉配合物,剖析了配合物的分子结构及浮选效果,研究了该抑制剂对微细粒级方解石的选择性抑制效果及作用机理。
2 实验材料及方法
2.1 实验样品
实验所用的白钨矿和方解石单矿物购买于广州市花都区花东叶氏石头标本商行,白钨矿单矿物破碎、磨矿至-38 μm,方解石则破碎、磨矿至-19 μm。细粒级白钨矿、方解石的平均粒径分别为15.304 μm、7.627 μm,累积含量80%的粒径分别是24.446 μm、11.092 μm。图1 为白钨矿和方解石的XRD 图谱,其结果表明两矿物的纯度均大于97%。
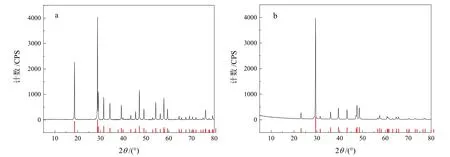
图1 单矿物X 射线衍射分析结果(a—白钨矿;b—方解石)Fig. 1 X-ray diffraction analysis of pure minerals (a: scheelite; b: calcite)
实验所用的实际矿石为湖南某多金属难选钨矿石,该实际矿石主要组成矿物含量如表1 所示,实际矿石中白钨矿和方解石的MLA 图谱如图2 所示。结果表明,钨矿物(白钨矿与黑钨矿)的总含量为0.33%,脉石矿物以方解石、石榴石为主。采用Pb-BHA 捕收剂配合盐化水玻璃(Al-Na2SiO3),可以在精选段有效地实现钨与硅酸盐矿物的浮选分离。而方解石粒度细、嵌布连生复杂且易泥化,因而该矿石浮选的关键在于微细粒方解石的抑制。

表1 主要矿物组成及含量分析结果Table 1 Analysis results of mian mineral composition and content

图2 实际矿石中白钨矿、方解石的MLA 彩图Fig. 2 MLA color map of scheelite and calcite in actual ore
2.2 实验药剂
实验所用的药剂信息如表2 所示。分析纯的可溶性淀粉与氢氧化钠按照5∶1 质量比,加入去离子水中,在恒温加热磁力搅拌器中90 ℃水浴加热并搅拌45 min,从而制得实验所用的苛化淀粉。制得的苛化淀粉与分析纯的硫酸铝,按照实验所需的不同质量比混合,在常温下搅拌20 min,从而得到所需的Al-淀粉。
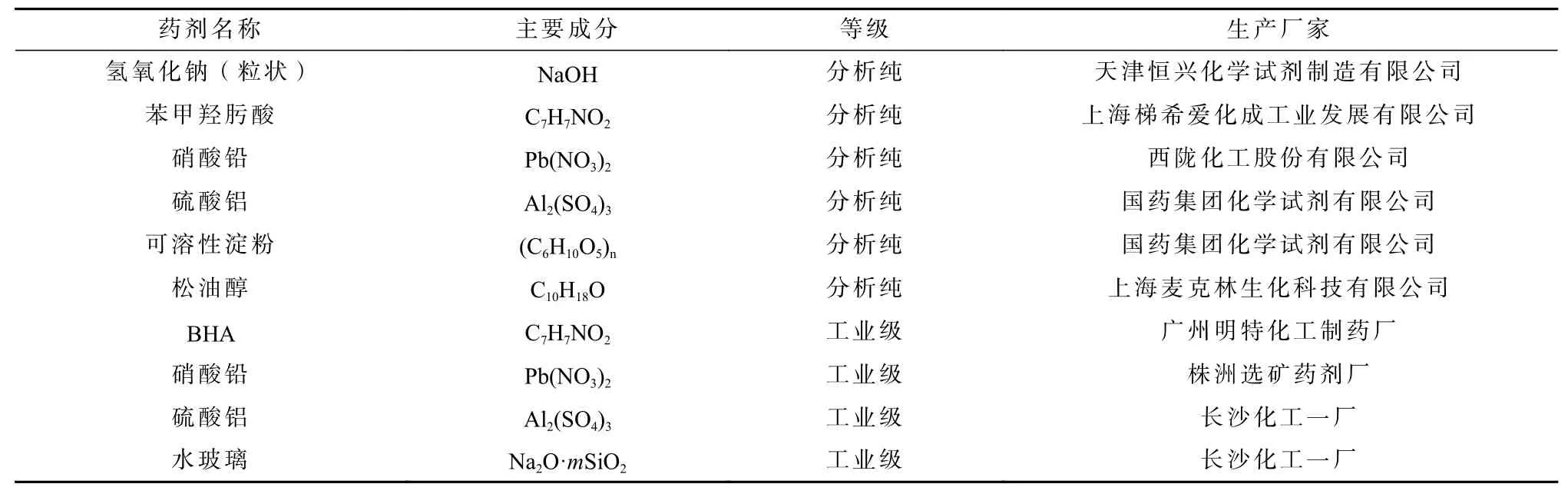
表2 实验所用药剂Table 2 Reagents used in experiments
2.3 浮选实验
2.3.1 单矿物实验
单矿物实验所用设备为XFG Ⅱ型实验室挂槽式浮选机(吉林省探矿机械厂),浮选槽规格为40 mL,转速为1 650 r/min,浮选温度为25 ℃。单矿物实验每次称取2.0 g 单矿物,加入35 mL 去离子水中制成浮选矿浆,依次加入抑制剂(Al-淀粉)、捕收剂(Pb 与BHA摩尔比1∶1 的Pb-BHA 配合物)、pH 调整剂(NaOH)、起泡剂(松油醇)。除去起泡剂搅拌时间为1 min 外,其他药剂加入后均搅拌3 min。药剂充分作用后,每隔6 s 刮一板,刮泡过程持续3 min,共计30 板。将刮出的泡沫精矿产品及浮选槽中的尾矿产品分别收集、过滤,在60 ℃下烘干、称重。按照公式(1)计算相应的回收率[24]:
式中:ε-精矿回收率,%;
m1-精矿产品的质量,g;
m2-尾矿产品的质量,g。
2.3.2 实际矿石实验
实际矿石实验所使用的设备型号为XFD Ⅳ型实验室单槽式浮选机(吉林省探矿机械厂),分别使用3 L、1.5 L、0.75 L 及0.5 L 浮选槽及其对应的浮选机。固定转速为1 900 r/min,浮温度为20~25 ℃。条件实验选用0.5 L 浮选机;开路实验粗选选用1.5 L 或3.0 L浮选机,精一选用0.75 L 的浮选机,精二、精三及后续精选选用0.5 L 的浮选机。浮选产品收集后烘干、称重、化验,并按照公式(2)计算回收率:
式中:εj-浮选环节中第j种成分的回收率,%;
m、m总-浮选环节的精矿质量、原矿总质量,g;
βj、β总-浮选环节精矿中第j种成分的品位、原矿品位,%。
2.4 Zeta 电位分析
Zeta 电位测试选用Mal ZEN3690/Nano ZS90 型(英国马尔文仪器有限公司)电位测试仪,测试温度为25 ℃。预先在玛瑙三头研磨机上细磨待测样品至-2 μm,并预先配制10 mmol/L 的KNO3溶液作为电解质溶液。每次测量称取20 mg 已预处理好的待测样品,加入40 mL 电解质溶液中,磁力搅拌器搅拌1 min,按照单矿物浮选的流程加入相应的药剂并调节pH 值。充分反应后静置10 min,取上清液注入Malvern Zetasizer样品池中,在Zetasizer Nano 软件中选定待测样品参数、分散剂类型及样品池类型并进行测试。每个样品测量3 次,记录相应的Zeta 电位值后取平均值[25]。
2.5 红外光谱分析
红外光谱测试选用NEXUS-670 型(美国Nicolet公司)傅立叶红外光谱仪,测试方法为漫反射法,测试范围为波长400~4 000 cm-1。待测样品的制备方法为:测试样品经玛瑙研钵研磨至粒度< 2 μm 后,按照单矿物浮选的方法,称取1.0 g 合格粒度的单矿物加入40 mL去离子水中,搅拌均匀后加入相应的药剂充分作用20 min,然后将样品过滤,洗涤3 次后在40 ℃下真空干燥。待测样品的测试方法:称取待测样品0.1 g,均匀地洒在漫反射专用样品台上,置入仪器内进行红外光谱测试,并记录相应的实验数据,每次实验重复三次。
2.6 X 射线光电子能谱分析
X 射线光电子能谱测试在K-Alpha 1063 型(Thermo Fisher Scientific)XPS 能谱仪上进行测试。待测样品的制备及测试方法:测试样品为单矿物浮选实验用的白钨矿、方解石单矿物,按照单矿物浮选的方法,称取2.0 g 单矿物加入40 mL 去离子水中,搅拌后加入相应的浮选药剂并充分反应30 min,然后用漏斗边过滤边冲洗,洗涤5 次后在真空干燥箱中40 ℃低温干燥。每次取0.5 g 样品进行测试,测试结果在XPS Peak 41软件上进行分峰、拟合等分析[26]。
2.7 团簇模型计算
团簇模型通过Gaussview 6.0 软件建立,并通过Gaussian 09 D.01 版本进行模型优化处理。所有的计算均依据B3LYP 密度泛函模型、采用DFT 方法进行量子化学计算。其中,H、C 和O 等轻原子采用了augccc-pvdz 的全电子基集,而Al 原子采用了具有相对有效核势的augc-cc-pvdz-pp 基集。此外,为了充分考虑溶剂化的影响,采用SMD 连续溶剂化模型,以水为溶剂来考虑溶剂化效应[27]。几何优化中,最大力、均方根力、最大位移和均方根位移的收敛公差分别设置为4.5 × 10-4、3.0 × 10-4、1.8 × 10-3和1.2 × 10-3,以保证在后续的频率分析中,优化后的结构均没有出现虚频。通过团簇模型计算,得到淀粉单分子及其金属离子螯合配位的最佳结构[28]。
3 实验结果与讨论
3.1 药剂分子的合成及产物表征
淀粉的化学式为(C6H10O5)n,其单分子为葡萄糖分子。主体为含O 的六元环,每个C 结合一个羟基(-OH),支链为-CH2OH,这使得淀粉在特定条件下具有类似于醇类有机物的化学性质。淀粉具有“五碳一氧”的环状结构,这部分环状结构较为稳定,一般情况下不会发生反应。环结构中碳原子之间连接的羟基(-OH),受环状结构的影响,性质不活泼。只有伯醇基支链(-CH2OH)中的羟基,受环状结构影响小,性质较为活泼。在碱性条件下,淀粉支链中的羟基可以与NaOH 反应,生成-CH2O-Na。由于含钠盐在水溶液中易离解出钠离子,在外加与淀粉单分子摩尔比为1∶1 的铝离子作用下,与氧连接的Na+被替代为Al3+,生成-CH2O-Al2+基团,反应如图3 所示。
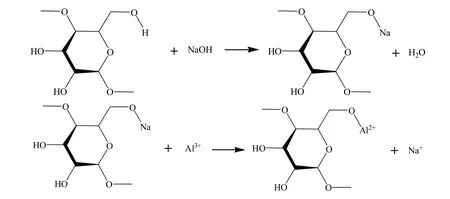
图3 Al-淀粉分子的合成反应Fig. 3 Synthetic reaction of Al-starch
淀粉单分子结构存在反式结构与顺式结构两种,其主要差别在于-CH2OH 支链中羟基的位置。图4a为淀粉单分子的反式结构,其不同的O 原子具有不同的带电子能力,支链羟基中的O6原子NPA 荷电最大,电荷值为-0.821;“五碳一氧”环结构中的O5原子NPA荷电最小,其值为-0.548。这一结果表明,淀粉单分子的O6原子的活性最高,而O5原子的活性最差。淀粉单分子的顺式结构的电荷分布也有类似的结果,如图3-b 所示。O1、O2、O3、O4、O5、O6的NPA 电荷分别为-0.803、-0.807、-0.804、-0.791、-0.655、-0.815。由此可知,支链羟基的O6原子是淀粉单分子结构中的活性原子,在与金属离子的结合过程中可能具有优先权。
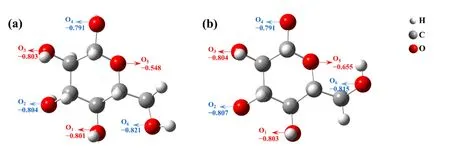
图4 淀粉单分子的NPA 电荷分布(a—反式结构;b—顺式结构)Fig. 4 NPA charge distribution of starch monomolecular optimization structure (a: trans-structure; b: Cis-structure)
铝离子与淀粉的团簇吸附模型如图5 所示。反式淀粉单分子与Al3+的配合物构型中,O1-Al-O6螯合配位结构的Al-O 平均键长最短,为1.727 Å(1 Å=0.1 nm);O4-Al-O5螯合配位构型的平均键长最大,达到了1.867 Å。顺式淀粉单分子与与Al3+螯合配位不同构型的平均键长则略有不同。O1-Al-O2和O2-Al-O3构型的平均键长最短,分别为1.745 Å和1.745 Å;O4-Al-O5螯合配位构型的最长,平均键长为1.844 Å。O1-Al-O6螯合配位构型的键长比其他构型都短,说明螯合配位过程中反式淀粉分子中的O1和O6与Al3+容易成键,O1-Al-O6结构更具有优势。

图5 铝离子与淀粉单分子螯合配位的优化模型(a1~e1—Al3+-反式淀粉分子;a2~e2—Al3+-顺式淀粉分子)Fig. 5 Optimal model of the chelation of aluminum ions and starch molecules (a1 ~ e1—Al3+-trans starch molecules; a2 ~ e2—Al3+-cis starch molecules)
铝离子与淀粉螯合配位后产生了特定的金属基团,通过红外光谱对特征峰的变化进行了表征,结果如图6 所示。结果表明,与铝离子螯合后,淀粉的C-H 变形振动吸收区峰由646.05 cm-1、717.40 cm-1和759.83 cm-1分别偏移至668.25 cm-1、739.61 cm-1和782.04 cm-1,O-H 面外变形振动吸收峰由862.04 cm-1和931.46 cm-1分别偏移至884.24 cm-1和953.67 cm-1,C-O、C-OH 和C-O-C 拉伸振动吸收峰分别由1 074.17 cm-1、1 143.60 cm-1、1 240.03 cm-1和1 342.24 cm-1分别偏移至1 096.39 cm-1、1 165.81 cm-1、1 262.23 cm-1和1 364.45 cm-1,C-O 变角区和C-H 不对称拉伸区振动吸收峰由1 645.01 cm-1和2 923.60 cm-1分别偏移至1 667.22 cm-1和2 849.39 cm-1,游离的O-H 拉伸振动吸收峰由3 345.95 cm-1分别偏移至3 246.66 cm-1。更重要的是,在3 518.58 cm-1波长处出现了缔合的O-H 拉伸振动吸收峰,对应羟基与金属离子反应生成的-O-Al 官能团。
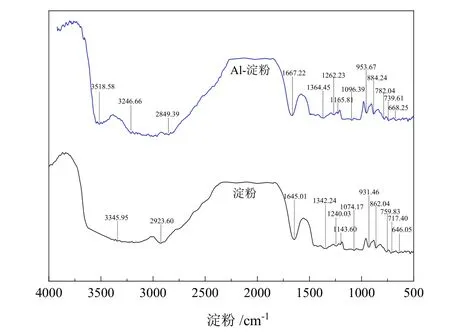
图6 淀粉和Al-淀粉红外特征峰的变化Fig. 6 Change of FTIR characteristic peaks of starch and Al-starch
这一结果表明,金属铝离子与淀粉反式结构的O1和O6,通过螯合配位作用形成稳定的Al-淀粉单分子,生成了新的-O-Al 官能团,这一官能团是提升抑制剂选择性的关键。
3.2 药剂的作用效果
3.2.1 单矿物浮选
细粒级白钨矿和方解石在Pb-BHA 作用下的浮选行为如图7 所示。无论是白钨矿还是方解石,其回收率随着pH 的增大,呈现出先增大后减小的变化趋势。更重要的是,在整个浮选pH 区间内,方解石的回收率始终高于白钨矿,但二者相差不大,说明在不添加抑制剂的前提下,两种矿物的浮选分离难以实现。
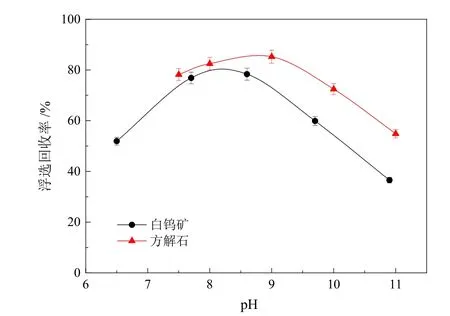
图7 Pb-BHA 捕收剂体系下细粒级白钨矿与方解石的浮选回收率(c(Pb-BHA) = 1.5×10-4 mol/L,c(松油醇) = 12.5 μL/L)Fig. 7 Flotation behaviors of scheelite and calcite under Pb-BHA collector system
不同质量比的Al-淀粉(固定苛化淀粉用量,改变铝离子用量)对白钨矿和方解石浮选的影响如图8 所示。单一淀粉的选择性较差,对白钨矿和方解石均会产生抑制作用。相比于苛化淀粉,Al-淀粉的选择性及抑制效果明显提升。质量比为1∶2 的Al-淀粉(5 mg/L的铝离子与10 mg/L 的淀粉反应制得),加入后白钨矿的回收率可达69.50%,且Al-淀粉质量比的增大基本不会影响白钨矿的回收率。方解石回收率的变化则明显不同,随着Al-淀粉质量比的增大,方解石的回收率由不加铝离子时的43.11%持续下降至22.74%。结果表明,Al-淀粉配合物的选择性明显优于单一苛化淀粉,可以选择性抑制方解石而不影响白钨矿。
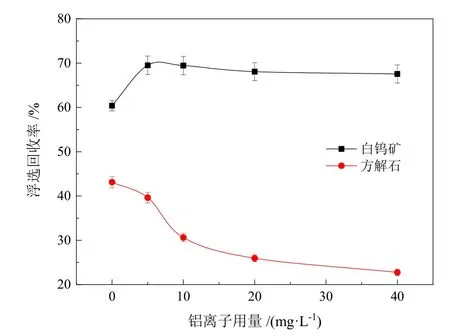
图8 不同质量比的Al-淀粉对白钨矿和方解石单矿物浮选的影响(pH = 8.5,c(淀粉) = 10 mg/L,c(Pb-BHA) = 1.5×10-4 mol/L,c(松油醇) = 12.5 μL/L)Fig. 8 Effect of Al-starch with different mass ratio on scheelite and calcite.
3.2.2 实际矿石浮选
在单矿物实验的基础上,开展实际矿石实验研究,最终确定如图9 所示的闭路实验流程,实验结果见表3。由结果可知,不加抑制剂时精矿WO3品位为31.44%、回收率为64.81%;加入Al-淀粉配合物后精矿WO3品位为40.51%、回收率为61.52%。同时,精矿中方解石含量由16%减少至5%以下。这一结果表明,相同闭路实验流程下,加入Al-淀粉配合物可以显著减少精矿中方解石含量、提升精矿WO3品位,实现浮选指标的大幅度提高。
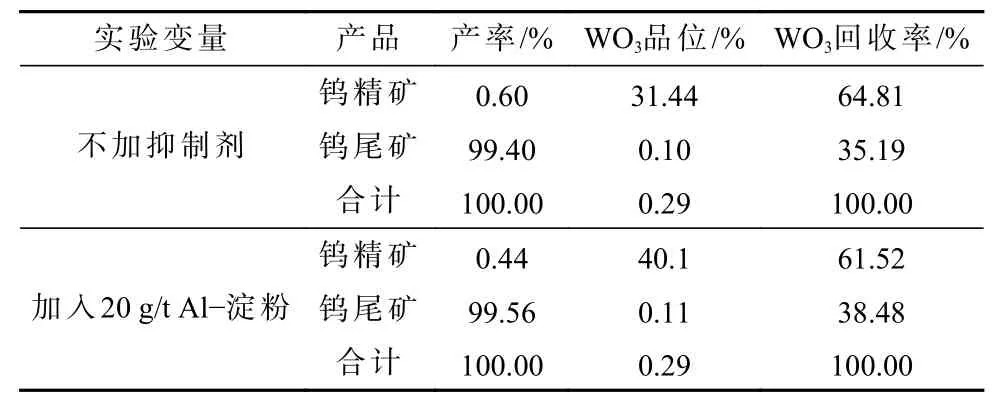
表3 闭路实验结果Table 3 Result of closed-circuit experiment
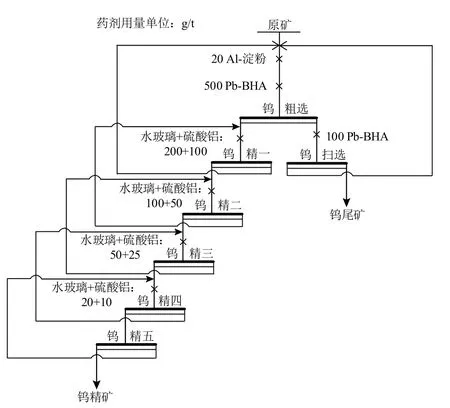
图9 Al-淀粉配合物闭路实验流程Fig. 9 Flowsheet of closed-circuit experiment of Al-starch complexes
3.3 药剂的抑制机理
3.3.1 Zeta 电位分析
苛化淀粉的Zeta 电位如图10a 所示,这一抑制剂的电位在整个测试区域内始终低于-15 mV,且随着pH 的增大而减小。铝离子与淀粉反应生成的配合物,其Zeta 电位大于苛化淀粉,增大幅度达到10~15 mV。
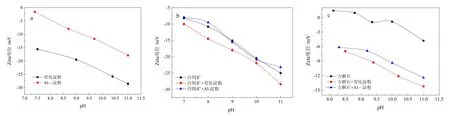
图10 抑制剂(a)及其对白钨矿(b)和方解石(c)Zeta 电位的影响Fig. 10 Zeta potential of depressants (a), scheelite (b) and calcite (c)
图10 b 为不同抑制剂处理前后白钨矿表面Zeta电位的变化。未经处理的白钨矿Zeta 电位介于苛化淀粉和Al-淀粉两种抑制剂之间。白钨矿的Zeta 电位在pH 为7.0 时达到-8.2 mV,且随着pH 的增加而减小;在pH 为11.0 时达到-25 mV。苛化淀粉处理后,Zeta电位减小2~3 mV,说明苛化淀粉在白钨矿表面发生弱吸附作用。不同的是,Al-淀粉处理后白钨矿的Zeta 电位保持不变,说明Al-淀粉没有吸附在白钨矿表面。
方解石表面Zeta 电位的变化如图10c 所示。未经处理的方解石Zeta 电位高于苛化淀粉和Al-淀粉,并随着pH 的增加呈下降趋势。方解石的等电点(IEP)在8.8~9.3 之间。苛化淀粉处理后,方解石的Zeta 电位在pH 8.0~11.0 时完全变为负值,降低幅度可以达到8~10 mV。方解石的Zeta 电位在Al-淀粉处理时也荷负电,降低幅度为7~9 mV,略小于苛化淀粉处理时。这一结果表明,苛化淀粉和Al-淀粉都能吸附在方解石表面降低其表面电荷,但Al-淀粉对白钨矿的表面电荷影响不大,而苛化淀粉能显著改变白钨矿的表面电荷。
3.3.2 XPS 分析
XPS 分析结果如表4 所示,方解石未处理表面存在Ca、O 和C 三种原子,其含量分别为18.96%、49.29%和31.75%。苛化淀粉与方解石表面反应后,O 的原子含量增大0.43 百分点,Ca 的原子含量减少0.53 百分点。尽管Al-淀粉处理后方解石原子浓度的变化与苛化淀粉类似,但该抑制剂作用时的影响更大。经过Al-淀粉处理后,方解石O 的原子含量增加1.92 百分点、Ca 的原子含量减小1.64 百分点。更重要的是,方解石表面出现Al 原子,其含量达到1.69%。结果表明苛化淀粉通过羟基、Al-淀粉通过特定的Al 原子,作用在方解石的表面。
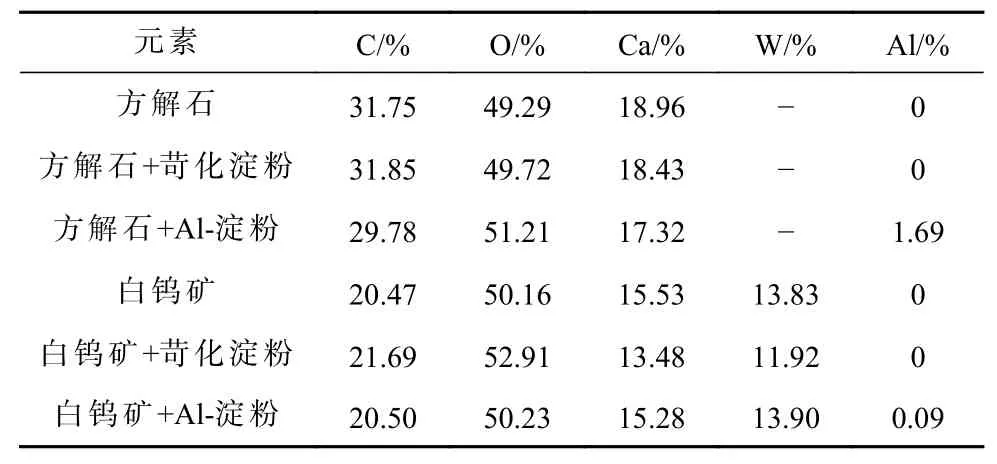
表4 不同条件下方解石和白钨矿的原子含量变化Table 4 Atomic content of calcite and scheelite with different treatment
白钨矿表面初始特征原子主要是Ca、O 和W,而C 原子是测试背景造成的。苛化淀粉处理后C 和O的原子浓度分别增加1.22 百分点和2.75 百分点,而Al-淀粉作用时白钨矿的特征原子浓度变化幅度较小,说明苛化淀粉可以在白钨矿表面发生吸附,而Al-淀粉未在白钨矿发生作用。
苛化淀粉和Al-淀粉的XPS 总能谱如图11a 所示。苛化淀粉的C 1s 和O 1s 能谱分别为285.19 eV 和532.19 eV,Na 1s 的特征原子出现在1 071.19 eV 的结合能处。类似地,Al-淀粉在相同的结合能下出现了C 1s、O 1s 和Na 1s 的特征峰,但Na 1s 峰的相对强度明显降低。同时,在结合能为75.09 eV 处出现了一个较强的峰,即Al 原子的特征峰。
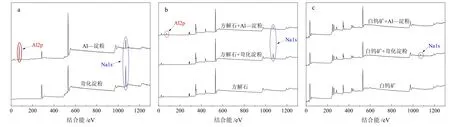
图11 抑制剂(a)、方解石(b)和白钨矿(c)的XPS 总能谱Fig. 11 XPS energy spectrum of reagents (a), calcite (b) and scheelite (c)
方解石的初始能谱如图11b 所示,主要包括C 1s、Ca 2p 和O 1s 的特征峰。苛化淀粉处理后,方解石表面在结合能1 071.19 eV 处出现了Na 1s 原子峰。同样地,Al-淀粉处理后,方解石表面也检测到1 071.19 eV结合能处的Na 1s 原子峰,这一峰的相对强度弱于苛化淀粉处理时。更重要的是,在结合能为75.09 eV 时出现了一个新的Al 原子峰。这些特征原子峰进一步证实了Al-淀粉和苛化淀粉均在方解石表面发生了化学吸附。
白钨矿表面特征原子总能谱如图11c 所示。白钨矿的初始能谱包括Ca 2p、W 4f 和O 1s 的峰,其在苛化淀粉和Al-淀粉处理后的特征原子总能谱则发生不同的变化。在苛化淀粉处理时,Na 1s 峰出现在结合能1 071.19 eV 处。而当Al-淀粉处理时,Na 1s 峰和Al 2p 峰均没有出现在相应的位置。这一结果与白钨矿浮选一致,即苛化淀粉在白钨矿表面发生化学吸附,产生抑制作用,而Al-淀粉不会在白钨矿表面发生吸附并产生抑制效果。
为了进一步研究不同抑制剂处理前后方解石特征原子的变化,对方解石特征原子对应的峰进行划分拟合,结果如图12 所示。未处理方解石表面Ca 原子的2p1/2 和2p3/2 峰分别在346.99 eV 和350.54 eV 的结合能处出现。O 1s 原子的峰由532.99 eV 的弱Ca-O峰和531.42 eV 的优势C-O 峰组成。经苛化淀粉处理后,Ca 原子的2p1/2 和2p3/2 峰分别偏移至346.89 eV和350.43 eV,偏移量分别为0.1 eV 和0.09 eV。Ca-O峰由532.99 eV 偏移至532.91 eV,偏移量为0.08 eV;C-O 峰由531.44 eV 偏移至531.36 eV,偏移量为0.06 eV。而当方解石表面与Al-淀粉作用时,Ca 2p1/2 和Ca 2p3/2分别偏移至346.93 eV 和350.50 eV,偏移量分别为0.06 eV 和0.04 eV。同时,Ca-O 峰和C-O 峰分别偏移至532.86 eV 和531.29 eV,偏移量分别为0.14 eV 和0.13 eV。这一结果证实了这两种抑制剂均能改变特征原子峰,苛化淀粉主要通过羟基作用于方解石表面的Ca 位点,而Al-淀粉主要通过金属基团作用于方解石表面的O 位点。
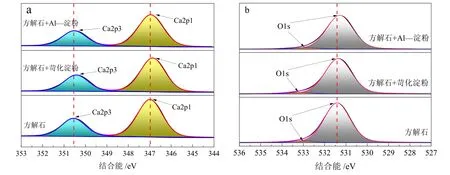
图12 方解石表面的Ca2p (a) 和O1s (b)能谱Fig. 12 XPS energy spectrum of Ca2p (a) and O1s (b) on calcite surface
不同抑制剂处理前后白钨矿特征原子的分峰结果如图13 所示。白钨矿的Ca 2p 和O 1s 峰在抑制剂处理后发生的变化明显不同。苛化淀粉处理时白钨矿的Ca 2p1/2 和Ca 2p3/2 峰的偏移量分别为0.08 eV和0.09 eV,Ca-O 峰的偏移量为0.48 eV,说明苛化淀粉主要作用于白钨矿的Ca 位点。不同于苛化淀粉,Al-淀粉很难在白钨矿表面位点发生吸附,因而Ca 2p、O 1s 峰则基本不发生偏移。这一结果进一步证明了Al-淀粉的选择性明显强于苛化淀粉。
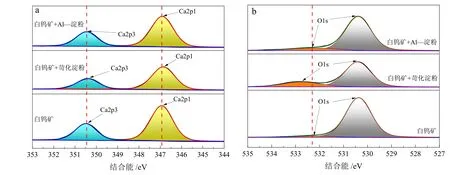
图13 白钨矿表面的Ca2p(a)和O1s(b)能谱Fig. 13 XPS energy spectrum of Ca2p (a) and O1s (b) on scheelite s urface
4 结论
(1)通过分步取代反应合成了Al-淀粉抑制剂,并通过团簇模型计算,发现铝离子与淀粉分子反式结构的伯醇基支链O6及相邻的O1发生螯合配位反应,生成键长最短的O1-Al-O6结构。同时通过红外光谱测试,确定了-O-Al 官能团的生成。
(2)单矿物浮选实验、实际矿石浮选实验均发现,Al-淀粉配合物的选择性优于苛化淀粉,该抑制剂可以选择性抑制微细粒方解石的浮选而不影响白钨矿,因而可以将精矿WO3品位由31.44%提升至40.51%,实现白钨矿与方解石的浮选分离。
(3)机理分析表明,苛化淀粉通过羟基官能团作用于白钨矿和方解石表面的Ca 活性位点,改变两矿物的表面电位、特征原子含量及特征峰。而Al-淀粉通过特有的金属基作用于方解石表面的O 活性位点,使其表面O 原子浓度明显增大、表面电位和特征峰产生负偏移,进而抑制方解石的浮选。但是,Al-淀粉不会作用于白钨矿表面的O 活性位点,因而不会对白钨矿的浮选产生抑制作用。
