超声造影联合混合现实技术在腹腔镜解剖性肝切除术中的应用效果
2023-12-15娄丽平张灵巧刘海潮
娄丽平,张灵巧,刘海潮
1郑州大学附属洛阳中心医院超声科,河南洛阳 471000;2郑州大学附属洛阳中心医院肝胆外科,河南洛阳 471000
原发性肝癌(primary liver cancer)是消化系统常见的恶性肿瘤[1],研究显示,肝癌在我国发病率居恶性肿瘤第4 位,病死率居恶性肿瘤第3 位[2-3]。手术切除仍是目前肝癌的主要治疗手段[4-5]。肝切除术经历了楔形肝切除、不规则局部切除、规则性肝叶切除、解剖性肝段切除等阶段,发展至今,腹腔镜技术在肝癌切除中的成熟应用明显减轻了患者创伤,加速了患者术后的康复进程[6-7]。但肝脏解剖结构复杂,加之腹腔镜技术缺乏“触感”及肿瘤的特异形态学特征,导致腹腔镜下肝切除术中肝内管道无法完全清晰显露,术中易出血;再者,虽然常规解剖性肝切除术在切除病灶的同时可最大限度保留正常肝脏组织的结构及功能,但因缺乏实时引导,切缘无法完全保证[8-9]。在现代精准外科时代,以最小创伤获取最佳治疗效果仍然是广大外科医师的追求目标,因此,如何充分利用现有技术为腹腔镜下解剖性肝切除术提供术中“精准导航”,从而确保手术顺利实施,提高治疗效果,是目前关注的热点问题。随着现代医学的不断发展,超声技术已由原来的常规超声逐步演变出超声造影(contrast-enhanced ultrasound,CEUS)、三维超声、断层超声等,且已应用于多种疾病的临床治疗中[10-12]。此外,目前人工智能时代已来临[13],其中混合现实(mixed reality,MR)技术已被初步应用于肿瘤的外科治疗,并取得了良好效果[14-15],其在术前评估、手术方案制定、术中导航等方面具有独特优势,已成为精准外科手术的新一代辅助工具。本研究探讨超声造影(CEUS)联合MR 技术在腹腔镜解剖性肝切除术中的应用效果,旨在进一步提高腹腔镜肝切除术的治疗效果及安全性。
1 资料与方法
1.1研究对象 回顾性分析2019 年1 月-2022 年6月在郑州大学附属洛阳中心医院行腹腔镜下解剖性肝切除术的45例原发性肝癌患者。所有患者术前行腹部薄层增强CT扫描检查,并采集数据构建肝脏三维可视化模型。根据术中影像学辅助方法不同将患者分为观察组(n=25,术中采用CEUS 联合MR 技术为手术提供精准导航)与对照组(n=20,行常规解剖性肝切除术,术中不实施CEUS 及MR 技术)。纳入标准:(1)原发性肝癌,未合并其他脏器转移;(2)单个肝段病灶数≤2 个;(3)肝功能Child 分级A-B 级;(4)可耐受全麻手术;(5)可接受规律随访。排除标准:(1)中国肝癌分期(China liver cancer staging,CNLC) Ⅱb-Ⅳ期;(2)术前接受经肝动脉化疗栓塞(transcatheter arterial chemoembolization,TACE)、肝动脉置管持续化疗灌注(hepatic artery infusion chemotherapy,HAIC)、联合肝脏离断和门静脉结扎二步肝切除术(associating liver partition and portal vein ligation for staged hepatectomy,ALPPS)等转化治疗的潜在可切除肝癌;(3)病例资料缺失。本研究获郑州大学附属洛阳中心医院伦理委员会审批(审批号:2018-12-A09),患者均签署知情同意书。
1.2 治疗方法
1.2.1 手术器械 超声工作站MyLab™X5、腹腔镜专用超声探头(频率10.0~12.0 MHz) (意大利Esaote百胜集团公司);SonoVue超声造影剂(上海博莱科信谊药业有限责任公司);4K 高清腹腔镜系统[Olympus(中国)有限公司];旭东3D 数字医学影像系统(深圳市旭东数字医学影像技术有限公司);微软HoloLens 2、MR 混合现实辅助系统(深圳一图智能科技有限公司);Ligasure(上海美敦力/科惠医疗管理有限公司);超声刀(上海逸思医疗科技股份有限公司)。
1.2.2 术前准备 术前24 h 采集患者晨起空腹状态下静脉血,检测术前肝肾功能[谷丙转氨酶(ALT)、谷草转氨酶(AST)、肌酐]。术前禁食水8 h,气管插管、全麻准备,针对不同肝段肿瘤选取相应手术体位。术前询问患者有无造影剂过敏史,完善腹部薄层增强CT扫描明确病变部位,将影像数据拷贝至旭东3D数字医学影像系统,由同一位工程师制作三维可视化图像,协助测量肝脏体积,并制定手术方案,同时将数据图像导入微软HoloLens 2,以便术中实施MR技术,协助制定手术方案(图1A、B)。
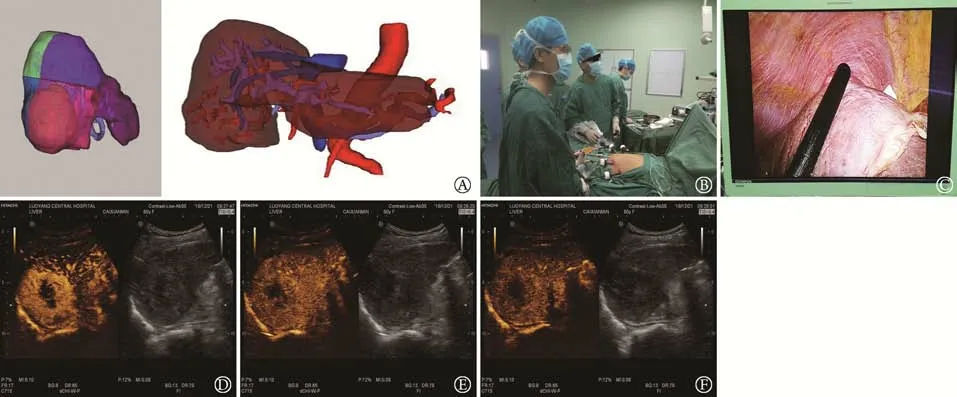
图1 原发性肝癌患者术前影像学评估及腹腔镜下解剖性肝切除术术中情况Fig.1 Preoperative imaging evaluation and intraoperative situation of laparoscopic anatomical hepatectomy in patients with primary liver cancer
1.2.3 术中CEUS 将5 ml 生理盐水注入SonoVue 超声造影剂中,震荡均匀形成混悬液。术中CEUS:置入探头,先以常规彩超观察病灶部位、大小、数目、回声特点、与肝内周围管道比邻等情况,然后更换专用探头,由手术医师紧贴肝脏表面,巡回护士抽取2.4 ml 造影剂混悬液,采用快速团注法注入肘静脉,再注入5 ml生理盐水冲管,专用探头实时观察、记录病灶灌注情况,进一步明确肿瘤大小、形态、位置,观察动脉相、门脉相、延迟相病灶回声变化情况,同时,小幅度侧动探头行相邻切面扇形扫查以观察病灶周围情况,了解病灶与该段肝静脉及肝蒂的关系。由超声科医师与外科医师协同阅读所示图像(图1C-F)。
1.2.4 手术过程 以肝右后叶切除术为例:探查腹腔内未见明确转移灶,其余脏器未见明显异常。离断肝圆韧带,游离镰状韧带至第二肝门处,游离右侧三角韧带及肝肾韧带,解剖肝后下腔静脉,仔细分离、结扎肝短静脉,充分游离右肝。第一肝门预留阻断带(必要时使用)。术者佩戴HoloLens 2 设备,将视野中显示的肝脏与腔镜系统中的肝脏按1∶1 比例进行融合,定位肿瘤位置。置入专用超声探头,探查肿瘤位置与MR 技术及术前增强CT 所示一致。断肝平面规划:选取肝表面解剖标志,结合术中CEUS 引导,标记病灶所在肝段标志性肝静脉为边界,同时确认病灶所在肝段肝蒂在肝表面投影及走行,通过术中超声对目标病灶肝蒂实施肝血流阻断,确认肝表面缺血线,在距缺血线边缘3 cm 处标记预切除线,确定离断范围,术者在CEUS及MR技术的实时引导下,结合术前三维重建,遵循Glissonean肝蒂途径(Glissonean pedicle approach),采取鞘外解剖方法,精准切除肿瘤。注意切除过程中肝断面具有重要意义的静脉血管应予以清晰显露。标本置入标本袋后完整取出。对照组除术中无CEUS及MR技术引导外,余精准肝切除步骤同上。
1.2.5 术后处理及随访 术后半卧位,禁食1 d、预防性抗感染、补液、对症治疗;观察术后并发症情况。术后随访至2023 年1 月,随访方式主要包括电话、门诊、微信随访等。随访内容主要包括了解患者出院后病情变化、康复情况、肿瘤有无复发及复发时间、目前有无新发症状等,同时提醒患者复诊时间、注意事项等。
1.3 观察指标 比较两组患者年龄、性别、病灶大小、病变部位、手术时间、术中出血量、术中输血量、选择性入肝血流阻断时间、术中及术后并发症、R0 切除率、病理结果、术后住院时间、肝肾功能、生存时间等。
1.4 统计学处理 采用SPSS 23.0 软件进行统计分析。符合正态分布的计量资料以±s表示,组间比较采用单因素方差分析,进一步两两比较采用LSD-t检验。不符合正态分布的计量资料以M(Q1,Q3)表示,组间比较采用Wilcoxon秩和检验。计数资料以例(%)表示,组间比较采用配对或成组χ2检验或Fisher确切概率法。P<0.05为差异有统计学意义。
2 结 果
2.1 一般情况 两组患者年龄、性别、病变部位、病理结果等一般资料比较,差异均无统计学意义(P<0.05,表1)。

表1 两组原发性肝癌患者一般资料比较Tab.1 Comparison of general information between two groups of patients with primary liver cancer
2.2 安全性评价 观察组术中选择性入肝血流阻断时间、手术时间明显短于对照组,术中出血量及输血量明显少于对照组,差异均有统计学意义(P<0.001);观察组术后24 h ALT 及AST 水平明显低于对照组,差异均有统计学意义(P<0.001);但两组术后24 h 肌酐水平差异无统计学意义(P>0.05)。此外,观察组发生术后肺部感染1例(1/25,4.0%),经非手术治疗后恢复;对照组发生术中大出血导致中转开腹3例(1/20,15.0%),术后肺部感染2例(2/20,10.0%),胃排空功能障碍2例(2/20,10.0%),均经非手术治疗后恢复,余13例术后恢复顺利,无并发症发生;两组患者术后均未发生腹腔内出血、胆瘘等其他并发症。观察组并发症发生率低于对照组,差异有统计学意义(P<0.001) (表2)。

表2 CEUS联合MR技术在腹腔镜肝切除术中的安全性Tab.2 The safety of CEUS combined with MR technology in laparoscopic hepatectomy
2.3 应用效果及随访结果 观察组25例均顺利完成腹腔镜手术,但对照组3 例术中中转开腹手术。观察组R0 切除率高于对照组,但差异无统计学意义(100.0%vs.90.0%,P>0.05),其中对照组2 例术后镜下病理学发现切缘阳性。观察组与对照组术后住院时间分别为(8.4±2.2) d、(8.9±1.9) d,差异无统计学意义(t=1.448,P=0.148);此外,观察组中位生存期长于对照组,但差异无统计学意义[18.5(9.2,24.5) 月vs.18.0(8.7,23.0)月,χ2=1.374,P=0.442]。
3 讨 论
腹腔镜下肝切除术目前已成为外科治疗肝肿瘤的主流方法[16],但术中如何更精准地定位肿瘤、界定浸润范围、保证切缘阴性的同时最大限度地保留剩余肝脏功能仍是目前困扰肝胆外科医师的主要问题,此外,肝内门静脉、肝动脉、胆管等管道众多,如何借助现代医学显像技术更加清晰地显露各类肝内管道结构、减少术中出血、提高手术安全性亦是值得探讨的问题。目前已有诸多研究将术中CEUS应用于腹腔镜肝切除术,且取得了良好效果[17]。例如,杨建荣等[18]发现,CEUS有助于肝癌患者手术方式的选择; 杜波等[19]将CEUS 与吲哚箐绿(indocyanine green,ICG)荧光染色应用于伴肝硬化肝癌患者的腹腔镜解剖性切除术中,发现相较常规腹腔镜下肝解剖性切除术,该方法有利于降低手术操作难度,且对术后肝功能的影响更小;刘金桥等[20]将术中超声与三维重建技术联合应用于儿童解剖性肝切除术中,发现该方法可有效减少术中出血量,使手术更加安全、精准、有效。但目前关于将CEUS与MR 技术相结合应用于腹腔镜下解剖性肝切除术中的研究仍较少。基于上述原因,本研究分析在本院肝胆外科行腹腔镜下解剖性肝切除术的45例原发性肝癌患者的临床资料,分析其安全性及应用效果,以期为后续临床研究提供一定参考价值。
本研究发现,观察组术中选择性入肝血流阻断时间、手术时间明显短于对照组,术中出血量及输血量明显少于对照组,提示相较于常规腹腔镜下解剖性肝切除术,术中CEUS联合MR技术有利于缩短手术时间,减少术中出血量,有助于确保手术的安全性。分析原因如下。一方面,术前三维重建不仅有助于系统分析病灶及与周围解剖结构的关系,清晰显现肝静脉、门静脉、肝动脉走行,以及有无血管变异等,为手术方案规划提供指导价值,为术中实施精准肝切除提供技术支持,而且术前还可对标准肝体积、剩余肝体积等进行精准测量,降低术后残肝体积代偿不足风险。此外,三维立体图像也能够让患者及家属更加直观地了解病情。另一方面,术中CEUS联合MR技术可充当外科医师的“第三只眼”,可快速、精准定位肿瘤,特别是对于直径<1 cm 的病灶,外科医师肉眼往往无法辨别,此时CEUS 显得尤为重要,且CEUS 联合MR 技术还可明确肿瘤浸润情况,指导术者实时调整断肝平面,在完整切除肿瘤的同时,尽可能避免切除过多剩余正常肝组织;可清晰显露肝内脉管结构,并以肝蒂为引导,降低手术难度的同时,避免不必要的血管损伤,减少了术中出血量,进而减少了选择性肝门阻断次数,缩短了整体手术时间。此外,两组术后24 h 肌酐水平并无明显差异,表明超声增强造影剂并未对患者肾功能代谢造成明显影响,与张天生等[21]的研究结果一致,进一步证实了CEUS 的安全性。观察组术后ALT 及AST 水平明显低于对照组,这与观察组患者借助于术中超声及MR 技术的实时引导,对血管的走行判定更加准确、清晰,减少了术中出血及选择性入肝血流阻断时间,进而减轻了肝脏缺血再灌注损伤有关[22],从另一方面体现出术中CEUS联合MR技术在腹腔镜解剖性肝切除术中的优势。再者,观察组中仅1 例术后发生肺部感染,经非手术治疗后顺利恢复,术后均无胆瘘、腹腔感染等其他并发症发生,而对照组术后发生肺部感染2例、胃排空功能障碍2例,观察组术后并发症发生率明显低于对照组,再次印证了CEUS联合MR技术在腹腔镜解剖性肝切除术中的安全性,特别是对于肝脏切除术后可能发生胆瘘的问题,CEUS 联合MR技术可清晰显示肝内胆管解剖结构,使得术者在离断胆管时能够做到“游刃有余”,减少胆瘘的发生。此外,对照组中有3 例因术中误损伤肝静脉引起大出血而被迫中转开腹,笔者认为这可能与常规腹腔镜解剖性肝切除术中缺乏CEUS的“实时导航”,加之缺乏MR 技术对病灶周围解剖结构的虚拟呈现,导致无法清晰显露肝内重要血管管道结构、无法准确把握切除平面而造成肝静脉的误损伤有关,也可能与术者操作技术有一定关系。
在应用效果及预后评价中,观察组R0 切除率(100.0%)高于对照组(90.0%),这可能是因为对照组缺乏术中CEUS引导,无法准确界定肿瘤浸润边界,导致标本肉眼可见切缘阴性但术后病理切缘阳性的情况发生。但两组R0切除率无统计学差异,可能与样本量较小有关。同时,两组住院时间无明显差异,表明术后虽部分患者存在手术相关并发症,但均未对术后康复造成明显影响。此外,观察组中位生存期长于对照组,进一步表明常规腹腔镜下解剖性肝切除术由于存在术后标本切缘阴性的不确定性,可能导致术后肿瘤复发,进而影响患者预后,而CEUS联合MR 技术有助于确保手术切缘阴性,提高治疗效果,一定程度延长了患者的生存期。
综上所述,本研究结果初步表明,CEUS 联合MR技术应用于腹腔镜下解剖性肝切除术中安全、有效,超声科医师与肝胆外科手术医师的紧密配合,可充分发挥CEUS及MR技术的优势,有助于确保手术安全,提高治疗效果,但本研究样本量较小,部分差异仍有待大样本、多中心随访研究验证。
