磁性g-C3N4 /CoFe2O4 光催化剂的制备及其性能研究
2023-12-14李云锋
罗 杰,常 薇,张 立,雷 超,李云锋,刘 斌
世界经济的高速发展和工业化应用范围的拓宽带来了一系列的环境问题,例如工业废水、农业废水和生活废水等都是目前急需解决的问题[1,2]。而工业废水中的印染废水因其难降解物质多、成分复杂、色度大和有毒等特点[3,4]难以进行降解处理。其中应用较多的碱性阳离子染料罗丹明B(RhB),其具有毒性、致癌性、难生物降解性,存在于水体中会对人体健康和水生环境都会造成严重影响[5]。因此,找到一种安全、高效、绿色、低成本,可重复利用的有机染料去除方法十分重要。
光催化降解技术作为一种新兴的高级氧化技术,能够将有机污染物完全矿化为CO2和H2O,因其独特的清洁工艺和解决水体污染的潜在价值,被认为是降解污染物最经济有效的方式[6]。 类石墨相氮化碳(g-C3N4)是一种新型非金属光催化材料,与传统的TiO2光催化剂相比,拥有更宽的吸收光谱范围。 其禁带宽度为2.7 eV,具有可见光响应,稳定性好、无毒、制备简单方便等优点[7-9]。 但由于其对可见光的吸收不强(<470 nm),光生电子-空穴的快速复合减弱了其光催化性能[10],这些限制了g-C3N4材料的实际应用。 经过大量研究表明,通过对g-C3N4进行掺杂改性能够增强其可见光的吸收强度,有效提升光催化活性[11-15]。
钴铁氧体(CoFe2O4)在半导体光催化领域得到了广泛的关注。 CoFe2O4是一种铁基半导体氧化物,具有高化学稳定性、低毒性、高矫顽力、中等磁化强度等特性[16,17],相比其它半导体光催化剂具有更可调的磁性和更高的吸收能力等优点[18,19]。 通过将CoFe2O4与g-C3N4复合,可以拓宽催化剂的可见光响应范围,提高电荷分离效率[20,21],然而其光催化降解有机污染物过程仍需要外界提供电子受体以此来产生更多参与降解反应的活性基团。 因而制备具有优异光催化活性的磁性光催化材料仍需更多的探索[22]。
本研究采用超声低温煅烧的方法制备具有特定结构的磁性g-C3N4/CoFe2O4复合纳米光催化材料,探究其对RhB 的光催化降解性能并对其使用稳定性和光催化降解机理进行了探讨。
1 材料与方法
1.1 试剂与仪器
试剂:尿素(CH4N2O),罗丹明B(RhB,C28H31ClN2O3),十六烷基三甲基溴化铵[CTAB(C19H42BrN)],硝酸铁[Fe(NO3)3·9H2O],硝酸钴[Co(NO3)2·6H2O],氢氧化钠(NaOH),无水乙醇 (C2H6O),以上试剂均为分析纯,国药集团化学试剂有限公司生产。
主要仪器:XPA-7 型光化学反应仪(南京胥江机电厂)、紫外-可见分光光度计 (UV-2450,日本岛津有限公司)、X 射线衍射仪 (XRD,Dmax-Rapid II,日本理学)、红外光谱仪(FT-IR,Lambda 950,珀金埃尔默仪器有限公司)和场发射扫描电子显微镜(JEOL JSM 6700F,FEI 公司)。
1.2 材料制备
1.2.1 g-C3N4 的制备
称取5 g 尿素置于30 mL 坩埚中放入马弗炉,以5 ℃·min-1加热至550 ℃,保温4 h,自然冷却后研磨得到淡黄色轻质粉末固体g-C3N4。
1.2.2 磁性CoFe2O4 的制备
配制70 mL Co 与Fe 物质的量之比为1 ∶2 的盐溶液置于三口烧瓶中,待其完全溶解后置于恒温水浴锅中,加入1.093 g CTAB 搅拌24 h 形成透明黏稠液体,然后将氢氧化钠溶液缓慢逐滴加入该溶液中,控制溶液pH 值约为12,升温至90 ℃反应1.5 h得到黑褐色沉淀,用乙醇和水洗涤多次后烘干研磨得到黑褐色粉末,之后在马弗炉中以5 ℃·min-1加热至500 ℃煅烧3 h,即得到CoFe2O4软磁材料。
1.2.3 g-C3N4/CoFe2O4 复合光催化剂制备
分别称取0.1、0.3 和0.5 g 制备好的g-C3N4和0.1 g 的CoFe2O4置于15 mL 乙醇中超声2 h,烘干后以5 ℃·min-1加热至350 ℃煅烧2 h,所得样品分别记为CNCF-1、CNCF-3、CNCF-5。
1.3 光催化降解实验
将所制备的样品称取30 mg 分别加入到30 mL(10 mg·L-1)RhB 溶液中,暗室搅拌吸附30 min,达到吸附-脱附平衡,用XPA-7 型光化学反应仪在500 W 氙灯下进行光催化反应,每间隔20 min 取样1 次,在550 nm 处测其吸光度,RhB 溶液浓度变化以C/C0表示,C0为初始溶液浓度,C表示光催化降解后溶液的浓度。
2 结果与讨论
2.1 XRD 分析
图1 所示为制备样品的XRD 图谱。

图1 制备样品的XRD 谱图Fig.1 XRD patterns of the prepared samples
由图1 可以看出g-C3N4在2θ=27.3°(002)处有1 个主衍射峰,对应于晶面间石墨的堆积(JCPDS 87-1526); CoFe2O4样品在 2θ= 30.08°、35.44°、43.06°、56.97°、62.58°和74.01°处出现的衍射峰来自于其220、311、400、511、440 和533 晶面的衍射(JCPDS 22-1086)[23]。 g-C3N4/CoFe2O4复合材料中均可观察到g-C3N4和CoFe2O4的衍射峰,且随着g-C3N4含量的增大,g-C3N4对应的峰强度逐渐增大而CoFe2O4所对应的峰强度逐渐减小,复合材料中没有检测到其它特征峰,说明没有其它杂质的掺入。
2.2 SEM 分析
图2 所示为制备样品的SEM 照片,照片显示CoFe2O4呈现表面光滑的细小颗粒状纳米结构,因具有磁性而呈现团聚状态[图2(a)]。 g-C3N4呈现为大小不一的多孔层状[图2(b)]。 图2(c)、图2(d) 和图2 (e) 分别为不同复合比例 g-C3N4/CoFe2O4材料的 SEM 图, 可知复合物中随着CoFe2O4含量的减少,显然层状多孔结构表面的细小颗粒状物质也逐渐减少,说明复合物之间形成了一种特定结构,并且团聚现象也得以改善。

图2 制备样品的SEM 图Fig.2 SEM image of the prepared samples
2.3 FT-IR 分析
图3 所示为制备样品的傅里叶红外光谱图。 从图中可观察到800 cm-1区域的弱吸收峰属于碳氮杂环的弯曲振动,810 cm-1是三嗪结构的弯曲振动特征峰,1 200 ~1 600 cm-1区域的几个吸收峰对应C—N 杂环的伸缩振动的吸收C—N(—C—)或者C—NH—C[24],以上属于g-C3N4特征吸收峰;在581 cm-1附近的吸收主要由CoFe2O4中的Fe—O 振动伸缩偏移所引起[25],说明复合材料被成功制备。
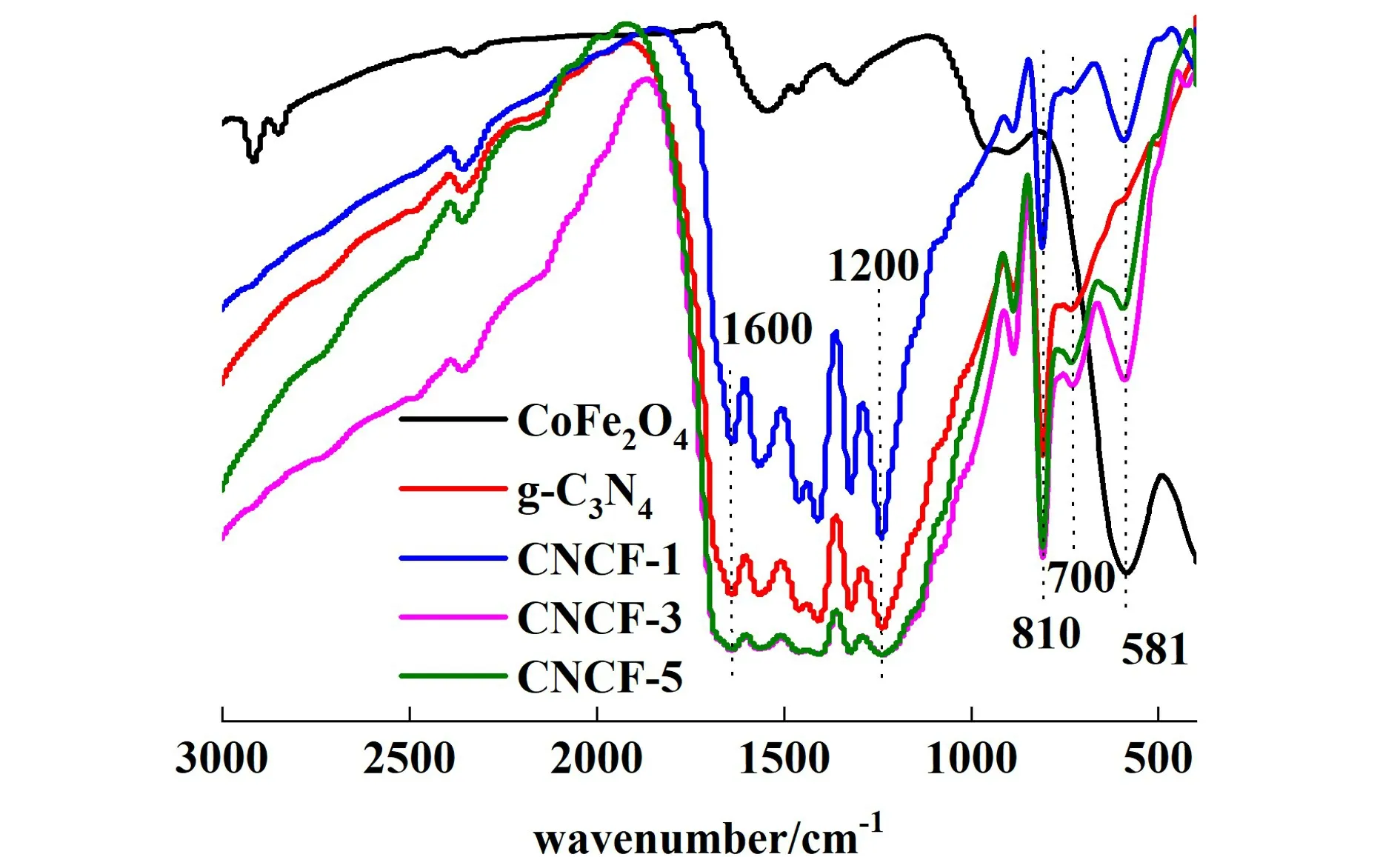
图3 制备样品的FT-IR 图Fig.3 FT-IR diagram of the prepared sample
2.4 UV-vis 漫反射光谱分析
g-C3N4/CoFe2O4光催化剂的UV-vis DRS 吸收光谱如图4 所示。

图4 (a) 制备样品的 UV-vis DRS 谱图;(b)带隙图Fig.4 (a) UV-vis DRS spectra of prepared samples;(b) band-gap energy
图4(a)显示了所有光催化剂的紫外可见漫反射光谱,结果表明:与纯g-C3N4相比,复合材料在可见光区域吸收均显著增强,可能由于复合光催化剂带隙之间发生跃迁,形成异质结构,这有助于提升复合材料的可见光响应能力从而提升其光催化性能。 分别以(Ahv)2和(Ahv)1/2为纵坐标,以能带宽度为横坐标作图[图4(b)],通过做切线与横坐标相交,交点即为禁带宽度Eg,可以得到样品CoFe2O4和g-C3N4禁带宽度分别为1.50 和2.63 eV,复合光催化剂禁带宽度在1.50 ~2.63 eV 之间。
2.5 光催化性能评价
制备样品光催化降解RhB 效果如图5 所示。
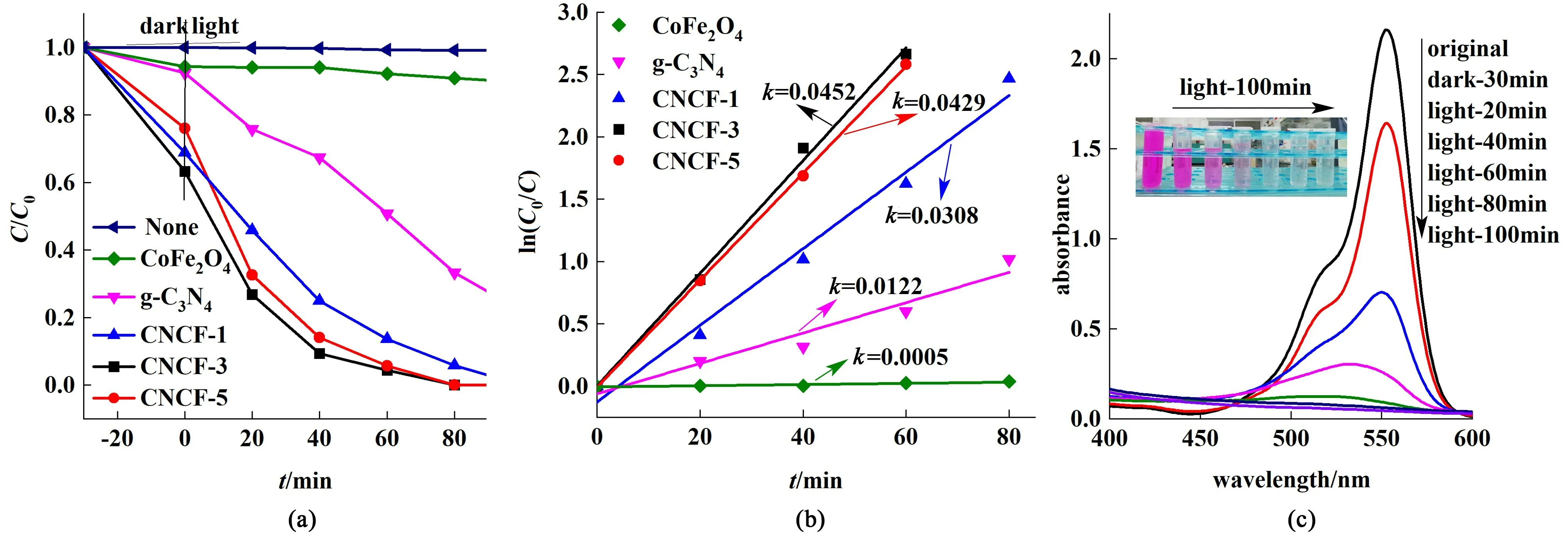
图5 (a) 光催化剂对RhB 的降解性能图;(b) 一级动力学曲线图;(c) CNCF-3 不同时间点降解RhB 的吸收光谱图Fig.5 (a) Photocatalyst degradation performance diagram of RhB;(b) first order kinetic curve;(c) CNCF-3 absorption spectra of degradation of RhB at different time points
图5(a)为制备样品的光催化降解图,可以看出在光照120 min 后,不加光催化剂的空白样溶液,RhB 的降解率几乎没有变化;加入制备样品后,复合光催化剂对RhB 的降解效果均优于单一g-C3N4和CoFe2O4光催化剂,100 min 降解率均能达到99%以上,其中CNCF-3 的光催化降解性能最好。 通过ln(C0/C)=kt线性拟合得到RhB 降解过程的一级动力学曲线,其中CNCF-3 为光催化剂时降解速率常数最大为0.045 2 min-1[图5(b)]。 图5(c)为CNCF-3 做光催化剂时不同光照时间RhB 溶液的吸收曲线图,图5(c)中照片为不同时间相对应的RhB溶液。 可以看出,经过100 min 光照后,RhB 溶液在可见光区的吸收几乎为0,相对应的溶液颜色消失,说明其中的RhB 基本降解完全。
2.6 催化剂稳定性评价
为了解所制备材料的实际应用可能性,进行了材料的重复使用性及磁分离效果实验,结果如图6所示。

图6 (a) 光催化剂5 次循环实验结果图;(b) 磁分离效果图Fig.6 (a) Experimental results of 5 cycles of photocatalyst;(b) effect drawing of magnetic separation
从图6(a)可以看出,经过5 次重复循环使用,RhB 的降解效率仍可达到92%以上。 并且通过外部磁场可将CNCF-3 与水溶液有效分离[图6(b)]。说明该复合材料不仅能有效降解RhB 染料且具有高回收率、易分离、无二次污染的特点,在光催化降解印染废水方面具有很大的应用潜力。
2.7 光催化剂机理
光生空穴、·OH 和·O-2是光催化降解有机物过程中的主要活性物质[26],为了探究复合催化剂的催化降解机理,使用乙醇、草酸铵(AO)和对苯醌(BQ)分别捕获·OH、光生空穴和·O-2,由图7 可知,3 种捕获剂均能明显降低 CNCF-3 对RhB 的光催化降解效率,加入乙醇和BQ 对光催化降解抑制作用较为明显,因此可以判断CNCF-3 光催化降解RhB 过程中主要的活性物质是·OH 和·O-2。
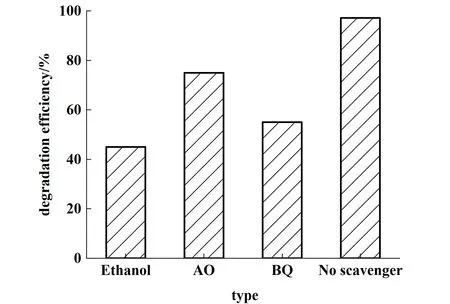
图7 不同捕获剂对CNCF-3 光催化降解RhB 的影响Fig.7 Effects of different capture agents on the photocatalytic degradation of RhB by CNCF-3
根据禁带宽度,可通过ECB=X-Ee-0.5Eg和EVB=ECB+Eg推算出价带和导带位置,其中ECB和EVB分别表示材料的导带和价带电势(eV),Ee是常数值为4.50 eV,Eg为半导体禁带宽度,X是半导体电负性值[27,28]。 推算得到g-C3N4与CoFe2O4的价带和导带电势分别为1.54、1.84 eV 和- 1.08、0.34 eV。 根据以上实验,其光催化机理分析如图8所示,当光照射在复合光催化剂表面,光子会被g-C3N4和CoFe2O4吸收,从而产生光生电子-空穴对。CoFe2O4导带中的光生电子转移到g-C3N4的价带中并与空穴重新进行结合配对,提升了光生载流子的空间分离效率。 g-C3N4导带中的光生电子将会积累更多,体系里的O2、H+、e-发生反应生成H2O2,而g-C3N4的导带电位(- 1.08 eV) 低于(0.69 eV)和(-0.33 eV),所以g-C3N4导带中的光生电子可以将H2O2激活生成高活性的·OH并和O2结合生成·O-2,从而降解有机污染物。
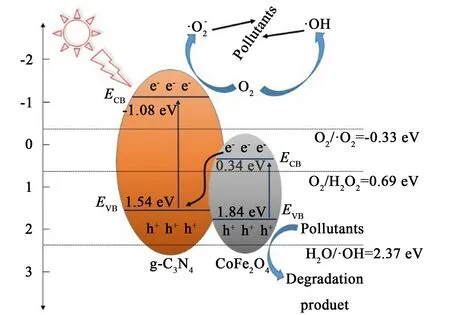
图8 g-C3N4/CoFe2O4 光催化机理分析图Fig.8 Photocatalytic mechanism analysis diagram of g-C3N4/CoFe2O4
3 结论
通过超声低温煅烧的方法成功制备了磁性g-C3N4/CoFe2O4复合光催化材料,其中当g-C3N4和CoFe2O4复合比例为3 ∶1 时,所得材料具有较适宜的光催化活性。 另外,g-C3N4/CoFe2O4具有良好的重复使用性且在外部磁场条件下极易分离回收,其优异的光催化活性主要是由于材料内部异质结结构的形成,有效降低了光生电子-空穴复合率,经过活性物质捕获实验表明,在降解RhB 过程中的主要活性物质为·OH 和·O-2。 该材料光催化活性高且环境友好易回收,在光催化净化废水方面具有一定的应用潜力。
