A 型塞内卡病毒胶体金免疫层析抗原检测试纸的研制
2023-12-11安满鑫魏子宇陈玉潇吴文璇袁万哲李丽敏
安满鑫,魏子宇,陈玉潇,吕 兰,吴文璇,袁万哲,2,马 明,李丽敏,2
(1.河北农业大学 动物医学院,河北 保定 071000;2.河北省兽医生物技术创新中心,河北 保定 071000;3.瑞普生物药业有限公司,河北 保定 071000)
A 型塞内卡病毒(Senecavirus A,SVA)是一种于2002 年在细胞培养物中首次发现的无包膜小核糖核酸病毒[1]。2008 年和2012 年分别在加拿大和美国报道了SVA 引起猪水疱病的病例,之后人们逐渐开始关注塞内卡病毒病[2]。近年来,巴西、美国、越南、哥伦比亚、中国等陆续出现猪SVA 水疱病,我国于2015 年3 月份在广东省报道了首例SVA 水疱病疫情[3]。随后,SVA 疫情陆续在我国湖北,黑龙江,福建,河南,甘肃,广西等省份出现[4],这表明SVA 在我国猪场内普遍存在。自然感染SVA的猪会出现与口蹄疫、水泡性口炎等水疱性病毒病相似的症状[5],但感染母猪在10~15 d 后可很快恢复,死亡率约为0.2%[6]。该病毒对仔猪危害较大,新生仔猪感染后死亡率最高可达70%[7],仔猪感染SVA 后临床症状主要表现为嗜睡、腹泻、皮肤充血、神经症状和猝死[8],因此需要快速且准确的检测方法对该病进行检测以减少养猪业的损失。
免疫层析技术由于其快速、简单、经济和非技术人员可使用的优点被广泛接受,使其成为迄今为止最成功的现场检测方法之一[9]。近年来,虽有关于以VP1 蛋白为标靶检测SVA 的免疫层析试纸的报道[10],但有研究表明SVA VP2 蛋白具有比VP1和VP3 蛋白更高的抗体亲和力和更高的免疫原性,且VP2 蛋白比VP1 和VP3 蛋白更保守[11]。因此,本研究认为VP2 蛋白比VP1 和VP3 蛋白更适合作为检测的靶蛋白。综上所述,本研究基于本实验室保存的重组pET32a(+)-SVA VP2 蛋白制备的SVA VP2 蛋白单克隆抗体为基础,研制了胶体金免疫层析试纸,以期提供一种在临床上更加快速准确的检测SVA 的方法。
1 材料与方法
1.1 材料
6 周龄的BALB/c 小鼠购买自河北伊维沃生物科技有限公司(No.20220713);SP2/0 细胞、BHK-21 细胞、重组pET32a(+)-SVA VP2 蛋白、猪瘟活疫苗、猪口蹄疫O 型、A 型二价灭活疫苗、猪繁殖与呼吸综合征活疫苗均由本实验室保存;SVA 感染性克隆毒株由河北农业大学食品卫生与检验实验室提供。
MONTANIDE ISA 201 VG 佐剂为SEPPIC 公司产品;HRP-羊抗鼠IgG 购于北京博奥龙生物科技有限公司;羊抗鼠IgG、TMB 显色液购于北京索莱宝科技有限公司;DAB 显色液、FITC-羊抗鼠IgG 购于中杉金桥生物技术有限公司;RMPI 1640 培养基购于Gibco 公司、DMEM 培养基购于韦森特生物技术有限公司、胎牛血清购于Dogesce 公司;HAT 选择培养基、HT 培养基、氯金酸为Sigma 公司产品;柠檬酸三钠、无水碳酸钾购于天津福晨化学试剂厂。
1.2 单克隆抗体的制备
用纯化的重组SVA VP2 蛋白[12]与MONTANIDE ISA 201 VG 佐剂按照4 ∶1 混合乳化,颈背部皮下多点免疫6 周龄BALB/c 小鼠(50 μg/只,200 μL),首次免疫后14 d 和28 d 进行第2 次免疫和第3 次免疫,第2 次和第3 次免疫剂量与途径同首次免疫相同。融合前3 d 腹腔免疫100 μg VP2 蛋白。将免疫脾细胞与SP2/0 细胞进行融合,利用HAT 进行培养,用间接ELISA 和间接免疫荧光筛选阳性细胞,进行多次亚克隆直至筛选出稳定分泌抗体的杂交瘤细胞株,采用小鼠体内诱生腹水法大量制备VP2 单抗,并进行相关特性鉴定。
1.3 抗原检测试纸条的制备
1.3.1 胶体金颗粒的制备与鉴定 参考文献[13]中的方法制备胶体金溶液,将制备好的溶液冷却至室温后于4 ℃冰箱保存备用。将胶体金颗粒经磷钨酸负染后通过透射电子显微镜观察粒径以及均一度。
1.3.2 最佳标记pH 及标记抗体量的确定 用K2CO3溶液将1 mL 胶体金溶液调节成不同pH,加入1D6 抗体静置15 min 后加入10%氯化钠溶液,混匀静置2 h,观察颜色变化。同时参考文献[14]中的方法,离心后检测OD520nm的值,吸光度最高的溶液的pH 作为最佳标记pH。用K2CO3溶液将胶体金溶液调节至最佳标记pH,向1 mL 胶体金溶液中加入不同量的1D6 抗体,静置15 min 后加入10%氯化钠溶液,混匀静置2 h,观察颜色变化,颜色最先与对照管保持一致的管的抗体量为稳定胶体金溶液的最低抗体量,在此基础上增加20%作为最佳抗体标记量。
1.3.3 金标抗体及金标垫的制备 将胶体金溶液调节至最佳pH,加入最佳标记量的1D6 抗体,搅拌60 min 后加入终浓度4%的BSA 继续搅拌40 min,将制备好的胶体金溶液10 000 r/min 离心40 min,弃上清,重悬沉淀,0.45 μm 滤膜过滤后4 ℃备用。金标垫经处理后浸泡于金标抗体悬液中吸附1 h,烘干后裁剪备用。
1.3.4 检测线和质控线抗体工作浓度的确定 将2C2 抗体稀释不同浓度印记于NC 膜作为检测线(T线),将羊抗鼠IgG 稀释为2 mg/mL 作为质控线(C线)印记于NC 膜,组装试纸条粗品,向样品垫滴加50 μL 500 μg/mL 的SVA VP2 蛋白进行检测,根据颜色变化确定检测线抗体最佳工作浓度,以同样的方法确定质控线抗体最佳工作浓度。
1.3.5 试纸条的组装及结果判定 将裁剪好的试纸条的各个部分按照如图1 所示进行组装,各个部分重叠2 mm。滴加样品后,若只有C 线出现颜色反应,则判为阴性;若T 线、C 线均出现颜色反应则判为阳性;若只有T 线出现颜色或T 线、C 线均无颜色则判为检测无效。
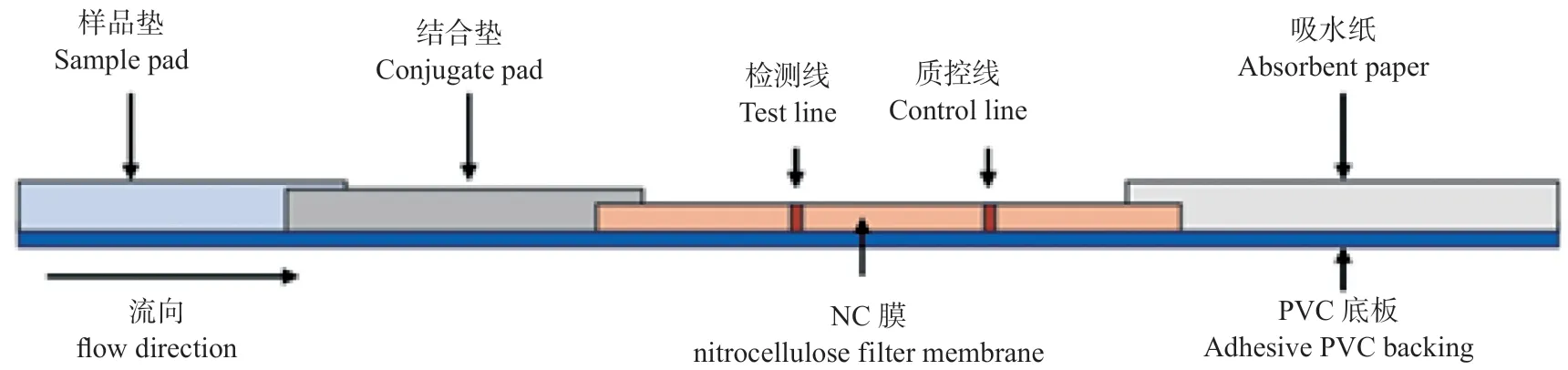
图1 试纸条组装示意图Fig. 1 Diagram of test strip assembling
1.4 试纸条性能检测
1.4.1 敏感性与特异性试验 将103.588TCID50/mL的SVA 病毒液做2 倍比稀释,使用制备的试纸条进行检测,确定试纸条的检测限。使用试纸条检测SVA 病毒液和猪瘟活疫苗、猪繁殖与呼吸综合征活疫苗、猪口蹄疫O 型、A 型二价灭活苗,判断试纸条是否与其他病毒发生交叉反应。
1.4.2 重复性实验 制备不同批次的试纸条,分别检测5 份不接毒的BHK-21 细胞培养上清(阴性)和5 份接毒后培养24 h 的BHK-21 细胞培养上清(阳性),每个样品重复3 次,计算变异系数。
1.4.3 临床样品检测 PCR 方法常被认为是病毒检测的金标准[15],因此用本研究研制的胶体金免疫层析试纸检测本实验室保存的27 份疑似感染SVA的经研磨处理的组织研磨液样品(淋巴结7 份、脾7 份、肺10 份、肾2 份、肝1 份),同时用RTPCR 方法进行检测,对比观察两者的检测结果。
2 结果与分析
2.1 单克隆抗体的鉴定
2.1.1 效价及饱和稀释度检测 使用间接ELISA 方法检测了1D6 和2C2 抗体的效价及饱和稀释度,经检测,1D6 和2C2 抗体的细胞培养上清效价分别为1 ∶2 560 和1 ∶5 120,腹水效价均为1 ∶1.56×106,两者饱和稀释度分别为1 ∶160 和1 ∶2 560。1D6和2C2 均具有较高的抗体效价,说明这2 株杂交瘤细胞株具有较强的抗体分泌能力。
2.1.2 抗体亚型鉴定 经小鼠单克隆抗体亚型鉴定试剂盒鉴定,2 株单抗轻链均为Kappa 型,重链均为IgG1 型。
2.1.3 免疫活性鉴定 Western blot 鉴定结果如图2A 所示,2 株单抗均能与SVA VP2 蛋白发生特异性结合;间接免疫荧光检测结果如图2B 所示,2 株单抗均能与SVA 病毒结合出现特异性荧光,阴性对照未出现荧光。以上结果表明,2 株单抗均具有良好的免疫活性。
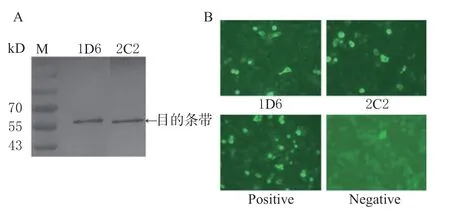
图2 单克隆抗体免疫活性鉴定Fig. 2 Identification of immunological activity of monoclonal antibodies
2.1.4 单抗识别表位分析 参考文献[16]的方法分析单抗识别的表位,结果如表1 所示,2 株单抗互相叠加的AI 值均大于10%,说明1D6 和2C2 这2 株单克隆抗体识别不同的表位。

表1 抗原识别位点分析Table 1 Analysis of antigen recognition site
2.1.5 单克隆抗体的纯化 使用饱和硫酸铵粗提IgG,SDS-PAGE 检测抗体的纯化效果,结果如图3所示,2 株单抗均在50 kD 附近和25 kD 附近出现了清晰、单一的重链和轻链,表明纯化效果较好。
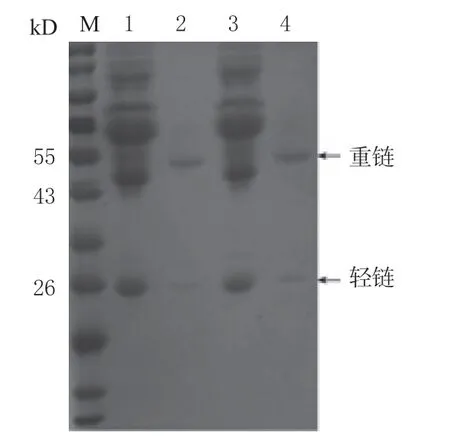
图3 单抗腹水纯化结果Fig. 3 Purification of monoclonal antibody ascites
2.1.6 亲和常数检测 参考文献[17]中的ELISA方法计算亲和常数,亲和常数≈150 000×A/抗体浓度,式中150 000 为IgG 抗体分子量,A 代表曲线达到平台期时的1/2OD 值所对应的抗体稀释倍数,抗体浓度以mg/mL 表示。经计算,单抗1D6 和2C2的亲和常数分别为5.4×109和4.2×109,均具有较高的亲和力。
2.2 试纸条的制备
2.2.1 胶体金颗粒的鉴定 胶体金溶液物理外观如图4A 所示,颜色酒红,通体透亮,无沉淀。胶体金颗粒在透射电镜下的观察结果如图4B 所示,金颗粒形态较均一,平均粒径约为20 nm,多为圆形或椭圆形,无不规则形状颗粒,说明制备的胶体金溶液质量较好。

图4 胶体金溶液质量鉴定Fig. 4 Quality identification of colloidal gold solution
2.2.2 抗体最佳标记pH 及最佳标记量的确定 当每毫升胶体金溶液添加2、4、6、8、10 μL K2CO3溶液时其颜色与对照管接近,因此将其离心后检测上清中OD520nm的值,结果如图5A 所示,当每毫升胶体金溶液添加8 μL K2CO3溶液时OD 值最高,说明抗体与金颗粒结合较好,因此以每毫升胶体金溶液添加8 μL K2CO3溶液时的pH 作为最佳标记pH,试纸检测pH 约为8.0;最佳抗体标记量的优化结果如图5B 所示,8 号管胶体金溶液颜色最先与对照管保持一致且不在发生明显变化,因此8 号管所对应的抗体量30 μg 被认为是稳定1 mL 胶体金溶液所需的最低抗体量,在此基础上增加20%作为最佳抗体标记量,即单克隆抗体1D6 的最佳标记量为36 μg/mL。

图5 抗体标记条件的优化Fig. 5 Optimization of antibody labeling conditions
2.2.3 检测抗体与质控抗体工作浓度的确定 如图6A 所示,当检测抗体2C2 浓度为2、1.5 和1 mg/mL时,检测线颜色清楚且彼此之间差别不大,将检测抗体2C2 浓度降为0.5 mg/mL 时检测线颜色明显变淡且不易观察,因此以1 mg/mL 的浓度作为单克隆抗体2C2 的最适工作浓度。同理如图6B 所示,当羊抗鼠IgG 浓度为以1.5 mg/mL 时,C 线颜色清晰易于观察,因此以1.5 mg/mL 的浓度作为羊抗鼠IgG 抗体的最适工作浓度。
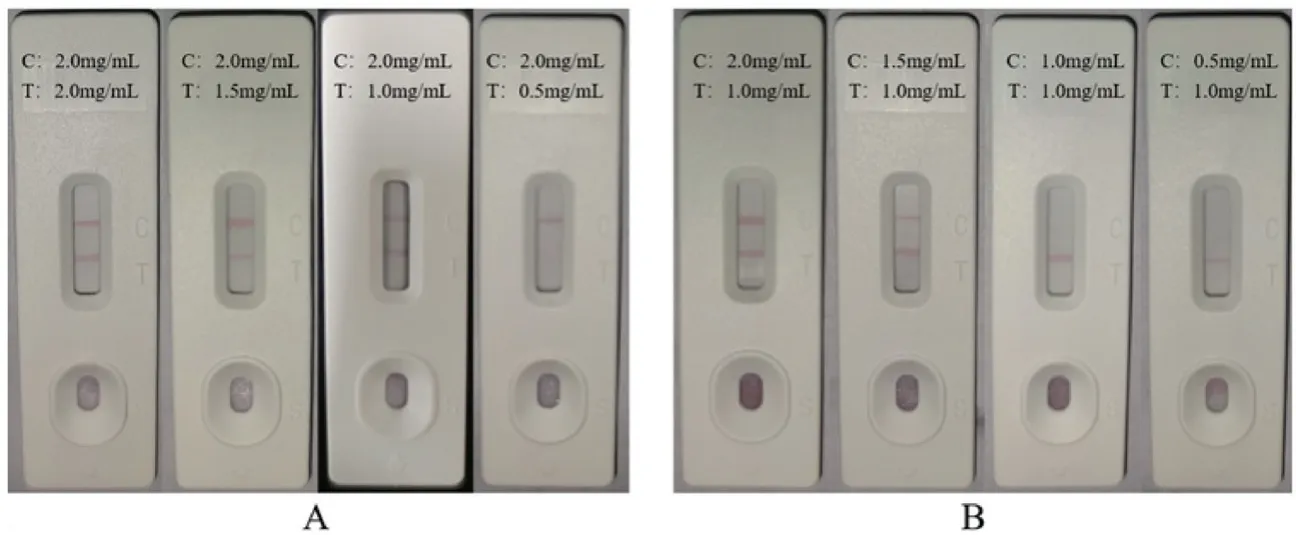
图6 检测线与质控线工作浓度的筛选Fig. 6 Selection of working concentration for detection and quality control lines
2.3 试纸条性能鉴定
2.3.1 敏感性与特异性试验 将SVA 病毒液稀释4个梯度用试纸条进行检测,结果如图7A 所示,当病毒滴度为4.8×102TCID50/mL 时出现微弱条带,进一步稀释则没有条带,表明试纸条的检测限为4.8×102TCID50/mL。特异性检测结果如图7B 所示,试纸条仅能检测SVA,与其他病毒在T 线处没有颜色反应,说明制备的试纸条具有良好的特异性。
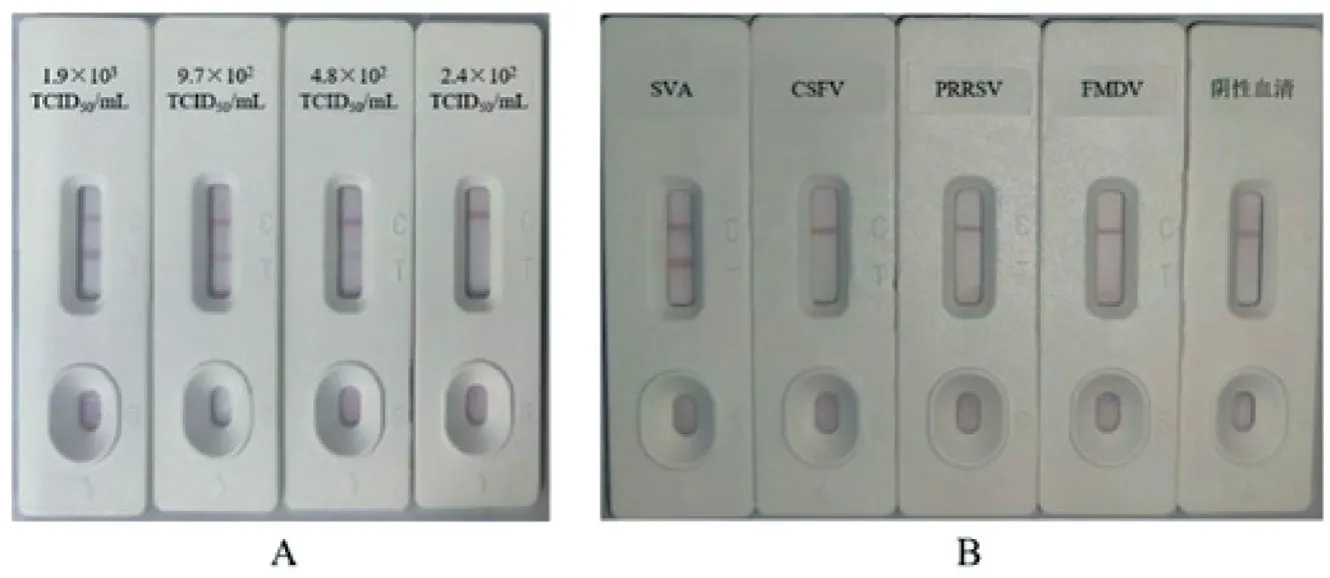
图7 试纸条的敏感性与特异性试验Fig. 7 The sensitivity and specificity assay of the strip
2.3.2 重复性试验 重复性结果如表2 所示。
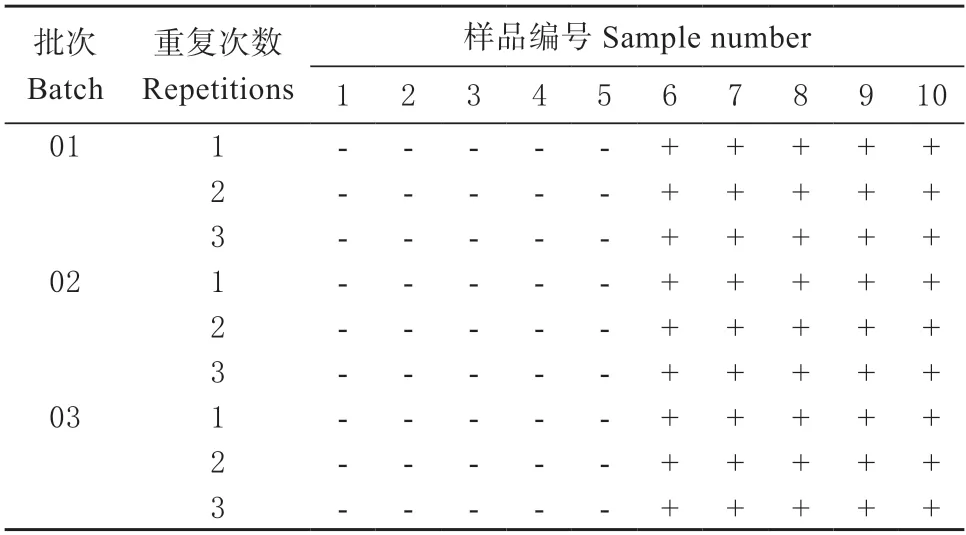
表2 重复性试验Table 2 Results of repetitive experiments

表3 临床样品检测Table 3 Test results of clinical samples
使用3 个不同批次的试纸条检测5 份阴性样品(编号1~5)和5 份阳性样品(编号6~10),每个样品重复3 次,结果均一致,批间批内变异系数均为0,说明制备的试纸条具有良好的重复性。
2.3.3 初步临床应用 27 份疑似感染SVA 的临床样品用RT-PCR 方法进行过鉴定,结果皆为阴性;用本研究的胶体金免疫层析试纸检测27 份临床样品结果同样均为阴性,结果与RT-PCR 检测方法结果一致,2 种方法对样品检测结果的一致率为100%。
3 结论与讨论
目前国内外已报道了多种SVA 抗原的检测方法,主要是各种PCR 技术,如王晨[18]等人建立的荧光定量PCR 方法,可检测10 copies/μL 的样品;Feronato[19]等建立了SVA 首个高敏感、高特异的巢式PCR 检测方法,检测限可达0.0181 ng/μL,但检测结果容易出现假阳性;Zhang[20]等建立了隔热等温PCR 用来现场检测SVA 抗原,具有良好的敏感性和特异性,但敏感性并不及荧光荧光定量PCR方法。这些检测方法虽然各有各的优点,但是其对检测人员技术要求较高,且检测时间相对较长、成本较高且需要依赖昂贵的仪器设备,导致这些方法虽有不错的检测性能,但是并不适合在基层猪场大范围普及与推广。现有的SVA 的检测技术从实验室到临床实际应用存在一定的局限,仍需解决技术和成本问题,研发一种更加灵活、经济的检测工具以用于SVA 的检测[21]。胶体金免疫层析技术作为一种免疫学检测方法,有着检测速度快,操作便捷,便于携带,经济实惠等特点,在猪病检测领域有着巨大的应用前景[22]。张涛[10]等人基于VP1蛋白单克隆抗体所制备的试纸的灵敏度为5×101.13TCID50/mL,检测时间为10~15 min,本研究所制备试纸的灵敏度(4.8×102TCID50/mL)与其相比虽然较低,但本研究所制备试纸的检测时间更快,5 min 即可判读结果。VP2 蛋白的保守性比VP1 蛋白更高[11],意味着该基因在不同毒株中的变异情况较少,这使得该检测方法更具特异性、对病毒检测的准确性更高。
目前在检测疑似感染SVA 的临床样品时仅检测到了阴性,并未检出阳性,后续若能收集到阳性样品则会对其进行补充。另外,试纸的制备为纯手工制作,金标垫采用浸泡的方式制备,对比机器喷涂的方式金标垫烘干后可能会出现金标抗体分布不均匀的情况从而影响检测性能,若能使用仪器设备大规模生产或者继续筛选出亲和力更高的单克隆抗体,则可能会进一步降低检测限,提高检测性能。
综上所述,本研究基于SVA VP2 蛋白单克隆抗体制备了胶体金免疫层析试纸,具备良好的敏感性、特异性及重复性,且操作简单、方便,为临床上SVA 疾病诊断和防控提供了新的选择。
