荧光法测定菠菜焯水过程中维生素B2的流失
——荧光法测定维生素B2的实验拓展
2023-12-11黄洋祺李誉李常耕朱颜孙维嘉范春涵李琰丁飞张晓光孔德明
黄洋祺,李誉,李常耕,朱颜,孙维嘉,范春涵,李琰,丁飞,张晓光,孔德明
南开大学化学学院,南开大学实验教学中心,天津 300071
维生素B2(Vitamin B2,简称VB2)是一种水溶性维生素,是人体内很多重要酶的组成成分,在维持人体代谢中起着重要作用。缺乏VB2会影响人体细胞的生长和机体的生物氧化,使代谢发生障碍,导致口、眼和外生殖器部位的炎症,如口角炎、唇炎、舌炎、眼结膜炎和阴囊炎等[1-3]。由于人体自身无法产生VB2,只能通过食物等外界来源摄取,因此对食源性VB2的研究具有重要意义。
VB2的分子式为C17H20N4O6,拥有三个芳香环(图1)。分子的平面刚性结构赋予了VB2较强的荧光性质,其最大的荧光发射波长大约在525 nm左右。“荧光法测定VB2的含量”是很多大学仪器分析课程的常用本科教学实验[4]。其基本的实验流程是在最佳的激发和发射波长下测定VB2标准溶液的荧光强度,利用荧光强度与浓度的线性关系制作标准曲线。在相同条件下测定未知溶液的荧光强度,并利用制作的标准曲线计算出未知溶液中VB2的含量。通过该实验,可以加深学生对分子荧光的理解,了解荧光光谱仪的基本结构,掌握仪器的基本使用步骤及荧光定量分析的基本操作,对于辅助仪器分析教学至关重要。但作为一个本科教学实验,其设计过于简单、实验内容偏少,学生往往很快就完成了全部实验内容。不仅使学生得不到充分的锻炼,而且无法凸显荧光分析法在人类生产和生活中的强大实际应用能力。为此,在原有实验内容的基础上开展进一步设计,拓展实验项目,开发内容更为丰富、且实验时间和操作难度适宜的本科教学实验,对于提升实验教学效果至关重要。

图1 VB2的化学结构式
很多食物,包括动物肝脏、肉类、蛋类、奶及奶制品中都含有大量的VB2。蔬菜也是人们获取VB2的一个重要来源,部分蔬菜的VB2含量如表1所示。菠菜是一种比较常见的蔬菜,每100 g菠菜中VB2的含量大约为0.11 mg[5],属于VB2含量较高的绿色蔬菜。但由于菠菜中含有大量的草酸(0.2-0.3 g/100 g),食用之后会与人体内的钙、镁发生反应,生成草酸钙和草酸镁等难以消化的物质。不仅不利于人体健康,长期食用还有可能引发结石。因此,在食用前通常需要对菠菜进行焯水处理以去除草酸[6],这一过程不可避免地会造成VB2的流失。本实验证明,利用荧光分析法可以考察菠菜焯水过程中VB2的析出情况。相关实验有望作为目前本科教学实验的一个拓展,不仅可以丰富教学内容,而且使实验更加贴近于人们的实际生活。有助于提升学生的学习兴趣,加深对所学内容的理解。
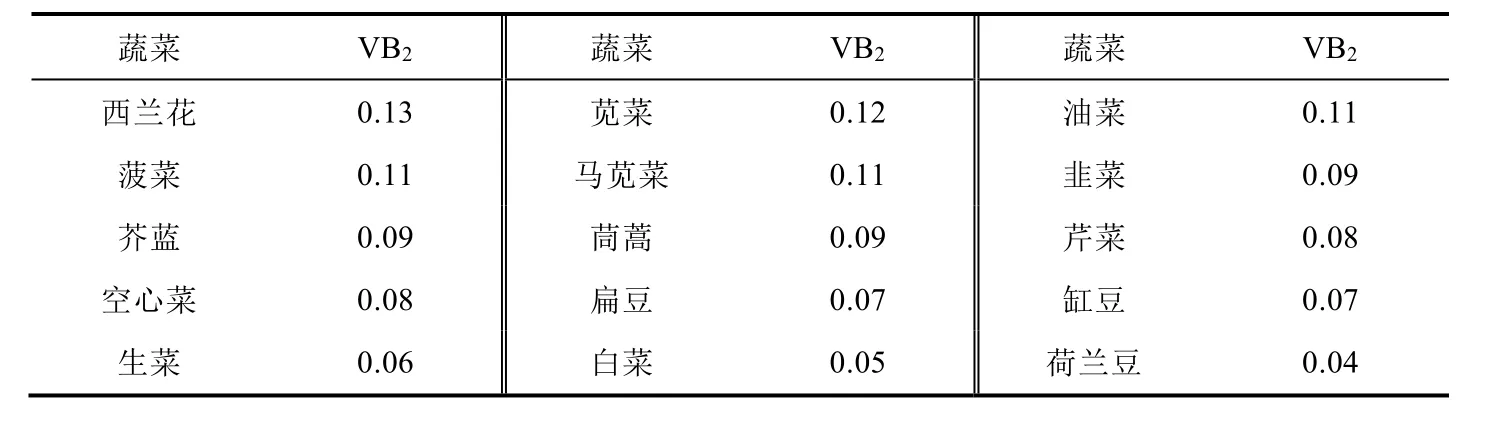
表1 部分蔬菜中VB2的含量(mg/100 g)
1 实验部分
1.1 实验原理
荧光是一种光致发光现象。荧光物质分子在吸收了特定波长的紫外光或可见光能量之后,从基态跃迁至相应的激发态。在通过振动驰豫和内转化等非辐射途径损失掉一部分能量后,积累到第一电子激发单重态的最低振动能级,再从该能级向基态的各个振动能级跃迁,产生分子荧光。在一定浓度范围内,荧光强度(F)与荧光物质浓度(C)之间成正比关系(F=kC),借此可以进行定量分析。
能够发出荧光的物质通常具有刚性平面和大共轭结构。VB2分子中由于存在由三个芳香环构成的共轭体系,且结构刚性,因此显示了良好的荧光性质。利用VB2产生的荧光信号,可以对菠菜焯水过程中释放出来的VB2进行定量分析,进而计算出该过程中VB2的流失率。
1.2 试剂和材料
1.00 μg·mL-1VB2标准贮备液:准确称取1.00 mg VB2,将其溶解于含有1%乙酸的蒸馏水中。转移至1 L容量瓶,并用含有1%乙酸的蒸馏水定容至刻度、摇匀。分装于棕色瓶中避光保存备用。
新鲜菠菜叶片:购于当地菜市场。
1.3 实验仪器
Shimadzu RF-5301PC型荧光光谱仪(日本岛津)、电加热套、Sartorius电子天平(德国赛多利斯)、25 mL比色管、10 mL离心管、5 mL移液管、500 mL锥形瓶、移液器。
1.4 实验内容
1.4.1 VB2标准系列溶液的配制
准确移取0、0.5、1.0、1.5、2.0和2.5 mL的VB2标准贮备液于25 mL比色管中,用蒸馏水稀释至刻度,摇匀。
1.4.2 菠菜焯水实验
(1) 选取新鲜的菠菜叶片,洗净,用吸水纸去除表面水分,晾干或用吹风机吹干备用。
(2) 向500 mL锥形瓶中加入400 mL蒸馏水,在电热套上加热至沸腾。此过程中将锥形瓶盖上锡纸以减少热量和水分损失。
(3) 准确称取40 g左右菠菜叶片,并快速加入至锥形瓶中,开始计时。每1 min用移液器从中取出2.5 mL水溶液至离心管中,冷却至室温备用。5 min后停止加热,此时取出两份水溶液,一份编号入上述的取出液系列,一份用于绘制取出液的荧光光谱。
1.4.3 荧光光谱的绘制
从1.4.1配制的标准溶液中选取一个浓度较大的用于荧光光谱的绘制。具体步骤如下:以525 nm作为发射波长绘制激发光谱,确定最佳激发波长。再用该激发波长绘制发射光谱,确定最佳发射波长。使用相同的步骤,绘制焯水5 min取出液的激发和发射光谱,并确定其最佳激发波长和最佳发射波长。此过程中,激发和发射狭缝分别设置为5 nm和3 nm。
1.4.4 菠菜中VB2流失率检测
分别选取463 nm和526 nm为激发和发射波长,依次测定1.4.1中VB2标准系列溶液的荧光强度。以荧光强度为纵坐标,VB2浓度为横坐标绘制标准曲线。在相同激发和发射波长下,测定1.4.2中每个焯水时间点下取出液的荧光强度。利用绘制的标准曲线计算出各取出液中VB2的浓度,进而计算出各个时间点下析出的VB2质量及流失百分率。
其中,菠菜中VB2总质量按每100 g菠菜中含0.11 mg VB2计算。
2 结果与讨论
2.1 荧光分析法用于菠菜焯水研究的可行性
VB2为水溶性维生素,室温下的溶解度为12 mg/100 mL。加热时,VB2在中性或酸性条件下具有较高的稳定性。也就是说,在焯水过程中,菠菜中的VB2可以释放到热水中,并在热水中稳定存在。因此可以推测,利用荧光分析法,可以对焯水过程中释放到水里的VB2含量变化进行监测,进而计算出VB2析出量随焯水时间的变化。为证明这一点,准确称取一定量(40.45 g)的菠菜进行焯水处理(图2)。为减少焯水过程中因水分蒸发所造成的体积损失,选用锥形瓶作为容器,并在实验过程中用锡纸密封锥形瓶口,只在取样时短暂打开。选取焯水5 min的取出液进行荧光光谱的绘制,并与VB2标准溶液进行对比。结果如图3所示,该取出液具有荧光性质,其最大激发波长(λex)和最大发射波长(λem)分别为463 nm和525 nm,与VB2标准溶液(λex= 466 nm,λem= 526 nm)非常接近。虽然菠菜中同时存在草酸、维生素C、维生素E、胡萝卜素和视黄醇等物质,但它们或者没有荧光,或者激发波长和发射波长与VB2差别较大。因此可以推断,图3b中所示的荧光信号是由菠菜焯水过程中析出的VB2所引起的。利用荧光光谱,可以对析出的VB2进行定量检测。

图2 (a) 菠菜样品;(b) 焯水装置;(c) 焯水不同时间的取出液

图3 VB2标准溶液(0.08 μg·mL-1) (a)和菠菜焯水5 min取出液(b)的激发和发射光谱
2.2 标准曲线绘制
测定VB2标准系列溶液的荧光强度,并绘制标准曲线。由于VB2标准溶液与菠菜焯水取出液的最大激发波长和发射波长略有不同,为使绘制的标准曲线适用于菠菜焯水取出液中VB2的定量分析,对激发和发射波长进行了折中选取。从图3可以看出,无论是标准溶液还是焯水取出液,在激发光谱中,荧光强度在最大激发波长前变化较缓,在最大激发波长后迅速下降,因此选择较小的463 nm作为激发波长。由于荧光光谱的对称性,发射光谱给出了相反的趋势,即荧光强度在最大发射波长前变化较大,在最大发射波长后变化减缓,因此选择较大的526 nm作为发射波长。在选取的激发和发射波长下,绘制的标准曲线如图4所示。在0.02-0.10 μg·mL-1的浓度范围内,荧光强度与VB2浓度呈现良好的线性关系。线性回归方程为F= 5203.13C(μg·mL-1) - 1.96,线性相关系数(R2)为0.9987。
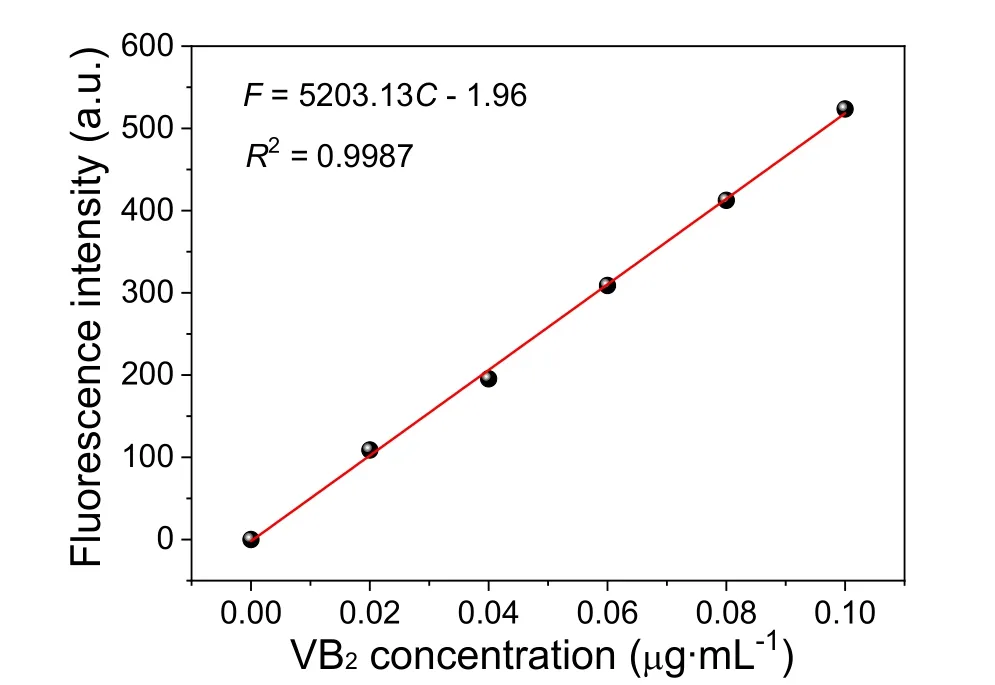
图4 VB2荧光分析的标准曲线
2.3 菠菜焯水过程中VB2的析出研究
将不同焯水时间点的取出液冷却至室温,在与绘制标准曲线相同的实验条件下测定荧光强度,并利用前面得到的标准曲线计算出每个时间点下取出液中VB2的浓度,进而计算出该时间点下VB2的总析出量。注意,在进行VB2总析出量计算时,需要把前面各时间点取出液中含有的VB2计算在内。举例而言,计算焯水3 min时VB2的总析出量,需要加上第1 min和第2 min取出液(各2.5 mL)里的VB2(各自时间点下取出液中VB2浓度 × 2.5 mL)。以每100 g菠菜中含有0.11 mg VB2计算,40.45 g菠菜中含有的VB2总量为0.04450 mg (44.50 μg)。利用此数据,可以计算出各个时间点下VB2的流失率。从表2和图5可以看出,在焯水过程中,VB2快速从菠菜中析出。在焯水1 min和2 min时,VB2的析出百分率分别为44.65%和62.74%。在0到1 min的时间段,VB2的析出速率最快。在1到2 min的时间段,仍保留了较快的析出。其中一个原因是当菠菜刚加入沸水中时,会使体系的温度下降。也就是说,在开始的1 min内,有一段时间锥形瓶中的水并没有处于沸腾状态,导致VB2未能充分析出。2 min后,VB2的析出速率变缓。当焯水时间为5 min时,VB2的析出百分率为73.82%。将焯水时间继续延长至10 min时,VB2的析出百分率达到76.66%。从以上结果可以看出,由于VB2在沸水中具有较高的溶解度,在焯水过程中,VB2极易从菠菜中析出。当焯水时间为3 min时,大约2/3的VB2将会进入到水中而流失。当焯水时间为5 min时,大约3/4的VB2将会析出。在此基础上继续延长焯水时间,对VB2的析出影响不大。考虑到人们在实际生活中并不会对菠菜进行过长时间的焯水,大约有1/2-1/3的VB2会保留在菠菜当中。从以上实验结果可以看出,虽然菠菜是VB2含量相对较高的一种绿色蔬菜,但由于食用前往往需要焯水处理以去除草酸,会造成一半以上的VB2流失,导致人们实际摄入的VB2并不多。平行进行三组实验以验证分析结果的重现性。实验结果表明(图5),该方法重现性良好,除在VB2快速析出阶段(0-3 min)相对偏差较大外(~7%),其他阶段,尤其是析出平衡阶段,偏差均在5%以内。
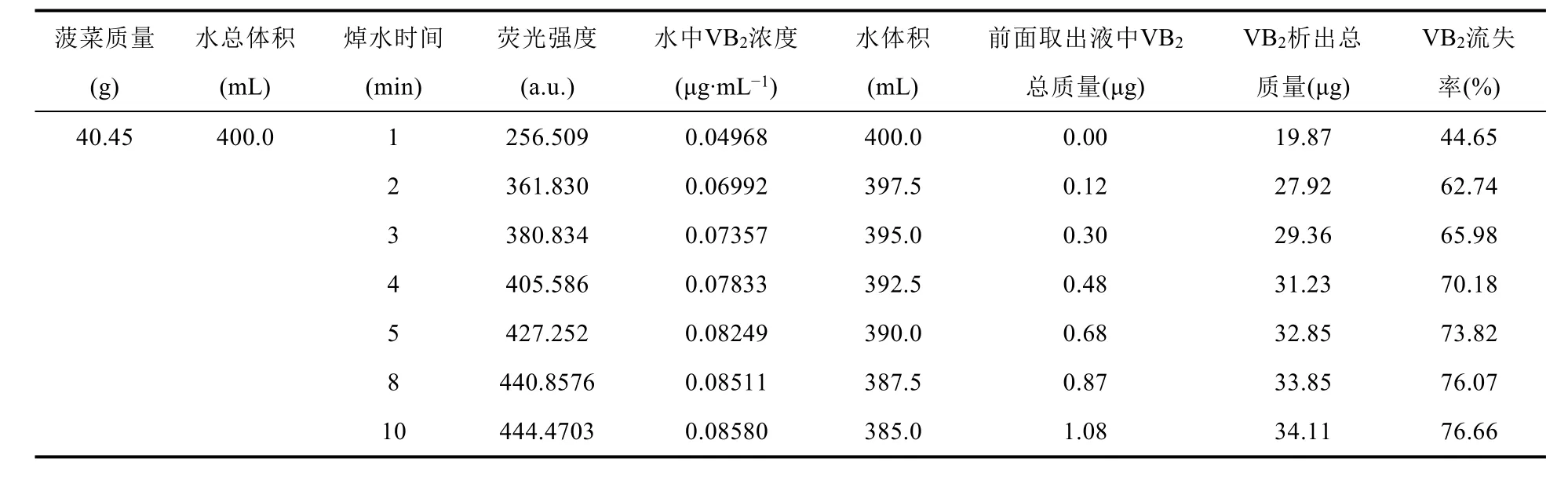
表2 不同焯水时间下VB2的流失率
2.4 将实验内容应用于本科教学的可行性
该实验可以有效克服原有实验内容偏少、学生得不到充分锻炼的问题。在原有实验基础上加入本部分内容后,全部实验可以在4个学时之内完成。另外,该部分实验内容对仪器设备要求简单,只需要引入化学实验室常备的电子天平、电热套和锥形瓶即可。以上特点使其尤其适用于本科实验教学。在两个学期的试运行中,学生普遍反映良好,被誉为印象最为深刻的仪器分析实验。学生给出了如下评价:实验既贴近生活,易于操作,又新颖有趣,通过实验,我们对理论知识有了更深的理解;实验揭示了有关菠菜焯水过程中维生素的流失情况,对指导我们的生活颇有意义;实验在原有课程实验的基础上,以分析技术证明生活中蔬菜焯水对某些营养素的影响,更加贴近生活;实验对原有课程进行了丰富补充,实验内容安全有趣,能够与日常生活紧密联系,起到对学生在学以致用方面的提示作用;实验生动有趣,与人们的生活密切相关,通过该实验,对将分析技术应用于人类生活有了更为深入的理解。
3 结语
在证明荧光分析法可以用于分析菠菜焯水过程中VB2流失情况的基础上,提出将该实验内容丰富到本科教学实验“荧光法测定维生素B2”的实验教学改革思路。这一改革思路具有如下优点:(1) 丰富了实验内容,克服了原有实验内容偏少、学生锻炼不足的问题;(2) 实验内容新颖有趣,既有利于提升学生的学习兴趣,又有利于加深学生对课堂知识的理解;(3) 研究内容贴近生活,有利于帮助学生培养学以致用的能力;(4) 实验时长适宜,对仪器要求低,使用化学实验室的常备仪器即可完成,尤其适用于推广为本科教学实验。
