土壤反硝化产物N2O/N2化学计量比例研究进展
2023-12-05李金澄吴迪
李金澄,吴迪
(中国农业大学资源与环境学院,北京 100193)
氮素是生态系统中重要的限制性养分之一,其作为蛋白质和核酸等重要生物聚合物的基本成分,为生命体提供必不可少的物质和能量[1]。在自然界中,氮素以分子氮、有机氮和无机氮的形式存在,这三种氮在大气圈、岩石圈、土壤圈、水圈等圈层间的相互转化构成了氮的生物地球化学循环[2]。土壤氮循环是全球陆地氮循环的重要环节,也是土壤生态系统元素循环的核心,影响着土壤质量、土壤肥力、土壤健康,并参与和调控多个其他物质或养分循环过程(如铁循环和硫循环)[3-4]。自然界中的大部分氮以惰性氮气(N2)的形式存在,另有一部分固定在有机化合物中,这两类化合物在大多数情况下都不能被植物直接利用。只有参与氮循环过程的微生物能将气态氮转化为氨,或通过矿化作用使有机结合氮具有生物有效性[5]。因此,土壤氮素生物地球化学循环几乎完全依赖于主要由微生物介导的一系列氧化还原反应[6],包括固氮作用、氨化作用、硝化作用和反硝化作用等[7]。自工业革命以来,燃料燃烧、化肥施用、畜牧业集约经营以及固氮植物的大量培育等人类活动导致人为活性对氮输入的贡献已远超过自然贡献[8],土壤环境的氮输入远超过生物需求,这给土壤氮循环带来了巨大的影响[5,9]。除对粮食生产的积极影响外,过量活性氮输入对生态系统的负面影响包括生物多样性降低、土壤酸化、水体富营养化、酸雨以及农业源温室气体排放等[10-11]。由土壤微生物介导的将活性氮转化为N2的自然过程,对减弱活性氮在土壤和大气中富集带来的负面影响至关重要[9-10]。在土壤氮循环过程中,微生物主要有两条途径可以将活性氮转化为N2,即反硝化(Denitrification)和厌氧氨氧化(Anammox)[12]。二者都是以硝态氮作为厌氧呼吸的电子受体,反硝化微生物将还原为N2,中间伴随氧化亚氮(N2O)等中间产物的产生[13];厌氧氨氧化微生物将和结合生成N2[14]。此过程中,由细菌和真菌介导的生物反硝化作用是最主要的活性氮移除途径之一[9,15]。作为氮循环的重要过程之一,生物反硝化是维系闭合氮循环所必需的氮素形态转化的重要环节[16],其释放的气态产物既可以是N2O(不完全反硝化)也可以是N2(完全反硝化)。N2O 是一种重要的温室气体,同时它还能参与大气中的光化学反应破环臭氧层,被认为是当前破坏平流层臭氧的首要化学物质[17]。N2O 对环境的危害还体现在其去除难度上,N2O 的大气寿命约为100 年,依靠平流层中的光解作用氧化成NO,然后才能通过干湿沉降从大气中清除[10]。因此,完全反硝化和不完全反硝化对大气环境的影响是完全不同的。
反硝化产物N2O 与N2化学计量比(N2O/N2)是研究土壤反硝化过程的重要特征值,其变化趋势可以反映反硝化进行的完全程度,明确土壤反硝化产物N2O/N2的影响因素对于调控反硝化源N2O 排放至关重要。虽然土壤反硝化过程早在19 世纪已被认知[18],但不同控制因素介导反硝化气态产物N2O/N2变化的相关机理以及这些因素之间的互作机制,仍是当前土壤氮循环研究领域最具挑战性的问题之一。这主要是由于反硝化产物N2O/N2具有极高的时空异质性[19-20];同时,N2在空气中的极高背景值导致量化反硝化N2排放速率十分困难[16,18-19]。本文综述了近些年来国际上对反硝化气态产物产生机理和不同环境因素介导下土壤反硝化产物N2O/N2响应的研究进展,以期为国内学者进行后续研究提供研究思路和背景。
1 反硝化气态产物N2O和N2的产生机理
对大部分土壤生态系统来说,反硝化微生物驱动的生物反硝化过程是氮循环中主要的氮氧化物还原途径,也是对环境变化影响较大的途径之一[10]。生物反硝化的本质是土壤中具有氮氧化物还原能力的微生物在厌氧或存在低溶解氧的条件下利用硝酸盐作为电子受体进行微生物呼吸的过程[13]。该过程的最终结果是将具有生物活性的硝态氮还原为气态氮素,其中涉及多种酶催化的代谢步骤,并受不同基因调控[21]。传统观点认为参与反硝化作用的微生物主要是细菌,其中大部分是异养、兼性厌氧菌,需要有机物提供能源和氮源[13,21]。近年来的研究表明,除反硝化细菌外,一些真菌、放线菌和古菌也能以硝态氮作为电子受体进行反硝化作用[22-23]。随着越来越多具有反硝化能力的微生物被发现,人们逐渐认识到,单一微生物的完全反硝化只是土壤中存在的特殊情况,许多微生物具有一种或几种氮氧化物还原能力,参与反硝化过程中的一个或几个还原步骤,土壤反硝化微生物的群落结构对于能否进行完整反硝化至关重要[24-25]。不同土壤环境中的反硝化微生物群落进行完全反硝化的能力不同,可能导致反硝化气态产物N2O/N2的差异。根据目前的研究,土壤中介导反硝化过程的微生物主要是反硝化细菌和反硝化真菌,二者分别驱动不同的反硝化路径,分泌的氮氧化物还原酶和相对应的功能基因均有所不同,反硝化细菌所驱动的反硝化过程的终产物为N2,反硝化真菌驱动的反硝化过程终产物则多为N2O[25–27]。
反硝化过程中N2O是由NO还原产生的。催化该过程的酶是一氧化氮还原酶(Nitric oxide reductases,NOR),其位于细胞膜上,由norB基因编码[28]。由于NOR 的特殊环境效应,它在全球范围的生态系统中广泛存在,土壤中的反硝化细菌主要分泌两种酶来催化NO 的还原,根据酶活性中心的不同它们可以分为以细胞色素c 亚基(Cytochrome c subunit)为活性中心催化反应的cNOR 和以醌为活性中心催化反应的qNOR[28-29]。与细菌不同,一些研究认为真菌的NOR系统似乎是独立于细菌进行进化的[27]。真菌分泌的一种细胞色素P450 可以在缺氧条件下过度表达,从而作为一类还原酶(P450NOR),起到还原NO 的作用[30]。与细菌NOR不同,P450NOR是由功能基因p450nor所编码的,它是一种水溶性酶,存在于线粒体和胞浆中,并直接以还原型辅酶Ⅰ(NADH)作为电子供体[31]。
反硝化过程中N2是由N2O还原产生的,该过程是细菌反硝化的最后一步。这一过程由氧化亚氮还原酶(Nitrous oxide reductase,NOS)所催化,土壤反硝化细菌所分泌的氧化亚氮还原酶(NOSZ)位于周质空间内,为可溶性含铜离子酶,其对应的反硝化功能基因为nosZ[26]。氧化亚氮还原酶已被发现存在于细菌和古菌之中,但真菌中尚未发现有NOS 的存在,这也是真菌反硝化过程最终无法生成N2的原因[32]。最新研究表明,已知的反硝化功能基因nosZ存在两个不同的分支,即分支Ⅰ(CladeⅠ)和分支Ⅱ(CladeⅡ)[33]。分支Ⅰ和分支Ⅱ在NOSZ 蛋白系统发育、nos 基因簇(NGC)组织、NOSZ酶促动力学特征、与反硝化其他途径的相关功能基因的共生频率方面都存在显著差异[34]。nosZⅠ是人们较为熟知的传统nosZ基因,通常由反硝化细菌携带;nosZⅡ是新发现的分支,由多种类型微生物所携带,其中大多数不具备反硝化过程中其他氮氧化物还原酶的编码基因[34-35]。这表明携带nosZⅡ的细菌主要是N2O 的消耗者,而非N2O 的产生者[35-36]。同时携带nosZⅡ的细菌群落对环境因素变化的敏感性高于携带nosZⅠ的细菌群落[37],且表现出更强的N2O 还原能力[38]。有研究发现反硝化气态产物比与土壤中nosZⅡ多样性呈负相关关系[39]。这一新发现的分支为减少N2O 排放、降低反硝化气态产物N2O/N2提供了新的思路[37]。
2 影响反硝化气态产物N2O/N2的主要环境因素
硝酸盐浓度、氧气(O2)、Cu离子有效性、土壤pH、土壤可利用碳等多个环境因素均可影响反硝化产物N2O/N2。然而,关于反硝化产物N2O/N2的直接调控因素还存在较多争议。有研究将影响土壤反硝化产物N2O/N2的因素分为关键因子和一般因子两类[40]。关键因子是指直接影响土壤反硝化微生物生命活动,并作为反硝化过程的反应底物及发生条件的一些因素,能决定完全反硝化过程是否发生,主要包括土壤中硝态氮、O2含量和Cu离子有效性;一般因子是指通过直接影响反硝化微生物群落结构及相关还原酶活性,或影响关键因子来间接影响土壤反硝化过程的一些因素,包括土壤电子供体量、pH、水分等。这些因素之间相互联系、相互作用,共同影响土壤反硝化进程。
2.1 关键影响因子
2.1.1 土壤硝态氮含量
硝态氮是土壤反硝化过程的反应底物和微生物进行硝酸盐呼吸的电子受体,也是影响和调控反硝化气态产物N2O/N2的重要因素。在适宜范围内,土壤溶液中的硝酸盐浓度与反硝化酶活性之间符合米氏动力学方程[41]。土壤中硝酸盐的含量在给定时间内取决于微生物的净矿化和硝化速率、植物氮素吸收、微生物固持速率以及硝酸盐通过淋溶和侧向流在土壤中的移动[42]。研究表明,土壤中的硝酸盐含量可能是反硝化气态产物N2O/N2的主要调节者[43–45]。这主要是因为硝酸盐和N2O 末端电子受体存在竞争作用,是比N2O 更为优先的电子受体,当电子供体有限时,反硝化细菌会优先将氧化程度更高的氮化合物作为电子受体还原,因此,N2O 在完全还原为N2之前有更多的机会释放到大气中[46-47]。Senbayram 等[48]研究发现,在0.2~20 mmol·L-1KNO3的浓度范围内,反硝化产物比随硝酸盐浓度的增加而升高,同时添加10 mmol·L-1的KNO3足以最大程度地抑制N2O 向N2的还原,并显著提高反硝化源N2O 的排放。较高浓度的硝态氮也会引起土壤溶液中的盐析效应,降低N2O 在土壤溶液中的溶解度并影响土壤微生物活性,导致更多的N2O 释放到空气中[49]。另外,高硝酸盐浓度可以改变土壤反硝化微生物的丰度和群落结构,使得携带nosZ基因的细菌减少[50]。Friedl等[50]和Wu等[51-52]研究发现,硝化抑制剂减排土壤N2O 的关键机制可能是其调控反硝化产物N2O/N2的降低,而这可能是由于硝化抑制剂缓解了土壤高浓度硝酸盐对功能基因nosZ丰度和还原酶NOSZ活性的抑制。
2.1.2 土壤O2含量
反硝化作用通常被认为是在厌氧条件下进行的微生物过程。因此,土壤中的O2含量是反硝化作用发生的关键性因子。一般来说,反硝化活性及其气态产物N2O 和N2的排放量均会随着O2含量的升高而降低,因为大部分反硝化菌是兼性厌氧菌,它们可以根据土壤中的O2含量采取不同方式进行呼吸,当O2存在时,好氧呼吸是首选的代谢途径[53]。同时厌氧细菌在O2存在时也无法维持自身的生态位,这会增强好氧细菌的竞争优势[54]。研究表明,反硝化产物比与O2含量通常呈正相关关系[44-45]。这是由于编码氧化亚氮还原酶的功能基因nosZ的表达被O2抑制,并且与其他反硝化功能基因的表达相比,其对O2含量更敏感[55]。反硝化气态产物N2O/N2随O2含量的变化还与相关酶的活性有关,一些研究发现不同的氮氧化物还原酶中,硝酸、亚硝酸和一氧化氮还原酶通常对O2耐受,而氧化亚氮还原酶即使在短暂的O2暴露下也可以失活[56-57]。此外,在较低O2含量下一些真菌仍可以发生反硝化过程且基本不受影响[58],这也从另一个方面解释了气态产物比升高的原因。同时硝化细菌反硝化和氨氧化也能在低氧条件下对N2O 排放产生不小的贡献[59],而N2O 的产生热点也转移到了厌氧区和好氧区之间[60]。
2.1.3 Cu离子有效性
反硝化还原酶需要重金属Cu、Fe、Mo 作为辅助因子完成蛋白质的组装过程,由于母质组成、生物或化学固定等原因而缺乏这些金属的可利用形态的土壤,可能会导致反硝化中间产物的大量积累或较低的反硝化活性[21]。其中Cu2+的有效性尤其值得关注,因为Cu2+是铜离子型亚硝酸还原酶(CuNIR)和氧化亚氮还原酶(NOSZ)的辅助因子,当Cu2+有效性较低时,两种酶的活性将受到抑制,从而导致NO-2和N2O 的积累。对亚硝酸还原酶而言,可被与CuNIR具有相同功能的、以Fe2+作为辅助因子的cd1NIR 所替代,而NOSZ的辅助因子只有Cu2+一种[25-26]。相关研究表明,Cu2+限制会影响反硝化功能基因nosZ的表达、氧化亚氮还原酶的活性以及相对应铜结合蛋白的组装[61-62]。因此,Cu2+有效性关系到反硝化微生物的N2O 还原活性,并可能直接影响反硝化气态产物比。目前,大多数研究表明Cu离子有效性与反硝化产物比呈负相关关系。Felgate 等[63]的研究表明在富缺Cu 的条件下,反硝化细菌可以通过部分关闭反硝化的最后一步并加强对硝酸盐消耗的方式继续生长繁殖,这会导致N2O 排放量升高;Sharma 等[64]在对湿地土壤的研究中发现当环境中的溶解Cu 含量低于或等于地壳丰度时,N2O 累积排放增多,而适当增加溶解Cu 含量将显著提高N2O 向N2的转化速率;而Chang 等[65]研究发现,在土壤中引入甲烷氧化变形杆菌后,其会与反硝化细菌竞争Cu离子,从而有效促进N2O排放。
2.2 一般影响因子
2.2.1 土壤电子供体量
土壤中的异养微生物需要电子供体以支持其生命代谢活动,这其中也包括了反硝化微生物。土壤活性有机碳是最常见的电子供体,可以为反硝化微生物提供电子和细胞能量[56]。多项研究发现,增加土壤活性碳可促进N2O 还原为N2,降低产物比[66-67]。然而,有研究表明,活性碳对反硝化产物比的调控与硝态氮密切相关,在不同的土壤硝酸盐含量条件下,有效碳的输入可以增加N2O和N2排放量,同时降低或不影响反硝化产物比[43-44,68]。这是因为增加碳源并不会直接促进N2O向N2还原,而是通过提高反硝化速率进而加速土壤中硝酸盐的消耗间接实现的[43-44]。此外,添加不同种类和化学性质的碳源也可以影响气态产物比的调控。例如一些有机酸和有机酸衍生物如乙酸乙酯、谷氨酰胺、醋酸盐等相较于葡萄糖作为唯一碳源输入土壤时,可以产生更低的N2O 排放峰值和气态产物比[66,69-70]。这可能与反硝化微生物对不同有效态碳的选择性利用有关,反硝化细菌在利用葡萄糖等有效性高的碳化合物的能力要强于真菌,而真菌偏好于利用一些更为复杂的有机物,如纤维素和木质素[71]。Eilers 等[72]发现向土壤中添加不同形式的可利用碳源会导致微生物碳化合物特定群落的形成,因此不同可利用碳源的添加可能会改变土壤中反硝化细菌和真菌的比例从而对反硝化气态产物比产生影响。而Giles等[70]给出了不同的看法,他们认为当不同可利用碳源作为单一输入添加时,N2O 和N2排放量及产物比变化的差异不是由反硝化微生物对碳化合物的选择性利用引起的,而可能是初始微生物底物利用效率的差异以及随后生长和呼吸之间碳分配的差异所驱动的。此外,活性碳还可通过促进其他土壤微生物的有氧呼吸来为反硝化微生物创造厌氧微区[53],以通过影响土壤O2含量的方式间接调控产物比。
有研究表明,部分无机底物与土壤反硝化过程存在耦合效应[73]。在某些土壤环境中,一些无机金属离子(如Fe2+、Mn2+)和一些无机盐离子(如硫酸盐)可以作为土壤反硝化的重要电子供体,促进氮氧化物的还原[74-75]。但有关这些不同的电子供体对反硝化气态产物比的贡献还鲜有研究。值得注意的是,有研究发现这些无机底物可能参与了真菌反硝化过程中的气态氮素的产生[27]。
2.2.2 土壤pH
土壤pH 的变化会引起细胞膜电荷的变化,从而影响反硝化微生物数量、种类、活性和氮素转化过程[76]。调节土壤pH 是调控反硝化气态产物比的重要途径之一。尽管不同环境中土壤的理化性质和外部气候条件存在很大差异,有研究表明在适宜范围内,随着pH 值的升高反硝化产物N2O/N2呈降低趋势[77-78],然而对于土壤pH 调控气态产物比的相关机理一直存在争议。研究表明,在酸性土壤环境下多种反硝化功能基因的表达受到抑制,其中nosZ的低表达量与土壤的低pH 显著相关[79]。同时,反硝化还原酶对环境中pH 的变化高度敏感,这可能与其大多位于细胞膜外侧有关[56]。其中氧化亚氮还原酶比参与反硝化的其他还原酶对低pH 更敏感[80],这可能与低pH 环境影响氧化亚氮还原酶组装过程周质中Cu2+的插入有关[81]。而在酸性环境下,与反硝化相关的几种辅因子的生物合成途径也会受到负面影响[82]。此外,还有一些研究发现酸性环境会导致游离亚硝酸(FDA)的累积,FDA 对氧化亚氮还原酶的抑制效果也在低pH 条件下被显著增强[83-84]。这意味着低pH 对氧化亚氮还原酶的抑制可能至少部分是通过FDA 间接进行的[85]。而Senbayram 等[45]发现pH 调控反硝化气态产物比的机制可能与土壤硝酸盐含量以及反硝化速率密切相关。土壤pH的升高会导致反硝化速率升高,加速硝酸盐的消耗,进而通过影响硝态氮的方式间接影响产物比。
此外,反硝化细菌和真菌对pH 改变的响应也不尽相同。Huang 等[86]研究发现,在pH 为3.8 的酸性土壤中反硝化真菌对N2O 排放的贡献可以达到70%,说明酸性环境下真菌对反硝化产物的贡献可能更大。Herold 等[87]发现反硝化细菌对土壤pH 的升高有积极响应,但真菌受pH 影响不大。故原则上调节土壤pH可以改变真菌和细菌对反硝化的贡献,进而影响反硝化产物比[88]。
2.2.3 土壤水分
由于土壤中的氧气主要存在于未被土壤水分占据的土壤孔隙中,而氧气在水中的扩散速度仅为空气中的万分之一,土壤水分和土壤物理性质在很大程度上决定土壤孔隙度和孔隙大小分布,影响氧气在土壤中的扩散[89-90]。因此土壤中的水分和氧气的变化在一定程度上是相互耦合的,就其含量而言,一定体积的土体内,含水量增多,则氧气含量减少,反之亦然[90]。而高土壤含水量也阻止了N2O 向空气中扩散,有利于N2O还原为N2。同时,土壤水分不仅决定氧气的有效性,还影响土壤基质中养分的扩散与运输、土壤的氧化还原电位以及微生物细胞和植物的代谢活性[91]。因为土壤水是硝酸盐等氮化合物的溶剂,也是植物或微生物吸收和利用氮素的介质,土壤水分可以通过控制氮化合物的生物转化和物理运输过程来影响土壤反硝化[47],进而间接调控反硝化气态产物比。
2.2.4 其他因素
除以上列举的因素外,土壤中的微量元素、土壤改良材料的添加、土壤动物活动等因素都可能影响反硝化气态产物比。如有研究发现微生物的磷(P)限制对反硝化功能基因nosZ的丰度有负面影响,并强烈抑制了反硝化还原酶活性,进而有可能对反硝化气态产物N2O/N2产生影响[92]。生物炭、半导体矿物、农药等在土壤中的应用也会影响反硝化产物比。研究表明,生物炭可以通过提高土壤pH值(进而提高氧化亚氮还原酶活性)[78]、吸附N2O[93]、吸附硝酸根和改良土壤孔隙度来抑制反硝化过程[94],还可以通过改变氮循环相关功能基因丰度[95]、促进电子向土壤反硝化微生物的转移[96]等方式降低反硝化气态产物N2O/N2。除生物炭外,向土壤中添加零价铁、纳米矿物颗粒和一些半导体矿物(如镍离子掺杂的二氧化钛、硫化镉和硫化锌)等也可以通过促进电子传递等方式促进氧化亚氮还原[97]。此外,农药的添加也可能会对气态产物比产生影响。Su等[98]研究发现施用百菌清(Chlorothalonil)可以通过直接抑制微生物电子传递活性影响反硝化过程,在不影响nosZ基因丰度的同时抑制N2O的还原,并显著促进N2O的排放。土壤动物也有可能影响反硝化过程,Shen等[99]报道了一种中型土壤动物——食真菌螨(Fungivorous mites),可以通过真菌的取食行为减少N2O排放,这可能为反硝化产物N2O/N2调控提供新思路。
总之,合理调控反硝化气态产物比对缓解N2O 排放导致的温室效应和提高氮素利用率具有重要意义。图1 列出了影响反硝化气态产物N2O/N2的主要土壤环境因素,以及农田管理措施。这些管理措施可以通过影响土壤环境条件调控反硝化产物比例。目前被广泛证实较为有效的通过影响反硝化气态产物比来降低N2O 排放的农田管理措施主要是添加硝化抑制剂/控释肥限制土壤硝酸盐含量[51-52],以及适量秸秆还田提高可利用碳含量[44],其他农田管理措施对N2O/N2调控的有效性还亟待更多的研究验证。
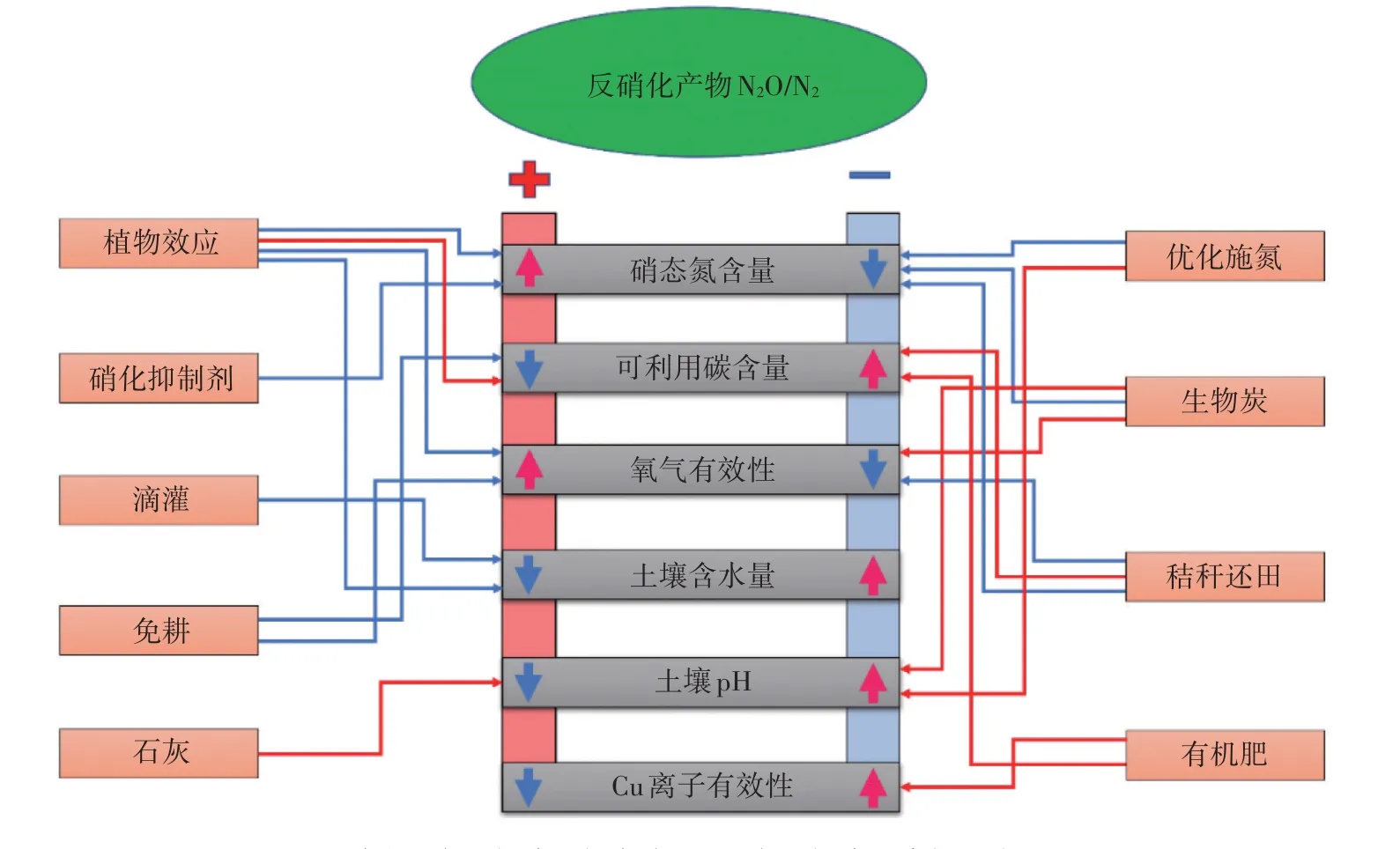
图1 影响土壤反硝化气态产物N2O/N2的主要因素[56]Figure 1 Main factors of affecting denitrification product ratio of N2O/N2[56]
3 结论
本文综述了反硝化气态产物N2O/N2的微生物产生机理和相关影响因素,主要结论如下:
(1)反硝化源N2O和N2主要是在土壤反硝化过程的最后两步产生,其中N2O还原为N2这一过程直接控制了反硝化气态产物比的变化,而由nosZⅠ或nosZⅡ基因编码的氧化亚氮还原酶在其中起到了至关重要的作用。
(2)作为土壤反硝化的反应底物和发生条件,硝态氮和O2含量是反硝化气态产物N2O/N2的最核心影响因素,二者含量升高均可抑制N2O 向N2的还原,导致N2O/N2升高。而Cu离子有效性由于与氧化亚氮还原酶的组装直接相关,也是影响反硝化产物比的核心因素之一。
(3)土壤电子供体量、pH、水分等通过与硝态氮、O2和Cu离子有效性之间的耦合或直接影响反硝化微生物活性及群落结构、反硝化功能基因丰度、氧化亚氮还原酶活性等途径调控气态产物比例。
(4)除以上因素外,土壤微量元素含量、土壤动物等也可能是影响气态产物N2O/N2的重要因素,但囿于研究数量有限,相关结论还有待进一步明确。
