可疑电子烟油中5 种吲哚或吲唑酰胺类合成大麻素的GCMS 定性和定量分析
2023-12-01刘翠梅贾薇宋春辉钱振华花镇东陈月猛
刘翠梅,贾薇,宋春辉,钱振华,花镇东,陈月猛
1.公安部禁毒情报技术中心 毒品监测管控与禁毒关键技术公安部重点实验室,北京 100193;2.中国药科大学药学院,江苏 南京 210009;3.贵阳市公安局禁毒支队,贵州 贵阳 550081
电子烟是新型烟草制品的主流产品,自2006 年以来,其市场规模和销量迅速扩张[1-2]。电子烟油中1,2-丙二醇(下文简称丙二醇)、丙三醇和水混合形成的雾化剂约占90%,尼古丁一般为0~3%[3]。近年来在电子烟油中添加四氢大麻酚(tetrahydrocannabinol,THC)、大麻酚(cannabinol,CBN)、大麻二酚(cannabidiol,CBD)、合成大麻素类(synthetic cannabinoid,SC)物质的案例逐渐增多[4-11]。
SC 物质是人工合成的大麻素受体(cannabinoid receptor,CBR)激动剂,天然大麻素与CB1R 或CB2R 结合,产生更强的生理药理作用[12]。自联合国毒品与犯罪办公室2009 年开始监测新精神活性物质(new psychoactive substance,NPS)以来,合成大麻素已成为涵盖物质种类最多、滥用最为严重的NPS 之一。合成大麻素从结构上可分为酰基吲哚类、萘甲基吲哚类、萘甲酰基吡咯类、二苯并吡喃类、苯己基酚类、吲哚酰胺类、吲唑酰胺类等,其中吲哚或吲唑酰胺类化合物是近年国内市场上出现的主要SC物质类型[8,13]。
目前,SC 物质被伪装成各类形态,以“电子烟油”“小树枝”“娜塔莎”等名称贩卖,主要滥用方式包括将其溶于电子烟油,喷涂于烟叶、烟丝、花瓣等植物表面,或者与其他毒品、NPS 混合吸食。这些合成大麻素制品对人体健康的危害具有很大的不确定性,究其原因,一是多采用“小作坊”的形式进行制作,添加合成大麻素的量具有随机性,因此很容易造成过量吸食,严重损害身体健康;二是添加合成大麻素的种类具有随机性,使得吸食后的成瘾性和危害性难以判断。国内外吸食者滥用合成大麻素制品后肇事肇祸、危害他人和社会的事件时有发生。为应对日益严重的合成大麻素滥用问题,我国于2021 年7 月1 日起,将SC 物质整类列入了《非药用麻醉药品和精神药品管控增补目录》。
电子烟油中合成大麻素的分析方法主要包括GC-MS、LC-MS、核磁共振波谱法(nuclear magnetic resonance,NMR)等[7-11]。GC-MS 是法庭科学实验室最常规的技术方法,广泛用于化合物的分析。与LC、GC、LC-MS、NMR 这些分析技术相比,采用GC-MS 进行分析具有选择性好、分离度高、检出限低、可用于同时定量分析多种成分等优点。
本研究拟基于GC-MS 全扫描模式(SCAN)和选择性离子监测模式(selective ion monitoring,SIM),建立5 种吲哚或吲唑酰胺类合成大麻素3,3-二甲基-2-[1-(4-戊烯-1-基)-1H-吲唑-3-甲酰氨基]丁酸甲酯(MDMB-4en-PINACA)、2-[1-(4-氟丁基)-1H-吲唑-3-甲酰氨基]-3,3-二甲基丁酸甲酯(4F-MDMBBUTINACA)、N-(1-氨基-3,3-二甲基-1-氧代丁-2-基)-1-丁 基-1H-吲 唑-3-甲酰胺(ADBBUTINACA)、2-[1-(4-氟丁基)-1H-吲哚-3-甲酰氨基]-3,3-二甲基丁酸甲酯(4F-MDMB-BUTICA)、2-[1-(5-氟戊基)-1H-吲哚-3-甲酰氨基]-3,3-二甲基丁酸甲酯(5F-MDMB-PICA)的定性和定量分析方法,并采用建立的GC-MS 法对25 份缴获电子烟油样品中的基质和合成大麻素进行定性和定量分析,同时研究吲哚或吲唑酰胺类合成大麻素的电子轰击(electron impact,EI)碎裂机理。
1 材料与方法
1.1 主要仪器与试剂
GCMS-QP2010 气相色谱-质谱联用仪(日本岛津公司),甲醇(色谱纯,德国Merk 公司)。
标准品MDMB-4en-PINACA(98.2%)、4F-MDMBBUTINACA(98.8%)、ADB-BUTINACA(98.8%)、4FMDMB-BUTICA(98.6%)、5F-MDMB-PICA(99.0%)、2-(2-甲氧基苯基)-1-(1-戊基-1H-吲哚-3-基)乙酮(简称JWH-250,99.3%)由公安部第三研究所提供。丙二醇(纯度99%)、丙三醇(纯度99%)、N,2,3-三甲基-2-异丙基丁酰胺(俗称WS-23,纯度98%)、三乙酸甘油酯(纯度99%)均购自北京百灵威科技有限公司,尼古丁购自美国PANPHY 公司。
25 份疑似含有合成大麻素的电子烟油样品由各地公安部门缴获后送至公安部禁毒情报技术中心毒品实验室进行检测。
1.2 仪器条件
1.2.1 GC-MS 分析条件Ⅰ
DB-35 MS石英毛细管柱(30 m×0.25 mm,0.25 µm;美国Agilent 公司)。升温程序:140 ℃保持3 min,20 ℃/min 升至320 ℃,保持12 min。载气为氦气,流速为1 mL/min,分流比为40∶1,进样量1 µL,溶剂延迟4 min,进样口温度280 ℃,EI 离子源的电子能量为70 eV,离子源温度230 ℃,传输线温度250 ℃,定性分析采集方式“SCAN”,质量扫描范围为m/z35~500。定量分析采 用SIM 模式,定量离子:m/z213(MDMB-4en-PINACA)、m/z219(4F-MDMB-BUTINACA)、m/z201(ADB-BUTINACA)、m/z218(4F-MDMB-BUTICA)、m/z232(5F-MDMB-PICA)、m/z214(JWH-250)。
1.2.2 GC-MS 分析条件Ⅱ
DB-35 MS石英毛细管柱(30 m×0.25 mm,0.25 µm)。升温程序:35 ℃保持2 min,20 ℃/min 升至55 ℃,保持3 min,40 ℃/min 升至310 ℃,保持12 min。载气为氦气,流速为1 mL/min,分流比为40∶1,进样量1 µL,溶剂延迟1.5 min,进样口温度280 ℃,EI 离子源的电子能量为70 eV,离子源温度230 ℃,传输线温度250 ℃,采集方式“SCAN”,质量扫描范围为m/z35~500。
1.3 内标溶液和标准曲线溶液的配制
内标溶液:准确称取JWH-250 50 mg,加入甲醇定容至100 mL,配制成质量浓度为0.5 mg/mL 的JWH-250 甲醇溶液。
标准储备液:准确称取合成大麻素标准物质各5 mg(称取量用各自纯度校正),转移至2 mL 容量瓶中,用内标溶液定容至2 mL,配成质量浓度为2.5 mg/mL 的标准储备液。
系列标准工作溶液:使用内标溶液对2.5 mg/mL的标准储备液进行逐级稀释,配制成质量浓度为1.0、0.5、0.25、0.1、0.05、0.025 mg/mL 的合成大麻素系列标准工作溶液。
1.4 样品处理
定性分析:移取约20 µL烟油样品,加入甲醇1 mL,涡旋混匀后进行GC-MS 分析,仪器采集条件见1.2.1节。分析烟油的基质,将20 µL/mL 的烟油样品用甲醇稀释10倍后,按1.2.2节进行GC-MS分析。
定量分析:准确称取40 mg 的烟油样品至2 mL 的容量瓶中,用内标溶液定容至2 mL,混匀后按照1.2.1节进行GC-MS 分析。如果样品含量过低,可以适当增加样品的称样量,从而保证样品浓度在标准曲线的线性范围内。
1.5 方法学验证
线性范围和定量限:配制成质量浓度为1、0.5、0.25、0.1、0.05、0.025 mg/mL 的混标溶液,按1.2.1 节条件进行分析,以目标物定量离子峰面积与内标定量离子峰峰面积的比值为纵坐标,以目标物浓度为横坐标,绘制标准曲线,确定目标物的线性范围,以线性范围的最低浓度为定量限。
基质加标回收率:采用空白烟油样品进行基质加标回收实验,取适量的空白电子烟油,分别加入不同量的质量浓度为5 mg/mL 的混标储备液,得到质量浓度为0.025、0.1、0.5 mg/mL 的基质加标混合标准溶液各3 份,按照1.4 节样品处理方法进行处理后测定,计算各目标物的加标回收率。
精密度:选取质量浓度为0.025、0.1、0.5 mg/mL 的基质加标混合标准溶液各1 份进行定量方法的精密度考察。同日内重复测定6 次计算日内精密度,6 d 内重复测定6 次计算日间精密度。
1.5 吲哚或吲唑酰胺类化合物EI-MS碎裂机理研究
通过分析EI-MS模式下MDMB-4en-PINACA、4FMDMB-BUTINACA、ADB-BUTINACA、4F-MDMBBUTICA、5F-MDMB-PICA 的碎片离子,对吲哚或吲唑酰胺类化合物在EI模式下的碎裂机制进行探讨。
2 结果与讨论
2.1 GC-MS 定性分析方法
通过将电子烟油样品中目标物的质谱图和保留时间与对应对照品的质谱图和保留时间进行比较,在25份检材中共检出5种合成大麻素,分别为MDMB-4en-PINACA、4F-MDMB-BUTINACA、ADB-BUTINACA、4F-MDMB-BUTICA、5F-MDMB-PICA(图1)。这5 种化合物的母核结构均为吲哚或吲唑酰胺,只是取代基不同,其中与酰胺的N 原子相连的取代基有2 种,分别为3,3-二甲基丁酰胺和3,3-二甲基丁酸甲酯;与吲哚或吲唑的N 原子相连的取代基有4 种,分别为丁基、4-戊烯基、4-氟丁基和5-氟戊基。为了保证5 种合成大麻素的有效分离,本研究选用了DB-35 色谱柱,在优化后的色谱条件下5 种合成大麻素和内标物均可实现基线分离,MDMB-4en-PINACA、4FMDMB-BUTINACA、ADB-BUTINACA、4F-MDMBBUTICA、5F-MDMB-PICA 的出峰时间分别为13.28、13.48、14.50、15.11、15.89 min(图2)。各化合物的质谱图见图3。

图1 5 种吲哚或吲唑酰胺合成大麻素化学结构式Fig.1 Chemical structures of five indole or indazole amide synthetic cannabinoids

图2 GC-MS 分析5 种合成大麻素和内标混标的总离子流色谱图Fig.2 Total ion chromatograms of five synthetic cannabinoids and internal standard obtained by GC-MS
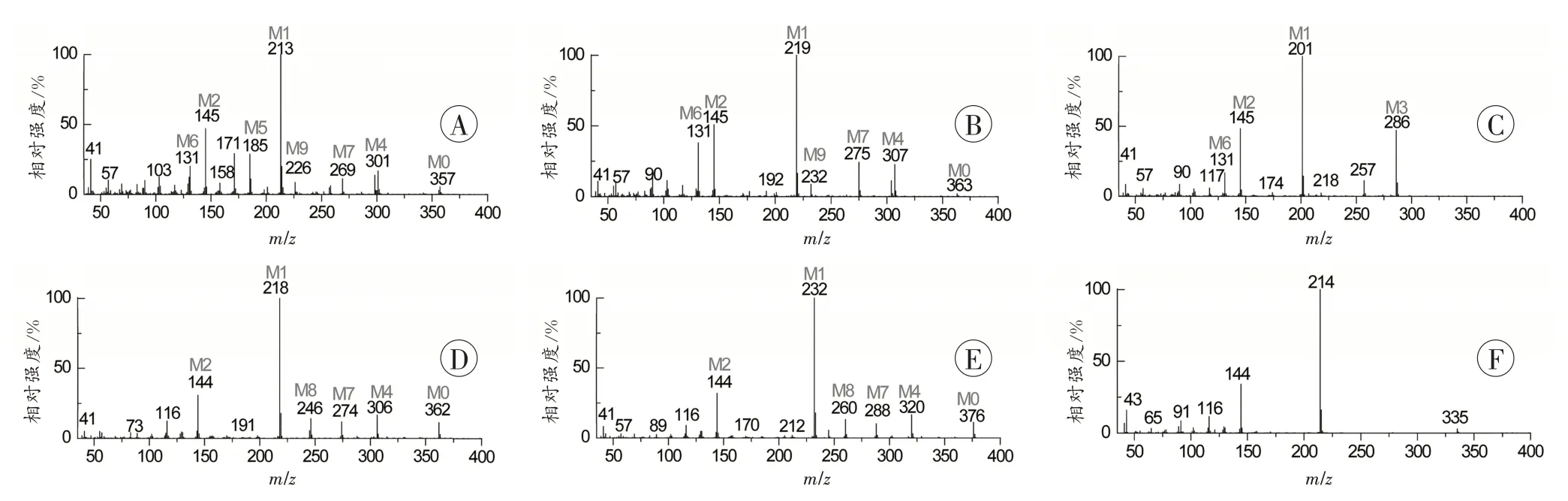
图3 5 种吲哚或吲唑酰胺合成大麻素和内标的EI-MS 图Fig.3 Five indole or indazole amide synthetic cannabinoids and the internal standard obtained by EI-MS
电子烟油的基质一般为丙二醇和丙三醇[6]。在1.2.1 节升温条件下,丙二醇和丙三醇的出峰时间较早,不能被检出。因此,在进行电子烟油基质检测时,采用起始温度更低的1.2.2 节条件升温,在该条件下,丙二醇的出峰时间为4.75 min,丙三醇的出峰时间为9.73 min(图4A),其质谱图见图5。

图4 实际缴获样品S-01 在不同程序升温条件下的总离子流色谱图Fig.4 Total ion chromatograms of seized sample S-01 obtained under different temperature programmed conditions

图5 电子烟油基质和主要添加物的EI-MS 图Fig.5 E-cigarette oil matrixes and main additives obtained by EI-MS
此外,在部分烟油样品中还发现了N,2,3-三甲基-2-异丙基丁酰胺(WS-23)、三乙酸甘油酯和尼古丁等添加物,其中WS-23、三乙酸甘油酯和尼古丁的出峰时间分别为4.28、4.94、5.12 min(图4B),质谱图见图5。WS-23 是一种凉味剂,具有薄荷香味[14]。三乙酸甘油酯是制造卷烟滤嘴常用的增塑剂[15]。尼古丁,俗称烟碱,是烟草的主要成分[15]。
2.2 吲哚或吲唑酰胺类合成大麻素EI 碎裂机制
5 种吲哚或吲唑酰胺类合成大麻素的EI-MS 图(图3)和可能的EI-MS 碎裂机制(图6)显示,该类物质的分子离子峰强度较低或不存在分子离子峰。这是由于该类物质的酰胺基侧链杂原子数量较多,且未形成稳定的共轭体系,易发生碎裂。与吲哚或吲唑环连接的羰基氧失去n电子形成正电荷中心,诱导羰基与邻近氮原子之间的化学键发生α 断裂形成稳定的偶电子离子M1。碎片离子M1 在所有质谱图中强度最高。碎片离子M1 可以继续发生γ-H 重排,其结果是取代基R2上的γ-H 转移至N 原子上,生成的碎片离子M2。M2 是吲哚或吲唑酰胺类合成大麻素的特征离子,M2 为144 时,表示母核结构为吲哚酰胺,M2 为145 时,表示母核结构为吲唑酰胺。碎片离子M1 进一步失去CO 后,生成碎片离子M5,碎片离子M5 经rH 重排得到碎片离子M6。末端酯基/酰胺基的羰基氧失去n电子形成正电荷中心,诱导羰基与邻近碳原子之间的化学键发生i断裂形成稳定的偶电子离子M3。分子离子峰发生麦氏重排可能会生成碎片离子M4 或M9。碎片离子M4 进一步失去CH3OH 和C2H4O2后,会生成碎片离子M7 和M8。

图6 吲哚或吲唑酰胺合成大麻素EI-MS 碎裂途径Fig.6 EI-MS fragmentation pathways of indole or indazole amide synthetic cannabinoids
2.3 GC-MS 定量方法
2.3.1 线性范围和定量限
为增加定量结果的准确性和方法的耐受性,本研究选用了与目标物的结构类似、出峰时间接近的合成大麻素JWH-250 作为内标。5 种合成大麻素在0.025~1.000 mg/mL 浓度范围内线性相关系数均大于0.998,线性良好;定量限均为0.025 mg/mL(表1)。
2.3.2 基质加标回收率及精密度
采用空白烟油样品进行基质加标回收实验,取适量的空白电子烟油,分别加入不同量的混标储备液,得到质量浓度为0.025、0.1、0.5 mg/mL 的基质加标混合标准溶液各3 份,按照1.4 节样品处理方法进行处理后测定,各合成大麻素的平均加标回收率的范围为94%~103%(表2)。
表2 5 种合成大麻素平均加标回收率Tab.2 Adding standard recovery of five synthetic cannabinoids (,%)

表2 5 种合成大麻素平均加标回收率Tab.2 Adding standard recovery of five synthetic cannabinoids (,%)
选取质量浓度为0.025、0.1、0.5 mg/mL 的基质加标混合标准溶液各1 份进行定量方法的精密度考察。结果表明,日内精密度相对标准偏差(relative standard deviation,RSD)小于2.5%,日间精密度RSD小于4.0%。
2.4 实际缴获样品分析
采用本研究所建立的方法对25 份缴获电子烟油样品进行定性和定量分析,检测结果(表3)显示,在25份电子烟油样品中检出了MDMB-4en-PINACA、4FMDMB-BUTINACA、ADB-BUTINACA 3 种吲唑酰胺类SC物质和4F-MDMB-BUTICA、5F-MDMB-PICA 2种吲哚酰胺类SC 物质。在22 份样品中只检出了1 种SC 物质,3 份样品中同时检出了2 种SC 物质。电子烟油样品中各SC 物质的含量范围为0.05%~2.74%。在25 份电子烟油样品中,19 份样品同时含有丙二醇和丙三醇,但含量比例不同,4 份样品(S-20、S-21、S-24、S-25)只含有丙二醇,2 份样品(S-18、S-19)只含有丙三醇(表3)。此外在部分烟油样品中还检出了WS-23、三乙酸甘油酯和尼古丁3 种主要添加物。
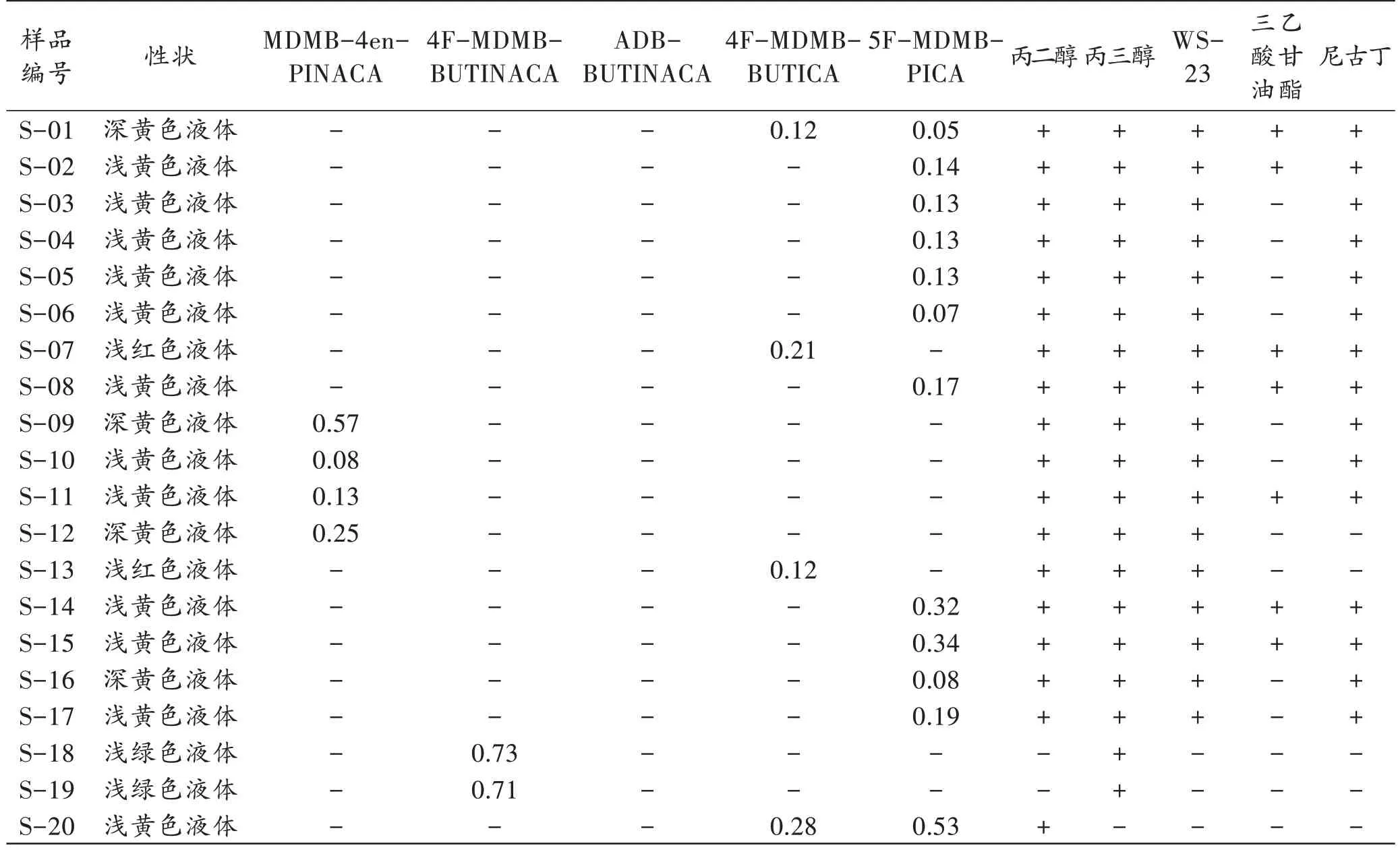
表3 缴获电子烟油样品定性、定量结果Tab.3 Qualitative and quantitative results of seized e-cigarette samples (%)
2.5 结论
合成大麻素整类列管以来,各地法庭科学实验室受理的电子烟油检材大幅增多。为便于各地涉SC 案件的顺利开展,本研究建立了电子烟油样品中合成大麻素和主要基质的GC-MS 定性和定量分析方法,并采用该方法对25 份缴获电子烟油样品进行了定性和定量分析。分析结果表明,MDMB-4en-PINACA、4FMDMB-BUTINACA、ADB-BUTINACA、4F-MDMBBUTICA 和5F-MDMB-PICA 5 种吲哚或吲唑酰胺类合成大麻素是目前国内市场上比较流行的合成大麻素的类别。电子烟油的基质主要为丙二醇和丙三醇,部分电子烟油样品中还添加了WS-23、三乙酸甘油酯和尼古丁等物质。25 种电子烟油样品中合成大麻素的含量范围为0.05%~2.74%。此外,本研究对吲哚或吲唑酰胺类SC 化合物的EI-MS 碎裂机制进行了详细的探讨,这将有助于法庭科学实验室在案件中鉴定该类物质或其他具有类似结构的化合物。
