18F-FDG摄取量诊断非酒精性脂肪性肝病患者罹患冠状动脉粥样硬化性心脏病探讨*
2023-11-18邵孝如葛颖颖
邵孝如,周 筱,葛颖颖
随着社会经济的发展和人们生活方式的转变,非酒精性脂肪性肝病(nonalcoholic fatty liver disease,NAFLD)患病率不断上升。有研究显示,NAFLD患者大多伴有糖脂代谢紊乱,脂肪沉积在NAFLD的发生发展过程中发挥重要作用[1,2]。在各种致病因素的作用下,NAFLD病情进展可能导致血管内皮细胞功能出现障碍,致使脂质细胞、单核巨噬细胞等沉积在血管内皮下,最终形成动脉粥样斑块,导致心脑血管疾病的发生[3]。冠状动脉粥样硬化性心脏病(coronary atherosclerotic heart disease,CHD)是导致NAFLD患者死亡的主要原因之一[4]。目前,临床常用冠状动脉CT血管成像(coronary computed tomography angiography,CCTA)和正电子发射计算机断层扫描成像(positron emission computed tomography,PET)等方法诊断动脉斑块形成,其中PET/CT可通过示踪剂18F-氟代脱氧葡萄糖(FDG)被CHD病变部位异常摄取实现检查目的,在心血管疾病的临床诊断方面应用较为广泛。本研究采用18F-FDG摄取量诊断NAFLD患者罹患CHD,分析了诊断效能,现报道如下。
1 资料与方法
1.1 一般资料 2020年1月~2021年12月我院诊治的NAFLD患者120例,男性86例,女性34例;年龄为41~70岁,平均年龄为(61.8±10.4)岁。符合《非酒精性脂肪性肝病诊疗指南(2018年修订版)》[5]的标准,CHD诊断以CCTA检查结果判定。纳入患者无饮酒史,无影像学检查禁忌证。排除标准:①患有乙型肝炎或丙型肝炎;②既往存在冠状动脉血管重建史;③合并严重的肾功能障碍。
1.2 临床指标 记录患者年龄、体质指数、合并症(代谢综合征、高血压、糖尿病)。入院次日采集空腹静脉血,使用美国贝克曼库尔特有限公司生产的AU-2700型全自动生化分析仪检测血生化指标。
1.3 CT心脏冠脉成像检查 使用美国GE公司生产的Light Speed 64排128层螺旋CT扫描仪,管电压为120 kV,管电流为100~450 mA,准直器为64 mm×2 mm×0.6 mm,厚度为0.75 mm,旋转时间为0.28 s。嘱患者平稳呼吸,经肘静脉注射造影剂优维显60 mL,注射速率为3.5 mL/s,行冠状动脉成像扫描。将扫描图像传输至专用工作站,由2名影像科医师进行影像评估。冠状动脉管腔狭窄程度﹥50%被诊断为CHD,冠状动脉斑块CT值﹤100 Hu被定义为非钙化斑块,CT值﹥130 Hu则为钙化斑块,而CT值为101~129 Hu为混合斑块。
1.418F-FDG PET/CT检查 使用美国GE公司生产的Discovery PET/CT扫描仪,禁食6 h以上。CT扫描参数:管电压120 kV,管电流180 mA,准直器64 mm×9 mm×0.625 mm,厚度为2.5 mm,旋转时间0.5 s。给予18F-FDG 5.18 MBq.kg-1静脉注射,静卧1 h。行三维模式PET扫描:视野576 mm×576 mm,矩阵256×256,层厚5 mm,层间隔5 mm。对PET数据经衰减校正、迭代重建,与CT图像一同传送至专用工作站,进行图像融合。分析冠状动脉图像钙化情况,测量心肌标准摄取值(standard uptake value,SUV)。在心脏横断面图像上绘制感兴趣区域(region of interest,ROI),逐层测量心脏的SUV,各层最大值记为SUVmyo。沿肝脏右叶周边绘制ROI,测量肝脏SUV,测量3次,取平均值,记为SUVliv,计算SUVmyo/SUVliv比值(SUVratio)。

2 结果
2.1 两组临床指标比较 经影像学检查,在本组NAFLD患者中发现CHD患者28例;NAFLD合并CHD组体质指数、空腹血糖、总胆固醇和甘油三酯水平均显著高于NAFLD组,合并代谢综合征、高血压和糖尿病占比均大于NAFLD组,差异有统计学意义(P<0.05,表1)。
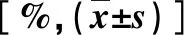
表1 两组一般资料比较
2.2 两组CCTA检查结果比较 CHD组非钙化斑块和非钙化斑块明显狭窄占比均显著大于NAFLD组,差异有统计学意义(P<0.05,表2)。

表2 两组CCTA检查结果[n(%)]比较
2.3 两组18F-FDG PET/CT检测指标比较 CHD组SUVmyo和SUVratio均显著低于NAFLD组,差异有统计学意义(P<0.05,表3)。
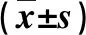
表3 两组18F-FDG PET/CT检测指标比较
3 讨论
NAFLD是指无过量饮酒史及其他明确的肝脏损伤因素,以肝细胞脂肪变性和脂肪沉积为主要特征的临床综合征,其形成机制较为复杂,糖脂代谢紊乱是主要因素之一。长期糖脂代谢紊乱导致动脉血管脂质沉积,单核细胞在斑块内浸润,释放炎性因子,损伤血管内皮细胞功能,形成血液高凝状态,从而发生粥样斑块[6]。NAFLD在肝脏的病变早期多属于单纯性脂肪肝。随着糖脂代谢紊乱的加剧,可导致线粒体功能紊乱,促使肝脏坏死性炎症及纤维化产生,并加速冠状动脉粥样硬化的进展[7]。研究显示,NAFLD常与肥胖、糖尿病、高血脂、高血压和代谢综合征合并存在。由于肥胖、高血压、糖尿病是促进CHD的常见危险因素,因此NAFLD与CHD之间的相关性逐渐受到临床关注[8]。本研究结果显示,CHD患者体质指数、空腹血糖、总胆固醇和甘油三酯水平均显著高于NAFLD患者,代谢综合征、高血压和糖尿病占比均显著高于NAFLD患者,说明NAFLD与心血管疾病联系紧密,与有关研究果相似[9]。
本研究结果还显示,CHD患者冠状动脉非钙化斑块和非钙化斑块明显狭窄占比均显著高于NAFLD患者。NAFLD和CHD存在共同的危险因素,例如胰岛素抵抗、代谢紊乱、炎症、氧化应激反应等。上述因素不仅促进NAFLD的发生,同时也促进了CHD的病变发展,而非钙化斑块通常为不稳定斑块,是导致CHD发生的主要因素[10]。
近年来,应用放射性同位素标记的分子探针技术进行冠状动脉粥样硬化斑块显像已成为研究热点之一。目前,临床常使用18F-FDG作为炎症标志物,其是血管炎症和低氧炎症成像的示踪剂,高度积聚在能量代谢增强的细胞,但其在冠状动脉成像方面还较少使用,可能是因为冠状动脉疾病患者大多合并糖尿病,进行18F-FDG PET/CT显像效果可能受到不同程度的影响[11]。有研究显示,18F-FDG不会被邻近心肌组织摄取,在冠状动脉显像方面表现出良好的对比度和显像效能,从而能够较好地反映冠状动脉粥样硬化斑块信息[12]。本研究结果显示,CHD患者SUVmyo和SUVratio均显著低于NAFLD患者。SUV降低与NAFLD和非钙化斑块及其引起的明显狭窄相关,提示18F-FDG PET/CT显像所获得的SUV在NAFLD患者与CHD患者之间存在摄取差异,而这种代谢差异可能来自于不同物质的代谢通道。应用18F-FDG PET/CT显像是基于炎性细胞浸润的葡萄糖代谢摄取,从而提供了冠状动脉粥样硬化斑块形成的信息[13]。
葡萄糖是心肌代谢的主要能量来源之一,而FDG是葡萄糖的类似物,可用于反映心肌的葡萄糖代谢状态。在临床实践中,常常能观察到非特异性生理性心肌FDG摄取现象,但却无法清楚地识别心肌的真正病理性改变[14]。NAFLD患者的心肌FDG摄取可能会在一定程度上增加,表明低SUV可能是肝脏脂肪变性和冠状动脉粥样硬化之间的中介因子[15]。因此,评估NAFLD患者的心肌FDG摄取状况具有重要的意义。据报道,葡萄糖通过葡萄糖转运蛋白(GLUT)进入心肌细胞。NAFLD与胰岛素抵抗密切相关。胰岛素敏感性降低可能增加心肌胰岛素抵抗,降低GLUT活性,因而可在NAFLD患者中观察到心肌FDG摄取受损,游离脂肪酸含量增加[16]。心肌葡萄糖和脂肪酸代谢改变可能引发其能量需求的改变,从而导致心脏病,其具体发生机制可能为心脏摄取FDG降低,可能会导致心脏功能受损,多见于缺血性心脏病和糖尿病性心肌病。游离脂肪酸增加可抑制丙酮酸脱氢酶(PDH)和丙酮酸的积累。丙酮酸转化为乳酸可导致心脏结构、形态和功能的改变[17,18]。此外,心肌摄取FDG受损和脂质代谢增加均与心外膜脂肪组织有关,被认为是冠状动脉粥样硬化发生发展的重要因素。因此,NAFLD患者心肌摄取FDG受损可能会产生动脉粥样硬化效应,促使冠状动脉粥样硬化病变进展,故应用18F-FDG PET/CT扫描评估NAFLD患者心肌摄取FDG变化可用来预测心血管事件的发生风险[19,20]。本研究的横向研究性质使其难以确定心肌摄取FDG与NAFLD或冠状动脉粥样硬化之间的因果关系。本研究未考虑内脏脂肪组织和皮下脂肪组织等因素的影响,从而可能影响了对心肌摄取FDG的准确性。影像学检查诊断的效能还需要冠状动脉造影结果的证实。