恩替卡韦治疗慢性乙型肝炎合并非酒精性脂肪性肝病患者疗效研究*
2023-11-18周季颖谢月红于翠霞
周季颖,谢月红,于翠霞
相关临床研究显示,慢性乙型肝炎(CHB)合并非酒精性脂肪性肝病(NAFLD)的发病率呈逐年升高趋势,而目前临床上关于NAFLD对抗病毒治疗CHB的影响尚未明确。有研究显示,CHB合并NAFLD患者的发病原因与代谢因素密切相关,但部分学者研究显示,HBV X蛋白能诱导肝细胞脂肪变性[1]。治疗CHB合并NAFLD患者的难度较大,可能影响病毒学和生化学应答,而CHB合并NAFLD可加速肝病进程,从而导致肝纤维化的发生,并增加肝癌的发生风险[2,3]。目前,临床治疗CHB合并NAFLD患者多以抗病毒治疗为主。恩替卡韦是一种抑制乙型肝炎病毒(HBV)复制的抗病毒药物,其属于鸟嘌呤类似物,其作用机制在于通过与天然底物脱氧鸟苷三磷酸盐竞争,从而抑制HBV聚合酶的活性,可有效减轻肝细胞损伤[4,5]。本研究主要探讨了应用恩替卡韦治疗CHB合并NAFLD患者,观察了疗效及其肝脏受控衰减参数(CAP)和肝组织脂肪变性程度的变化,现将研究结果报道如下。
1 资料与方法
1.1 病例来源 2019年6月~2021年8月我院收治的CHB患者63例,男性43例,女性20例,年龄为20~56岁,平均年龄为(35.78±12.29)岁;CHB合并NAFLD患者43例,男性25例,女性18例,年龄为21~55岁,平均年龄为(36.02±12.55)岁。CHB诊断符合《慢性乙型肝炎防治指南(2015年更新版)》[6]的标准,NAFLD诊断符合《非酒精性脂肪性肝病防治指南(2018年版)》[7]的标准。排除标准:妊娠或哺乳期妇女;存在精神疾病或智力异常者;存在其他脏器器质性病变者;患有恶性肿瘤者。患者及其家属签署知情同意书,本研究经我院医学伦理委员会审核并批准。
1.2 治疗方法 给予两组患者恩替卡韦分散片(正大天晴药业集团股份有限公司,国药准字H20100019)0.5 mg口服,1次/d,治疗观察12个月。
1.3 检测与检查 常规检测血生化指标;采用荧光定量聚合酶链式反应法检测血清HBV DNA载量;采用化学发光法检测血清HBeAg和HBsAg(试剂盒购自上海信帆生物科技有限公司);采用ELISA法检测血清反应性氧化物(ROS)、脂联素(ADPN)和肿瘤坏死因子-α(TNF-α,试剂盒购自上海蓝基生物科技有限公司)水平;使用法国Echosens公司生产的Fibroscan-502型肝脏弹性检测仪行肝脏硬度检测(LSM)和CAP检测。

2 结果
2.1 两组疗效比较 在治疗6个月和12个月,CHB组血清ALT复常率均显著高于CHB合并NAFLD组(P<0.05,表1)。
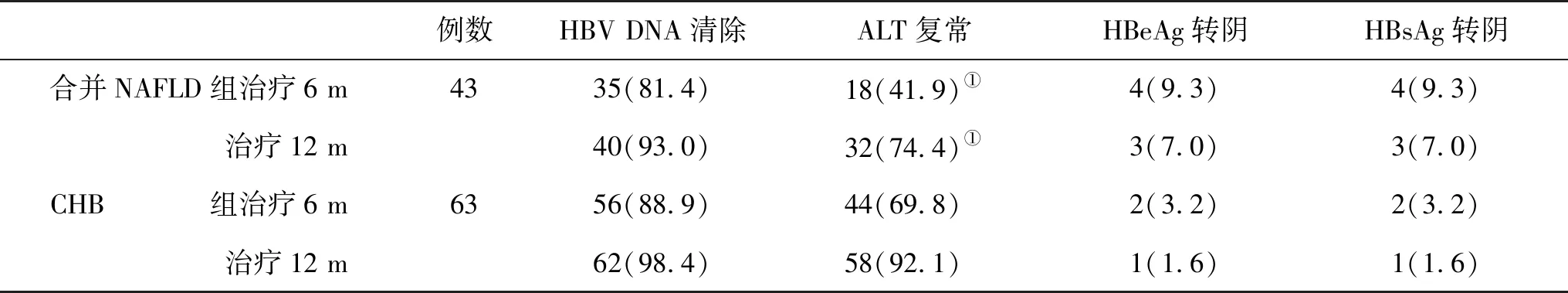
表1 两组疗效(%)比较
2.2 两组相关指标比较 在治疗12个月末,CHB合并NAFLD组血清ALT和CAP显著高于CHB组,差异均有统计学意义(P<0.05,表2)。
表2 两组相关指标比较
2.3 两组血清ROS、ADPN和TNF-α水平比较 在治疗12个月末,CHB合并NAFLD组血清ROS和TNF-α水平均显著高于CHB组(P<0.05),而血清ADPN水平显著低于CHB组,差异均有统计学意义(均P<0.05,表3)。
表3 两组血清ROS、ADPN和TNF-α水平比较
3 讨论
作为一种全球性传染性疾病,CHB是严重威胁公共卫生安全的重大疾病。根据相关调查研究结果显示,CHB患者仍占上报的传染病很大的比例。因此,做好CHB的防控工作意义重大[8,9]。CHB的发生原因主要由于持续感染HBV引起,且HBV可经血液、母婴垂直等途径传播,其临床症状多表现为乏力、食欲减退、肝区不适等。随着病情的不断进展,可出现肝病面容、脾脏肿大等[10]。CHB与NAFLD均属于肝脏类疾病,CHB患者发病后,其肝脏中的胆汁可持续累积,从而导致肝功能受损,而NAFLD是指非酒精因素引发的弥漫性肝细胞大泡性脂肪性病变。对于CHB合并NAFLD患者,若未采取及时有效的治疗措施,可导致肝硬化或肝癌,对患者的生命安全造成严重威胁[11]。
目前,临床治疗该病多采用抗病毒药物,其可有效延缓疾病进展,效果较好。但由于CHB合并NAFLD受肝脂肪变性的影响,可因为肝脏脂肪沉积,导致病情加重,从而使抗病毒的治疗效果受到影响。作为一种新型核苷酸类药物,恩替卡韦服用后可使磷酸向活性三磷酸盐转化,并使乙型肝炎病毒的三磷酸脱氧鸟嘌呤核苷竞争被抑制,将病毒多聚酶启动途径被阻断,从而使肝纤维化的进程延缓,具有见效快、安全性高等特点[12-15]。同时,相关研究显示,恩替卡韦具有推动肝脏蛋白质合成作用,从而发挥保护患者肝功能的作用[16]。CHB合并NAFLD患者疾病发展为肝硬化的病理学基础为肝纤维化,其发生原因与患者肝细胞内的炎性介质作用相关。CAP则是目前临床上常用的判断肝脂肪变进程的指标[17-19]。在本研究,在治疗6个月时,CHB合并NAFLD组血清ALT复常率显著低于CHB组,其机制可能与以下原因有关:非酒精性脂肪性肝病可引发肝脏脂肪代谢功能障碍,从而使肝细胞内贮存大量脂肪物质,不仅使肝组织正常生理结构异常,且使细胞色素P450被抑制,从而使恩替卡韦接触肝细胞的面积减小,影响恩替卡韦的抗病毒治疗效果。NAFLD患者肝细胞脂肪的变化使肝组织的纤维化加重,从而使恩替卡韦的抗病毒生物化学应答受影响。非酒精性脂肪性肝病患者机体的自然杀伤细胞活性下降,从而使特异性和非特异性免疫应答受影响,进而导致恩替卡韦对HBV的清除效果下降[20-22]。同时,本研究结果还显示,在治疗12个月时,CHB合并NAFLD组血清ALT复常率显著低于CHB组,而两组血清HBV DNA清除率和HBeAg转阴率比较,差异均无统计学意义。由此可见,随着恩替卡韦治疗时间的延长,CHB合并NAFLD组生物化学应答率也随之改善,有助于提高治疗效果。
TNF-α属于临床常见的一种血清炎症因子,其可诱导炎性介质的大量释放,在肝炎、肝纤维化等疾病的发生和发展过程中具有重要的作用。血清ROS则可使线粒体功能受损,从而使游离脂肪酸代谢过程受影响,且过多的游离脂肪酸可使炎症信号通路被激活,刺激炎症因子的大量释放,使肝组织炎症反应加重,促使肝纤维化的形成。作为一种脂肪细胞因子,ADPN的主要作用在于参与胰岛素信号通路的调节,在糖脂代谢等多种疾病的发生和发展过程中起推动作用。同时,ADPN还可使炎性介质的生成被抑制,在糖尿病和NAFLD等疾病的发病过程中发挥主要作用[23,24]。本研究在治疗12个月,两组血清ALT、HBV DNA载量、CAP、ROS和TNF-α水平均较于治疗前显著下降,而合并NAFLD组显著不如CHB组明显,血清ADPN水平相较于治疗前显著上升,而合并NAFLD组上升不如CHB组,提示应用恩替卡韦治疗CHB患者,在改善血清ALT和HBV DNA载量方面效果显著,但血清TNF-α、ROS、ADPN等应答稍差,不及CHB患者应答好。有临床研究显示,肝细胞脂肪变是影响恩替卡韦抗病毒治疗CHB患者效果的影响因素之一[20]。
综上所述,应用恩替卡韦治疗CHB患者的治疗效果优于CHB合并NAFLD患者,可有效降低血清ALT水平和HBV DNA载量。合并NAFLD的CHB患者可能由于肝内脂肪变影响了生化学应答率,其氧化应激和炎症反应不能被控制,显然干扰了抗病毒治疗疗效。因此,对于合并NAFLD的CHB患者在采取常用的药物抗病毒治疗时,需要认真研究同时存在的肝脂肪变的处理方法,比如加强科学的运动,适度地控制饮食,是否能提高生化学应答。在选择这些患者入组时,需要告知同时存在的脂肪肝对肝功能和抗病毒治疗的影响,加强对体质量和血生化指标的监测,以期提高治疗效果。