miR-148b-3p通过调节脂代谢基因对肝癌细胞恶性生物学行为的影响*
2023-11-18王迪迪黄玉荣王建君左常茜何磊杨杰
王迪迪,黄玉荣,王建君,左常茜,何磊,杨杰*
(1.贵州医科大学附属医院 消化内科,贵州 贵阳 550025; 2.六盘水市人民医院 消化内科,贵州 六盘水 553000)
肝癌在癌症死因中排在第4位[1],其常用治疗方法有外科手术切除、肝动脉栓塞、放化疗及分子靶向治疗等,但治愈率仍然很低[2]。有研究发现miR-148a-3p在肝癌中可通过调节胆固醇和甘油三酯来影响肝癌细胞的生物学行为[3]。miR-148b-3p作为miR-148/152家族成员之一,理论上与同族miR-148a-3p可以靶向同源基因,可能具有相似的生物学行为[4],但其在肝癌脂代谢中的作用却鲜有报道。本研究通过探索miR-148b-3p对肝癌细胞的恶性生物学行为和肝癌中脂质代谢的影响,以寻找治疗肝癌的潜在靶点,为后续的临床转化提供一定的理论依据。
1 材料与方法
1.1 实验材料
1.1.1细胞来源 人肝脏细胞LO2和肝癌细胞系Huh7、Hep1均从中国科学院上海生命科学院细胞库购买。
1.1.2主要试剂 细胞培养基DMEM、胎牛血清(fetal bovine serum,FBS)、胰蛋白酶均购于美国Gibco公司,CCK8试剂盒、miRNA逆转录试剂盒、RNA逆转录及扩增试剂盒、油红染料、棕榈酸、油酸及BCA蛋白定量试剂盒均购自北京金式金生物技术有限公司,miRNA转染试剂盒、miR-148b-3p mimics以及阴性对照(miR-148b-3p mimics NC)均购自广州锐博生物公司,Matrigel基质胶和Transwell小室购自美国Corning公司;miR-148b-3p引物、U6引物及脂代谢相关引物由上海生工生物工程有限公司合成,蛋白激酶AMP激活的非催化亚基γ2(PRKAG2)、胰岛素诱导基因2(INSIG2)、染色体结构域解旋酶DNA结合蛋白9(CHD9)、脂肪酸合成酶(FASN)、硬脂基辅酶A去饱和酶1(SCD1)、过氧化物增殖物激活受体γ(PPAR-γ)一抗及辣根过氧化物酶(HRP)标记的山羊抗兔二抗购自美国Abcam公司。
1.1.3实验仪器 SW-CJ-2FD超净工作台购于苏州安泰空气技术有限公司,CKX31倒置显微镜购于日本Olympus公司,5840R高速离心机购于德国Eppendorff 公司,3131细胞培养箱、Scientific全波段酶标仪、ND-2000超微量核酸蛋白定量仪均购于美国Thermo公司。
1.2 研究方法
1.2.1交集基因筛选 运用TCGA数据库(https://portal.gdc.cancer.gov/)获取肝癌、miR-148b-3p、脂代谢通路三者交集的靶基因,使用R语言cor.test函数对miR-148b-3p进行相关性检验,筛选条件为cor<-0.2 &P<0.001,找出共表达关系的基因;使用String软件对共表达基因构建蛋白互作网络,得到蛋白的相互作用关系;使用Cytoscape软件对miR-148b-3p调控网络进行可视化,得到网络图;使用TargetScan软件对目标miR-148b-3p进行靶基因预测,得到其靶基因结果;使用R语言筛选miR-148b-3p靶基因和共表达基因的交集基因,得到韦恩图和交集基因列表;将miR-148b-3p的共表达基因、靶基因和脂代谢通路取交集,得到交集基因和韦恩图。
1.2.2细胞培养及分组 人肝脏细胞LO2和肝癌细胞系Huh7、Hep1细胞分别用含有10%FBS和1%青链霉素的DMEM完全培养基于37 ℃、5%CO2中培养,检测miR-148b-3p在3种细胞中的表达水平;选取肝癌细胞系中miR-148b-3p表达量最低的细胞系Huh7作为研究对象,继续培养传代,待培养皿中生长达到80%的细胞时,将细胞分为对照组(转染miR-148b-3p NC)及实验组(转染miR-148b-3p mimics),接种于6孔板中,培养密度至50%,备用。
1.2.3PRKAG2、INSIG2、CHD9、FASN、PPAR-γ及SCD1的mRNA表达 采用荧光定量逆转录-聚合酶链反应(reverse transcription-polymerase chain reaction,RT-PCR)法测定Huh7实验组和对照组中PRKAG2、INSIG2、CHD9、FASN、PPAR-γ及SCD1的mRNA表达水平。使用Trizol提取细胞和组织的总RNA并测定核酸浓度,取0.4~1 μg RNA 按miRNA加尾法逆转录试剂盒或RNA逆转录试剂盒说明书进行cDNA的合成;分别以U6或β-acting为内参,以cDNA为模板进行RT-PCR,miR-148b-3p、PRKAG2、INSIG2、CHD9、FASN、PPAR-γ及SCD1的引物序列见表1;计算各基因在实验组及对照组中的相对水平(RQ=2-ΔΔCt);重复实验3次,每次3个复孔。

表1 引物序列
1.2.4细胞增殖能力 通过CCK8实验检测细胞活性:实验组和对照组的肝癌Huh7细胞均以2×103个/100 μL接种于96孔板中,每孔绕边缘一圈加入100 μL PBS以减少蒸发,随后放入培养箱中,待细胞贴壁后观察;分别在0 h、24 h、48 h、72 h、96 h时间点每孔加入10 μL的CCK8试剂后避光孵育1 h;在波长450 nm下检测其吸光度值(OD值),实验组和对照组每组各设置8个复孔。用克隆形成实验检测细胞克隆数:按照500个/孔细胞种植于6孔板中,并加入1.5 mL的完全培养基孵育,每3天观察1次细胞状态;在第10天显微镜下观察克隆形成情况,每孔加入4%多聚甲醛1 mL于4 ℃冰箱内固定60 min,PBS清洗1次;每孔加入0.1%结晶紫染液1 000 μL,染2 min,双蒸水洗涤数次,晾干后拍照并计数;每组设3个复孔。
1.2.5细胞迁移能力 通过划痕实验检测细胞迁移能力:实验组和对照组的肝癌Huh7细胞均按5×105个/孔加入6孔板中37 ℃培养过夜,待每孔内细胞长满时,用200 μL的枪头垂直于底部的水平线划线,随后用PBS清洗3次;加入无血清培养基,于0 h、48 h在微镜下拍照并测定划痕宽度,记为划痕距离,同一位置的0 h划痕距离与48 h的划痕距离之差即为各组迁移距离(迁移距离=0 h划痕距离-48 h的划痕距离),重复3次,结果用Image J软件进行分析。
1.2.6细胞侵袭能力 Transwell实验检测转染后细胞侵袭能力:取浓度为 5×105个/mL的实验组和对照组Huh7细胞悬液200 μL加入到Transwell小室内(含孵育后无血清培养基水化基底膜),下室加入含10% FBS的DMEM 600 μL,37 ℃培养箱中孵育24 h;PBS清洗后4%多聚甲醛中固定20 min,随后放入0.1%结晶紫中染色20 min、自来水中清洗30 s~1 min后取出,中性树脂封片后在倒置显微镜下观察并拍照,每张玻片在200倍下随机拍取3个视野并计数,取平均值,重复3次。
1.2.7油红O染色观察脂滴形成 将实验组和对照组的肝癌Huh7细胞用脂性培养基(油酸钠∶棕榈酸钠=2∶1)刺激,再培养24 h后,用1×PBS清洗3次,4%多聚甲醛2 mL固定30 min(常温),双蒸水清洗掉固定液,随后加入100%丙二醇1 mL 脱水5 min,加入经滤菌和预热处理的0.5%油红O染液1 mL于37 ℃孵箱中孵育30 min,85%丙二醇1 mL洗1 min,再用双蒸水漂洗3次,最后加入l mL的双蒸水在孔中防止脂滴破裂,随后在显微镜下观察细胞中脂滴形成并拍照。
1.2.8PRKAG2、INSIG2、CHD9、FASN、CD36、PPAR-γ蛋白表达 Western blot法测定各基因蛋白表达的相对水平:取实验组和对照组中转染后生长状态良好的肝癌Huh7细胞,依据BCA蛋白定量试剂盒使用说明提取总蛋白并检测浓度和定量;将定量的蛋白样品分别进行电泳、电转,以GAPDH作为内参,将目标蛋白通过SDS-PAGE分离,随后转至PVDF膜并在常温下用含5%脱脂奶粉的TBET封闭1 h、TBST清洗4次,使用PRKAG2、INSIG2、CHD9、FASN、CD36、PPAR-γ、GADPH一抗(1∶1 000)孵育,在4 ℃冰箱中过夜,TBST缓冲液洗膜3次,使用辣根过氧化酶二抗(1∶5 000)孵育1 h,TBST洗膜3次,最后打开V3蛋白印记检测分析系统显色、曝光、拷贝,利用软件Image J将蛋白曝光图片进行灰度值统计,重复3次。
1.3 统计学分析
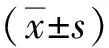
2 结果
2.1 交集基因筛选
将miR-148b-3p的共表达基因、靶基因和脂代谢通路取交集,得到交集基因韦恩图,共找到了3个交集基因,即PRKAG2、CHD9、INSIG2,说明miR-148b-3p在肝癌中可能通过这3个基因调节脂代谢通路。如图1。
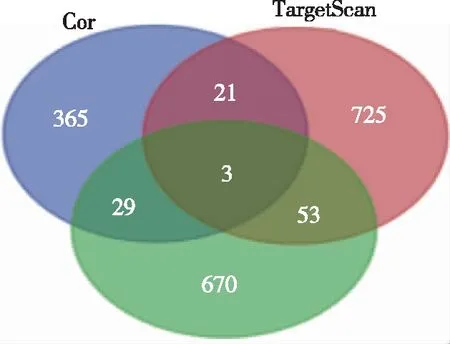
图1 miR-148b-3p的共表达基因、靶基因和脂代谢通路交集情况
2.2 miR-148b-3p表达
结果显示,肝癌细胞系Huh7中miR-148b-3p的表达量显著低于Hep1细胞(P<0.01)和正常肝细胞系LO2(P<0.001),Hep1中的表达量也低于LO2(P<0.05)。如图2。
2.3 细胞增殖能力
实验组Huh7细胞增殖能力在24 h、48 h、72 h、96 h时间点均弱于对照组,提示Huh7细胞的增殖能力受到了miR-148b-3p的抑制(P<0.05);实验组Huh7细胞克隆形成数目要显著少于对照组(P<0.01)。如图3、图4。

注:(1)与对照组比,P<0.05。

注:A、B分别为对照组和实验组Huh7细胞克隆形成结晶紫染色的结果,C表示细胞克隆形成数的相对定量结果;(1)与对照组比,P<0.01。
2.4 细胞的迁移能力
转染48 h后,实验组Huh7细胞的伤口愈合能力较对照组显著减弱,说明miR-148b-3p能够抑制肝癌细胞Huh7的迁移能力(P<0.05)。如图5。

注:图A表示划痕实验的镜下结果,B图为划痕测量结果;(1)与对照组比较,P<0.05。
2.5 细胞的侵袭能力
Transwell实验发现实验组细胞穿过基底膜的数量要明显少于对照组,说明miR-148b-3p能够显著抑制Huh7的侵袭能力(P<0.01)。见图6。
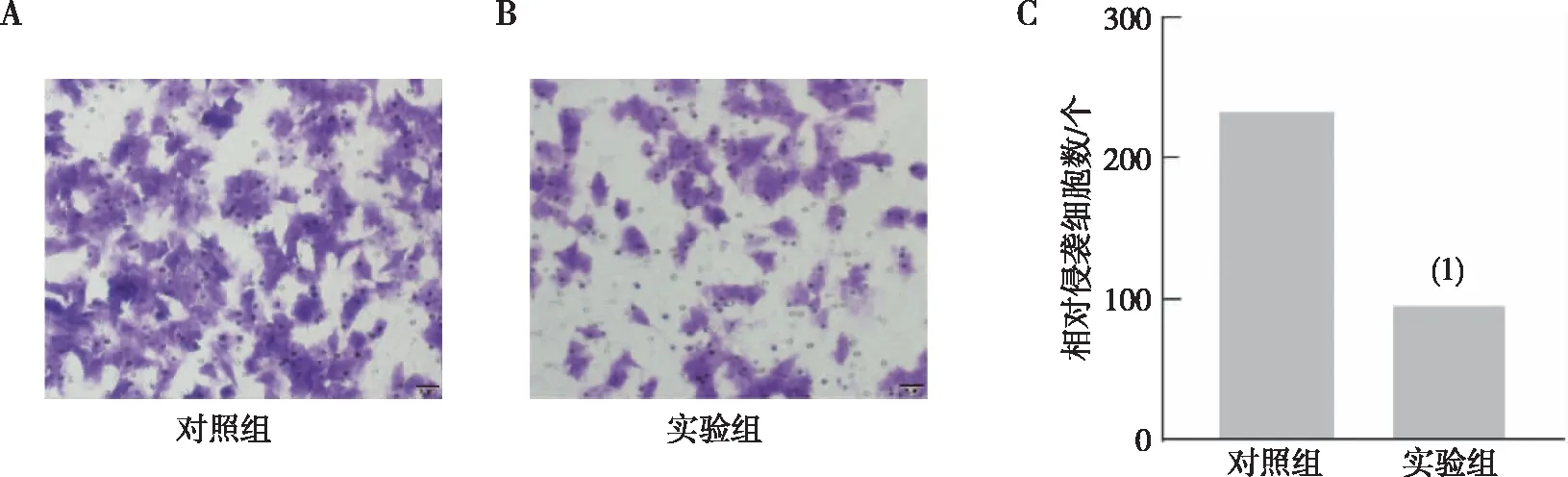
注:A、B分别表示对照组和实验组Huh7细胞结晶紫染色结果,C表示侵袭细胞数的定量结果;(1)与对照组相比,P<0.01。
2.6 油红O染色检测脂滴形成情况
油红O染料发现,实验组脂滴形成较对照组明显减少(P<0.01),说明miR-148b-3p抑制了细胞中的脂滴的形成。见图7。
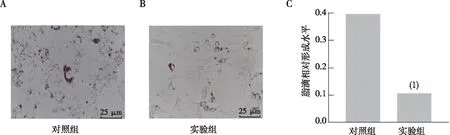
注:A、B分别表示对照组和实验组Huh7细胞脂滴形成的结果,C表示脂滴形成的定量结果;(1)与对照组相比,P<0.01。
2.7 肝癌细胞中交集基因及脂肪生成指标基因mRNA相对表达量
RT-PCR实验发现在对照组与实验组Huh7细胞中,交集基因PRKAG2及INSIG2在实验组中的表达量较对照组升高(P<0.01、P<0.01),而CHD9则降低(P<0.001),脂肪生成指标FASN、PPAR-γ、SCD1 mRNA水平在实验组中的表达量较对照组均降低(P<0.001、P<0.001、P<0.01)。见图8和表2。
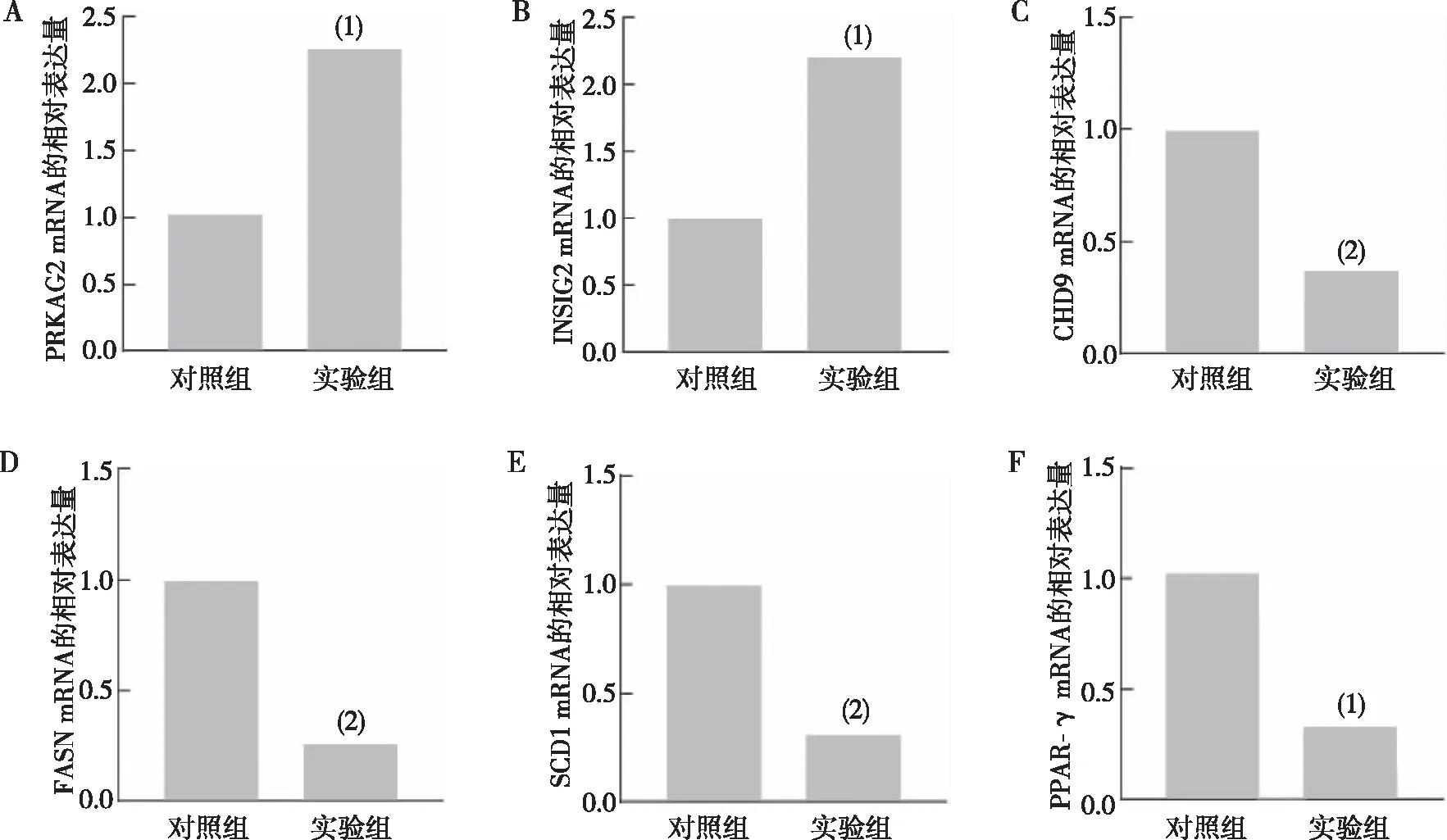
注:A—F表示各基因mRNA相对表达量;与对照组相比,(1)P<0.01,(2)P<0.001。
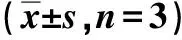
表2 实验组和对照组转染miR-148b-3p后交集基因及脂肪生成基因mRNA水平
2.8 肝癌细胞中交集基因及脂肪生成指标基因蛋白的表达
Western blot实验发现,过表达miR-148b-3p 能够引起肝癌细胞系Huh7中交集基因PRKAG2蛋白表达量显著升高(P<0.01)、INSIG2蛋白表达量升高(P<0.05)、CHD9蛋白表达量降低(P<0.05);脂肪生成指标基因FASN蛋白表达量显著降低(P<0.01)、PPAR-γ蛋白表达量降低(P<0.01)、SCD1蛋白表达量降低(P<0.01)。见图9和表3。
注:A—F表示蛋白相对表达量,G、H表示蛋白条带结果;与对照组相比,(1)P<0.05,(2)P<0.01。
表3 实验组和对照组Huh7细胞转染miR-148b-3p后交集基因及脂肪生成基因蛋白
3 讨论
异常脂质代谢在癌细胞中普遍存在,其不仅改变细胞膜的组成成分及细胞通透性,还能产生多种脂毒性物质,从而诱发异常的生物学行为[5-7]。这些变化都源自于癌细胞需要适应局部环境的代谢变化,也就是肿瘤细胞的“代谢重编程”。脂质代谢受到多种信号通路的调节,并与调节细胞生长、增殖、凋亡等信号网络相互关联[8]。
miR-148/152家族在肝癌发生发展中扮演着重要角色[9-11]。miR-148b-3p可通过调节相关通路抑制肝癌的进展,其机制除了抗炎,抗血管形成外,也存在调节脂质代谢的可能[9,12]。在本研究中,通过数据库初步证实miR-148b-3p与肝癌脂代谢通路中存在的交集基因:PRKAG2、INSIG2和CHD9。
PRKAG2是蛋白激酶(AMPK)的亚基基因,它的经典功能包括减少肝脏和脂肪组织中的脂肪合成、增加脂肪酸氧化、刺激肌肉葡萄糖摄取和糖酵解[13-14]。INSIG2主要参与脂肪酸和胆固醇合成的调节[15],在小鼠体内敲除INSIG2后,小鼠肝脏中的胆固醇和甘油三酯积累增多[16]。CHD9的低水平表达能够激活Notch信号的传导[17],该信号传导被认为是新陈代谢的关键调节剂,且Notch1 的单倍体不足会促进脂肪生成和积累[18-19]。由此可见,以上3个基因与脂代谢的关系密切相关,这为研究miR-148b-3p与脂代谢的关系提供了理论依据。
在脂肪生成指标基因FASN、PPAR-γ、SCD1中,FASN是脂肪酸从头合成过程中的关键酶,也是恶性肿瘤治疗的靶点。FASN特异性抑制剂如cerulenin、C75、奥利司他及TVB-2640等,能够在体内外对各种恶性细胞产生抑制作用[20-22]。PPAR-γ在脂质的储存和动员、葡糖糖代谢和炎症反应中起关键作用[23]。在肝细胞中,PPAR-γ不仅促进细胞内脂质的沉积,还促进游离脂肪酸(free fatty acids,FFA)及甘油三酯摄取的增加[24]。SCD1是硬脂基辅酶A去饱和酶1,其敲低可以降低脂肪肝细胞中甘油三脂的水平[25]。
在本研究中,过表达miR-148b-3p能够显著抑制肝癌细胞中脂滴的形成,肝癌细胞增殖、迁移和侵袭的作用也明显受到抑制。通过上调miR-148b-3p的表达水平发现,交集基因中PRKAG2、INSIG2基因的mRNA表达水平升高,CHD9基因的mRNA表达水平下降,前者功能与抑制脂肪生成有关,后者是促脂肪生成的基因,这说明上调miR-148b-3p在肝癌中能够抑制脂肪的生成。脂肪生成指标基因FASN、PPAR-γ、SCD1mRNA表达量及对应蛋白表达量均因miR-148b-3p高表达而降低,提示miR-148b-3p在肝癌脂代谢的上游调控效应中,可能存在多靶点的作用。
综上所述,过表达miR-148b-3p可抑制肝癌细胞的增殖、转移和侵袭能力,可能与miR-148b-3p抑制了肝癌细胞的脂代谢有关。
