L(934)正交试验法优选3 种静脉用难溶性抗菌药物调配方法*
2023-11-14伊迪热斯江艾力刘玉花艾则孜江艾尔肯
伊迪热斯江·艾力,刘玉花,艾则孜江·艾尔肯,周 静,宋 涵
(新疆医科大学第一附属医院,新疆 乌鲁木齐 830011)
对静脉用药调配中心(PIVAS)进行全面质量管理,特别是调配环节的质量控制,是规避调配风险、提高药品质量、确保患者静脉用药安全的重要保证[1-2]。不溶性微粒是指在药物生产、使用过程中经各种途径引入的微小颗粒,粒径介于1~50 μm,为肉眼不可见、易动性、非代谢性的粒子[3],是《中国药典(一部)》《美国药典》《英国药典》《日本药典》中均明确规定的输液常规检查项目。不溶性微粒能引起炎性反应、肉芽肿、血管栓塞、热原反应,甚至可能引起肿瘤[4]。研究表明,难溶性粉针剂在调配过程中易出现不溶性微粒数超出药典标准的现象[5-6]。我院PIVAS 药师在调配中发现,哌拉西林他唑巴坦钠、头孢呋辛钠、头孢哌酮钠舒巴坦钠3 种粉针剂溶解速率慢,初溶时间长,药品说明书中无详细的调配过程描述,尚无溶解完全的统一判断标准,缺乏统一、标准的调配操作规程,导致调配结果参差不齐。为此,本研究中采用L9(34)正交试验法优选上述3 种静脉用难溶性抗菌药物的调配方法,为PIVAS 调配环节的标准化管理提供参考。现报道如下。
1 仪器与试药
1.1 仪器
BSC-ⅡA2型生物安全柜,SW-CJ-1B型水平层流台,均购自苏净集团苏州安泰空气技术有限公司;TL - 2000 型振荡器(泉州鲤城区东坝实验仪器厂);30 mL 一次性使用无菌溶药注射器(山东威高集团医用高分子制品股份有限公司);0.45 μm 微孔滤膜(上海市新亚净化器件厂);SGO-PH200A 型生物显微镜(深圳市深视光谷光学仪器有限公司)。
1.2 试药
注射用哌拉西林钠他唑巴坦钠(商品名特治星,Hanhui Pharmaceuticals Co,Ltd,批号为22024121,规格为每支4.5 g);注射用头孢呋辛钠(山东润泽制药有限公司,批号为5220400306,规格为每支1.5 g);注射用头孢哌酮钠舒巴坦钠(商品名舒普深,辉瑞制药有限公司,批号为FR2228,规格为每支1.5 g);5%葡萄糖注射液(新疆华世丹药业股份有限公司,批号为211016115);灭菌注射用水(批号为22041004B),0.9%氯化钠注射液(批号为G122052807),均购自四川科伦药业股份有限公司。
2 方法与结果
2.1 不溶性微粒测定与计数
溶液调配均由专业药学人员按无菌操作,在百级洁净条件下对静脉用药进行混合调配。调配后,按2020年版《中国药典(四部)》通则0903 不溶性微粒检查法,用注射器抽取标示装量为100 mL的药液25 mL,沿滤器内壁缓慢注入经预处理的滤器(滤膜直径25 mm)中。静置1 min,缓慢抽滤至滤膜近干,再用微粒检查用水25 mL,沿滤器内壁缓慢注入,洗涤,并抽滤至滤膜近干,用平头镊子将滤膜移至平皿上,微启盖子,使滤膜适当干燥,闭合平皿,置显微镜载物台上,调好入射光,放大100 倍进行显微测量,调节显微镜至滤膜格栅清晰,移动坐标轴,测定有效滤过面积中粒径大于10 μm的微粒数,计算3 个供试品测定结果的平均值。根据显微计数法统计难溶性抗菌药物溶解后不溶性微粒的数量,在显微镜下(放大100 倍)观察药物溶解不完全时的观测结果见图1 A,溶解完全时的观测结果见图1 B。
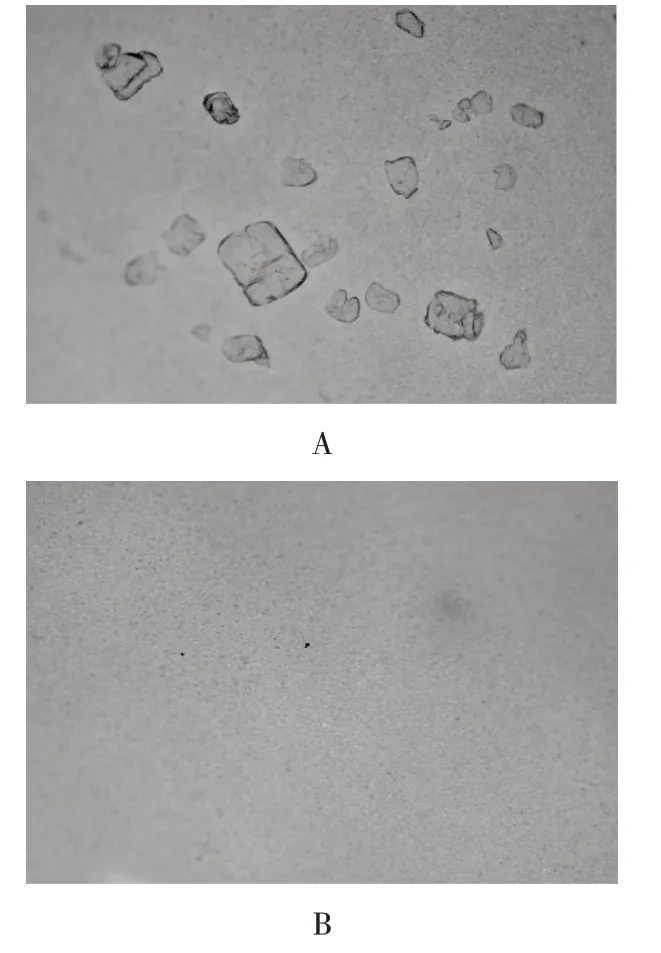
A.溶解不完全时 B.溶解完全时图1 头孢呋辛钠显微镜观测结果(×100)A.When cefuroxime sodium is incompletely dissolved B.When cefuroxime sodium is completely dissolvedFig.1 Microscopic observation results of cefuroxime sodium(×100)
2.2 调配方法优选
正交试验设计与结果:根据3种难溶性抗菌药物的药品说明书确定各自的调配方法,即先将药物与一定体积的初溶溶剂混合,振摇,再加入溶剂至医嘱/处方规定的总量。据以往工作经验可知,振荡时间(因素A)、初溶溶剂体积(因素B)、溶剂品种(因素C)是影响药物调配效果的主要因素,以复溶后药液不溶性微粒数量为考察指标,并根据每种药品的溶解特性、西林瓶体积,同时兼顾调配效率,确定每种药品正交试验中各因素的水平值。L9(34)正交试验因素与水平见表1,试验设计与结果见表2。可见,各因素的影响大小依次为振荡时间>初溶溶剂体积>溶剂品种;哌拉西林钠他唑巴坦钠、头孢呋辛钠、头孢哌酮钠舒巴坦钠的优选调配条件分别为A2B3C2,A2B2C2,A2B3C2。
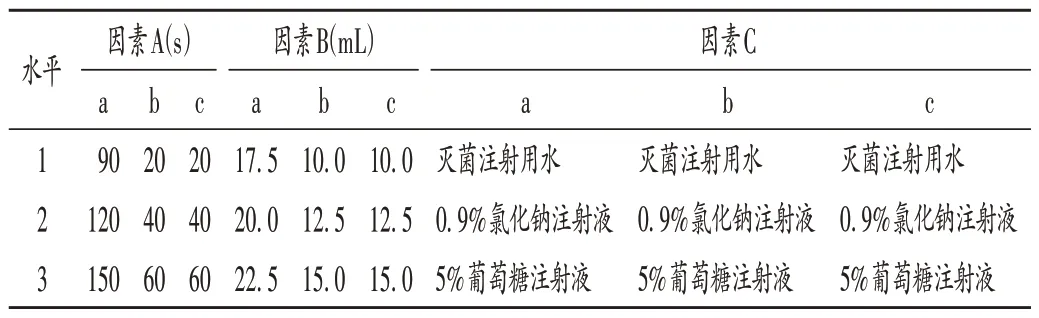
表1 L9(34)正交试验因素与水平Tab.1 Factors and levels of the L9(34)orthogonal test
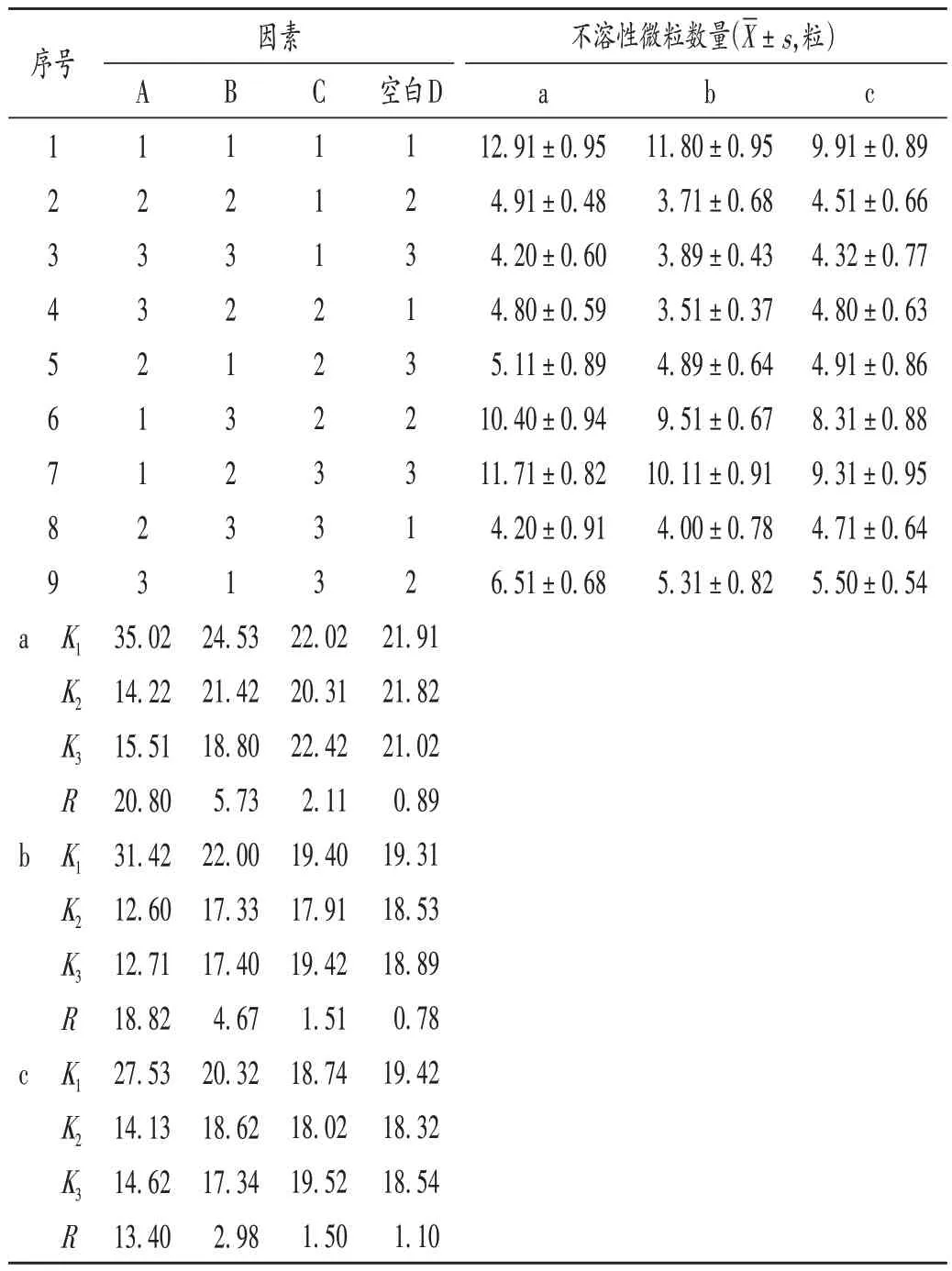
表2 L9(34)正交试验设计与结果Tab.2 Design and results of the L9(34)orthogonal test
Shapiro-Wilk 正态性检验:采用SPSS 19.0 统计学软件进行正态性检验,P<0.05 为差异有统计学意义。由表3 可知,3 种药品每组样本的检验结果均无显著差异(P >0.05),表明接受原假设,3种药品每组样本均具有正态性特质。

表3 Shapiro-Wilk正态性检验结果(n=3)Tab.3 Results of the Shapiro - Wilk normality test(n=3)
方差分析:采用SPSS 19.0统计学软件分析,P<0.05为差异有统计学意义。由表4 可知,溶剂品种对3 种药品的不溶性微粒数量均无显著影响(P>0.05)。哌拉西林钠他唑巴坦钠的振荡时间和初溶溶剂体积的水平变化对结果均有显著影响(P>0.05),结合直观分析结果可确定调配方法,即采用22.5 mL溶剂(灭菌注射用水、0.9%氯化钠注射液、5%葡萄糖注射液)预溶后,置振荡器上振荡120 s,稀释,调配。头孢呋辛钠的振荡时间和初溶溶剂体积的水平变化对结果均有显著影响(P<0.05),结合直观分析结果可确定调配方法,即采用12.5 mL溶剂(灭菌注射用水、0.9%氯化钠注射液、5%葡萄糖注射液)预溶后,置振荡器上振荡40 s,稀释,调配。头孢哌酮钠舒巴坦钠仅振荡时间水平变化对结果有显著影响(P<0.05),结合直观分析结果可确定调配方法,即采用10.0 mL 溶剂(灭菌注射用水、0.9%氯化钠注射液、5%葡萄糖注射液)预溶后,置振荡器上振荡40 s,稀释,调配。

表4 方差分析结果Tab.4 Results of the ANOVA
2.3 验证试验
以0.9%氯化钠注射液为溶剂,按优选的调配方法进行验证试验,结果3种难溶性抗菌药物中不溶性微粒数量均显著减少(P<0.05),表明优选的调配方法稳定、可行。详见表5。
表5 优化前后3种难溶性抗菌药物中不溶性微粒数量比较(±s,粒)Tab.5 Comparison of the number of insoluble particles of three intravenous insoluble antibacterial drugs before and after optimization(±s,n)

表5 优化前后3种难溶性抗菌药物中不溶性微粒数量比较(±s,粒)Tab.5 Comparison of the number of insoluble particles of three intravenous insoluble antibacterial drugs before and after optimization(±s,n)
时间优化前优化后t值P值a b c 18.60±0.50 3.60±0.21 37.070 0.001 15.31±0.67 3.11±0.24 25.570 0.002 16.88±0.66 3.91±0.30 53.970 0.000
3 讨论
3.1 溶剂量选择
由前期单因素试验结果可知,溶解难溶性药物的初溶溶剂量少,导致溶解时间延长,且溶解不完全;溶剂量多,增加抽吸力度和调配难度。对于较难溶解的哌拉西林钠他唑巴坦钠,为防止药物外溅,溶解药物时所抽取药液以不超过注射器的3/4为宜,我院无菌操作常用注射器量程一般为30 mL,故选择最大水平点为22.5 mL。
3.2 pH 值对药物溶解性的影响
头孢哌酮钠的pH 值应为4.5~6.5[7],输液中加入头孢哌酮钠后pH 值为4.0 左右[8],表明溶液中存在游离酸。而头孢哌酮游离酸在水中极微溶,故溶液易呈混悬状。当不同pH 值的输液与头孢哌酮钠混合,澄清或混浊一般以pH 值4.08为限,混浊的原因可能为混合溶液pH 值小于4.08时部分头孢哌酮游离。但本研究结果显示,灭菌注射用水、0.9%氯化钠注射液、5%葡萄糖注射液均可用于调配头孢哌酮钠舒巴坦钠,其原因可能为我院采用的溶剂对调配液的pH 影响不显著,未明显影响头孢哌酮钠的溶解行为,同时提示溶剂中离子强度对主药的溶解行为影响较小。
3.3 药品规格、药物溶解速率和平衡时间三者的关系
药物的表观溶解度会受到药品粉末过量的影响,这可能是由结晶速率和溶解速率间的竞争所致[9]。平衡溶解度虽不取决于溶液中固体过量的量[10],但达到饱和的最终速率可能与溶液中固体过量的量成正比,过量越大,饱和速率越快[11]。另外,溶解体积对平衡溶解度的测定结果也有影响,这是由于振摇过程中减小溶剂体系的体积会加快饱和速率,使溶液更快达到平衡[12]。故调配难溶性静脉用药品时不可选用过大的初溶溶剂剂量,否则,不仅会降低溶解饱和速率,还会影响调配人员的工作效率。
3.4 研究意义
本研究中通过对混合调配后的成品输液进行不溶性微粒测定,对我院PIVAS 的难溶性静脉用药品的不溶性微粒数量进行严格管控,难溶性静脉用药品的调配方法可作为规范推广。其研究意义在于:1)建立了难溶性静脉用药品的调配标准,可减少成品输液中不溶性微粒的含量;2)建立了完善的药品调配方法,可提高PIVAS 工作效率;3)可严格保证静脉用药品的质量,提高临床治疗效果。
