高效液相色谱法测定达原饮中槟榔生物碱的含量
2023-11-06张莹刘冰陈秀梅黄涛杨芳雨张博雄
张莹,刘冰,陈秀梅,黄涛,杨芳雨,张博雄
(襄阳职业技术学院医学院,湖北襄阳,441050)
0 引言
达原饮最早出自明代医家吴又可所著的《瘟疫论》[1],作为治疗“湿浊”的抗疫古方,具有“辟秽化浊、开达膜原的功效”[2,3],为我国新型冠状病毒感染诊疗方案中第三版至第七版中医治疗的推荐处方[4]。在临床治疗和药理学研究中效果甚佳[5-8]。达原饮药方原文记载为:“槟榔二钱、厚朴一钱、草果仁五分、知母一钱、芍药一钱、黄芩一钱、甘草五分。右用水二盅,煎八分,午后温服。”其中,槟榔为君药,厚朴和草果仁为臣药,知母、芍药和黄芩为佐药,甘草为使药。槟榔生物碱为君药槟榔中的主要有效成分,具有抗血栓的作用[9]。臣药厚朴的有效成分为厚朴酚与和厚朴酚,主要起抗炎抗氧化的药理作用[10];草果仁的主要成分为草果黄酮,具有抗氧化的作用[11]。目前,达原饮多以传统中药汤剂的形式在临床中使用。中药汤剂的制备是多环节的系统工程,中药饮片的产地、种植、采集、加工炮制、煎煮等环节均会影响汤剂的质量,而汤剂的质量对中医临床而言至关重要,它直接影响着临床治疗的疗效。目前对于达原饮中有效成分的质量控制较少,并且现有的研究主要针对芍药苷、黄芩苷和芒果苷等在传统C18色谱柱上容易保留的物质[12-14]。而对达原饮中君药槟榔中槟榔生物碱的质量控制未见报道。槟榔中的生物碱主要有槟榔碱、去甲基槟榔碱、槟榔次碱和去甲基槟榔次碱[9,15]。本研究利用高效液相色谱法,建立了采用离子色谱柱同时测定达原饮中4种槟榔生物碱含量的检测方法,并对其方法进行了验证,为达原饮全面的质量控制提供了理论支撑。
1 材料
达原饮的七味中药饮片,即槟榔、厚朴、草果仁、知母、芍药、黄芩、甘草均购于当地中药房(襄阳普天独活大药房);对照品去甲槟榔碱(批号:Q-075-180930,成都瑞芬思生物科技有限公司)、氢溴酸槟榔碱(批号:Q-043-191022,成都瑞芬思生物科技有限公司)、去甲槟榔次碱盐酸盐(批号:Q-047-170929,成都瑞芬思生物科技有限公司)和槟榔次碱(批号Q-164-190830,成都瑞芬思生物科技有限公司),以上对照品的纯度均大于98%。甲醇为色谱纯,水为纯净水,其他试剂纯度均为分析纯。
Agilent 1100高效液相色谱仪(四元泵、VWD检测器、自动进样器,美国安捷伦科技有限公司),BSA224S型分析天平(德国赛多利斯),TGL-16M 台式高速离心机(湖南湘仪实验室仪器开发有限公司),中药自动煎煮壶(九阳股份有限公司)。
2 方法
2.1 供试品溶液的配制
经典名方达原饮的出处为《瘟疫论》,原文记载:“槟榔二钱、厚朴一钱、草果仁五分、知母一钱、芍药一钱、黄芩一钱、甘草五分。右用水二盅,煎八分,午后温服。”据此确定中药达原饮的制备工艺:称取槟榔10 g、厚朴5 g、草果仁2.5 g、知母5 g、芍药5 g、黄芩5 g、甘草2.5 g,平行称取6份,分别加入300 mL纯净水浸泡60 min;头煎,使用武火煎煮10 min待溶液沸腾后,转文火慢煎20 min;用真空过滤器进行过滤,收集滤液;将滤渣进行二次煎煮,加入100 mL纯净水,使用武火煎煮10 min待溶液沸腾后,转文火慢煎10 min;用真空过滤器进行过滤,收集滤液,将两次煎煮滤液合并混匀,定容至400 mL,放冷,使用0.22 μm微孔滤膜过滤,作为供试品溶液待测。
2.2 对照品溶液的配制
精密量取去甲槟榔碱、槟榔碱、去甲槟榔次碱和槟榔次碱各5.00 mg,分别置于10 mL容量瓶中,用纯甲醇溶解并定容至刻度,作为单个对照品溶液待用。精密吸取上述四种单个对照品溶液各1 mL,置于10 mL容量瓶中,用纯甲醇溶解并定容至刻度,作为槟榔生物碱混合对照品溶液待用。
2.3 色谱条件
色谱柱:Venusil SCX 色谱柱(4.6 mm×250 mm,5 μm,300 Å,天津博纳艾杰尔科技有限公司);流动相:甲醇:0.2%磷酸(氨水调节pH值至3.8)=60:40;检测波长:210 nm;柱温:30℃;流速:1.0 mL·min-1。
3 结果
3.1 HPLC图谱
槟榔生物碱混合对照品溶液(A)和达原饮供试品溶液(B)的HPLC图谱如图1。
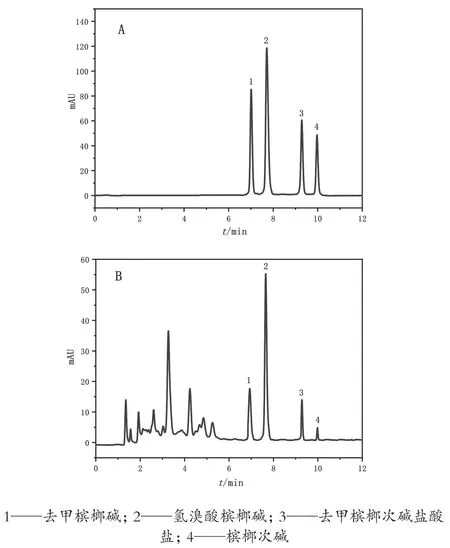
图1 槟榔生物碱混合对照品(A)和达原饮供试品溶液(B)的HPLC图谱
从图1中可以看出,在此测试条件下,槟榔生物碱的4种对照品完全基线分离,分离度良好,各对照品峰型基本对称,分离时间较短,并且在供试品中与其他组分无干扰。
3.2 线性关系的考察
取按2.2制备的槟榔生物碱混合对照品溶液2.0 mL、4.0 mL、6.0 mL、8.0 mL和10.0 mL置于20 mL容量瓶中,用50%甲醇定容至刻度,配制一系列质量浓度的混合对照品,按照2.3色谱条件依次进样,记录色谱峰面积。以色谱峰面积为纵坐标(y),对照品浓度为横坐标(x)分别绘制四种槟榔生物碱的标准曲线,拟合得到线性回归方程。线性回归方程见表1。从表1中可以看出,4种槟榔生物碱各自的浓度范围内,浓度与峰面积的线性关系良好。

表1 4种槟榔生物碱的回归方程、相关系数和线性范围
3.3 检出限与定量限
将按2.2项下配制的槟榔生物碱混合对照品用50%的甲醇溶液进行逐级稀释定容,按照2.3项下的色谱条件进行进样检测。信噪比(S/N)为3:1时,混合对照品溶液浓度为本检测方法的检出限(LOD);信噪比(S/N)为10:1时,混合对照品溶液浓度为本检测方法的定量限(LOQ),本方法的LOD和LOQ值见表1。
3.4 精密度试验
取按2.2项配制的槟榔生物碱混合对照品,按照2.3项下的色谱条件,连续进样6次,记录峰面积,分别计算四种槟榔生物碱对照品6次峰面积的相对标准偏差(RSD)(n=6)值。去甲槟榔碱、槟榔碱、去甲槟榔次碱和槟榔次碱的RSD值分别为1.21%、1.52%、1.43%和1.32%,此结果表明仪器精密度良好。
3.5 稳定性试验
取2.1项下制备的同一份供试品溶液,在0、4h、8h,16h和24 h按照2.3项下的色谱条件进样,分别记录四种槟榔生物碱的峰面积和保留时间。n=6时,去甲槟榔碱、槟榔碱、去甲槟榔次碱和槟榔次碱峰面积的RSD值分别为1.12%、1.19%、1.30%和1.23%;保留时间的RSD值分别为0.91%、0.87%、0.91%和0.94%。结果表明在24 h内供试品的稳定性较好。
3.6 重复性试验
取按2.1项制备的6份供试品溶液,分别按照2.3项下的色谱条件进样,记录四种槟榔生物碱的峰面积和保留时间。n=6时,去甲槟榔碱、槟榔碱、去甲槟榔次碱和槟榔次碱峰面积的RSD值分别为1.42%、1.32%、1.41%和1.34%;保留时间的RSD值分别为0.81%、0.80%、0.87%和0.90%。结果表明本检测方法的重复性较好。
3.7 加标回收率试验
精密移取按2.1项制备的同一份达原饮药液供试品5.0 mL共9份,每3份为一组,每组按照供试品中槟榔生物碱含量的80%、100%和120%加入对照品溶液,稀释定容,按2.3项下的色谱条件进样。加标回收率结果见表2。从表2中可以看出,达原饮中去甲槟榔碱、槟榔碱、去甲槟榔次碱和槟榔次碱的平均加标回收率分别为100.41%、101.01%、102.11%和98.37%,RSD值分别为1.91%、1.25%、1.04%和1.18%,RSD值均小于2%。此加标回收率试验结果表明该分析检测方法准确度较好,可用于达原饮中4种槟榔生物碱含量的测定。
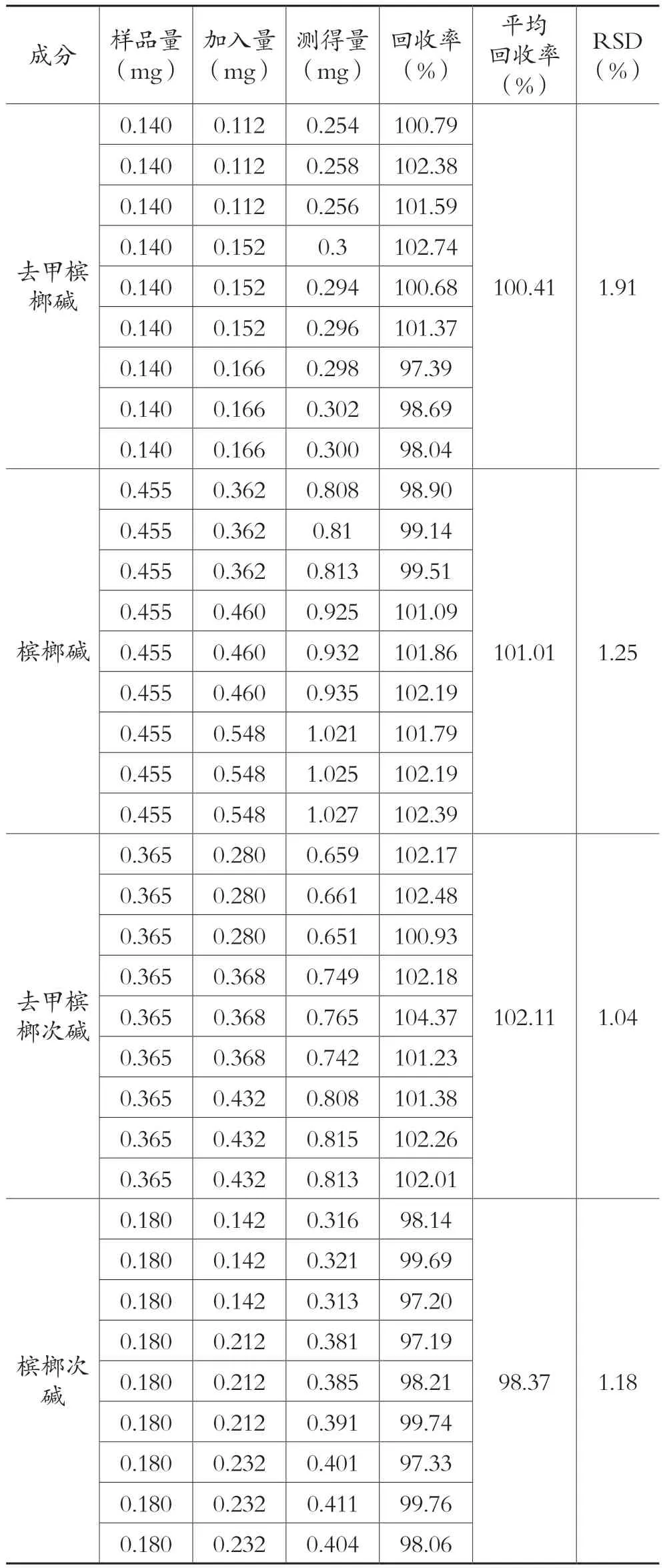
表2 达原饮中4种槟榔生物碱的加标回收率(n=9)
3.8 含量测定
将按2.1制备的达原饮药液按照2.3项下的色谱条件进行检测,测得达原饮药液中去甲槟榔碱、槟榔碱、去甲槟榔次碱和槟榔次碱的含量分别为0.014 mg·mL-1、0.046 mg·mL-1、0.036 mg·mL-1和0.018 mg·mL-1。
4 结论
槟榔为中药抗疫名方达原饮中的君药,其中的槟榔生物碱是达原饮发挥药理作用的主要成分之一,因此建立达原饮中槟榔生物碱的检测方法以对其质量进行控制十分必要。本文首次建立了达原饮中4种槟榔生物碱含量测定方法,采用高效液相色谱法对达原饮中4种槟榔生物碱的含量进行测定。色谱条件为Venusil SCX 色谱柱(4.6 mm×250 mm,5 μm,300 Å);流动相:甲醇:0.2%磷酸(氨水调节pH值至3.8)=60:40;检测波长:210 nm;柱温:30℃;流速:1.0 mL·min-1。经过方法学验证,结果表明,在49.6~250.5 μg·mL-1浓度范围内线性较好,稳定性和重复性良好,准确度较高,达原饮药液中去甲槟榔碱、槟榔碱、去甲槟榔次碱和槟榔次碱的含量分别为0.014 mg·mL-1、0.046 mg·mL-1、0.036 mg·mL-1和0.018 mg·mL-1。该方法为达原饮药液的质量控制提供了依据。
