OSAHS 对小气道功能影响的研究
2023-11-06顾东升张志存张耀庭刘婷黄春梅
顾东升 张志存 张耀庭 刘婷 黄春梅
睡眠是一种复杂的状态,相比清醒状态,睡眠状态下人体诸多机能发生改变。睡眠期间,呼吸的调控发生改变,呼吸的动力学也发生改变——上气道阻力增加,功能残气量减少;肺容量的减少使上气道更容易阻塞、吸气流量减少,而这些现象的确切机制尚不明确[1,2]。
睡眠呼吸暂停低通气综合征(Obstructive Sleep Apnea Hypopnea Syndrome, OSAHS)是最常见的睡眠障碍,已经受到广泛研究[3,4]。可能导致OSAHS 的关键生理特征包括:咽部解剖结构塌陷;通气控制系统增益(环路增益);上气道响应呼吸机驱动增加而扩张/变硬的能力;唤醒阈值[3]。尽管大气道和小气道属于肺的同一解剖结构,但现有对OSAHS 的病理生理学研究主要集中于上(大)气道的功能。本研究关注OSAHS 患者小气道的功能,并与健康对照组进行了比较。
资料与方法
1 一般资料
本研究共纳入了50 例轻度至重度OSAHS 患者,包括33 例男性和17 例女性,平均年龄52.1 岁,无合并症;另纳入20 例健康对照,包括14 例男性和6 例女性,平均年龄49.5 岁,见表1。OSAHS 组和对照组均于2019 年7 月~2020 年7 月期间因睡眠相关症状在我科就诊。
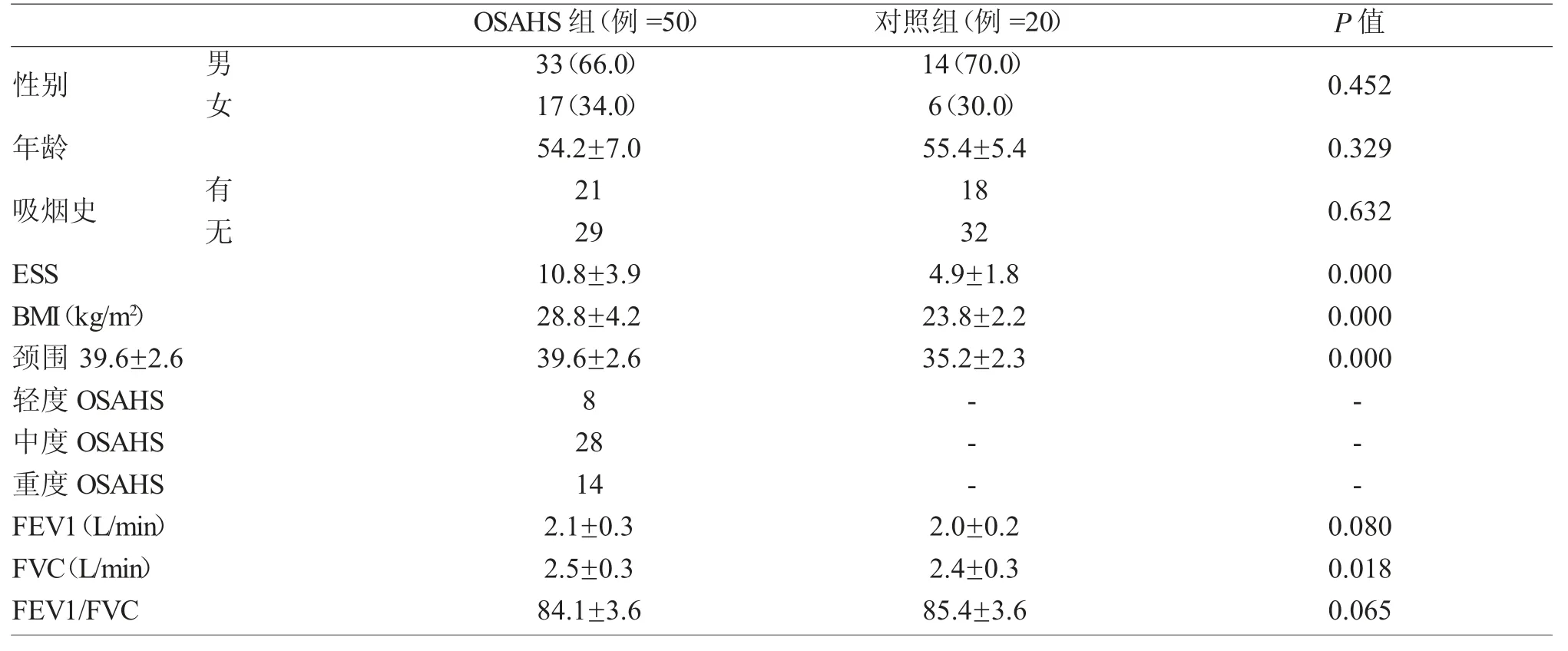
表1 OSAHS 组与对照组特征
具有以下任何一项的受试者被排除:①重度肥胖(BMI>40kg/m2);②吸烟指数>300 年支;③同时患有其它肺部疾病(例如慢性阻塞性肺病、哮喘、间质性肺病、活动性肺结核);④患有其他睡眠相关疾病的患者;⑤有临床上显著的肾、心血管、神经、内分泌、免疫、精神、胃肠道、肝脏或血液学异常的患者;⑥孕妇。
2 方法
详细询问包括睡眠障碍症状在内的病史并进行体格检查,使用Epworth 嗜睡量表(Epworth Sleepiness Scale, ESS)评价白天嗜睡情况,测量体重(kg)和身高(m)并计算BMI(kg/m2),并在环甲软骨高度测量颈围(cm)。
OSAHS 组和对照组受试者都接受了多导睡眠监测(Polysomnography, PSG),记录包括以下参数:脑电图、眼电图、双侧颏下肌和胫骨前肌肌电图、心电图。麦克风应放置在气管上方或颈部侧面,用口鼻热敏电阻和压力传感器检测气流,用手指脉搏血氧计检测氧合血红蛋白饱和度,用胸腹特殊松紧带记录胸腹壁的运动和身体位置,以评价呼吸用力。呼吸暂停低通气指数(Apnea Hypopnea Index, AHI)≥5 即可诊断为OSAHS,其严重程度分为:轻度,5≤AHI<15;中度,15≤AHI<30;重度,AHI≥30。
OSAHS 组和对照组均以坐姿和仰卧位做了肺活量测定。
3 小气道功能评估
使用氦氧流量-容积法评估小气道功能。受试者取坐位,并按指示呼吸室内空气或80%He 加20%O2的混合气体,同时测最大呼气流量-容积曲线。在记录呼吸He-O2混合气体时的流量-容积曲线前,受试者应至少3 次极限量吸入He-O2混合气。呼吸室内空气和He-O2混合气体时的两条流量-容积曲线以肺总量(Total Lung Capacity, TLC)为基准相叠加。若两者的用力肺活量(Forced Vital Capacity, FVC)相差小于5%,即可接受(我们的数据中,两者平均相差<3%)。如果两条曲线的FVC 明显不同,则以残气量(Residual Volume, RV)为基准将两条曲线叠加[5,6]。两条曲线的流量值变得相同时的容量值记为等流量容积(Volume of Equal Flows,VisoV)。计算了两条曲线的VisoV 和50%最大呼气流量(Vmax50)的流量差(ΔVmax50),以此代表小气道的功能[5]。
参照Dosman 及其同事的方法,VisoV 表示为其相比FVC 的百分比。用如下公式计算ΔVmax50:
表示为其相比呼吸空气时V'max50 的百分比[6]。
4 统计学分析
对受试者的特征进行了描述性统计分析。使用单样本Kolmogorov-Smirnov 检验和图形检查评估了连续变量分布的正态性。连续变量表示为平均值±标准差(SD)或中位数和25、75 百分位数。适用时,以独立样本T 检验和独立Mann-Whitney U 检验评估连续变量之间的差异。使用Fisher 精确检验评估分类变量之间的差异。使用线性回归分析评估OSAHS 与VisoV 的关联,并针对BMI 做了调整。Wilcoxon 配对符号秩检验用于坐位和仰卧位的比较。对于所有测试,P<0.01 被认为具有统计学意义。所有统计分析均使用SPSS 26.0(IBM Corporation,Illinois, US)和Stata 13.0(StataCorp, College Station,TX, US)完成。
结果
患者和对照的人口统计数据、吸烟习惯、肺功能测试(Pulmonary Function Tests,PFTs)和睡眠相关数据详见表1。OSAHS 组和对照组的BMI、ESS 和颈围有显著差异(P<0.05)。
小气道功能数据详见表2。与对照组的VisoV(5.6±1.7)相比,OSAHS 组患者的VisoV(19.1±3.9)显著升高(P=0.000);OSAHS 与较高的VisoV 显著相关,这种关联与BMI 无关。OSAHS 患者中,VisoV与ESS 或颈围无显著关联。OSAHS 组患者ΔVmax 50%(27.1±8.0)较对照组的ΔVmax50%(37.4±2.0)显著降低(P=0.000)。坐位状态下,OSAHS 组和对照组FVC 均值、1 秒用力呼气量(Forced Expiratory Volume in 1s, FEV1)、FEV1/FVC、25-75%的中段最大呼气量(Maximal Midexpiratory Flow, MMEF25-75)、50%的中段最大呼气量(Maximal Midexpiratory Flow at 50%, MEF50)无显著差异。而在仰卧位,OSAHS 患者的上述肺功能指标相比坐位显著下降。

表2 OSAHS 组与对照组坐位小气道功能参数比较
讨论
小气道是外周膜性细支气管,直径小于2mm。它们构成了非常大的表面积,其功能和临床特性难以评估,治疗手段也难以企及[7,8]。本研究的主要发现是OSAHS 患者的小气道功能发生改变,表现为基线肺活量正常的情况下VisoV 增加和ΔVmax50%的下降;OSAHS 组的坐位与仰卧位相关小气道的参数差异明显,而对照组坐位与卧位无明显差异。
OSAHS 的发病有多方面的原因,上呼吸道及其肌肉组织的解剖学和功能变化可导致睡眠期间上呼吸道部分或完全地反复阻塞。解剖学变化可导致上气道直径减小,而功能性变化导致气道塌陷,更易发生阻塞,这些变化可能相互作用,即结构变化可能影响功能性变化,反之亦然[9]。众所周知,睡眠期间的呼吸模式会随睡眠阶段发生显著变化[10]。此外,还有报导称OSAHS 患者的肺容量在NREM 睡眠期间持续变化,这可能导致上气道被动塌陷[11]。然而,在睡眠期间,最常观察到的是功能残气量(Functional residual capacity, FRC)或呼气末肺容积(End Expiratory Lung Volume, EELV)趋于降低,即使它可能会有波动。以低肺容量呼吸时,肺的弹性恢复力(弹性反冲力)会降低,肺实质对气道施加的径向牵引力也会降低,以保持气道畅通、降低气流阻力[12]。这种情况也发生在睡眠正常的受试者中,并且在睡眠障碍患者中异常增强[1]。
此外,还有研究表明,对于肥胖的OSAHS 患者,肺容量的减小还间接导致上气道狭窄和阻塞[13]。Jordan 等[14]的研究表明,OSAHS 患者中,颏舌肌有时无法稳定住呼吸,而这可能与肺容量减少有关。因此,大多数有关OSAHS 的病理生理学研究都集中于上气道塌陷。而我们的研究发现,OSAHS 患者小气道的功能也发生了改变。我们推测这可能是由于低肺容量时气道压力的突然变化引起了小气道的打开和关闭。众所周知,在上气道阻塞时,气道压力会增加以重新打开塌陷部位并启动吸气气流。完成吸气后,气道压力会突然大幅降低。这种气道压力的变化会传递至整个呼吸系统,并可能导致膜状小气道的塌陷和扑动。与之一致的是,一些动物研究表明,低肺容量下的通气会导致小气道异常连续打开和关闭;这种周期性的连续关闭和打开,为终末细支气管和肺泡区域的炎症和氧化应激创造了条件,这可能导致肺实质的破坏[15]。
2002 年,D’Angelo 等[16]报导称,小容量通气会导致正常家兔的外周气道损伤并增加气道阻力,这可能是外周气道的反复打开和关闭所导致的。此外,Yalcin 等[17]在气道重新开放的体外模型中观察到显著的上皮细胞损伤。此外,Zerah-Lancner 等[18]对170 例患者的睡眠研究发现,随着OSAHS 严重程度的增加,V50 和V25 处的FEV1/FVC 比率显著降低。Baydur 等[19]发现COPD 和OSAHS 患者的呼气流量均受限,但他们的结果无法区分这两个队列。Abdeyrim 等[20]和Cai 等[21]的结果也也印证了我们的结果,他们使用脉冲振荡技术表明肥胖OSAS 患者的外周气道阻力增加。此外,Abdeyrim 等[21]的研究表明,5Hz 处的阻抗与外周气道阻力和FRC 降低相关。此外,Avraam 等[22]报导称,仰卧位FVC 降低和体重增加可能导致OSAHS 恶化。与这些研究一致,我们的结果显示,患者仰卧位的肺功能参数值与坐姿相比显著降低,见表3。这也支持我们的观点:低肺容量呼吸可能会对小气道功能产生负面影响。此外,Heinzer 等[23]的研究表明,在非快速眼动睡眠期间,肺容量增加可减少OSAHS 患者的睡眠障碍并改善睡眠结构。

表3 OSAHS 组坐位与仰卧位小气道功能参数比较
1974 年,Hutheon 等[24]引入了等流量容积测试作为检测小气道功能障碍的新方法。在VC 的最后10%至15%,呼吸He-O2和空气时的流速相同,这就是等流点的容积[25]。因为小气道中的气流是层流的,与气体密度无关,所以会发生这种等流量现象[26]。VisoV 表示为VC 的百分比,在正常不吸烟受试者中,以RV 为基准,VisoV 占VC 的10%至15%[26]。小气道半径减小会使层流发生在更高的肺容量(VisoV增加),提示小气道功能障碍[27]。
Despas 等[6]报导称,使用He-O2混合气可以在轻度哮喘患者中检测到外周气道阻塞的早期表现。此外,Dosman 等[5]的研究表明,使用Heliox 方法分析最大呼气流量动作,可检测到肺活量指数尚处于正常范围内的吸烟者的肺功能异常。该技术也被Siafakas 等[28]用于研究小气道在肢端肥大症中的功能改变。我们也使用该技术研究了小气道在非呼吸系统疾病(如炎症性肠病)中的功能改变,并取得了有趣的结果。与本研究的结果一致,他们发现仅VisoV 指数发生变化,而ΔVmax50 无显著改变,并认为ΔVmax50 不能作为早期检测小气道功能障碍的敏感指标[29]。
众所周知,肺部的小气道,即所谓的“安静区”[29,30],是一个难以企及的解剖区域,因此难以研究其功能。多种方法被提出用于研究肺的这一区域,包括一些复杂和侵入性的方法。然而,尚无得到广泛认可的方法来研究小气道功能[31]。一些研究质疑密度依赖性测试的可变性,以及用其检测小气道狭窄的有效性[32],然而大多数研究显示这些测试与小气道功能密切相关[33]。虽然患者与对照的BMI 存在显著差异,但回归分析显示OSAHS 患者的VisoV'显著高于对照,且这种关联不依赖于BMI。类似地,Abdeyrim 等[21]报道称,OSAHS 患者的FRC 和呼气储备量减少与BMI 无关。
我们的研究受限于非常小的样本量。仅纳入了50 例OSAHS 患者和20 例对照。不过,VisoV 结果可明确地将患者与对照组区分开来。最后,初步结果显示OSAHS 患者在使用CPAP 治疗后小气道功能参数有改善的趋势。因此,未来有必要研究针对OSAHS 的治疗对小气道功能的影响。
结论
本研究的主要发现是OSAHS 患者的小气道功能发生改变,OSAHS 降低了患者的小气道功能。OSAHS 对小气道功能的影响可能是由于肺容量的减少、小气道反复打开和关闭、以及随后的炎症和氧化应激[34]。然而,尚需要更大规模的研究来验证我们的结果。
