向日葵非倍半萜成分及生物活性研究进展
2023-10-30杨舜伊袁纯红
杨舜伊,袁纯红
(昆明工业职业技术学院,昆明 650302)
向日葵(Helianthus annuusL.)为菊科(Compositae)向日葵属(Helianthus)一年生草本植物,又名丈菊,原产于南美洲,欧洲、北美洲、中国都有分布。向日葵种子含油量很高,为半干性油,味香可口,供食用。向日葵花穗、种子皮壳及茎秆可作饲料及工业原料,花穗也可供药用[1,2]。1931 年向日葵被报道具有化感作用,随后科研工作者从化学组成角度对向日葵进行了广泛的研究。研究表明,向日葵植物中主要含有倍半萜、二萜、三萜、木脂素、黄酮、苯丙素、甾体等生物活性成分,其生物活性主要为抗菌、抗肿瘤、抗氧化、化感作用等[3-7]。由于向日葵化学成分复杂,而且具有多种生物活性,因而引起国内外学者对其化学成分和生物活性的较大关注[3-7]。本研究对向日葵的非倍半萜成分及其生物活性进行系统综述,以便中国科研工作者对向日葵进行更加深入的研究,充分利用和开发丰富的向日葵资源。
1 向日葵非倍半萜成分
1.1 二萜类化合物
从向日葵叶中分离得到14 个二萜类化合物,主要有trachylobane 型和贝壳杉烷型2 种结构类型,大多数为二萜酸,菊科植物中二萜酸的存在是非常特殊的。Pyrek[8,9]、Mitscher 等[10]从向日葵中分离得到2 个二萜酸化合物和2 个非常稀有的天然二萜酯,分别是trachyloban-19-oic acid(1)、(-)-kaur-16-en-19-oic acid(2)、thujanol ester of ent-kaur-16-en-19-oic acid(3)和thujanol ester ent-trachyloban-19-oic acid(4)。Melek 等[11]从向日葵叶中分离得到3个二萜化合物,分别是grandifloric acid(5)、ciliaric acid(6)和17-hydroxy-ent-isokaur-15(16)-en-19-oic acid(7)。Alfatafta 等[12]从向日葵的叶中分离得到ent-kaur-16-en-19-oic acid(8)、grandifloric acid(9)、grandifloric acid angelate(10)、15α-hydroxytrachyloban-19-oic acid(11)、7-oxo-trachyloban-15α,l9-diol(12)。Morris 等[13]从向日葵中分离得到2 个二萜醇,分别是ent-kauran-16α-ol(13)和ent-atisan-16α-ol(14)。化合物(1)至(14)的结构见图1。

图1 二萜类化合物结构
1.2 三萜及其苷类化合物
有关向日葵中三萜及其苷类化合物报道的较少,Ukiya 等[14,15]从向日葵花粉和花瓣中分离得到12 个三萜及其苷类,主要包含甘遂烷型和齐墩果烷型2 种类型。其中6 个为C-3,C-4 位键断开重排的甘遂烷型三萜,分别是sunpollenol(15)、(24S)-24,25-epoxysunpollenol(16)、(24R)-24,25-epoxysunpollenol(17)、(23E)-23-dehydro- 25-hydroxysunpollenol(18)、(24S)-24,25-dihydroxysunpollenol(19)、(24R)-24,25- dihydroxysunpollenol(20);另外6 个为齐墩果烷型三萜皂苷,分别命名为helianthoside 1(21)、helianthoside 2(22)、helianthoside 3(23)、helianthoside 4(24)、helianthoside 5(25)和helianthoside B(26)。化合物(15)至(26)的结构见图2。
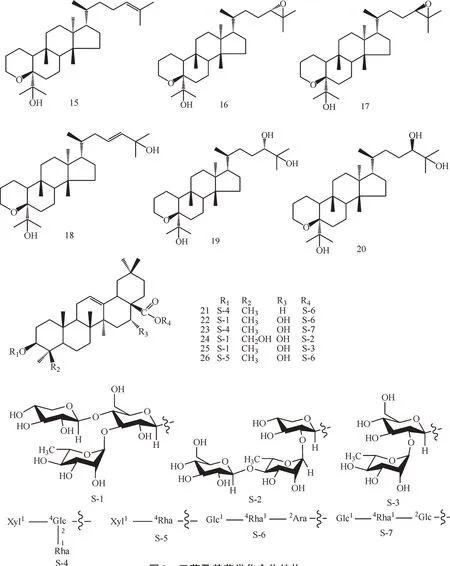
图2 三萜及其苷类化合物结构
1.3 其他萜类化合物
Macías 等[16]从向日葵的叶中分离得到倍半萜二聚体化合物helivypolide G(27)。Torres 等[17]从向日葵的叶中分离得到4 个新骨架二萜-倍半萜聚合物,由1 个倍半萜内酯和1 个贝壳杉烷型二萜酸聚合而成,倍半萜部分碳谱和氢谱数据与已知的倍半萜内酯helivypolide L 非常相似,二萜部分碳谱和氢谱数据与已知的16α-hydroxy-ent-kauran- 19-oic acid非常相似,分别命名为helikaurolides A 至D(28 至31)。化合物(27)至(31)的结构见图3。
1.4 木脂素类化合物
Macías 等[18]从向日葵的叶中分离得到10 个木脂素类化合物,报道了向日葵中的木脂素成分。分别命名为pinoresinol(32)、medioresinol(33)、syringaresinol(34)、buddlenol E(35)、lariciresinol(36)、7-hydroxylariciresinol(37)、tanegool(38)、neo-olivil(39)、dihydro-dehydrodiconiferyl alcohol(40)、l-(4-hydroxy-3-methoxyphenyl)-2-[4-(3- hydroxypropyl)-2-methoxyphenoxy]-propane-l,3-diol(41)。化合物(32)至(41)的结构见图4。
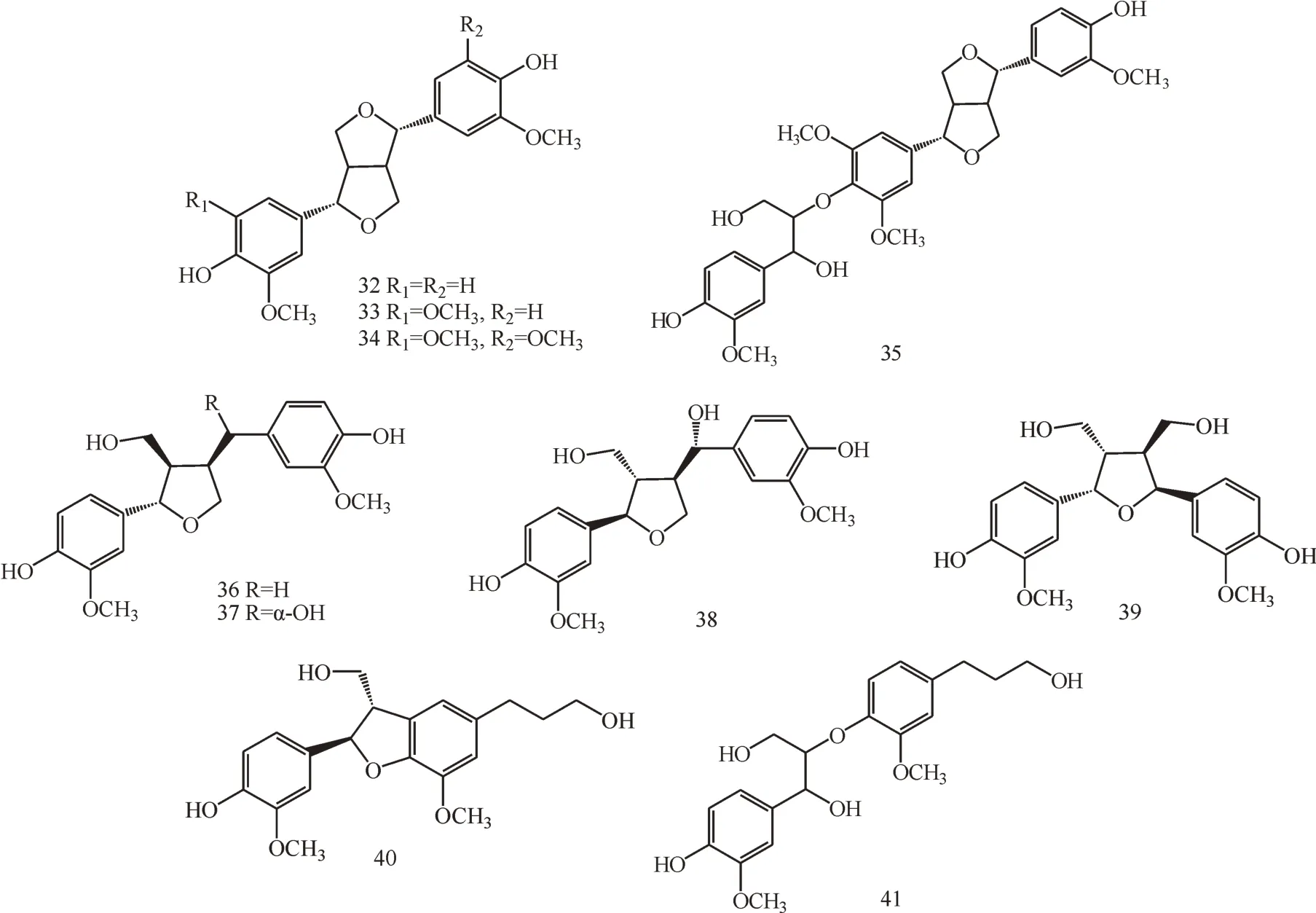
图4 木脂素类化合物结构
1.5 黄酮类化合物
向日葵中报道的黄酮类化合物较少,截至2022年,报道的黄酮类化合物共有8 个,其中包括黄酮醇、查尔酮和黄烷酮类型。Alfatafta 等[12]从向日葵的叶中分离得到2 个黄酮类化合物,分别为nevadensin(42)、5-hydroxy-4,6,4’-trimethoxyaurone(43)。Macías 等[19,20]从向日葵的叶中分离得到5 个黄酮类化合物,1 个黄酮醇tambuline(44)、1 个查尔酮kukulkanine B(45)、heliannone A(46)、2 个黄烷酮heliannones B-C(47 至48)。Amakura 等[21]从向日葵的叶中分离得到黄酮类化合物eriodictyol 5-O-β-Dglucoside(49)。化合物(42)至(49)的结构见图5。

图5 黄酮类化合物结构
1.6 苯丙素化合物
Macías 等[18]从向日葵的叶中分离得到3-(4-hydroxy-3,5-dimethoxyphenyl)-propan-1- ol(50)。Amakura 等[21]从向日葵的叶中分离得到8 个苯丙素类化合物,分别是β-D- apiofuranosyl-(1→6)-β-D-(4-O-caffeoyl) glucopyranoside(51)、caffeic acid(52)、methyl caffeoate(53)、chlorogenic acid(54)、4-O-caffeoylquinic acid(55)、3-O-caffeoylquinic acid(56)、methyl chlorogenate(57)、3,5-di-O-caffeoylquinic acid(58),化合物(50)至(58)的结构见图6。
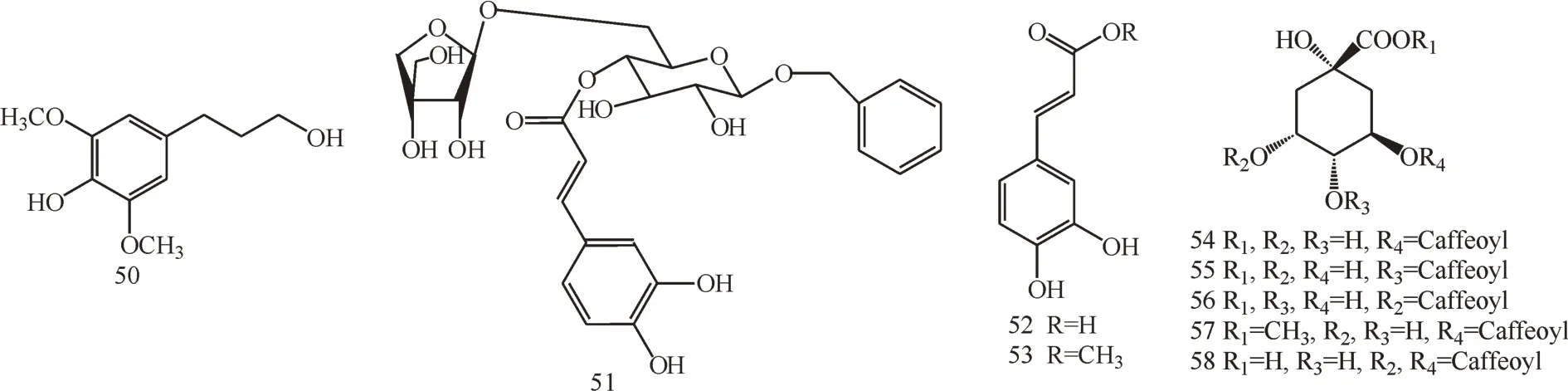
图6 苯丙素类化合物结构
1.7 其他化合物
除了以上类型化合物之外,Homberg 等[22]从向日葵种子油中分离得到6 个甾体类化合物,鉴定了其中的5 个,分别是△7-stigmastenol、△7-campestenol、△7,24(28)-stigmastenol、△7,24(25)-stigmastenol 和△7,9(11),24(28)-stigmastenol。Macías 等[19]从向日葵的叶中分离得到单萜内酯loliolide。Ohno 等[23]从向日葵种子中分离得到sundiversifolide。Ceccarini 等[24]从向日葵叶和花中共分离鉴定了69 种挥发分,主要成分是α-蒎烯、桧烯、柠檬烯、大根香叶烯、乙酸异龙脑酯、樟脑和β-蒎烯。单萜为挥发油的主要成分,其中α-蒎烯在花中占72.6%,在叶中占28.6%,向日葵叶和花中挥发分组成没有明显的区别。张玲玲等[25]对向日葵花盘挥发油成分进行气相色谱-质谱联用法(GC-MS)定性分析,共鉴定了29 种化学成分,其中萜类化合物较多,含量较高的成分为α-蒎烯、桧烯、β-蒎烯、白菖油萜、大根香叶烯、4-松油醇和柠檬烯。何昶毅等[26]应用水蒸气蒸馏法提取向日葵盘精油,利用气相色谱-质谱联用法(GCMS)分析其化学成分,共鉴定出49 种化学成分,占精油总量的91.16%,其中α-蒎烯、柠檬烯、α-蛇麻烯、反式-β-金合欢烯和莰烯为主要成分。
2 生物活性
2.1 抗菌活性
陈小强等[27]以向日葵茎髓为原料,制得3 种极性向日葵茎髓提取物,研究发现,3 种极性向日葵茎髓提取物对4 种受试菌都具有抑菌活性,其中乙酸乙酯萃取部位对金黄色葡萄球菌和大肠杆菌的最低抑菌质量浓度(MIC)均为0.78 g/L,半数抑制质量浓度(IC50)分别为(1.11±0.01)g/L 和(1.59±0.03)g/L。Al-shukaili等[28]报道向日葵的花和种子提取物对革兰氏阳性菌和阴性菌均有明显的抑菌作用,其中花的提取物中水相部分活性较强,而丁醇部分活性较弱;种子的提取物中水相部分活性较强,而甲醇部分活性较弱。
2.2 抗肿瘤活性
李梅等[29]报道向日葵茎芯煎剂对小鼠移植性肿瘤有明显抑制作用。苏晓琴等[5]在筛选植物性食物防癌中发现向日葵籽有良好的防癌作用。
2.3 化感作用
Macías 等[18]对8 个木脂素和1 个苯丙素进行生物活性测定,研究发现,pinoresinol(32)、lariciresinol(36)、dihydro-dehydrodiconiferyl alcohol(40)和3-(4-hydroxy-3,5-dimethoxyphenyl)-propan-1-ol(50)能够抑制水芹、番茄和小麦萌芽及芽的生长,其中dihydro-dehydrodiconiferyl alcohol(40)活性最强。
2.4 抗氧化活性
钟姣姣等[30]对向日葵中绿原酸提取物采用邻二氮菲-Fe2+氧化法进行抗氧化性测定,结果表明,向日葵叶中绿原酸提取液对羟基的清除率随质量浓度的增加而增大,清除率最大为80.9%,比维生素C的抗氧化能力强。何昶毅等[26]研究发现,向日葵盘精油具有一定的体外抗氧化活性,其清除DPPH 自由基、ABTS 自由基的半数有效浓度(EC50)分别为0.47、0.30 g/L,明显高于阳性对照BHT 的半数有效浓度EC50(分别为8.21、6.16 mg/L)。索金玲等[31]对向日葵粗多糖进行体外抗氧化性试验,结果显示,当粗多糖浓度为5 mg/mL 时,对羟基自由基清除率为78.1%,对超氧阴离子抑制率可达82.0%,表明向日葵粗多糖具有一定的抗氧化能力。孟潇等[32]采用醇提取法制取向日葵提取液,提取液对羟基自由基和DPPH 自由基具有较好的清除效果,半数清除浓度EC50分别为0.495、7.400 g/L。
3 结论与展望
向日葵在中国种植广泛,资源丰富。然而,中国对向日葵的利用仅局限于食用价值,而对向日葵的研究主要集中在绿原酸、果胶和多糖的提取工艺及活性[33,34],对向日葵化学成分的研究较少。同时,已报道的生物活性研究主要集中在化感作用,其他活性研究较少,缺少构效关系研究。因此,有必要继续对向日葵进行系统的化学成分和生物活性研究,阐明其药效物质基础,为进一步开发利用向日葵资源提供科学依据。
