口腔黏膜溃疡损害出现短暂自愈的朗格汉斯细胞组织细胞增生症1例
2023-10-13张晓玲薛宁宁阮敏慧曾昕
张晓玲 薛宁宁 阮敏慧 曾昕
口腔疾病防治全国重点实验室 国家口腔医学中心 国家口腔疾病临床医学研究中心四川大学华西口腔医院口腔黏膜病科,成都 610041
朗格汉斯细胞组织细胞增生症(Langerhans cell histiocytosis,LCH)是一组骨髓来源的朗格汉斯细胞增殖聚集导致的疾病,为我国《第一批罕见病目录》所收录的疾病[1]。常见于儿童,也可发生于成年人。LCH 分为勒-雪病、汉-许-克病、嗜酸性肉芽肿、先天性自愈性朗格汉斯细胞组织细胞增生症4 种临床类型[2]。根据疾病受累的范围,又分为单系统性LCH 和多系统性LCH。LCH 的临床表现和预后根据受累的组织器官而不同,累及脾脏、肝脏、骨髓等器官的LCH 预后较差。约80%的LCH 病例中,皮肤黏膜损害是首发临床表现,也常是诊断的主要线索[3]。皮肤损害常表现为脂溢性皮炎、红斑、鳞状丘疹、斑块等[4]。口腔黏膜损害常表现为经久不愈的溃疡。本文报道1例口腔黏膜病损出现短暂自愈的儿童LCH。
1 病例报告
患儿,女,1 岁7 个月,2020 年8 月11 日因“腭部溃疡1 个月,发热5 d”就诊于四川大学华西口腔医院口腔黏膜病科。1个月前无明显诱因发现患儿腭部溃疡,伴口臭,患儿拒食、易哭闹。5 d前于外院输液后出现发热,体温39~40.3 ℃。患儿平素体质较好,近来睡眠差,大小便正常。既往有左外耳道狭窄史。家族史、过敏史无特殊。
专科检查:口腔黏膜检查,硬腭左侧可见形状不规则溃疡,直径约2.5 cm,被覆黄色假膜,周围黏膜充血肿胀;硬腭右侧可见一溃疡直径2 mm,周围黏膜充血发红(图1A)。乳牙无松动。体格检查:双侧颞部皮肤及双耳后皮肤可见大面积暗红色皮疹;双下肢、胸腹部和背部可见大面积密集浅红色皮疹,外阴黏膜及周围皮肤充血发红,被覆白色假膜(图1B~E)。
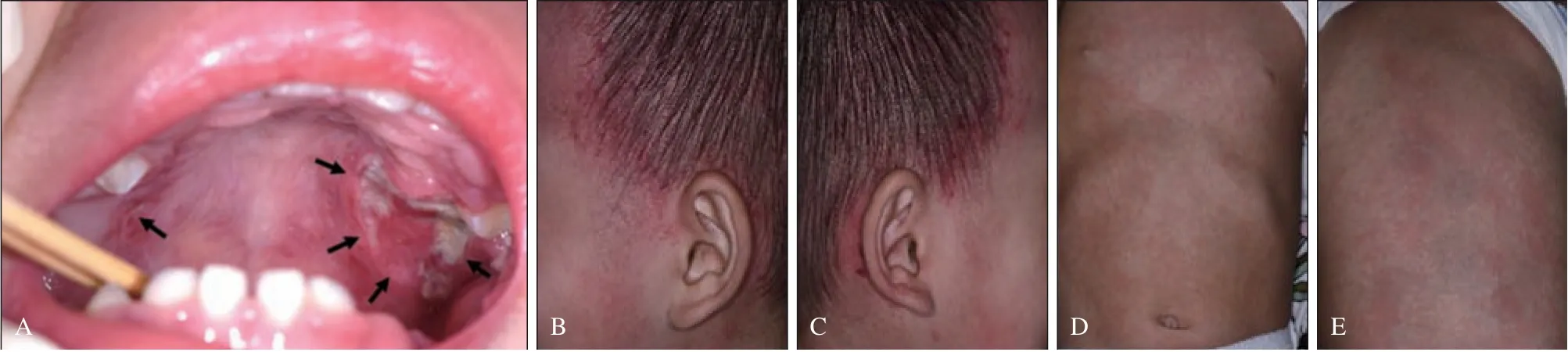
图1 初诊时患者硬腭及皮肤表现Fig 1 The appearance of hard palate and skin at the first visit
临床印象:腭部溃疡待诊(LCH待排)。
辅助检查:血常规检查示单核细胞百分比12%(正常参考值2.4%~10.6%),单核细胞绝对值1.01×109/L(正常参考值0.1×109~0.6×109/L),平均血红蛋白量23.1 pg(正常参考值23.8~29.8 pg);C-反应蛋白9.9 mg/L(正常参考值0~8 mg/L)。肝肾功能示:丙氨酸氨基转移酶133 IU/L(正常参考值<40 IU/L),门冬氨酸氨基转移酶103 IU/L(正常参考值<35 IU/L),谷氨酰转肽酶391 IU/L(正常参考值<45 IU/L)。头颅CT示:左侧上颌窦软组织肿块,周围骨质破坏,多系肿瘤性病变,颈部淋巴结增大。
初步处理:建议患儿于口腔颌面外科行腭部溃疡活检术,明确诊断;建议于四川大学华西医院耳鼻喉科会诊上颌窦病损。
等待活检阶段复诊。初诊后第9 天(2020 年8月20日),患儿未经任何治疗,硬腭溃疡病损愈合(图2A、B);双侧颞部、双耳后、胸腹部、背部皮疹消退(图2C~F);外阴黏膜及周围皮肤充血减轻,白色假膜消退。初诊后第18 天(2020 年8月29日),家长发现患儿腭部溃疡复发。初诊后第23 天(2020 年9 月3 日)检查,硬腭左侧可见4 处直径1~5 mm 的不规则溃疡,被覆黄色假膜,周围黏膜充血发红;硬腭右侧可见1 处5 mm×2 mm 的溃疡,周围黏膜充血发红(图3A、B)。皮疹未见复发。四川大学华西医院耳鼻喉科会诊头颅CT 检查结果后,建议行单光子发射计算机断层显像(single photon emission computed tomography,SPECT)全身骨显像,结果示左侧颌面部骨代谢轻度增高灶,考虑肿瘤累及;全身其余骨骼未见确切肿瘤骨转移征象。肝脏、胆囊、胰腺、脾脏彩超未见明显异常。
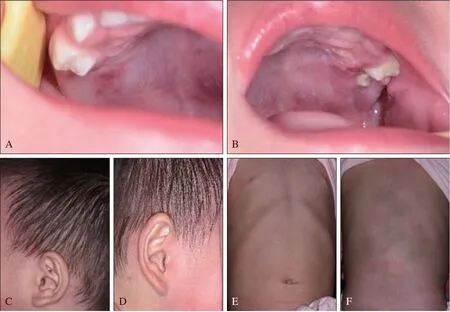
图2 第一次复诊(初诊后第9天)Fig 2 The first revisit (the 9th day after first visit)
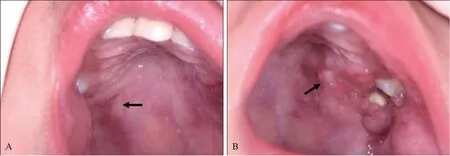
图3 第二次复诊(初诊后第23天)Fig 3 The second revisit (the 23rd day after first visit)
经多学科会诊,建议于四川大学华西医院耳鼻喉科入院行活检术。2020 年9 月12 日患儿全麻下行导航鼻内镜下左侧鼻窦开放+左侧上颌窦活检术。术后病理示淋巴细胞、嗜酸性粒细胞背景中见少量卵圆形细胞聚集。进一步免疫组织化学检查示,CD117(-),CD1a(+),S100(+),Lan‐gerin(+),CD3(-),CD30(-),类胰蛋白酶(Tryptase)(-),CD31(-),间变性淋巴瘤激酶(anaplastic lymphoma kinase,ALK)-1(-),CD-34(-),CD68(部分+),髓过氧化物酶(myelo‐peroxidase,MPO)(-),Ki-67(+,约25%)(图4)。Braf 基因突变分析:15 号外显子点突变(V-600E)。结合形态学、免疫组织化学和基因检测结果,病理诊断为:LCH。

图4 活检组织的苏木精-伊红染色和免疫组织化学染色 × 20Fig 4 Hematoxylin-eosin staining and immunohistochemical staining of biopsy tissue × 20
最终诊断:LCH。
治疗:患儿转入四川大学华西医院血液科进一步化疗,化疗药物包括强的松、长春花碱、巯嘌呤。
化疗阶段复诊:患儿化疗1个月后于口腔黏膜病科复诊,硬腭左侧可见1 处直径3 mm 的不规则溃疡(图5A);硬腭右侧溃疡已愈合(图5B)。家长述患儿腭部溃疡在化疗2个月后完全愈合,且无复发。化疗结束11 个月后于黏膜病科复诊,口内黏膜未见明显异常(图6A、B)。
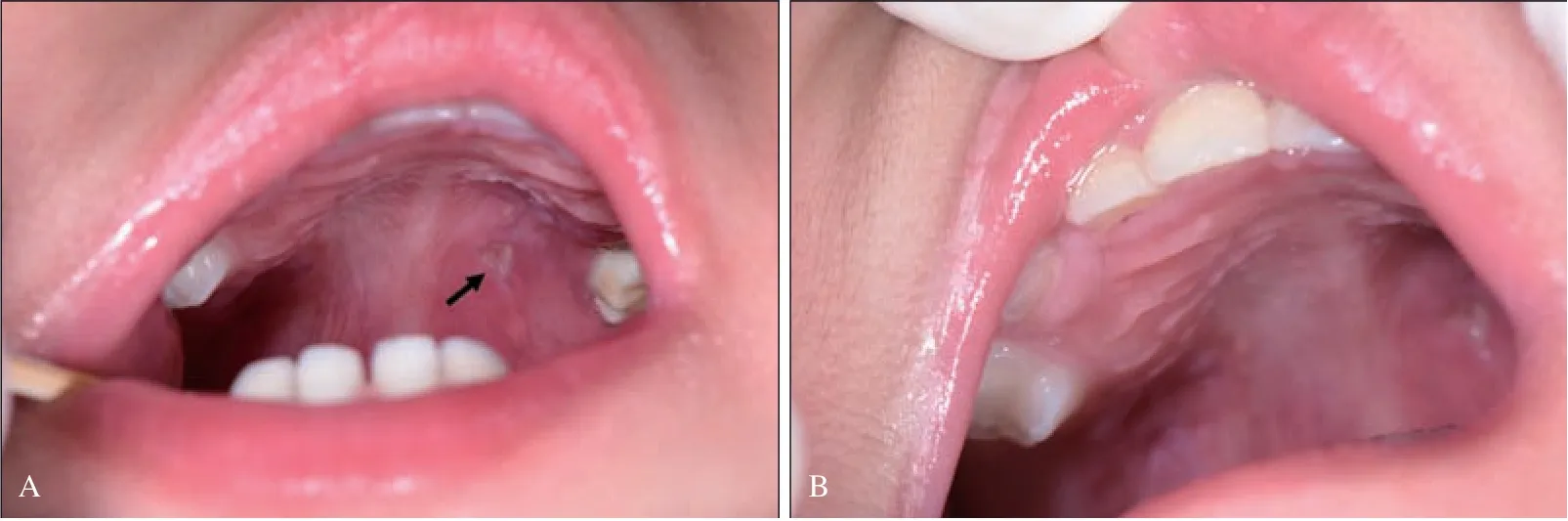
图5 化疗阶段(化疗1个月)Fig 5 Phase of chemotherapy (1 month of chemotherapy)
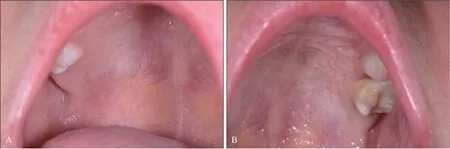
图6 化疗结束11个月后Fig 6 11 months after chemotherapy ends
2 讨论
LCH 是一种罕见病,多发于儿童,儿童的发病率为2/100 万~9/100 万[5]。LCH 发病机制尚不明确,主要有两种理论。1)肿瘤假说。超过一半的LCH 病例中发现BRAF-V600E 突变,V600E 是BRAF 基因最容易癌变的位点,BRAF 蛋白是MAPK信号通路的关键成分,可激活对细胞增殖至关重要的转录因子[6-7]。BRAF-V600E 突变的发现是了解LCH 发病机制的重大突破。部分LCH 中发现了MAP2K1、KRAS、TP53 基因突变[8]。2)免疫失调假说。该假说是基于增殖的组织细胞异质性,病变中异常组织细胞比例低,相关炎症细胞的浸润提出的[7]。有学者[8-9]猜想,其可能与母体IgG 通过胎盘转移到胎儿体内刺激胎儿朗格汉斯细胞合成细胞因子有关。除上述两种理论,还有学者[10-11]认为,人疱疹病毒6 型可能与LCH 中朗格汉斯细胞的增殖有关。根据2016 年组织细胞协会修订的组织细胞病分类,将LCH 定义为炎症性骨髓性肿瘤[12]。
LCH 临床表现复杂多样,可影响全身任何器官或系统。最容易受累的系统是骨骼(约占80%),其次是皮肤(33%)。LCH 骨骼受累主要表现为溶骨性损害;皮肤受累主要表现为脂溢性皮炎、红斑、鳞状丘疹、斑块等;淋巴结受累主要表现为淋巴结肿大,触诊质软或质硬,以颈部淋巴结肿大最为常见;肝脏受累时可见肝肿大和肝功能障碍;骨髓受累时可导致贫血、白细胞减少和/或血小板减少;垂体受累可引起中枢性尿崩症[3,13]。口腔黏膜病损可能是LCH 的首发表现,口腔黏膜受累主要表现为硬腭[14]、牙龈、颊黏膜溃疡性病变,溃疡病变周围充血发红,触痛明显,溃疡经久不愈[15-16]。硬腭、牙龈黏膜溃疡可以继发于颌骨溶骨性病变累及表面黏膜,也可独立存在不伴颌骨病变。Neves-Silva 等[15]曾报道1 例63 岁女性LCH 患者仅有硬腭黏膜及牙槽嵴黏膜溃疡,不伴其他组织器官病变,给予皮质类固醇激素局部治疗2年后病损仍未愈合,最终行外科手术切除口腔黏膜病损。
LCH 的诊断需要结合临床诊断和病理诊断,其中病理是诊断LCH 最重要的依据。当临床发现上述特征性改变,需进一步病灶活检以明确诊断,包括对皮肤黏膜病损、软组织肿块、溶骨性病损、肿大淋巴结、肝等病灶进行苏木精-伊红染色和免疫组织化学染色。通常优先选择溶骨性病变或皮肤病损活检[17]。其组织病理诊断标准如下:1)苏木精-伊红染色显示LCH 细胞与不同数量的嗜酸性粒细胞、淋巴细胞、巨噬细胞混杂在一起。LCH细胞胞浆呈嗜酸性,胞核呈圆形、卵圆形或咖啡豆样,可见核沟,核分裂象少见。2)免疫组织化学显示,CD1a 和CD207 阳性。除以上标准外,S100、CD68、花生凝集素也可作为辅助诊断LCH的标志物[18-19]。
本病例以腭部溃疡和皮肤损害为首发表现,最终确诊为LCH,诊断依据包括:1)硬腭溃疡,双侧耳颞部、胸腹部、背部、双下肢皮肤密集红色皮疹,外阴黏膜充血发红。2)影像学检查显示左侧上颌骨溶骨性变化、上颌窦软组织肿块,SPECT 显示左侧颌面部骨代谢轻度增高。3)左侧上颌窦软组织肿物活检术后病理显示淋巴细胞、嗜酸性粒细胞和卵圆形细胞聚集;进一步免疫组织化学显示CD1a(+)、S100(+)、CD68(+)、Ki-67(+,约25%)。
与既往病例口腔黏膜溃疡若未经治疗则经久难愈的特征不同,本病例患儿在检查过程中其腭部黏膜溃疡曾出现短暂自愈,间隔1周后复发。硬腭复发溃疡经化疗2个月后才完全愈合。其皮肤病损在未经任何治疗的情况下自行消退,且消退后未留痕迹且未复发。针对上述特征,笔者查阅文献进一步探究口腔黏膜溃疡病损短暂自愈和皮肤病损自愈的原因。
LCH 有一种亚型为先天性自愈性朗格汉斯细胞组织细胞增生症(congenital self-healing Langer‐hans cell histiocytosis,CSHLCH),最早于1973 年由Hashimoto 和 Pritzker 提出,也称为Hashimoto-Pritzker 病[20]。临床表现为患儿在出生时或新生儿期皮肤出现丘疹、水疱或结节等病损,少数可有血管瘤样改变,病损可在数周至数月内逐渐愈合[21-22]。该病具有良性、自限性的特点[21]。大部分CSHLCH 病损仅累及皮肤,近年来也有病损累及皮肤以外组织器官的CSHLCH 病例报道。如有3例累及皮肤和肺的CSHLCH。这3例患儿出生时出现皮肤病损,影像学检查发现肺部结节,经过皮肤病损活检最终确诊为CSHLCH,皮肤和肺部病损均在数月后自行愈合,且无病损复发[9,23-24]。Riz‐zoli 等[25]发现了1 例新生儿CSHLCH 除了在皮肤表现为水疱、脓疱、红斑外,该患儿舌部出现散在点状糜烂,皮肤及舌部病损在2 个月内完全消退,患儿5月龄随访时未见复发。CSHLCH通常在出生时或新生儿期出现,但也有少数在新生儿期后发病的CSHLCH 报道,并将其称为晚发型CSH‐LCH[26]。Nakahigashi 等[26]曾报道1 例晚发型CSH‐LCH 在8 岁时发病,表现为面部和上肢皮肤红棕色丘疹,无其他组织器官受累,经皮肤病损组织活检发现真皮中弥漫的单核细胞浸润,免疫组织化学显示CD1a、S-100 阳性。皮损在数月内完全消退,在10 个月的随访中没有任何复发和全身受累的情况。在一项对126 例CSHLCH 病例研究分析中,复发率约10%(13/126),所有病例均在1年内复发。复发病例中约有31%(4/13)的死亡率,即总死亡率3%(4/126)[27]。由于长期随访数据的不足,CSHLCH 实际复发率和死亡率可能高于原文数据。Hatakeyama等[28]曾报道1例仅有皮肤损害的CSHLCH 皮损完全消退2 个月后发生胸腺LCH,表现为发热、咳嗽、左侧锁骨上区肿胀,X线显示纵隔增大,CT 显示胸腺增大伴有点状钙化,经锁骨上肿块活检确诊,行化疗2个月后纵隔肿块明显消退,2 年后随访患者无复发。综上,可见CSHLCH 临床表现复杂,即使CSHLCH 有自限性,仍需长期随访。本病例并非出生时或新生儿期发病,皮肤病损完全自愈无复发,口腔黏膜溃疡病损仅出现短暂(仅9 d)自愈,且出现上颌骨破坏,与上述已报道CSHLCH 病例相比显著不同,故不能确诊为CSHLCH。而其口腔黏膜溃疡的短暂愈合和皮损的完全消退现象有待进一步探究。
目前LCH 自愈的机制尚不明确,有学者[22,29]认为在免疫系统的调节作用下,组织细胞发生退变而使病损自愈。此外,有研究[30]表明,表达BRAF-V600E 的人黑色素细胞痣表现出衰老的特征,BRAF-V600E 表达可诱导人黑色素细胞进入细胞周期阻滞,这表明癌基因诱导的衰老是一种生理保护过程。因此有学者[31]提出,BRAF-V600E突变诱导的细胞衰老可能导致CSHLCH病损自愈。
本例LCH腭黏膜溃疡短暂自愈后又出现复发,此前尚未有类似的病例报道,可能导致将其口腔病损误诊为小儿常见的溃疡性疾病(如复发性阿弗他溃疡、创伤性溃疡等)或病毒感染性疾病(如疱疹性口炎、手足口病等)。提示临床上要关注LCH这一新发现的现象,避免漏诊和误诊。
综上,对于婴幼儿疑为LCH 导致的口腔黏膜溃疡,即使出现自愈,也应密切观察,酌情根据溃疡复发情况和骨及其他器官损害情况制定进一步检查和治疗方案。
利益冲突声明:作者声明本文无利益冲突。
