用抗坏血酸+琥珀酸浸出废三元锂电池中的镍锂
2023-10-10杨鹏飞陈燕萌张秋连蓝峻峰叶有明谢雪珍
杨鹏飞,陈燕萌,张秋连,蓝峻峰,曾 军,叶有明,谢雪珍
(广西科技师范学院 食品与生化工程学院,广西 来宾 546100)
目前,三元废锂电池的回收技术主要有火法、湿法和生物冶金法。采用火法[6-7]工艺易产生二氧化碳、一氧化碳、二氧化硫、挥发性有机化合物等,需大量能源和气体清洁系统,成本较高;生物冶金法是在生物浸出过程中,用天然存在的微生物代谢产物从废锂电池中提取有价金属[8],但目前该技术仍处于基础研发阶段、动力学反应缓慢且菌种不易培养[9]。湿法工艺包括无机酸浸出法[10-12]、有机酸浸出法、氨浸出法等。其中,无机酸浸出法的金属浸出率可达98%以上,但该法易腐蚀设备,产生难处理强酸性废液[13],且具有强腐蚀性的无机酸还易产生酸雾,污染环境,危害人体健康;氨浸出法具有绿色环保等优点,但金属浸出率不高[14]。因此,近年来,对乙酸[15]、枸橼酸[16-17]等天然有机酸浸出体系回收三元废锂电池中的有价金属逐渐成为研究热点。
抗坏血酸是一种具有烯醇式己糖内酯立体结构的酸性己糖衍生物,结构中2个相邻烯醇式羟基极易解离而释放出H+,故抗坏血酸虽不含自由羧基,但仍具有有机酸的性质[18],也因易脱氢,稳定性较弱而具有较强的还原性。琥珀酸因含有2个羧基(—COOH)和2个亚甲基(—CH2—)相连结构具有良好的稳定性和水溶性。
试验研究了以抗坏血酸+琥珀酸浸出体系从废三元锂电池中回收镍、锂,考察了琥珀酸加入量、抗坏血酸浓度、浸出时间、浸出温度对镍、锂回收率的影响,并通过XRD和SEM探究了反应前后废锂电池的组成变化和表面形态。
1 试验部分
1.1 试验原料、试剂与仪器
试验原料:废三元锂电池(可充式锂聚合物电池,EPT334460型,由深圳市量能科技有限公司提供)。经放电、拆卸、清洗、离心、干燥、研磨等预处理后所得正极材料。正极材料经王水消解后分析主要元素组成,结果见表1,正极材料的XRD图谱如图1所示。由表1看出,锂、镍含量较高,钴含量极低,仅有0.024 mg/L;由图1看出,正极材料的主要物相为LiNiO2。
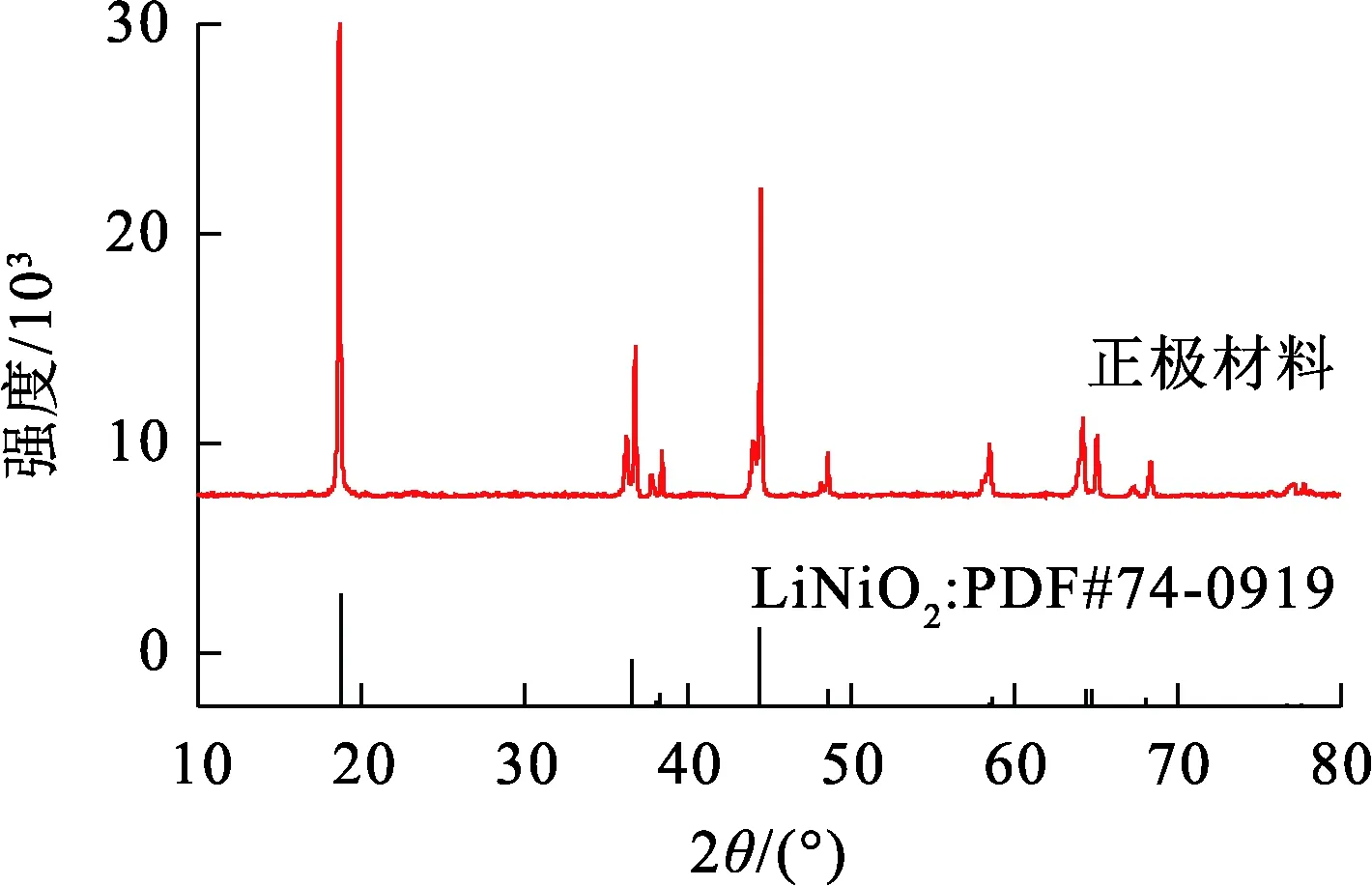
图1 处理后正极材料XRD图谱

表1 正极材料的主要元素组成 mg/L
试验试剂:氯化钠(天津市大茂化学试剂厂)、N-N二甲基甲酰胺(国药集团化学试剂有限公司)、琥珀酸(天津市大茂化学试剂厂)、抗坏血酸(成都市科隆化学品有限公司)、硝酸(成都市科隆化学品有限公司)、盐酸(成都市科隆化学品有限公司),均为分析纯。试验中不同浓度抗坏血酸均现配现用(水为溶剂)。
主要仪器:X射线衍射仪(Ultima Ⅳ型,日本株式会社理学公司)、扫描电子显微镜(SEM,MIRA LMS型,捷克泰斯肯贸易有限公司)、原子吸收分光光度计(AA-6300CF型,日本岛津企业管理有限公司)。
1.2 试验原理与方法
1.2.1 试验原理
综上所述,微信群护理人员培训手段的应用,是近几年来临床上新兴的一种护理理论培训措施,其主要是通过对需要培训的护理人员在工作后的业余时间,配合完成各项护理理论知识的培训,确保护理工作有序开展,也是一种培养优秀护理人才的好的培训方法。同时在培训过程中不断总结经验,探讨改进措施,完善培训方法,努力提高培训质量。
在抗坏血酸+琥珀酸体系中,抗坏血酸因具有还原性,可还原镍酸锂,Ni3+被还原成Ni2+,发生的化学反应见式(1);琥珀酸溶解在抗坏血酸溶液中,既可使体系酸性增强,还会与Ni2+、Li+发生螯合反应,使其充分浸出,发生的化学反应见式(2)。正极材料在抗坏血酸+琥珀酸体系中发生的总化学反应见式(3)。

(1)

(2)

(3)
1.2.2 试验及分析方法
取100 mg正极材料于研钵中,按照一定质量比加入琥珀酸,混合研磨后置于圆底烧瓶中,加入一定浓度抗坏血酸50 mL,控制固液质量体积比为2 mg/1 L;将烧瓶置于水浴锅中,调节至设定温度,并开启搅拌,反应一定时间后真空抽滤,分离浸出液和浸出渣。用原子吸收分光光度计测定浸出液及王水溶解正极材料后溶液中的镍、锂金属离子质量浓度,按式(4)计算金属浸出率。
(4)
式中:xB—金属(镍、锂)浸出率,%;ρB0—浸出液金属(镍、锂)质量浓度,mg/L;ρB1—王水溶解正极材料后溶液中金属(镍、锂)质量浓度,mg/L。
采用X射线衍射仪(扫描角度5°~80°,扫描速率2°/min)分析浸出前、后正极材料物相;采用扫描电子显微镜(SEM)观察浸出前、后正极材料形貌。
2 试验结果与讨论
2.1 各因素对Ni2+、Li+浸出率的影响
2.1.1 琥珀酸加入量的影响
在抗坏血酸浓度0.2 mol/L、浸出时间60 min、浸出温度80 ℃条件下,琥珀酸加入量(m(琥珀酸)/m(正极材料))对Ni2+、Li+浸出率的影响试验结果如图2所示。
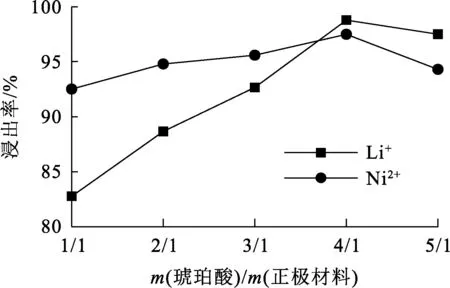
图2 琥珀酸加入量对Ni2+、Li+浸出率的影响
由图2看出,随琥珀酸加入量增大,Ni2+、Li+浸出率呈先升高后降低趋势:琥珀酸加入量增至4/1时,Ni2+、Li+浸出率均达最大,为97.49%、98.78%;之后继续增大琥珀酸加入量,Ni2+、Li+浸出率均小幅下降,这是因为琥珀酸过量会降低正极材料与浸出剂的接触概率,导致反应不充分。综合考虑,确定琥珀酸加入量以4/1为佳。
2.1.2 抗坏血酸浓度的影响
在琥珀酸加入量4/1、浸出时间60 min、浸出温度80 ℃条件下,抗坏血酸浓度对Ni2+、Li+浸出率的影响试验结果如图3所示。

图3 抗坏血酸浓度对Ni2+、Li+浸出率的影响
由图3看出,抗坏血酸浓度对正极材料中Ni2+、Li+浸出率影响较显著:随抗坏血酸浓度增大,Ni2+、Li+浸出率大幅升高,在抗坏血酸浓度增至0.2 mol/L时,分别升至96.86%和98.65%;继续增大抗坏血酸浓度,Ni2+、Li+浸出率趋于稳定,几乎无变化。这是因为抗坏血酸既是浸出剂也是还原剂,其较强的还原性可将正极材料中高价态金属氧化物还原成低价态,从而使金属浸出效率提高。综合考虑,确定抗坏血酸浓度以0.2 mol/L为佳。
2.1.3 浸出时间的影响
在琥珀酸加入量4/1、抗坏血酸浓度0.2 mol/L、浸出温度80 ℃条件下,浸出时间对Ni2+、Li+浸出率的影响试验结果如图4所示。可以看出,随浸出时间延长,Ni2+、Li+浸出率先升高后趋于稳定:浸出40 min时,Ni2+、Li+浸出率达最大,分别为96.64%、96.60%;之后继续浸出,Ni2+、Li+浸出率仅有小幅波动,变化不明显。综合考虑,确定浸出时间以40 min为佳。
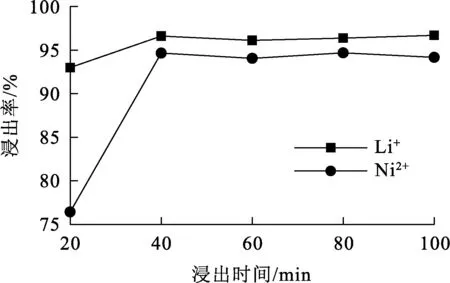
图4 浸出时间对Ni2+、Li+浸出率的影响
2.1.4 浸出温度的影响
在琥珀酸加入量4/1、抗坏血酸浓度0.2 mol/L、浸出时间40 min条件下,浸出温度对Ni2+、Li+浸出率的影响试验结果如图5所示。

图5 浸出温度对Ni2+、Li+浸出率的影响
由图5看出,随浸出温度升高,Ni2+、Li+浸出率呈先升高后降低趋势:温度升至80 ℃时,Ni2+、Li+浸出率均达最大,分别为93.67%、96.45%;之后继续升高温度,Ni2+、Li+浸出率呈小幅下降趋势,这是因为温度过高会使抗坏血酸分解失去还原能力,导致金属浸出率下降。综合考虑,确定浸出温度以80 ℃为佳。
2.2 浸出渣的XRD、SEM表征
正极材料浸出前后XRD图谱如图6所示。可以看出:镍酸锂正极材料在经抗坏血酸与琥珀酸体系浸出后,其主要物相的特征峰明显消失,说明在该体系中有价金属得到充分浸出。

图6 浸出前、后正极材料的XRD图谱
浸出前、后正极材料的SEM照片如图7所示。可以看出:正极材料位球状多晶颗粒,分布均匀且规整;而浸出渣中没有观察到球状颗粒,而是出现小颗粒团聚现象,说明抗坏血酸与琥珀酸体系对正极材料中Ni2+、Li+浸出效果较好。
2.3 不同浸出体系的浸出效果对比
在固液质量体积比2 mg/1 mL、琥珀酸加入量4/1、抗坏血酸浓度为0.2 mol/L、浸出时间40 min,浸出温度80 ℃最佳浸出条件下,进行3组验证试验,结果见表2。可以看出:Li+平均浸出率为97.57%,Ni2+平均浸出率为95.58%。
不同体系对废三元锂电池中Ni2+、Li+浸出率的对比结果见表3。可以看出:该浸出体系的浸出效果与无机酸浸出法相当;相较于氨浸出法及其他浸出体系,该浸出体系表现出较好的浸出效果。
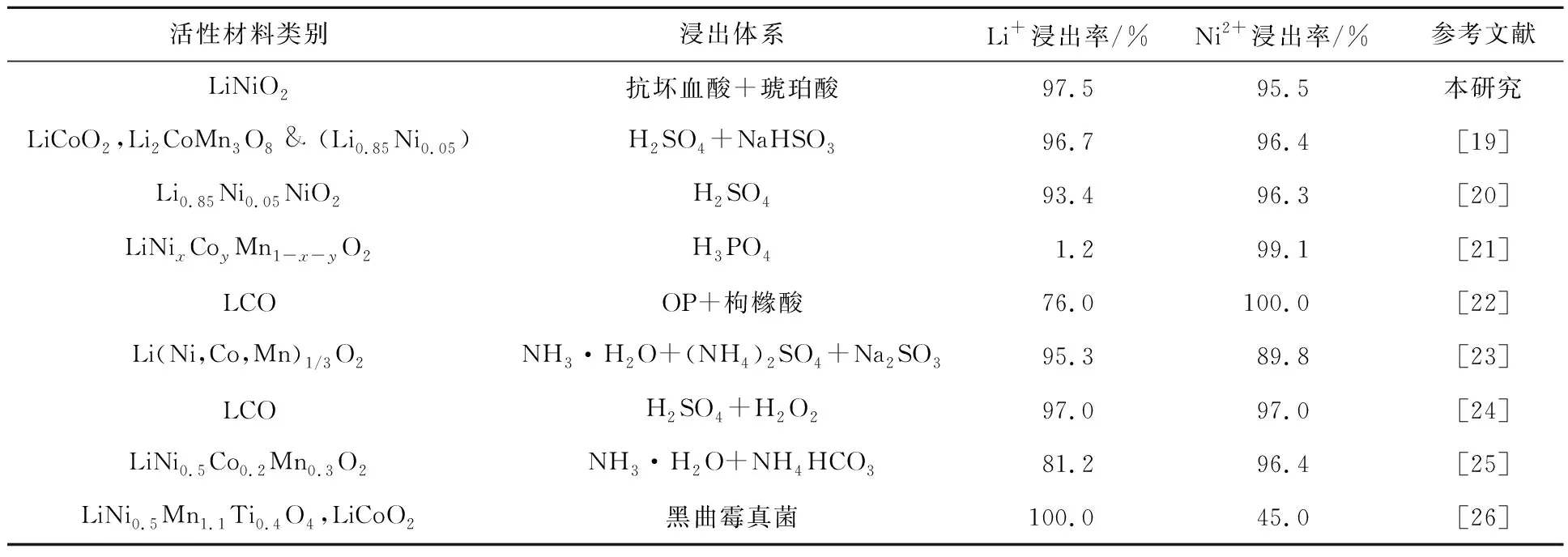
表3 不同体系对废三元锂电池中Li+、Ni2+浸出率的对比结果
3 结论
以抗坏血酸+琥珀酸为浸出体系从废三元锂电池中回收镍、锂是可行的,适宜条件下Ni2+和Li+浸出率为95.58%和97.57%。该有机酸体系对镍、锂的浸出效果与无机酸体系的浸出效果相当,可实现废三元锂电池正极材料中有价金属有效回收,减少环境污染,缓解镍锂资源短缺问题。
