Mn2+掺杂CsCdCl3微米晶发光性能及其LED应用
2023-10-08王瑞张铭程宋玉曾敏周莉魏立杰李根杨柳胡永明顾豪爽李岳彬
王瑞, 张铭, 程宋玉, 曾敏*, 周莉, 魏立杰,李根, 杨柳, 胡永明, 顾豪爽, 李岳彬,3*
(1. 湖北大学微电子学院 微纳电子材料与器件湖北省重点实验室, 湖北 武汉 430062;2. 江苏永鼎股份有限公司, 江苏 苏州 215211; 3. 湖北大学 潜江产业技术研究院, 湖北 潜江 433100)
1 引 言
CsPbX3(X= Cl,Br,I)作为最典型的三维(3D)金属卤化物钙钛矿材料,具有吸收截面大、荧光量子产率(PLQY)高、半峰宽窄、载流子迁移率高等优异的光电性能,在太阳能电池、光电探测器、照明与显示等光电子器件领域展示出广阔的应用前景[1-2]。然而,铅基钙钛矿对水、光、热、有机配体极度敏感,导致发光性能不稳定,在一定程度上限制了其应用[3-4]。最近,镉基钙钛矿CsCdCl3因其出色的稳定性和可调谐的发射光谱引起了研究者的关注。CsCdCl3属于1/3角共享和2/3面共享的非典型3D钙钛矿[5],具有非吸湿性,其中角共享的孤立八面体单元形成准0D结构,而面共享的二聚体单元形成准1D结构。这种独特的八面体键合方式不仅会产生自陷激子(Self-trapped excitons,STEs)发射,而且为离子掺杂带来了更多可能。由于在CsCdCl3的合成过程中容易形成杂质相(如Cs2Cd-Cl4和Cs3Cd2Cl7),因此以往有关CsCdCl3的研究主要集中在理论计算、拉曼散射和电子顺磁共振等方面,而对发光性质的研究较少[5-8]。近年来,随着合成化学技术的不断发展,纯相CsCdCl3已被成功研制出来。目前所报道的纯相CsCdCl3大多为单晶,其最高PLQY为42%[9],但是单晶不利于器件的制备。然而,CsCdCl3微米晶的PLQY最高只有4.75%[10],远远达不到固态照明器件的要求。因此,如何提高CsCdCl3的发光效率已成为目前发光领域的研究热点。
离子掺杂是一种调控钙钛矿光物理特性的有效手段[11-14]。由于过渡金属离子Mn2+具有3d5电子构型,d-d跃迁能量受晶体场环境的影响较大,通过选择不同的主体基质和改变掺杂浓度可以实现发光颜色从绿光到深红色可调,Mn2+掺杂还可以改善主体基质的稳定性[15-16]。这些特性使Mn2+成为最受欢迎的激活剂之一。例如,Huang[17]和He[18]等采用溶剂热法合成了CsCdCl3∶Mn2+单晶,通过调节Mn2+掺杂浓度来调控晶格畸变程度甚至CsCdCl3→CsMnCl3·2H2O相变,实现了发射波长在570 ~640 nm之间连续可调,最高PLQY为91.4%,同时该材料还表现出非常优异的热和水稳定性。Jia等[10]分别采用重结晶法、溶剂热法、热注入法合成了CsCdCl3∶Mn2+多晶、单晶、纳米晶,其相应的PLQY分别为74%、35%、8%。Wen等[19]采用共沉淀法成功制备了单组分白光CsCd1-x(Cl1-yBry)3∶xMn微米晶,通过灵活调节x和y的比例可以获得不同色温的白光LED,但其PLQY未知。目前关于CsCdCl3∶Mn2+的报道大部分都是采用溶剂热法制备的单晶形貌[6,17-18,20],然而微米晶形貌却鲜有报道[19,21],其PLQY(35%)值远低于单晶的值。
鉴于此,本文通过简单的室温溶液法制备出了一种高效稳定的Mn2+掺杂六方相CsCdCl3微米晶荧光粉。在254 nm紫外灯激发下,CsCdCl3∶5%Mn2+样品呈现出最明亮的橙黄光,发射峰位于约598 nm,半峰宽为75 nm,PLQY高达99.1%。此外,Mn2+掺杂将激发光波长从小于350 nm的紫外光拓展至460 nm的蓝光,使其与商用紫外和蓝光芯片更匹配。更重要的是,放置在室温下保存4个月后的荧光粉没有发生结构破坏,耐热温度高达600 ℃,浸没在水中18 h且经过持续的紫外灯光照后仍然发射出比较明亮的橙黄光。进一步将其涂覆在265 nm LED芯片封装成黄光LED-1,相关色温(CCT)为1 497 K,显色指数(CRI)为41。采用265 nm LED芯片、商用蓝色荧光粉BaMgAl10O17∶Eu2+(BAM∶Eu)、商用绿色荧光粉BaSrSiO4∶Eu2+(BSSO∶Eu)以及橙黄色荧光粉CsCdCl3∶5%Mn2+封装的白光LED-2,CCT为4 371 K,CRI高达91。采用420 nm LED芯片、BSSO∶Eu、CsCdCl3∶5%Mn2+封装的白光LED-3,CCT为3 412 K,CRI为83。这充分说明该材料有望成为一种新型高效稳定的橙黄色发光材料,在固态照明领域具有潜在的应用价值。
2 实 验
2.1 化学药品
氯化铯(CsCl,99%)购于上海麦克林生化科技股份有限公司。氯化镉(CdCl2,98%)和氯化锰(MnCl2,99%)购于上海阿拉丁生化科技股份有限公司。浓盐酸(HCl,37%)和无水乙醇(分析纯)购于中国国药控股化学试剂有限公司。所有药品使用前均未进行纯化。
2.2 样品制备
采用室温溶液法制备了一系列不同浓度Mn2+掺杂的CsCdCl3微米晶荧光粉,即CsCdCl3∶x%Mn,其中x%为Mn/Cd投料量(x% = 0%,3%,5%,7%,10%,15%)。以CsCdCl3∶10%Mn为例:称取680.24 mg CsCl(4 mmol)溶解于装有5 mL浓盐酸的玻璃瓶A中,称取748.24 mg CdCl2(4 mmol)和50.84 mg MnCl2(0.4 mmol)共同溶解在装有5 mL浓盐酸的玻璃瓶B中,然后将A、B瓶置于磁力搅拌台上进行室温搅拌。待反应物溶解完毕后将A瓶中的CsCl溶液倒入B瓶中,继续搅拌30 s得到白色浑浊液。将得到的产物进行离心并收集沉淀,用无水乙醇洗涤三次后置于60 ℃的干燥箱中烘干10 h,得到白色粉末样品。
2.3 样品表征
采用X射线粉末衍射仪(XRD,D8 Advance,Bruker)对样品的物相结构进行表征,测量范围为10° ~ 70°,步长0.000 1°,辐射源为Cu靶Kα射线(λ= 0.154 06 nm)。借助场发射扫描电子显微镜(SEM,JSM 7100F)对形貌进行分析,加速电压为30 kV。利用X射线光电子能谱仪(XPS,ESCALAB 250Xi)进行化学成分和价态检测,以284.8 eV的C1s峰进行校准。Mn2+离子的实际掺杂浓度由电感耦合等离子体原子发射光谱仪(ICP-AES,Optimal 8000)进行测量。通过紫外-可见分光光度计(UV-Vis,PerkinElmer Lambda 950)测试吸收光谱和漫反射光谱。荧光激发光谱(PLE)和发射光谱(PL)由荧光光谱仪(FluoTime 300)进行表征,荧光衰减寿命和绝对PLQY通过爱丁堡荧光光谱仪(FLS 980)及其配备的标准积分球测试。热重-差示量热分析采用热重分析仪(TG-DTA,Netzsch STA449C),升温范围为室温 ~ 1 000 ℃,升温速率为15 ℃/min,氮气气氛。
2.4 LED器件制作
橙黄光LED的制作(LED-1):将上述制备的橙黄色荧光粉CsCdCl3∶5%Mn与ZWL8820有机硅胶以粉胶质量比1∶0.6充分混合后涂覆在商用265 nm LED芯片上,并将器件在80 ℃下固化1 h得到固态LED-1。
白光LED的制作(LED-2和LED-3):将橙黄色荧光粉CsCdCl∶35%Mn、商用蓝色荧光粉BaMgAl10O17(BAM)、商用绿色荧光粉BaSrSiO4∶Eu2+(BSSO:Eu)以及ZWL8820有机硅胶以粉胶质量比1∶0.6充分混合涂覆在商用265 nm LED芯片的表面,并将器件在80 ℃下固化1 h得到LED-2。将CsCdCl3∶5%Mn、BSSO∶Eu以及ZWL8820有机硅胶以粉胶质量比1∶0.6充分混合涂覆在商用420 nm LED芯片表面,并将器件在80 ℃下固化1 h得到固态LED-3。使用虹谱OHSP-350M测试所封装的LED器件的光电特性。
3 结果与讨论
3.1 晶体结构、形貌和成分表征
CsCdCl3化合物属于六方晶系,由面共享的[Cd2Cl9]5-二聚体和孤立的[CdCl6]4-八面体组成,每个二聚体单元(Cd2)与其他6个孤立的八面体单元(Cd1)以共顶点的形式形成非典型的3D结构框架(图1(a))。值得注意的是,二聚体结构单元具有C3V对称性,发生了轻微畸变,会产生STEs发射,而孤立的八面体结构单元具有D3D对称性[18,22]。Mn2+掺杂倾向于取代正常的Cd1位置[23]。采用室温溶液法合成不同浓度Mn2+掺杂的CsCd-Cl3∶x%Mn荧光粉。Mn2+的实际浓度由ICP-AES测定,Mn2+投料浓度为3%、5%、7%、10%、15%的实际测量浓度分别为2.0%、2.8%、4.3%、6.2%、8.3%(表S1)。图1(b)为CsCdCl3∶x%Mn的XRD图谱,所有样品的衍射峰与六方相CsCdCl3的标准卡片(PDF#70-1615)完全吻合,表明轻掺杂Mn2+没有引入杂质相。随着Mn2+掺杂浓度的升高,XRD衍射峰逐渐向大角度偏移,这是由于离子半径较小的Mn2+(r= 0.083 nm,CN = 6)取代离子半径较大的Cd2+(r= 0.095 nm,CN = 6)导致了晶格收缩,证明Mn2+被成功掺入到CsCdCl3晶格中。图1(c)为CsCdCl3∶x%Mn的SEM图,可清晰地观察到表面比较光滑的六边形结构,尺寸约为1.5 μm,意味着晶体结晶情况良好。XPS元素分析表明10%Mn2+掺杂的样品中含有Cs、Cd、Cl、Mn四种元素(图S1)。Mn的信号峰位于652.1 eV和641.3 eV,说明Mn以+2价存在。Cd 3d 的XPS峰(411.6 eV和404.9 eV)和Cl 2p的XPS峰(199.2 eV和197.6 eV)发生了微小偏移(图1(i)~(l)),表明Mn2+占据了Cd2+格位从而引起Cd2+与Cl-周围的电子云密度发生改变。

图1 (a)CsCdCl3∶Mn的晶体结构示意图;(b)CsCdCl3∶x%Mn(x = 0%,3%,5%,7%,10%,15%)的XRD谱,青色谱代表六方相CsCdCl3的标准卡片(PDF#70-1615),右图为(110)晶面衍射峰的放大谱;CsCdCl3∶x%Mn的SEM图:(c)x = 0%,(d)x = 3%,(e)x = 5%,(f)x = 7%,(g)x = 10%,(h)x = 15%;CsCdCl3(上)和CsCdCl3∶10%Mn(下)的高分辨XPS能谱:(i)Cs 3d,(j)Cd 3d,(k)Cl 2p,(l)Mn 2p。Fig.1 (a)Schematic crystal structure diagram of CsCdCl3∶Mn.(b)XRD patterns of CsCdCl3∶x%Mn(x = 0%, 3%, 5%, 7%,10%, 15%), and the cyan lines stands for the standard XRD pattern of hexagonal CsCdCl3(PDF No.70-1615). The right figure shows the enlarged diffraction patterns of (110) plane. SEM images of CsCdCl3∶x%Mn: (c)x = 0%, (d)x = 3%,(e)x = 5%,(f)x = 7%,(g)x = 10%,(h)x = 15%. High-resolution XPS spectra of Cs 3d(i), Cd 3d(j), Cl 2p(k),Mn 2p(l) of CsCdCl3(up) and CsCdCl3∶10%Mn(down).
3.2 光学性能
图2(a)为CsCdCl3∶x%Mn样品的UV-Vis吸收光谱,所有样品均在240 nm左右存在一个宽的吸收峰,属于电荷转移带[21]。随着Mn2+掺杂量的增加,该吸收峰逐渐红移,这是由于Mn2+离子取代了Cd2+离子,在禁带中引入了中间能级使带隙变小所致。CsCdCl3∶x%Mn微晶在300 ~ 500 nm之间的吸收随着Mn2+掺杂量的增加明显增强,且在330 nm处和360 nm处各出现了一个新的吸收峰,420 nm左右出现两个新的峰,460 nm处出现一个新的峰,吸收强度也随着Mn2+掺杂浓度的增加而增强。这些新出现的窄峰均是来自Mn2+离子的dd跃迁吸收[24]。由于Mn2+的实际掺杂浓度较小(< 8.3%)以及Mn2+离子对光的吸收弱于基质的Cl-→Cd2+荷移跃迁吸收,故Mn2+离子在该范围内的吸收峰不是十分明显。如图2(b)所示,随着Mn2+的增加,样品的紫外吸收边缘都位于500 nm以下,归因于Mn2+的d-d跃迁,与所报道的一致[17]。
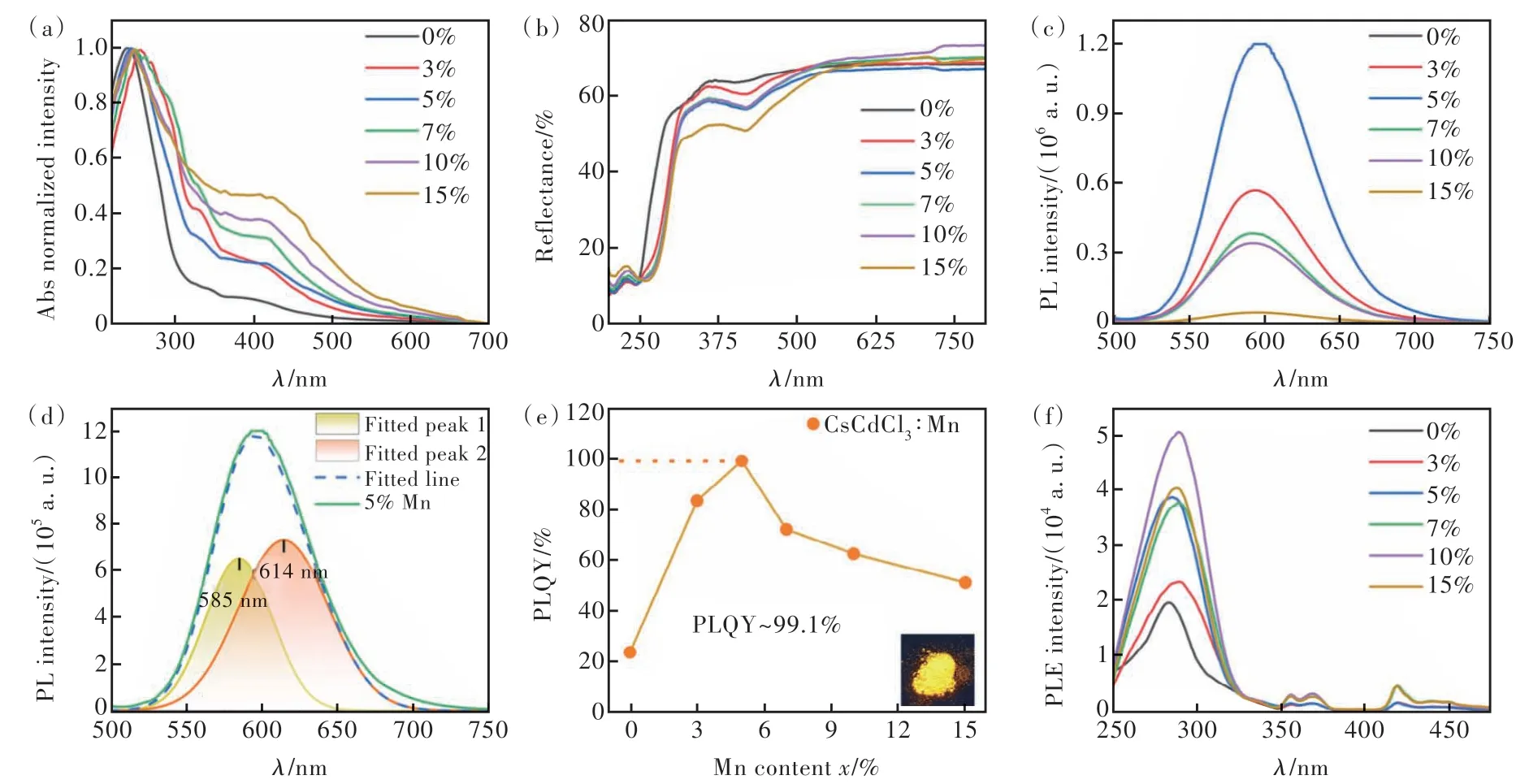
图2 CsCdCl3∶x%Mn的UV-Vis吸收光谱(a)、漫反射光谱(b)、发射光谱(c)(激发波长为254 nm);(d)CsCdCl3∶5%Mn发射光谱的峰位拟合结果;(e)PLQYs随Mn2+掺杂浓度x%的变化趋势,插图为CsCdCl3∶5%Mn在254 nm紫外灯照射下的数码照片;(f)598 nm监测波长下的激发光谱。Fig.2 Optical properties of CsCdCl3∶x%Mn samples. (a)UV-Vis absorption spectra. (b)Diffuse reflection spectra. (c)PL spectra under 254 nm excitation. (d)Fit peaks of CsCdCl3∶5%Mn emission spectra. (e)PLQYs values as a function of Mn2+content. Insert is the image of CsCdCl3∶5%Mn under 254 nm UV lamp. (f)PLE spectra monitored at 598 nm.
在254 nm紫外光激发下,未掺杂样品的发射峰位于500 ~ 750 nm范围内,峰值在570 nm处,半峰宽为97 nm,Stokes位移为316 nm,属于典型的STEs发射。Mn2+掺杂后不仅将发射波长红移至598 nm左右,半峰宽减小至75 nm,而且大幅提高了荧光发射强度(图2(c)和S2)。CsCdCl3∶5%Mn样品在500 ~ 750 nm范围内的宽谱发射峰可拟合为585 nm(2.43 eV)和614 nm(2.31 eV)两个峰(图2(d))。第一个峰的中心波长接近未掺杂样品中STEs发射的中心波长,而第二个长波长的峰来自Mn2+离子的4T1(G)→6A1(S)跃迁[18]。此外,荧光强度高度依赖于Mn2+离子的掺杂浓度,随着Mn2+浓度的增加,发光强度呈现先增后减的趋势,与文献报道的一致[18]。PLQYs也呈现同样的变化趋势,其中5%Mn2+掺杂的发光最强,发射出明亮的橙黄光,PLQY高达99.1%,是未掺杂样品的4.2倍(23.7%)(图2(e)和图S3)。根据Dexter理论,当激活剂之间的距离小于0.5 nm时,激活剂之间存在交换相互作用。在CsCdCl3晶格中,当Mn2+掺杂浓度较低时Mn2+离子之间的距离比较远,避免了Mn-Mn之间的交换作用,因此具有较高的PLQY;当Mn2+浓度增加至5%以后会形成Mn-Mn耦合对,造成Mn2+离子之间非辐射能量转移损失从而降低PLQY。因此,最佳Mn2+离子的投料比例确定为5%。为了使所制备的材料与蓝光芯片适配,我们进一步研究了420 nm蓝光激发下的发射光谱。如图S4所示,随着Mn2+含量增加,荧光强度逐渐增强,直到掺杂浓度为10%时强度达到最大,发射峰位于604 nm;继续增加掺杂浓度导致强度下降,这是由于Mn2+浓度过高产生了浓度猝灭效应。
图2(f)是通过监测CsCdCl3∶x%Mn荧光粉在598 nm处的发射测得的激发光谱。Mn2+掺杂前后的样品在250 ~ 325 nm之间的激发峰形状大致相同,证明存在CsCdCl3到Mn2+离子的能量传递过程。该范围内的紫外吸收强度随着Mn2+掺杂浓度的增加呈现明显增强的趋势,并且吸收范围出现宽化,这归因于Cl-→Mn2+荷移跃迁吸收[10]。另外,对于Mn2+掺杂的样品,在360,370,420,440 nm处出现了4个新的激发峰,分别属于d-d型Mn2+从基态6A1(6S)到激发态4Eg(4D)、4T2g(4D)、[4A1g(4G)、(4Eg)]、4T2g(4G)的跃迁。该结果说明Mn2+掺杂不仅提高了CsCdCl3微米晶在深紫外区域的吸收强度,而且成功地增加了荧光粉对350 nm以上紫外光和蓝光的吸收,使其与商用紫外甚至蓝光芯片更匹配。
为了进一步研究Mn2+掺杂使CsCdCl3的吸收峰发生红移的原因,对未掺杂和CsCdCl3∶5% Mn2+的能带结构进行了理论计算。第一性原理计算使用密度泛函理论(DFT)和Perdew-Burke-Ernzerhof(PBE)的广义梯度近似(GGA),在Materials Studio软件中计算出的能带结构和态密度(DOS)如图3所示。结果表明,Mn2+掺杂CsCdCl3和未掺杂CsCdCl3都是一种直接带隙半导体,CsCdCl3在Γ点的禁带宽度为2.452 eV,高于CsCdCl3∶5% Mn2+的禁带宽度2.363 eV(图3(a)、(b))。这说明Mn2+部分取代Cd2+后缩小了CsCdCl3的带隙,将造成吸收峰红移,与实验结果吻合。CsCdCl3的DOS曲线如图3(c)所示,价带最大值(VBM)主要由Cl的p轨道和Cd的d轨道组成,导带最小值(CBM)主要由Cd的s轨道和Cl的p轨道组成。从CsCdCl3∶5% Mn2+的DOS曲线(图3(d))可以看出,VBM主要由Mn的d轨道和Cl的p轨道贡献,CBM主要由Mn的s轨道和Cl的p轨道贡献。Cs+对价带和导带几乎没有贡献。Mn2+掺杂后的DOS在价带出现一个新峰,由Mn的3d轨道贡献,但Mn2+掺杂对导带的影响很小。

图3 (a)计算的CsCdCl3的能带结构;(b)计算的CsCdCl3∶5%Mn的能带结构;(c)CsCdCl3的态密度;(d)CsCdCl3∶5%Mn的态密度。Fig.3 (a)Calculated energy band structure diagram of CsCdCl3.(b)Calculated energy band structure diagram of CsCdCl3∶5%Mn.(c)Density of state diagram of CsCdCl3.(d)Density of state diagram of CsCdCl3∶5%Mn.
3.3 发光机理
为了进一步研究Mn2+掺杂CsCdCl3的发光机理,我们测试了不同浓度Mn2+掺杂CsCdCl3微米晶的荧光寿命衰减曲线。如图4(a)和表S2所示,双指数函数拟合结果显示未掺杂CsCdCl3微米晶的平均发光寿命为20 μs,符合STEs发光的重要特征。随着Mn2+掺杂浓度的增加,短寿命τ1总体上呈现逐渐减小、其所占比例逐渐增加的趋势,而长寿命τ2的大小和比例均相应地减小,可能是由于越来越多的Mn2+占据了Cd2的位置,形成Mn-Mn对或簇。二聚体的形成一方面会导致晶格畸变从而增加STEs的发射几率,另一方面会造成浓度猝灭而降低Mn2+的发光寿命,这说明微秒级寿命τ1可能对应STEs辐射复合,毫秒级寿命τ2对应Mn2+的d-d跃迁[21]。当掺杂量为5%时,STEs(46%)发射和Mn2+的d-d跃迁(54%)所占比例最接近,与图2(d)的结果一致,此时的发光效率达到最高。上述结果表明,低掺杂浓度的Mn2+离子很可能占据孤立的八面体中心Cd1的位置,Mn-Mn之间的距离大于0.5 nm,无相互作用;当掺杂浓度增加时,越来越多的Mn2+占据Cd2的位置,形成Mn-Mn二聚体,Mn2+离子之间的能量传递概率增加从而导致寿命衰减,发生浓度猝灭。CsCdCl3∶x%Mn的发光存在两种电子跃迁过程。如图4(b)所示,在254 nm紫外光激发下,价带电子获得能量跃迁至导带形成自由激子,然后分别向STE能级和Mn离子的4T1能级发生能量转移。由于STE与Mn2+的4T1在能量上接近,因此STEs可将能量有效地传递给Mn2+离子[18],进而实现STEs发射和Mn2+离子的dd跃迁(4T1→6A1)。
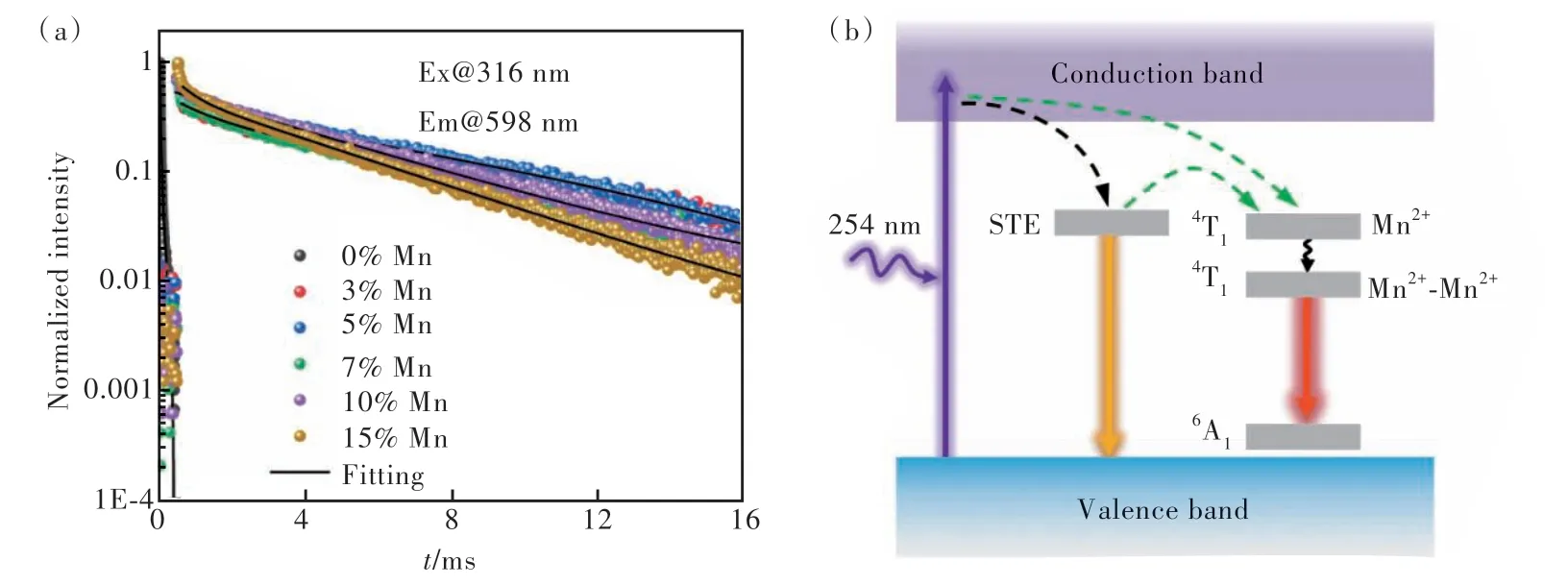
图4 (a)CsCdCl3∶x%Mn的PL衰减曲线,激发波长为316 nm,发射波长为598 nm;(b)CsCdCl3∶x%Mn的发光机理。Fig.4 (a)PL decay curves of CsCdCl3∶x%Mn monitored at 598 nm, excited under 316 nm. (b)Luminescence mechanism diagram of CsCdCl3∶x%Mn.
3.4 稳定性分析
稳定性是评估材料能否获得实际应用的重要条件。我们对发光效率最高的样品CsCdCl3∶5%Mn分别进行了空气、热、水稳定性研究。图5(a)为CsCdCl3∶5%Mn微米晶样品在空气中存放4个月前后的XRD谱,其物相未发生明显变化,说明该材料具有优异的空气稳定性。热重(TG)曲线显示CsCdCl3∶5%Mn荧光粉在24 ~ 1 000 ℃之间有两段失重过程(图5(b))。第一次失重发生在24 ~ 600 ℃范围内,失重率为1.0%,这个轻微的失重过程可归因于样品表面的水分挥发,这主要是因为样品存放在自然环境中难免吸收一些水分子。第二次失重发生在600 ~ 1 000 ℃范围内,这个严重的失重(96.5%)是由于晶体结构的热分解所致。热稳定性实验说明所制备的微米晶荧光粉的耐热能力高达600 ℃。金属卤化物钙钛矿是离子型材料,对环境中的湿气极度敏感,但CsCd-Cl3晶体具有共价性质,使其成为一种耐湿性钙钛矿。为了验证CsCdCl3的耐湿性,我们将CsCdCl3∶5%Mn粉末直接浸泡在去离子水中,在254 nm紫外灯持续照射下拍摄不同时刻的照片。如图5(c)所示,该样品在水中连续浸泡18 h后依然保持着比较明亮的橙黄色,表明该材料的抗水性较好,可能与Cd—Cl键具有共价特征有关[5]。可见,Mn2+掺杂CsCdCl3荧光粉具有比较优良的空气、热、水稳定性,在固态照明领域具有潜在的应用前景。
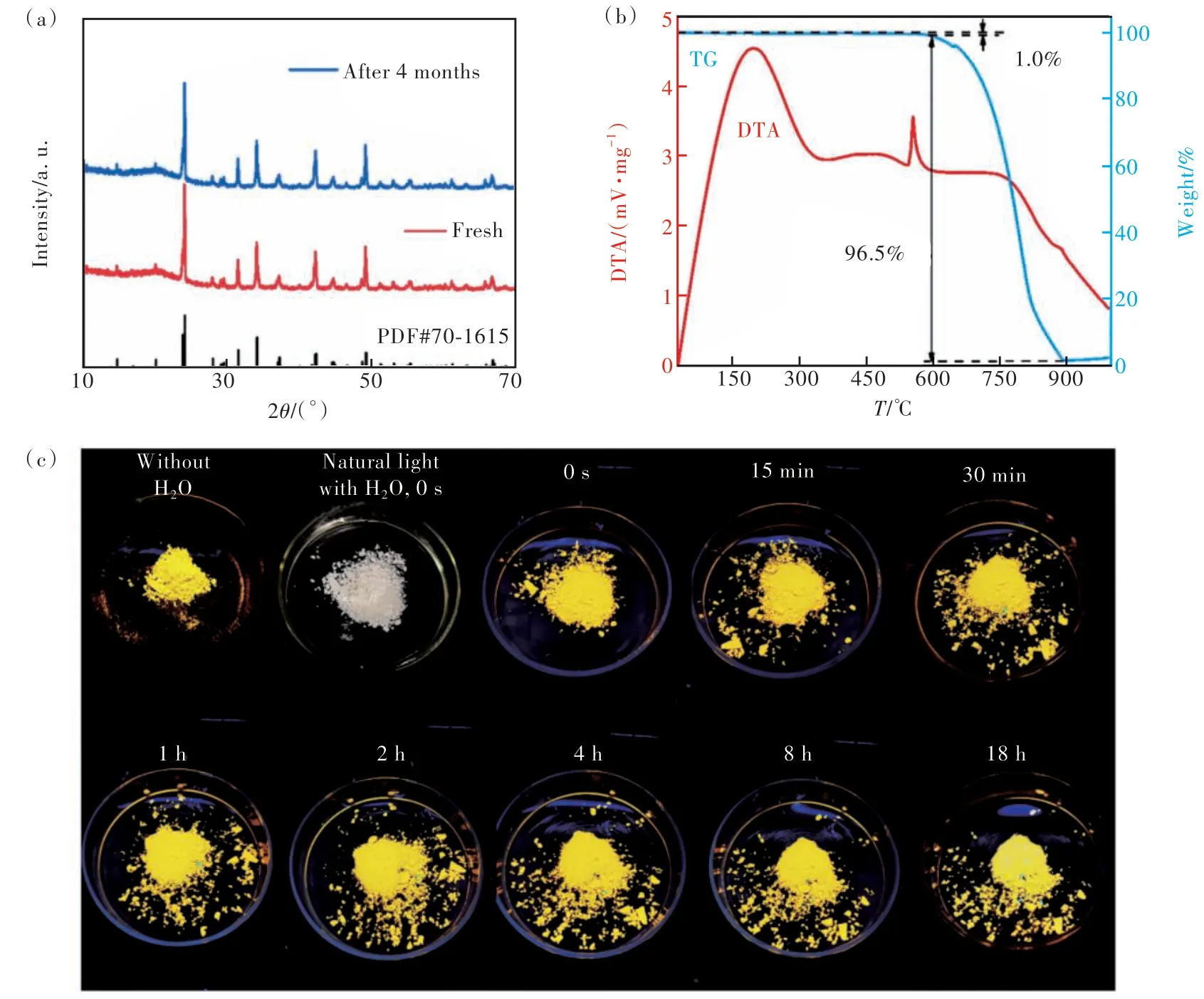
图5 (a)CsCdCl3∶5%Mn样品在空气中存放4个月前后的XRD谱;(b)CsCdCl3∶5%Mn的TG-DTA测试曲线;(c)在254 nm紫外灯持续照射下CsCdCl3∶5%Mn荧光粉浸入去离子水中不同时刻的数码照片。Fig.5 (a)XRD patterns of CsCdCl3∶5%Mn before and after 4 months in air. (b)TG-DTA curve of CsCdCl3∶5%Mn. (c)Images of CsCdCl3∶5%Mn phosphor immersed in deionized water at different time intervals under a 254 nm UV lamp.
3.5 在LED上的应用
为了探究CsCdCl3∶5%Mn荧光粉在LED上的应用前景,我们封装了三种不同的LED器件。如图6(a)所示,将CsCdCl3∶5%Mn粉末和商用265 nm LED芯片进行封装得到的LED-1器件发出明亮的橙黄光,CCT为1 497 K,CRI为41。这种低色温的黄光LED在病房照明以及皮肤病治疗领域有巨大的潜力。图6(b)是将蓝色荧光粉BAM∶Eu、绿色荧光粉BSSO∶Eu和橙黄色荧光粉CsCdCl3∶5%Mn混合后涂覆在265 nm LED芯片上得到的LED-2器件的发射光谱,在60 mA工作电流驱动下发出明亮的白光,CCT为4 371 K,CRI高达91。如前文所述,Mn2+掺杂将CsCdCl3的激发光波长从深紫外拓展至蓝光波段,为此,我们还制备了LED-3器件。如图6(c)所示,采用420 nm LED芯片、BSSO∶Eu和CsCdCl3∶5%Mn封装的LED-3器件发出暖白光,CCT为3 412 K,CRI为83。图S5中LED-1、LED-2和LED-3的色度坐标(CIE)分别为(0.59,0.40)、(0.36,0.35)、(0.40,0.36)。此外,在不同工作电流驱动下,三种LED的发射光谱的形状和位置没有发生改变(图S6),证实了用CsCdCl3∶Mn制备的LED器件具有良好的颜色稳定性。为了研究CsCdCl3∶Mn封装成LED后的稳定性,我们模拟了LED工作环境下的荧光粉稳定性(图S7)。在80 ℃下加热10 h以及在6 W的254 nm紫外灯照射下保持10 h后,LED依然能发射出明亮的橙黄光,且XRD衍射峰也未发生明显的变化。因此,可以推测采用该荧光粉封装的LED器件同样具有良好的稳定性。上述结果表明CsCdCl3∶Mn将在固态照明中具有重要的应用价值。

图6 (a)由265 nm LED芯片和CsCdCl3∶5%Mn封装的LED-1在40 mA电流驱动下的PL光谱;(b)由265 nm LED芯片、BAM∶Eu、BSSO∶Eu、CsCdCl3∶5%Mn封装的LED-2在60 mA电流驱动下的PL光谱;(c)由420 nm LED芯片、BSSO∶Eu、CsCdCl3∶5%Mn封装的LED-3在20 mA电流驱动下的PL光谱。插图为相应的LED通电后的实物图。Fig.6 (a)PL spectrum of LED-1 fabricated with 265 nm LED chip and CsCdCl3∶5%Mn, driven by an operating current of 40 mA. (b)PL spectrum of LED-2 fabricated with 265 nm LED chip, BAM∶Eu, BSSO∶Eu and CsCdCl3∶5%Mn, driven by an operating current of 60 mA. (c)PL spectrum of LED-3 fabricated with 420 nm LED chip, BSSO∶Eu and CsCdCl3∶5%Mn, driven by an operating current of 20 mA. The inserts are the corresponding photos of LED devices in operation,respectively.
4 结 论
本文采用简便的室温溶液法成功制备了Mn2+掺杂六方相CsCdCl3∶x%Mn微米晶荧光粉。在紫外光激发下,CsCdCl3∶5%Mn呈现出最明亮的橙黄光发射,峰值位于598 nm处,半峰宽为75 nm,PLQY高达99.1%,发光通道来自STEs发射和Mn2+离子的d-d跃迁。这一优异的发光性能归因于高效的CsCdCl3→Mn2+能量传递以及独特的3D晶体结构阻断了Mn2+离子之间的能量转移损失。此外,CsCdCl3∶5%Mn还具有优异的空气、热、水稳定性。我们进一步展示了CsCd-Cl3∶5%Mn微米晶在黄光LED和白光LED器件上的应用,均表现出比较优异的显色指数和良好的稳定性,在固态照明领域具有很大的发展潜力。
本文补充文件和专家审稿意见及作者回复内容的下载地址:http://cjl.lightpublishing.cn/thesisDetails#10.37188/CJL.20230125.
