QuEChERS结合HPLC-Q-TOF MS 快速筛查霜膏类化妆品中297种风险物质
2023-09-21曾广丰侯颖烨蔡翠玲肖可茵张宪臣李嘉仪谢建军
王 璐,曾广丰,侯颖烨,董 洁,蔡翠玲,肖可茵,张宪臣,李嘉仪,谢建军*
(1.广州海关技术中心,广东 广州 510623;2.国家级进出口食品质量安全风险验证评价实验室(化妆品),广东 广州 510623;3.中山海关技术中心,广东 中山 528400)
我国作为世界化妆品消费第一大国,化妆品安全问题日益成为关注焦点。化妆品禁用原料目录包括1 284项禁用物质[1],其种类繁多,数量庞大,然而现有的检测标准和文献方法有限,可能会使某些违法添加行为处于监测盲区[2]。因此,对于化妆品中风险物质的检测,亟需建立一种满足定性与定量要求的快速、高效的广谱筛查模式。
常见的广谱筛查技术包括组学[3]、指纹图谱[4]、拉曼光谱[5]、高分辨质谱[6-8]等,其中,以飞行时间质谱(TOF MS)为代表的高分辨质谱技术因具有质量分辨率高、扫描速度快、采集信息量大等优势,在有毒有害化合物筛查鉴定方面被广泛应用[9-12]。例如,曾广丰等[13]运用高效液相色谱-四极杆-飞行时间质谱(HPLC-Q-TOF MS)非靶向快速筛查凉茶中的非法添加物;章璐幸等[14]建立了谷物中18 种真菌毒素的HPLC-Q-TOF MS 非靶向筛查方法;黎梓城等[15]利用超高效液相色谱-四极杆-飞行时间质谱(UPLC-Q-TOF MS)建立了同时检测食品接触用塑料中50种添加剂迁移量的方法。
本研究选择45 种化合物作为质控化合物,基于超高效液相色谱-三重四极杆串联质谱(UPLC-MS/MS)技术,建立了霜膏类化妆品的QuEChERS 前处理方法,并扩展运用于297 种风险物质的HPLC-QTOF MS 靶向筛查,构建了化妆品风险物质的高分辨质谱筛查列表。风险物质的种类覆盖β-受体激动剂、阻断剂类、大环内酯类、磺胺类、喹诺酮类、硝基咪唑类、非甾醇消炎药类、苯并咪唑类、激素类、β-内酰胺类、酰胺醇类、农药等。该方法可用于化妆品中风险物质的识别和发现,能有效解决化妆品风险物质“检不全,检不快”的问题,为化妆品质量安全监管提供了重要的技术手段。
1 实验部分
1.1 标准品、试剂及样品
297种标准品均购自天津阿尔塔科技有限公司,纯度为89.3%~99.9%,质量浓度均为100 mg/L。其中45 种质控化合物分为2 组,组1:盐酸克伦特罗、盐酸妥布特罗、林可霉素盐酸盐、甲苯噻嗪、甲氧苄氨嘧啶、环丙沙星、恩诺沙星、氟罗沙星、氧氟沙星、奥比沙星、甲磺酸培氟沙星、2-氨基氟苯达唑、5-羟基甲苯咪唑、坎苯达唑、氟苯达唑、氨基甲苯咪唑、丙氧苯咪唑、噻苯哒唑、乙氧酰胺苯甲酯、氮哌酮、杀虫脒、金刚烷胺、头孢匹啉、头孢拉定、阿莫西林三水合物、替诺昔康;组2:苯甲酰磺胺、磺胺甲基异唑、磺胺苯吡唑、磺胺喹啉、氟尼辛葡甲胺、苯硫胍、甲芬那酸、胺丙畏、泼尼松、曲安西龙、丙磺舒、二甲双胍、盐酸萘甲唑啉、胍乙啶、盐酸苯乃嗪、布坦卡因盐酸盐、非诺唑酮、异唑肼、帕拉米松。
甲醇、乙腈、无水乙醇、甲酸均为HPLC 级,购自美国Thermo Fisher 公司。氯化钠、中性氧化铝(Al-N)、氨丙基粉(NH2)、石墨化炭黑(GCB)、N-丙基乙二胺(PSA)、硅胶粉、十八烷基键合硅胶(C18)均购自上海安谱公司。实验用水为Milli-Q超纯水。
霜膏类化妆品样品主要为实验室送检样品,包括面霜、护手霜、粉底霜等。
1.2 仪器条件
1.2.1 UPLC-MS/MS条件色谱条件见表1。质谱条件:API 4000Q Trap UPLC-MS/MS(美国AB公司),配备ESI离子源;正离子扫描;多反应监测(MRM)模式;气帘气压力:1.03×105Pa;雾化气压力:3.45×105Pa;加热辅助气压力:3.45×105Pa;碰撞气压力:Medium;电离压力:5 500 V;离子源温度:550 ℃。

表1 仪器色谱条件Table 1 Instrument chromatographic conditions
1.2.2 HPLC-Q-TOF MS 条件色谱条件见表1。质谱条件:LC-20AD 液相色谱系统(日本岛津公司),TripleTOFTM5600高分辨质谱仪(美国AB公司),配备ESI和APCI离子源,样液为ESI离子化方式,APCI 源连接自动校正系统,每10个样品自动校正1次;正负离子分别扫描;一级TOF MS扫描范围m/z:100 ~1 000 Da,采集时间100 ms;二级IDA-MS扫描范围m/z:50~1 000 Da,采集时间50 ms;气帘气压力:2.76×105Pa;锥孔电压:5 500 V;离子源温度:650 ℃;去簇电压:100 V;碰撞能量:40、55 eV。
1.3 实验方法
1.3.1 样品前处理准确称取0.5 g(精确至0.001 g)样品于10 mL具塞比色管中,加入1.0 mL饱和氯化钠溶液使样品均匀分散,加入8 mL 无水乙醇,涡旋振荡1 min,使试样与提取溶剂充分混匀,超声提取15 min,用无水乙醇定容至10 mL,摇匀,以10 000 r/min 离心5 min。吸取1.00 mL 上清液于装有50 mg C18粉的1.5 mL 离心管中,涡旋振荡2 min,以12 000 r/min 离心5 min,取上清液过0.22 μm 有机滤膜,待HPLC-Q-TOF MS测定,并采用空白样品提取液配制标准曲线。
1.3.2 建立筛查列表将1 mg/L 的混合标准溶液按照“1.2.2”方法上机测定,得到所有化合物的一级和二级质谱图,并与文献报道进行比较,建立297 种化合物的高分辨质谱筛查表,包括化合物的名称、分子式、离子化模式、保留时间、母离子及子离子等信息。
1.3.3 筛查方法利用PeakView 2.0 软件进行数据分析,将筛查表中化合物的英文名称、分子式、离子化模式导入软件,设置精确质量数偏差范围为± 1×10-5,保留时间偏差范围为±0.2 min,比较化合物的一级、二级精确质量数、保留时间、碎片离子丰度比的实测值和筛查列表理论值,匹配则锁定为“可疑目标物”,并采用UPLC-MS/MS进行定量确证。
2 结果与讨论
2.1 QuEChERS前处理质控研究
选择不同类别、不同结构、不同极性的45 种代表性化合物作为质控化合物,包括β-受体激动剂、阻断剂类、大环内酯类、磺胺类、喹诺酮类、硝基咪唑类、非甾醇消炎药类、苯并咪唑类、激素类、β-内酰胺类、酰胺醇类、农药等,以保证各类化合物的提取、净化效果。质控研究通过UPLC-MS/MS进行数据采集,并进行方法验证,以确保方法稳定可靠。
2.1.1 净化剂种类及用量的优化考察了C18、PSA、NH2、Al-N、GCB、硅胶粉6 种吸附剂在相同用量下的净化效果及最佳用量,结果显示,C18对45 种质控化合物的吸附最小,回收率为56.0%~103%,其他5种吸附剂均影响较大,其中头孢匹啉、头孢拉定和替诺西康等的回收率不足40%,部分化合物的回收率偏高。同时考察了C18用量(30、50、70、90、110 mg)对净化效果的影响,发现当C18用量为50 mg时,45种质控化合物的回收率在99.5%~121%之间,吸附影响最小;当用量≥70 mg时,随着用量的增大,吸附影响越来越大。因此,选择50 mg C18作为最佳净化剂。
2.1.2 提取溶剂的选择考察了甲醇、无水乙醇、乙腈对霜膏类化妆品的提取效果,发现使用甲醇作为提取溶剂时,大环内酯类、喹诺酮类、β-内酰胺类等的回收率偏低;使用乙腈和无水乙醇作为提取溶剂时,质控化合物的回收率总体较好,而无水乙醇提取的响应和峰形优于乙腈提取,因此,优先考虑使用无水乙醇进行提取。考虑到霜膏类化妆品较为粘稠,分散溶剂穿透能力强,可使样品更均匀,因此使用常见的饱和氯化钠溶液作为分散溶剂,再使用无水乙醇提取的方法进一步优化环丙沙星、噻苯哒唑等的回收率。结果显示,45种质控化合物的回收率为87.0%~119%,效果较好。
2.1.3 基质效应通过标准曲线法考察基质效应,采用无水乙醇和空白基质溶液分别配制标准曲线。结果发现,用无水乙醇配制的标准曲线进行定量分析时,林可霉素盐酸盐、甲氧苄氨嘧啶、恩诺沙星等化合物的回收率偏低,最低仅为19.4%;5-羟基甲苯咪唑、头孢匹啉等的回收率偏高,最高达316%。而用基质配制的曲线定量时,回收率为83.8%~119%。因此,本研究采用空白样品提取液配制标准曲线以消除基质效应。
2.1.4 方法验证在空白霜膏类化妆品中添加不同低浓度水平的质控化合物标准溶液,处理后按“1.2.1”条件进行分析,部分质控化合物的MRM 离子流色谱图如图1所示。结果显示,45种质控化合物在对应的质量浓度范围内呈良好的线性关系,相关系数(r2)>0.99。检出限(LOD)为0.01~0.20 mg/kg,定量下限(LOQ)为0.04~0.40 mg/kg(见表2)。采用空白基质进行低、中、高3个浓度水平的加标实验,同时进行6 组平行实验,结果显示,45 种质控化合物的回收率为81.5%~117%,相对标准偏差(RSD)为2.0%~14%,回收率和RSD均满足要求。

图1 部分质控化合物的MRM离子流色谱图Fig. 1 MRM ion flow chromatograms of partial quality control compounds A:clenbuterol hydrochloride;B:tulobuterol hydrochloride;C:lincomycin hydrochloride
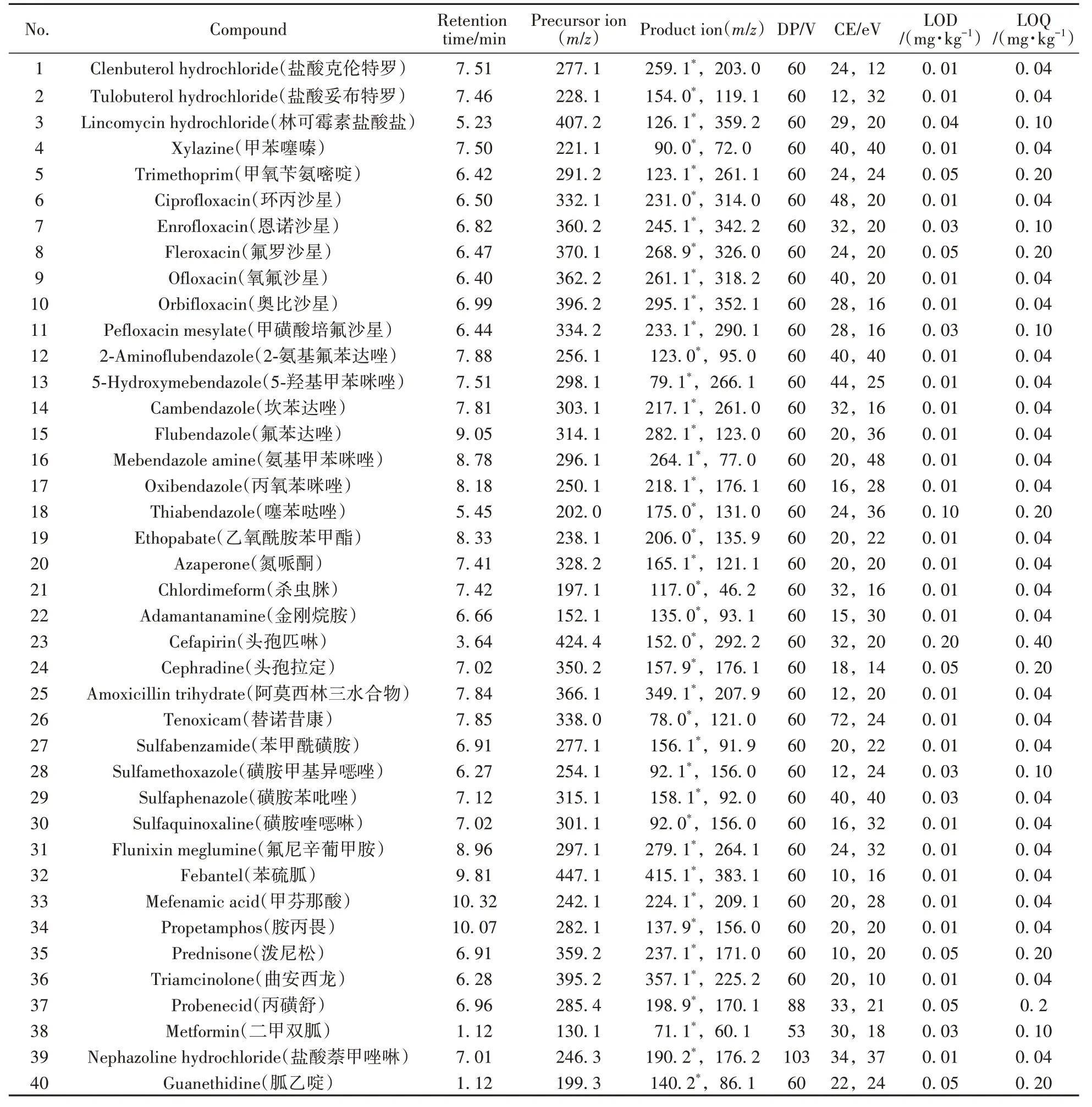
表2 45种化合物的保留时间、质谱参数、检出限与定量下限Table 2 Retention times,MS parameters,limits of detection and limits of quantitation of 45 compounds
2.2 HPLC-Q-TOF MS 快速筛查
基于“2.1”所建立的QuEChERS前处理方法可知,其稳定性好、灵敏度高,将其进一步扩展应用于霜膏类化妆品中297种风险物质的靶向筛查。样品经提取、净化,HPLC-Q-TOF MS 上机测定,采集一级质谱信息(如保留时间、精确质量数等)并与所建立的筛查列表(见表3)进行比对分析,对精确质量数偏差在± 1×10-5内,保留时间偏差在± 0.2 min 内的化合物,继续进行二级碎片离子信息的比对,若二级碎片离子及丰度比匹配,则锁定“可疑目标物”,再采用UPLC-MS/MS 进行确证分析。UPLCMS/MS确证后则判定为检出。本方法完全满足霜膏类化妆品中297种风险物质快速筛查的方法学要求。

表3 297种风险物质的名称、分子式、离子化模式、保留时间、母离子与子离子Table 3 Names,formula,ion modes,retention times,precursor ions and product ions of 297 risk substances
2.3 实际样品检测
随机抽取29份霜膏类化妆品样品,采用“1.2.2”方法快速定性筛查297种风险物质,检出的风险物质再进行定量分析。结果表明,两款面霜筛查出风险物质,其中一款面霜检出甲芬那酸、盐酸赛庚啶、克林霉素,检出量分别为0.099 4、318 0、0.042 mg/kg,另一款面霜检出甲芬那酸、盐酸赛庚啶和林可霉素,检出量分别为0.102 2、0.157 4、412 mg/kg。
3 结 论
本研究基于 QuEChERS 结合HPLC-Q-TOF MS 建立了霜膏类化妆品中297 种风险物质的筛查方法。选择45 种化合物作为质控化合物,优化了QuEChERS 前处理条件,建立了297 种风险物质的高分辨质谱筛查列表。该方法操作简单,具有较好的灵敏度和准确度,实现了对多种风险物质残留的快速筛查,解决了化妆品风险物质残留“检不全,检不快”的问题,可助力我国化妆品行业健康发展。
